受极端耐受生物启发,表达利用天然和设计的极端耐性相关蛋白在人体细胞中表达
2022-05-01
极端微生物对抗极端环境的生存策略是近年来的研究热点之一。2021年12月,麦吉尔大学的科学家从南极洲麦克默多干谷15万年前的永久冻土层中分离出新型嗜极酵母,发现了它在低温下可从呼吸作用转为乙醇发酵适应寒冷。
近日,哈佛大学Wyss生物启发工程研究所的研究人员,在ACS Synthetic Biology期刊上,在线发表了论文Natural and Designed Proteins Inspired by Extremotolerant Organisms Can Form Condensates and Attenuate Apoptosis in Human Cells。论文指出,许多生物体被置于极端条件下时,能够存活并成功地恢复到正常生存状态。出现这种极端耐受行为,部分原因是,生物体面对极端环境启动自我保护机制,上调蛋白表达,涉及到的蛋白包括重复蛋白、两亲性蛋白质和天然无序蛋白。
其中的保护机制尚不清楚,对此有以下两种主要假说。
一种假说认为,这些蛋白质中至少有一部分介导了整个细胞内物质的凝胶或玻璃状状态的形成,以保护其免受损害。该模型假设这些蛋白质与膜和其他蛋白质杂交,增加细胞内黏度,保护脆弱结构。

另一种假说认为,这些蛋白质形成细胞内相分离的无膜隔室,具有不同的物理参数(此处称为凝聚物),可划分关键的应力敏感细胞成分。在这些致密的蛋白质结构中,基本成分被隔离并保护免受损害。
两种假说并不相互排斥。例如,在耐干燥的情况下,持续脱水可能导致相分离的隔室融合,并促进玻璃态材料状态。
目前,越来越清楚的是生物相分离可能发挥重要作用,且人类细胞可以采用类似的策略在压力条件下生存。
极端耐受相关蛋白的序列特征可能与哺乳动物的应激耐受途径有关,包括减少细胞凋亡。之前的报道已经表明,极端耐受相关蛋白进行异源表达时,也表现出类似的保护特性。例如,在脱水过程中线虫Aphelenchus avenae上调的LEA蛋白,在人類细胞中表达会抑制PABPN1-A17的聚集(眼咽型肌营养不良的标志),改善肌营养不良症状;类似的案例还有,来自非洲蠓的LEA蛋白和来自缓步动物的TDP蛋白,在人类细胞中表达均呈现类似保护作用。这些发现加强了将保护性表型从其自身环境转移到人类细胞的潜力。
研究人员组装了一个包含大约300种天然存在和设计的极耐受相关蛋白的文库,以评估它们保护人类细胞免受化学诱导的细胞凋亡的能力。蛋白质库包括104种自然存在的蛋白质,166种螺旋区截断或分离的蛋白质,以及19种从头设计的蛋白质。

蛋白文库
为了验证序列特征及其与相分离和细胞凋亡关系的假设,研究人员在ExTol蛋白组的基础上设计了新的蛋白。这些新设计采用了三种方法:对蛋白质进行截断,聚焦于重复蛋白、两亲性蛋白质和天然无序蛋白区域;分离出具有所需序列特征的单个螺旋;以及从头设计含有α螺旋的蛋白质,使其自我组装成高阶结构。
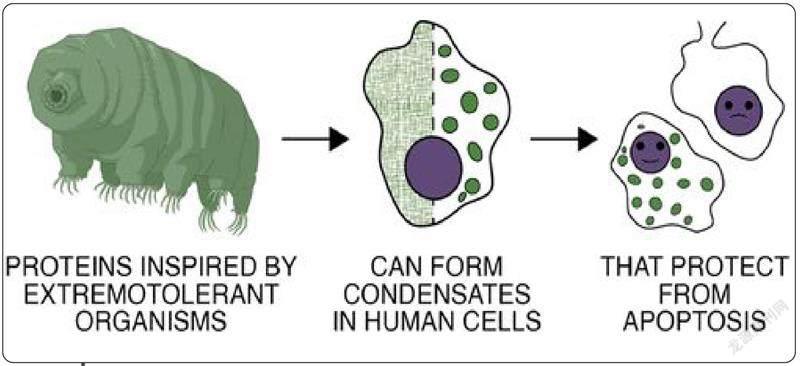
研究表明,来自缓步动物、线虫和中国大鲵的几种蛋白质具有细胞凋亡保护作用。设计合成的蛋白质比天然存在的蛋白质具有更强的功能。
值得注意的是,研究人员确定了人类APOE蛋白的一个区域也可以防止细胞凋亡,该区域与极耐受相关蛋白相似。另外,一种合成蛋白DHR81也有同样效果。
APOE在健康人体内的极低密度脂蛋白中发现,主要合成场所为肝脏,是一种能够结合和转运脂质的特殊蛋白,同时也参与着体内总胆固醇的逆向转运,是一种多态性蛋白,可调节多种生物学功能。
研究数据表明,凝聚物的形成在这些蛋白质的抗凋亡中起作用,且通过工程诱导系统增加凝聚物的量,能够增强减少细胞凋亡的作用。但除了凝聚物的形成外,仍存在尚未发现的其它保护机制。
总而言之,该研究扩展了对凝聚物形成与细胞生理学之间关系的理解,展示了凝聚物积累如何有助于减少细胞凋亡,同时还确定了极端耐受相关的多种新蛋白质结构域。(综合整理报道) (编辑/多洛米)
