妊娠期糖尿病孕妇正常范围糖化血红蛋白与不良妊娠结局的相关性 *
2022-04-24肖江波诸清逸石中华
肖江波,诸清逸,石中华
(南京医科大学附属妇产医院产科,南京市妇幼保健院,南京 210004)
妊娠期糖尿病(gestational diabetes mellitus,GDM)是指孕期首次发生或发现的糖代谢异常。在国际糖尿病与妊娠研究组(the International Association of Diabetes in Pregnancy Study Groups,IADPSG)标准下,根据世界卫生组织最新统计,截至2018年中国GDM发病率约为13%,在全球范围内处于较高水平[1]。大量研究表明,GDM可增加妊娠期高血压疾病、巨大儿、大于胎龄儿、死胎、新生儿低血糖等并发症的发生率[2-3]。因此,对于妊娠期高血糖的筛查、诊断和管理策略等问题均应引起关注。近年来,作为近3个月平均血糖水平的预测指标,糖化血红蛋白(hemoglobin A1c,HbA1c)在GDM的诊断与治疗中得到极大的关注。目前已有多项研究表明,妊娠早期HbA1c可作为GDM预测指标,并与不良妊娠结局相关,并建议以5.9%的阈值用于诊断高血糖和确定孕妇亚组[4-5]。这些研究主要关注妊娠早期HbA1c水平。由于妊娠期间HbA1c浓度存在显著双相变化,最初在24周时逐渐下降到最低点,随后缓慢回升至峰值[6],因此孕中期HbA1c可能存在更低正常阈值。早期研究显示,HbA1c为5.5%反映了在非妊娠女性人群和妊娠妇女孕中期HbA1c最高的正常参考值[7],同时我国建议GDM孕妇妊娠期HbA1c宜<5.5%[8]。目前已有研究初步提示,在非GDM孕妇中,孕中期HbA1c与母婴不良妊娠结局具有较好的相关性[9-10]。同时另一项研究也指出,非妊娠人群中HbA1c的临界水平(5.6%~6.4%)或高水平(>6.5%)更可能发生药物治疗性糖尿病[11]。然而在GDM妊娠人群中,正常范围内的HbA1c(<5.5%)是否也与不良妊娠结局相关不得而知。鉴于此,本研究旨在探讨正常范围内更高的HbA1c水平是否增加GDM孕妇不良妊娠结局。
1 资料与方法
1.1 研究对象 选取2018年1月1日至2019年8月30日于南京市妇幼保健院建卡并分娩的单胎GDM孕产妇及其新生儿,回顾分析相关临床数据,包括人口统计学特征、实验室检查、孕产妇及新生儿妊娠结局等。
1.2 GDM诊断标准及治疗 采用IADPSG标准(孕24~28周行OGTT试验:FPG≥5.1mmol/L、1h 血糖≥10.0mmol/L、2h 血糖≥8.5mmol/L,满足一项即可诊断GDM)[12]确诊GDM。对于GDM患者,给予医学营养和运动指导。血糖控制目标:餐前血糖≤5.3mmol/L,餐后2h血糖≤6.7mmol/L,对饮食及运动管理血糖控制不良者,给予胰岛素进一步控制血糖。
1.3 排除标准 孕前患有1型、2型糖尿病;孕期被诊断为糖尿病合并妊娠(pregestational diabetes mellitus,PGDM)或HbA1c>5.5%;多胎妊娠、妊娠未满28周流产、胎死宫内或死产;患有影响红细胞存活时间疾病(任何溶血性贫血、慢性肾衰竭、严重肝病和慢性疾病贫血等);临床资料部分缺失。最终共有8292例孕产妇及其新生儿被纳入研究。
1.4 不良妊娠结局的范畴 不良母婴结局,包括早产、巨大儿、大于胎龄儿、子痫前期、产后出血、羊水过少、羊水过多、胎盘早剥、前置胎盘、妊娠期肝内胆汁淤积症(intrahepatic cholestasis of pregnancy,ICP)、新生儿低血糖、新生儿窒息、新生儿呼吸窘迫综合征(neonatal respiratory distress syndrome,NRDS)、新生儿湿肺、新生儿高胆红素血症等。诊断均符合《妇产科学》及《儿科学》第9版中的诊断标准[8,13]。
2 结 果
2.1 孕妇一般资料 G4组的年龄及孕前BMI高于其它3组,同时G3和G2组的年龄及孕前BMI高于G1组(P<0.05)。G4组的分娩孕周低于其它组(P<0.05),G2和G3组的分娩孕周低于G1组(P<0.05)。G4组的初产妇比例高于G1和G2组(P<0.05);同时G4组的胰岛素使用及OGTT三项异常比例高于其它3组(P<0.05)。见表1。
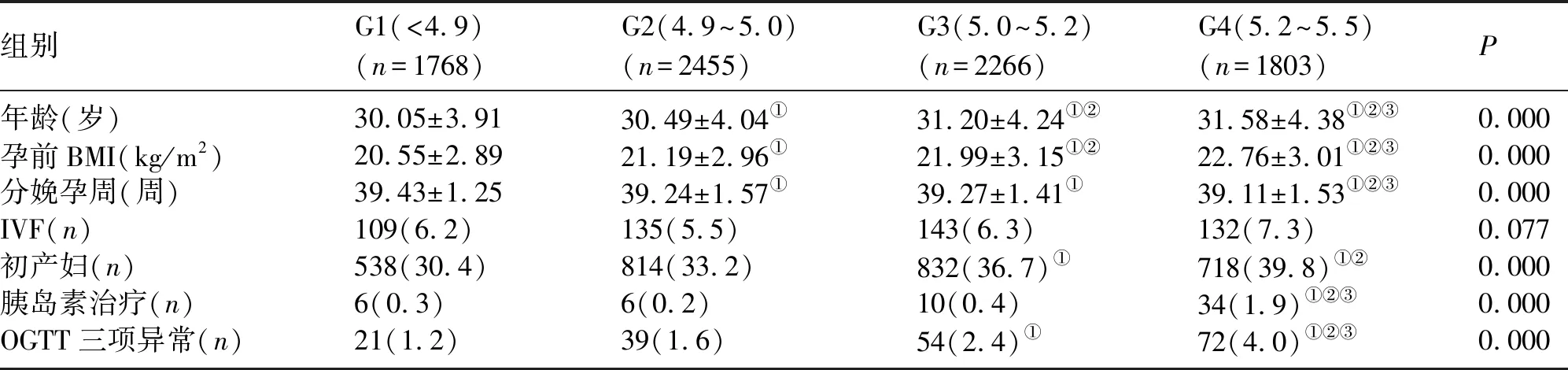
表1 各组孕妇一般资料比较
2.2 妊娠结局 早产、首次剖宫产、子痫前期发生率均随着糖化血红蛋白的升高而增加(Pfor Trend<0.05)。两两比较发现,G4组的早产率明显高于其它3组,G2和G3组高于G1组(P<0.05);G3和G4组的首次剖宫产发生率高于G1和G2组,G2组高于G1组(P<0.05);G4组的子痫前期发生率高于G1和G2组,G3组高于G1组(P<0.05)。围产儿结局方面,巨大儿、大于胎龄儿的发生率均随着糖化血红蛋白的升高而增加(Pfor Trend<0.05)。两两比较发现,G4和G3组的巨大儿发生率高于G1和G2组,同时G4组的大于胎龄儿发生率大于其它3组(P<0.05)。见表2、3。

表2 各组孕妇不良结局比较[n(%)]

表3 各组新生儿不良结局比较[n(%)]
2.3 孕妇妊娠中期HbA1c浓度与不良妊娠结局的相关性 在未调整的模型中,孕中期HbA1c与巨大儿、大于胎龄儿、早产发生率显著相关,OR值分别为2.642(95%CI为1.909~3.606)、2.844(95%CI为2.164~3.736)、2.223(95%CI为1.480~3.340);调整混杂因素仍存在相关性,OR值分别为1.585(95%CI为1.131~2.222)、1.603(95%CI为1.204~2.135)、2.848(95%CI为1.859~4.363)。见表4。

表4 妊娠不良结局logistic回归分析
3 讨 论
近年来,随着研究的深入,在非妊娠人群中,HbA1c被广泛用于糖尿病和前驱糖尿病的监测、筛查和诊断中,HbA1c>6.5%已成为孕前糖尿病诊断标准之一[14]。这提示HbA1c在糖尿病的诊疗中有着不可替代作用。然而对于GDM来说,由于受限妊娠所带来的生理变化,HbA1c的作用尚未被完全阐明。
HbA1c水平代表着近3个月的平均血糖控制水平,一般情况下,高水平HbA1c代表较差的血糖控制水平。本研究发现,高水平的HbA1c存在于更高的年龄、孕前BMI孕产妇中,这提示年龄、孕前BMI可能影响血糖受损程度,这也与GDM危险因素研究结果类似[15]。另一方面伴随着HbA1c的增高,OGTT 3项异常人数明显增加。研究表明,伴随OGTT受损数目增加,可能具有更差的临床预后[16]。这可能提示正常水平HbA1c仍具有不同程度糖耐量受损的情况,更重要的是,药物治疗的GDM人数伴随着HbA1c水平的升高而明显增加,进一步提示孕中期正常水平HbA1c可能反应不同的代谢水平,可作为药物治疗GDM的一个预测指标。
本研究发现,高水平HbA1c与早产、巨大儿和大于胎龄儿发生率显著相关。早产是新生儿死亡的主要原因[17]。巨大儿和大于胎龄儿也是新生儿结局的危险因素[18]。相关证据表明,对于PGDM孕产妇,HbA1c与早产[19]及分娩大于胎龄儿密切相关[20]。另一方面,日本的一项前瞻性全国出生队列研究发现,HbA1c每增加1%(11mmol/mol),早产发生为1.27倍(95%CI为1.10~1.47),大于胎龄儿发生为1.16倍(95%CI为1.04~1.29)[21]。本研究结果类似,在排除混杂因素影响后,妊娠中期HbA1c水平与GDM孕产妇早产、大于胎龄儿发生率显著相关。研究表明,孕妇胰岛素抵抗水平是巨大儿的独立影响因素[22],这可能解释了随着HbA1c增加,巨大儿及大于胎龄儿的发生率显著增加。然而,在本研究结果中,HbA1c并未影响新生儿低血糖、RDS及新生儿高胆红素血症等不良围产儿结局,这可能提示HbA1c在预测不良妊娠结局方面具有较好的针对性,这与文献报道类似[5]。另一方面也可能由于对GDM的检测和管理而导致了这种不明显的差异性。
综上所述,在IADPSG诊断标准下,GDM发病率显著增加,诊疗资源的缺乏导致许多严重的GDM被忽视和疏于管理。本研究提供了进一步的证据来评估妊娠中期正常范围内不同水平的HbA1c作为监测不良分娩结果指标的临床意义。一方面,鼓励妇女在适龄期间怀孕,同时在备孕期控制体重,防止孕期不良代谢疾病的发生。另一方面,对于GDM人群,妊娠期较高HbA1c水平是早产、巨大儿和大于胎龄儿的独立危险因素,因此应重点关注这部分人群,积极地对其进行及时的监测与干预,这可能有助于预防不良的分娩结果。鉴于本研究为单中心的回顾性研究,研究结论需更多的循证医学依据来支持。
