幽门螺旋杆菌感染与非酒精性脂肪肝的相关性研究
2022-04-23郭月欢甘惠中
郭月欢,甘惠中
(安徽医科大学第三附属医院消化内科,安徽 合肥 230000)
非酒精性脂肪肝(nonalcoholic fatty liver disease,NAFLD)是一种与胰岛素抵抗和遗传易感性密切相关的代谢应激性肝损伤[1]。NAFLD 已被认为是全球公共卫生问题,影响普通人口的20%~45%,在2 型糖尿病(type 2 diabetes mellitus,T2DM)患者中上升至70%,在病态肥胖患者中上升至90%[2,3]。NAFLD 是肝硬化、肝细胞癌和肝移植的主要原因。NAFLD的自然史分为单纯脂肪变性和非酒精性脂肪性肝炎(nonalcoholic steatohepatitis,NASH),可伴或不伴有纤维化,如果不积极预防或治疗,NAFLD可进展为肝硬化和肝细胞癌。幽门螺旋杆菌(Helicobacter pylori,H.pylori)是寄生于消化道的微需氧菌,其与慢性胃炎、消化性溃疡、胃癌等消化道疾病的发生关系密切。与NAFLD的高流行率类似,H.pylori也在世界范围内广泛流行,其平均患病率约为58%[4]。近年来国内外研究表明[5-8],H.pylori 感染可能促进NAFLD的发生和发展,H.pylori 有望成为临床上逆转非酒精性脂肪肝病情的新靶点。但是也有部分学者认为[9-11],NAFLD 和H.pylori 之间没有关系,甚至有报道提出H.pylori的患者比非感染者具有更低的NASH 率。基于此,本研究主要探讨H.pylori 感染与NAFLD的关系,以期为临床治疗提供参考。
1 资料与方法
1.1 一般资料 选取2019 年5 月-2021 年6 月安徽医科大学第三附属医院体检中心进行健康体检的人群共960 人,其中男570 人,女390 人。纳入标准:行14C-尿素呼气实验检测H.pylori及腹部超声检查,且具有完整体检数据。排除标准:①近1 个月使用过抗生素、铋剂、质子泵抑制剂、H2受体拮抗剂;②有病毒性肝炎、药物性肝病、全胃肠外营养、肝豆状核变性、自身免疫性肝病等可导致脂肪肝的特定疾病;③有肿瘤病史,有胃部分或全部切除手术史,严重肝肾功能不全者;④过去12 个月每周摄入乙醇量≥210 g(男)或≥140 g(女)者。本研究经医院伦理委员会批准,研究对象知情同意并签署知情同意书。
1.2 方法
1.2.1 一般资料收集 通过问卷调查以及电话随访的方式收集患者的吸烟史、饮酒史、既往病史(糖尿病史、高血压史、肝肾疾病史、肿瘤病史、手术史等)资料、体格检查资料[体检当日测量身高、体重、血压,由经过培训的专业人员使用专用仪器测量。计算体质量指数(BMI)=体重/身高2]。根据《中国成人超重和肥胖症预防控制指南》标准[12]:BMI<18 kg/m2时为消瘦;BMI<24 kg/m2且≥18 kg/m2时为正常;≥24 kg/m2且<28 kg/m2时为超重;≥28 kg/m2时为肥胖。
1.2.2 血液化验检测 受检者清晨空腹采集静脉血,检测空腹血糖(GLU)、糖化血红蛋白(HbA1c)、甘油三酯(TG)、总胆固醇(TC)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)、谷氨酰转肽酶(GGT)、碱性磷酸酶(ALP)、丙氨酸氨基转移酶(ALT)、天门冬氨酸氨基转移酶(AST)、尿酸等指标。
1.2.3 腹部B 超检查 应用飞利浦(意大利)PHILIPSIU22 高分辨率多功能彩色多普勒超声诊断仪检测。受试者空腹10~12 h,每位受检者由2 名技术精湛、经验丰富的超声科医师进行腹部超声检查,并统一出具报告。
1.2.4 H.pylori 检测 采用14C-尿素呼气试验试剂盒检测,由专业医务人员进行检测;检测方法:受检者空腹或禁食2 h 以上接受检测,维持正常呼气,将吸管插入1 个样品管底部,用吸管将气呼入样品管持续4~5 s,拔出吸管,立即扭紧试管盖,此收集的为0 min 呼气;受试者用80~100 ml 凉饮用水送服尿素14C 颗粒后,静坐;30 min 后受试者按上述收集方法收集呼气,将收集的0、30 min的呼气样品管在相应的仪器上进行检测。根据《第五次全国幽门螺杆菌感染处理共识报告》,14C-尿素呼气试验阳性可诊断H.pylori 现症感染[13]。
1.2.5 分组方法 根据体检数据,将人群分为NAFLD组和非NAFLD 组。NAFLD 诊断标准符合中国肝病学会2011 年临床诊断标准[14]:①腹部B 超检测肝脂肪变性;②肝脏附近回声呈弥漫性增强,强于肾、脾;③肝脏远场回声逐渐减弱;④肝内导管结构不清晰;⑤无明显饮酒量或每周<210 g(男)或<140 g(女)饮酒量;⑥无慢性肝病的共存原因,如丙型肝炎、药物治疗、肠外营养、威尔森氏病或严重营养不良。
1.3 统计学方法 采用SPSS 25.0 统计软件进行数据分析,计量资料以()表示,采用t检验;计数资料以[n(%)]表示,采用χ2检验;多因素分析应用非条件Logistic 回归分析,以P<0.05 表示差异有统计学意义。
2 结果
2.1 NAFLD 组和非NAFLD 组临床资料比较NAFLD 组吸烟史、高血压病史、糖尿病病史、H.pylori阳性检出率、颈部血管斑块检出率、BMI、ALT、AST、GGT、ALP、TG、TC、LDL-C、尿酸、HbA1c 水平高于非NAFLD 组,HDL-C 水平低于非NAFLD 组,差异有统计学意义(P<0.05);两组性别比较,差异无统计学意义(P>0.05),见表1。
表1 NAFLD 组和非NAFLD 组临床资料比较[,n(%)]
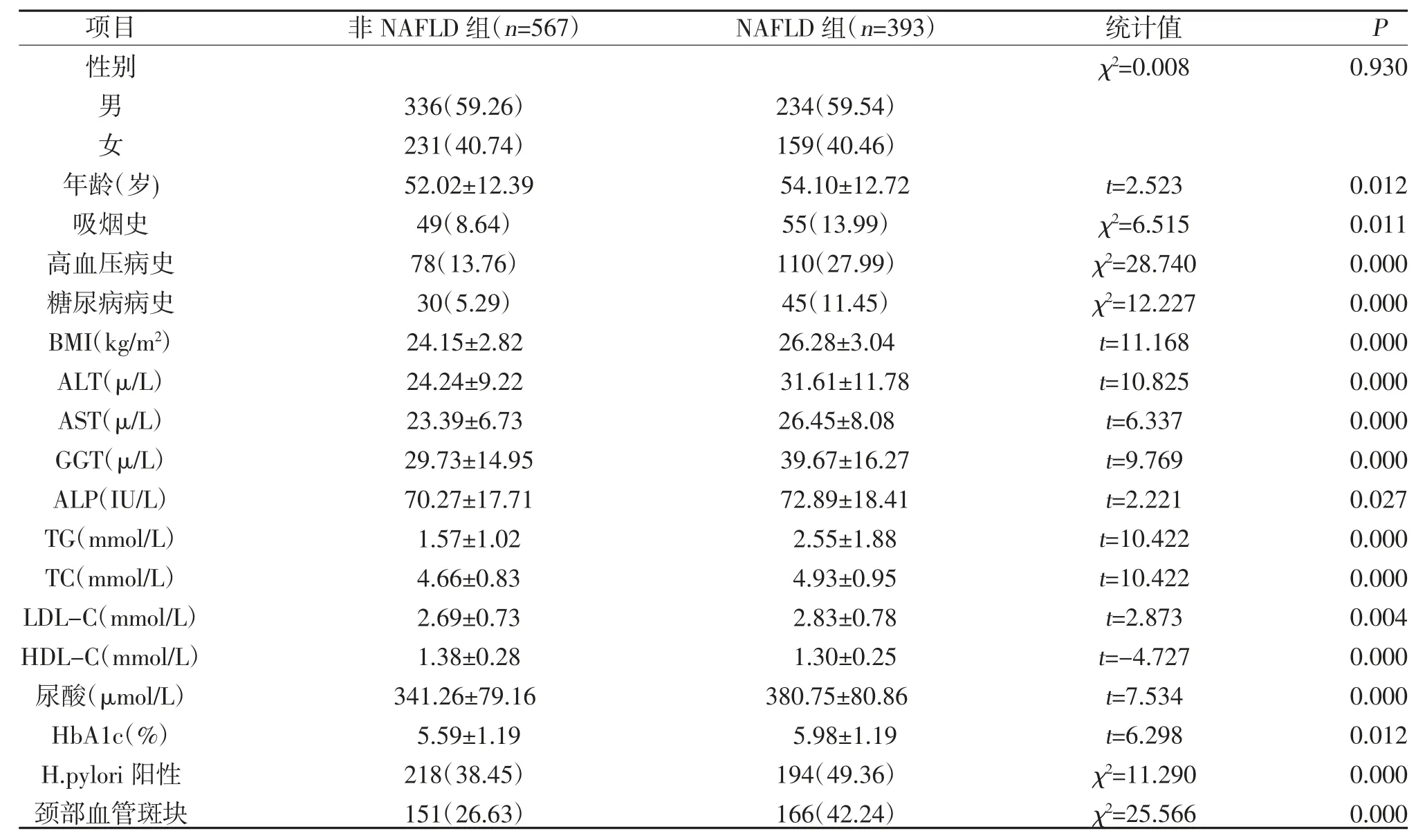
表1 NAFLD 组和非NAFLD 组临床资料比较[,n(%)]
2.2 NAFLD 组中H.pylori 阳性与H.pylori 阴性者临床资料比较 H.pylori 阳性者高血压病史、颈部血管斑块检出率、BMI、TC、LDL-C 高于H.pylori 阴性者,差异有统计学意义(P<0.05);其余指标比较,差异无统计学意义(P>0.05),见表2。
表2 NAFLD 组中H.pylori 阳性与H.pylori 阴性临床资料比较[,n(%)]

表2 NAFLD 组中H.pylori 阳性与H.pylori 阴性临床资料比较[,n(%)]
2.3 NAFLD 多因素回归分析 多因素Logistic 回归分析显示,BMI、TG、HbA1c、H.pylori 感染是NAFLD的相关因子(P<0.05),见表3。

表3 NAFLD 多因素Logistic 回归分析
3 讨论
研究指出[15],在病态肥胖患者中活动性H.pylori感染与NAFLD 独立相关。另有研究表明[16],与H.pylori 阴性者相比,H.pylori 阳性者的NAFLD 患病率、ALT、AST、空腹血糖水平均显著升高,且H.pylori感染是NAFLD的独立危险因素,与脂肪变性程度的增加有关。目前较多研究指出H.pylori 影响NAFLD的机制可能如下:①H.pylori 感染增加胃肠道上皮的渗透性,从而有利于肠道微生物群及其代谢物易位到门脉循环中,在肝细胞激活炎症,从而促进NAFLD的进展;②通过诱导某些血管活性和促炎介质的释放,包括白细胞介素(IL-1、IL-6、IL-8、IL-10、IL-12、TNF-α、干扰素-γ、白三烯、前列腺素)和急性期蛋白(C 反应蛋白和纤维蛋白原),它们与代谢综合征(MetS)和NAFLD的病理生理学有关;③H.pylori相关的氧化应激诱导与维生素B12/叶酸缺乏相关的萎缩性胃炎、细胞凋亡和脂联素的下调可能构成了H.pylori 和NAFLD 之间的其他致病联系[17]。
本研究结果表明,NAFLD 组吸烟史、高血压病史、糖尿病病史、H.pylori 阳性检出率、颈部血管斑块检出率、BMI、ALT、AST、GGT、ALP、TG、TC、LDL-C、尿酸、HbA1c 水平高于非NAFLD 组,HDL-C 水平低于非NAFLD 组,差异有统计学意义(P<0.05);H.pylori 阳性者高血压病史、颈部血管斑块检出率、BMI、TC、LDL-C 高于H.pylori 阴性者,差异有统计学意义(P<0.05),表明H.pylori 感染可能通过影响脂质代谢,从而影响NAFLD的发生发展。此外,本研究中多因素Logistic 回归分析显示,BMI、TG、HbA1c、H.pylori 感染是NAFLD的相关因子(P<0.05),与Cai O 等[18]研究结果较不一致,其原因可能与H.pylori的检测方法不同、受检者脂肪肝的严重程度不同、样本量有限等因素有关。
NAFLD的发病机制复杂,“多重平行打击”机制认为包括胰岛素抵抗(IR)、脂肪组织分泌的激素、营养因素、肠道微生物群在内的多重损伤共同作用于遗传易感者以诱发NAFLD。本研究结果发现,BMI、TG、HbA1c、H.pylori 感染是NAFLD的相关因子[19]。肥胖人群常常合并长期高糖或高脂肪饮食,富含碳水化合物或脂肪的饮食会导致肝脏中过多的脂肪堆积,从而成为NAFLD 发病机制的起点。体内大量游离脂肪酸(FFA)和TG 在肝脏组织蓄积,导致脂肪细胞肥大,从而导致脂肪因子(如瘦素/脂联素比率增加,白介素和肿瘤坏死因子释放)改变,使肝脏处于慢性低度炎症状态。脂肪以TG 形式积聚到肝细胞中,当TG 堆积超过肝脏的代偿范围,便会出现脂毒性,活性氧产生,脂肪炎症和肝细胞功能障碍,从而导致NAFLD/NASH的发展。HbA1c 可以反映近2~3 个月平均血糖水平,血糖升高会促进胰岛素释放,长时间的高血糖刺激容易产生IR。IR 一方面导致脂肪组织中的脂肪分解,为肝脏提供FFA,另一方面促进肝脏从头脂肪生成,导致脂肪在肝脏中进一步积累。本研究指出合并H.pylori 感染的NAFLD患者血脂水平更高,提示H.pylori 感染可能通过干扰脂质代谢和胰岛素敏感性参与NAFLD的发展。
综上所述,NAFLD 与肥胖、H.pylori 感染、TG、HbA1c 水平升高有关。IR 可能是连接上述相关因子与NAFLD的桥梁。H.pylori 可能通过干扰脂质代谢和胰岛素敏感性参与NAFLD的发展。
