亚低温护理对颅脑损伤患者神经功能及氧化应激反应的影响研究
2022-04-21蔺欣欣
王 会 张 伟 蔺欣欣
(新乡市中心医院,新乡医学院第四临床学院 新乡453000)
颅脑损伤是危害我国人民健康的重要疾病,其死亡率居各类创伤首位。近年来,我国颅脑损伤发生率的日趋升高,采取有效的治疗方案以完善临床救治体系,提高重型颅脑损伤的救治水平、降低死亡率、改善预后、提高患者生活质量是神经创伤领域研究的重要课题。临床上,颅脑损伤患者以神经功能进行性下降为主要病理特征,亚低温作为脑保护治疗体系的重要组成部分,主要通过降低机体温度而减少中枢神经系统的耗氧量,减少神经元细胞坏死及创伤对机体造成的极度应激反应,发挥多机制、多途径的神经损伤预防及修复作用。目前,亚低温在控制颅内压、减轻脑水肿等方面已得到广大学者的认可,本研究以我院收治的80例颅脑损伤患者为研究对象,探讨亚低温护理的实施方法及临床价值,现报道如下。
1 资料与方法
1.1 临床资料
选取2020年6月~2021年6月我院收治的颅脑损伤患者80例为研究对象。病例纳入标准:(1)有完整的病历资料者;(2)对本研究方案知悉且签署知情同意书者;(3)于损伤发生后24h内入院进行治疗者。排除标准:(1)有亚低温干预禁忌症者;(2)合并其他部位严重损伤者;(3)大量出血休克者。确定病例样本后,予以患者随机顺序编号,根据编号结果将其分为常规组和亚低温组各40例,对两组患者的一般资料进行比较,差异无统计学意义(P>0.05),见表1。

表1 常规组和亚低温组患者基线资料分布比较
1.2 方法
常规组40例患者实施常规护理,主要包括体征持续监测、基础生理护理、体温调整、营养支持等。
亚低温组40例患者在常规护理的基础上联合开展亚低温护理,具体干预措施:(1)物理降温。将患者安置在安静、清洁的独立病室中,设置室温于22℃~24℃之间,相对湿度于50%~60%之间,为机体循环代谢及温度调节提供基础条件。待患者进入冬眠状态时开始物理降温,即于病床上铺垫冰毯(循环水温设置为 4℃~10℃),患者平躺于冰毯上,促使毯面接触皮肤进行散热、降温; 将冰帽及冰袋放置于患者头部周围和全身大血管处,起到循环降温的作用。同时,在采取上述物理方法使患者全身处于亚低温状态的过程中需严格控制患者体温下降幅度,使肛温下降速度为每 1h~3h降低 1℃,最终控制在33℃~35℃[1],防止降温过快而引起呼吸抑制。(2)循环功能及体温监测。亚低温干预中加强患者循环功能指标(如心律、动脉压、中心静脉压、心排血量等)的连续监测,准确判断患者心脏射血功能,以便及时发现异常,并迅速做出反应。同时,予以患者体温变化的持续监测,若患者体温超过36℃,则提示亚低温干预效果不佳;若体温低于33℃,则提示患者呼吸、循环功能异常;若体温低于28℃,则提示室颤风险。而针对体温过低的患者应遵医嘱适当降低冬眠合剂的量,必要时停用并对患者提供加盖被子、温水袋等保暖措施。(3)体位调整及并发症预防。患者亚低温干预中躯干部、背臀部血循环减弱,每1~2h需更换体温,防止压疮。同时,加强患者凝血功能指标的密切监测,加强皮肤护理,防止皮肤冻伤;加强呼吸监测,一旦发现有点头样呼吸,应考虑呼吸中枢抑制过度,应保持呼吸通畅。(4)“循序渐进”式复温。于亚低温干预完成后,以每4h上升1℃左右的原则予以患者遵循“循序渐进”式复温,保证患者体温至37.5 ℃左右的复温时间为12h,防止复温速度过快而引发循环障碍及颅内压增高。
1.3 观察指标
1.3.1神经元因子
于两组患者护理干预前后,分别采集血液标本,离心分离血清后检测神经元因子:神经肽Y(NPY)、神经元特异性烯醇化酶(NSE)、神经特异性蛋白(S100β)。
1.3.2氧化应激反应指标
于两组患者护理干预前后,分别采取静脉血,离心分离血清后检查氧化应激反应指标:谷胱甘肽过氧化物酶(GSH-Px)、超氧化物歧化酶(SOD)、丙二醛(MDA)。
1.3.3远期预后
予以两组患者为期3个月的随访观察,采用GOS评分标准予以患者远期预后评价。
1.4 统计学方法

2 结果
2.1 两组患者神经元因子比较
护理前两组患者血清NPY、NSE、S100β比较,差异无统计学意义(P>0.05);护理后亚低温组患者血清NPY、NSE、S100β均低于常规组,差异有统计学意义(P<0.05),见表2。

表2 常规组和亚低温组患者血清NPY、NSE、S100β比较
2.2 两组患者氧化应激反应指标比较
护理前两组患者血清GSH-Px、SOD、MDA比较,差异无统计学意义(P>0.05);护理后亚低温组患者GSH-Px、SOD高于常规组(P<0.05),亚低温组患者MDA低于常规组(P<0.05),见表3。
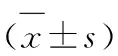
表3 常规组和亚低温组患者氧化应激反应指标比较
2.3 两组患者远期预后比较
常规组40例患者中预后良好25例,预后不良15例,预后良好率为62.50%(25/40);亚低温组40例患者中预后良好32例,预后不良8例,预后良好率为80.00%(32/80)。亚低温组患者预后良好率高于常规组(χ2=8.476,P=0.005)。
3 讨论
亚低温又称冬眠疗法,是采用镇静药物使患者进入睡眠状态后,联合应用冰毯、冰帽、冰袋等物流降温方法使患者体温处于一种可控性的低温状态。目前,亚低温作为重症医疗体系的重要组成部分,是国内外医学广泛证实有效的脑保护措施之一[2]。同时,亚低温作为神经重症领域的重要干预措施,国内外诸多前沿文献报道强调,亚低温干预可有效改善颅脑损伤患者的神经系统功能,对改善患者预后具有重要的作用。自20世纪90年代以来,随着欧洲两项大规模随机对照临床研究试验的开展,得出亚低温可促进受损神经功能恢复的结论以来,关于亚低温在颅脑损伤中的应用研究日益展开,在欧美、日本等许多医院已将其广泛应用于重型颅脑损伤患者的治疗。而临床上有关亚低温在颅脑损伤中作用机制的研究层出不穷,包括循环功能途径、氧化应激损伤途径、神经修复途径等[3]。
本研究中,常规组和亚低温组患者分别开展常规护理、常规护理+亚低温护理,研究结果显示:亚低温护理可有效减轻颅脑损伤患者机体的氧化应激刺激。颅脑损伤后,随着病情的进展会引起脑内稳态失衡及循环代谢功能障碍,可通过氧化应激、炎症反应等多种途径参与脑组织的损伤和进行性损伤,是导致患者预后不良的重要危险因素。本研究中,护理后,亚低温组患者GSH-Px、SOD高于常规组(P<0.05),亚低温组患者MDA低于常规组(P<0.05),即通过亚低温护理可有效改善脑损伤患者的氧化应激反应。一方面,亚低温护理不仅可有效改善体液循环,减少细胞毒性物质及炎症介质的释放,且可抑制兴奋性氨基酸和氧自由基等内源性有害因子的生成,起到改善全身或脑组织氧化应激损伤的作用[4];另一方面,亚低温能够保护或提高内源性抗氧化能力,发挥降低机体应对不良氧化应激刺激的能力[5]。因此,将亚低温干预理念引入颅脑损伤的干预中,填补了脑损伤治疗领域上的空白,对改善患者预后具有显著作用。
同时,本研究结果显示,亚低温治疗可有效减轻神经损伤。NPY作为神经元调节剂,其过量表达易抑制神经元再生,不利于受损神经细胞的修复;NSE是反映神经损伤程度的特异性指标;S100β为中枢神经系统损伤的标志蛋白。本研究中,护理后亚低温组患者血清NPY、NSE、S100β均低于常规组(P<0.05),即亚低温治疗可有效减轻颅脑损伤患者的神经损伤。近年来国内外临床关于亚低温与神经损伤之间相关作用机制的研究日渐成熟,结果表明亚低温具有预防神经损伤及修复受损神经细胞的双重作用。一是脑组织耗氧量占全身耗氧量的20%~30%,对缺血、缺氧性损害敏感[6]。颅脑损伤后通过亚低温干预可有效减少脑组织耗氧量,预防脑组织缺氧性损伤,且利于维持正常的脑细胞代谢功能[7];二是亚低温干预可从神经元入手,促进受损神经细胞的修复,并通过对神经元的激发而重新建立起神经传导的通路和环路,从而发挥修复神经损伤的作用[8~9]。同时,亚低温下可有效保证各个脏器灌注,对机体多个破坏性程序起到阻断作用,起到恢复或改善循环功能的作用。
另外,本研究结果显示:干预后,亚低温组患者预后良好率为80.00%,高于常规组的62.50%(P<0.05),即通过亚低温护理可有效改善患者预后,提高其生存质量。
综上所述,通过予以颅脑损伤患者亚低温护理能有效降低机体氧化应激刺激和神经损伤程度,改善患者预后,值得临床推广应用。
