基于丙烯酸/丙烯酰胺/苯乙烯的新型磁性水凝胶吸附重金属的研究
2022-04-08张浩然王士凡朱文友庄文昌董黎明堵锡华
袁 源,张浩然,王士凡,朱文友,庄文昌,董黎明,堵锡华
(徐州工程学院 材料与化学工程学院,江苏 徐州 221018)
随着现代化的不断推进,水污染处理尤其是重金属离子废水的处理显得尤为重要。重金属离子毒性极大,不易排出体外;若不慎摄入人体,可能会致癌、致畸,甚者产生生命危险。工业废水中常含有大量Pb2+,Cd2+等重金属离子,若不处理直接排放到环境水系中,会导致严重的水污染事件发生。处理这些重金属离子废水常用化学沉淀法、离子交换法、电化学法和吸附法等[1]。其中,吸附法是目前处理重金属离子废水的有效方法之一,具有操作简单灵活、去除率高、多数吸附材料易回收、成本低等优点[2]。同时,对吸附法所用新型吸附材料的要求日益增高,既要求具有高吸附量、易回收、重复利用性好等优良性能,又需要易制备,低成本,于环境无害。
吸附法常用吸附剂包括活性炭、碳纳米吸附材料、生物吸附剂以及复合高分子吸附材料。活性炭的比表面积大,且多微孔、中孔,已在重金属离子处理中得到广泛应用[3]。目前,对碳纳米材料的回收率较低,排放到环境中可能会对环境、人体造成危害,因此对环境友好型复合材料的研究显得比较重要[4]。生物吸附剂来源广泛,典型生物吸附剂(如木质素、壳聚糖等非生命生物质以及藻类、微生物等生物质)具有原料易得、可生物降解、无二次污染等优点,对重金属离子吸附效果较好,然而吸附完成后分离困难[5]。高分子吸附材料是吸附材料研究热点之一,具有吸附性高、稳定性较好、易制备等优点,且多数高分子吸附材料可回收循环利用[6]。其中,水凝胶吸附材料对环境友好,性能稳定,对重金属离子的去除率高,且制备方便,价格低廉[7]。在水凝胶吸附材料的基础上复合磁性材料所制备的磁性水凝胶吸附材料,易回收且具有较好的再生性。吴鹏等[8]用丙烯酸(AA)、丙烯酰胺(AM)、对苯乙烯磺酸钠制备的三元共聚水凝胶对重金属离子吸附效果较好;Zhang Hong等[9]以磁膨润土、羧甲基壳聚糖、海藻酸钠为原料制备的复合水凝胶对Cu2+去除率达92.62%;Sahraei等[10]以改性生物高聚物黄芪胶、聚乙烯醇和氧化石墨烯为原料,采用凝胶法制备的新型磁性水凝胶吸附材料对重金属离子有较高的去除率;Sanchez等[11]以聚乙烯醇、膨润土、磁性纳米粒子和介孔碳制备了复合磁性水凝胶,对Cd2+有较高的吸附率,且磁性纳米粒子填料越高,吸附效率越高。
本工作以AA,AM和苯乙烯(St)为原料制备了具有高吸附性的水凝胶[P(AA-AM-St)][12];再以P(AA-AM-St)与SiO2包裹的Fe3O4(Fe3O4@SiO2)为原料制备了磁性水凝胶[P(AA-AM-St)/Fe3O4@SiO2],研究其吸附性能,以及pH值、离子浓度、吸附时间、离子共存等对水凝胶吸附典型重金属离子的影响,并分析其热稳定性、再生性能以及吸附动力学、热力学。
1 实验部分
1.1 主要原料与仪器
AA,AM,St,Fe3O4@SiO2,NaOH,KPS,三水合硝酸铜,N,N′-亚甲基双丙烯酰胺(MBA),四水合硝酸镉,四水合硝酸镍,硝酸铅:均为分析纯,国药集团化学试剂有限公司。去离子水,自制。
Z-5000型原子吸收分光光度计,日本日立公司;AlpHA型傅里叶变换红外光谱仪,德国布鲁克公司;XRD-7000S/L型X射线衍射仪,日本岛津企业管理有限公司;Q50型热重分析仪,美国TA仪器公司;PHS-2F型pH测试仪,上海仪电科学仪器股份有限公司;V-Sorb 2800型比表面孔径分析仪,北京金埃谱科技有限公司。
1.2 P(AA-AM-St)/Fe3O4@SiO2的合成
取3.14 mL AA,加入NaOH溶液中和,冷却至室温;然后依次加入1.11 g AM,0.61 mL St和0.10 g KPS,搅拌10 min后再加入0.027 g MBA和1.00 g Fe3O4@SiO2,升温至80 ℃,继续搅拌8 h,水洗,烘干,粉碎得到粒径约75 μm的P(AA-AM-St)/Fe3O4@SiO2,合成示意见图1。

图1 P(AA-AM-St)/Fe3O4@SiO2的合成示意Fig.1 Synthesis of P(AA-AM-St)/Fe3O4@SiO2
1.3 P(AA-AM-St)/Fe3O4@SiO2的吸附实验
将5份0.10 g的P(AA-AM-St)/Fe3O4@SiO2分别置于装有质量浓度为1 000 mg/L,体积为50 mL的重金属离子溶液的锥形瓶中,将重金属离子溶液的pH值分别调至2,3,4,5,6,于30 ℃搅拌2 h。采用原子吸收分光光度计测定溶液中的重金属离子浓度,计算吸附量。
分别取25 mL,2 000 mg/L的不同重金属离子溶液加入到锥形瓶中,配制成Pb2+/Cd2+,Pb2+/Ni2+,Pb2+/Cu2+混合溶液;分别称取定量(PbNO3)2,Cd(NO3)2,Cu(NO3)2,Ni(NO3)2溶解后定容,配制成每种重金属离子质量浓度均为1 000 mg/L的Pb2+/Cd2+/Cu2+/Ni2+混合溶液。分别取50 mL上述4组重金属离子混合溶液,加入0.20 g P(AA-AMSt)/Fe3O4@SiO2,于200 r/min,25 ℃振荡2 h,静置沉降,取上清液,测定溶液中Pb2+的含量;用浓盐酸进行解吸附。重复吸附解吸附实验10次,同时进行3次平行实验。计算P(AA-AM-St)/Fe3O4@SiO2对应的吸附量。
1.4 测试与表征
傅里叶变换红外光谱(FTIR)分析:采用傅里叶变换红外光谱仪测试,波数为400~4 000 cm-1;X射线衍射(XRD)分析:扫描速率为5(°)/min,衍射角(2θ)为10°~80°;热重(TG)分析:N2氛围,以20 ℃/min从室温升高到800 ℃;采用比表面积测试(BET)法对水凝胶的微观结构进行表征。
2 结果与讨论
2.1 FTIR分析
从图2可以看出:3 429,3 439 cm-1处为—NH与—OH的伸缩振动峰;2 960,2 940 cm-1处为—CH2的伸缩振动吸收峰;1 596,1 531 cm-1处为苯环的伸缩振动峰;1 392,1 393 cm-1处为—COONa中—C=O—的对称伸缩振动峰;776 cm-1处为Si—O的对称伸缩振动峰;620 cm-1处为Fe3O4上Fe—O的伸缩振动吸收峰[13]。说明Fe3O4@SiO2与P(AA-AMSt)成功复合。
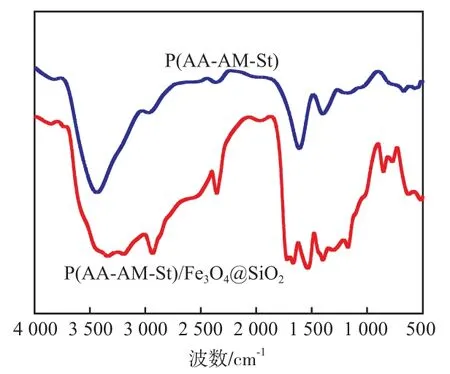
图2 水凝胶的FTIR图谱Fig.2 FTIR spectra of hydrogels
2.2 XRD分析
从图3可以看出:P(AA-AM-St)/Fe3O4@SiO2谱线上,2θ为30.5°,35.4°,43.3°,54.5°,57.5°,63.1°处的特准衍射峰分别归属于反尖晶石结构Fe3O4(220),(311),(400),(422),(511),(441)晶面[14],再次说明了Fe3O4@SiO2与P(AAAM-St)成功复合。
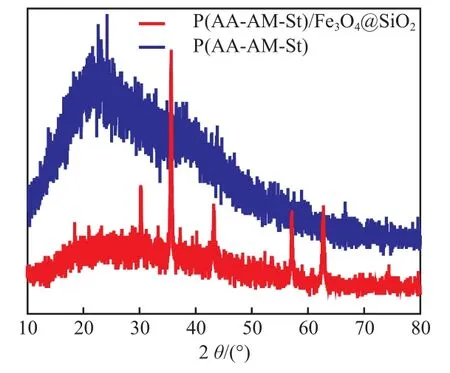
图3 水凝胶的XRD曲线Fig.3 XRD patterns of hydrogels
2.3 TG分析
从图4可以看出:温度低于340 ℃时,P(AAAM-St)/Fe3O4@SiO2的质量损失率为12.5%;在340~422 ℃时,质量损失率为30.5%,这是一些低聚物和水凝胶链上较为稳定的基团断裂分解;422℃之后,质量损失率缓慢降低。P(AA-AM-St)/Fe3O4@SiO2质量损失5%时的温度达到205 ℃,说明其具有较为良好的热稳定性。

图4 P(AA-AM-St)/Fe3O4@SiO2的TG曲线Fig.4 TG curves of P(AA-AM-St)/Fe3O4@SiO2
通过BET法得到P(AA-AM-St)/Fe3O4@SiO2的比表面积、孔体积、平均孔直径分别为2.90 m/g,0.004 cm3/g,3.4 nm,属于介孔材料。
2.4 吸附测试
2.4.1 吸附条件对P(AA-AM-St)/Fe3O4@SiO2吸附性能的影响
从图5可以看出:与其他几种重金属离子相比,P(AA-AM-St)/Fe3O4@SiO2对Pb2+的吸附效果较为显著,因此,以下选择50 mL,1 000 mg/L Pb2+溶液为对象,研究P(AA-AM-St)/Fe3O4@SiO2的吸附性能。
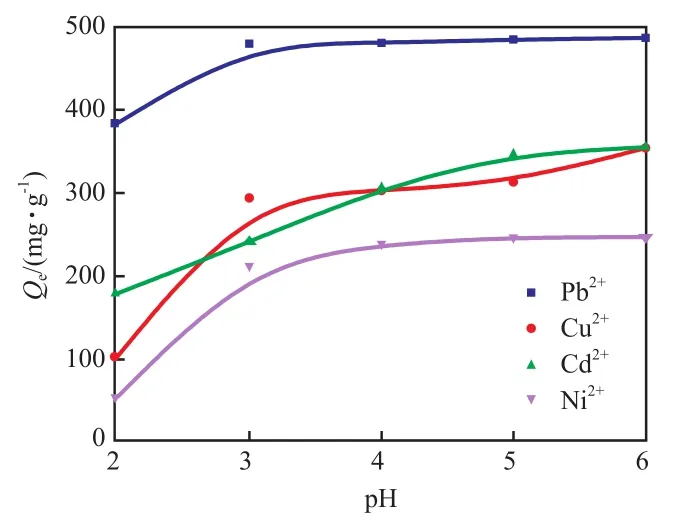
图5 不同pH值时P(AA-AM-ST)/Fe3O4@SiO2对典型重金属离子的吸附曲线Fig.5 Adsorption curves of typical heavy metal ions by P(AA-AM-St)/Fe3O4@SiO2 at different pH values
从图5还看出:pH值为2~4时,吸附量上升;pH值为4~6时,吸附量上升趋势相对较慢。可能原因是pH值低时水凝胶中的NH3+会因为—NH2进行质子化而大量溢出,对重金属离子产生静电排斥,最终降低P(AA-AM-St)/Fe3O4@SiO2对重金属离子的吸附性能[15]。在pH值为5时,对Pb2+的吸附量达484 mg/L。
从图6a看出:随吸附时间的增加,吸附量先迅速增加后趋于平缓,在180 min时饱和,达478 mg/g。这主要是因为随反应进行,P(AA-AM-St)/Fe3O4@SiO2吸附位点逐渐被Pb2+占据。从图6b看出:在不同温度条件下,P(AA-AM-St)/Fe3O4@SiO2的吸附量随浓度增大而增加,当初始质量浓度为300 mg/L时较适宜,最大吸附量皆超过495 mg/g。

图6 吸附时间、吸附温度与初始质量浓度对P(AA-AM-St)/Fe3O4@SiO2吸附性能的影响Fig.6 Effects of adsorption time,adsorption temperature and concentration on adsorption performance of P(AA-AM-St)/Fe3O4@SiO2
2.4.2 竞争与再生测试
在Pb2+/Cd2+/Cu2+/Ni2+,Pb2+/Cd2+,Pb2+/Ni2+,Pb2+/Cu2+这四个体系中,Pb2+的竞争吸附量受影响较小,仍分别达到466,456,465,454 mg/g,说明P(AA-AM-St)/Fe3O4@SiO2对Pb2+的亲和力较大。从图7可以看出:随着吸附次数的增加,P(AAAM-St)/Fe3O4@SiO2对Pb2+的吸附量略微下降。10次吸附中仍能对Pb2+溶液有418 mg/g的吸附量,这说明P(AA-AM-St)/Fe3O4@SiO2具有优异再生能力。
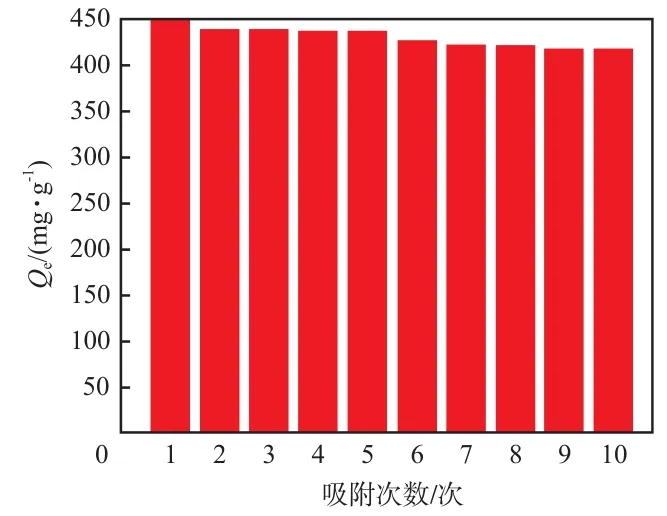
图7 P(AA-AM-St)/Fe3O4@SiO2的重复利用性测试结果Fig.7 Reusability test of P(AA-AM-St)/Fe3O4@SiO2
2.4.3 动力学与热力学研究
为研究吸附机理,采用准一级、准二级动力学和颗粒扩散模型拟合动力学数据,从图8和表1看出:所得准二级动力学的相关系数高于准一级动力学;准二级动力学所得理论吸附量更接近于实验所得的吸附量[16],因此,P(AA-AM-St)/Fe3O4@SiO2对Pb2+的吸附动力学更符合准二级动力学模型,表明化学吸附为该反应的主要控制步骤[17]。
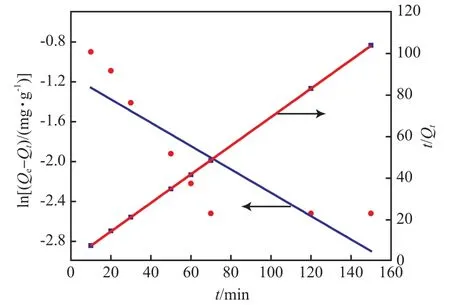
图8 吸附动力学模型Fig.8 Dynamic adsorption model of P(AA-AM-St)/Fe3O4@SiO2
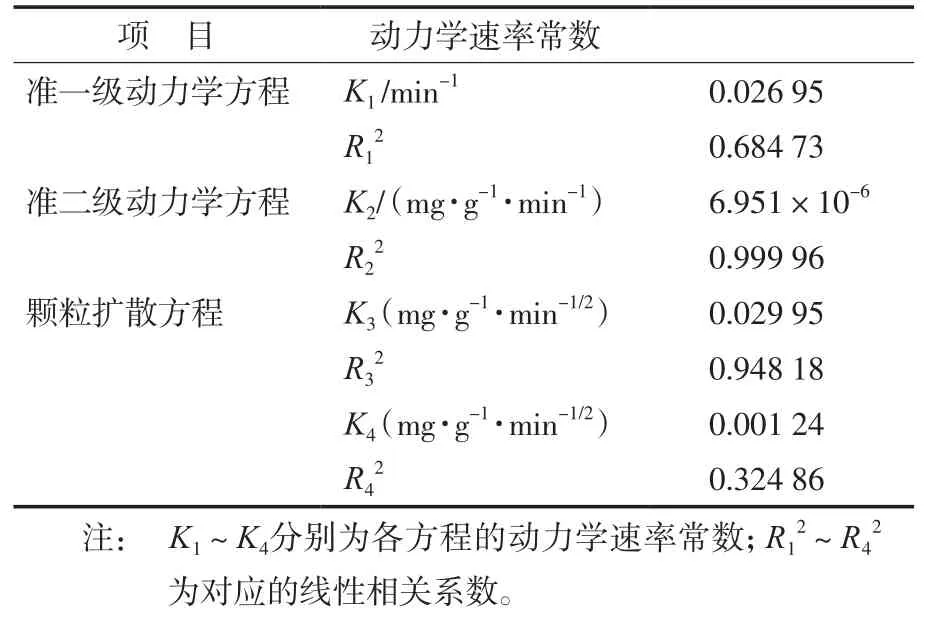
表1 P(AA-AM-St)/Fe3O4@SiO2对Pb2+吸附的准一级、准二级动力学模型拟合参数与颗粒扩散模型拟合参数Tab.1 Pseudo-first class and second class dynamics model fitting parameters and particle diffusion model fitting parameters of P(AA-AM-St)/Fe3O4@SiO2 to Pb2+
从图9可以看出:P(AA-AM-St)/Fe3O4@SiO2的颗粒扩散可分为表面吸附与孔道缓慢扩散两个吸附过程。直线都不经过原点,说明内扩散不是控制吸附过程的唯一方式。
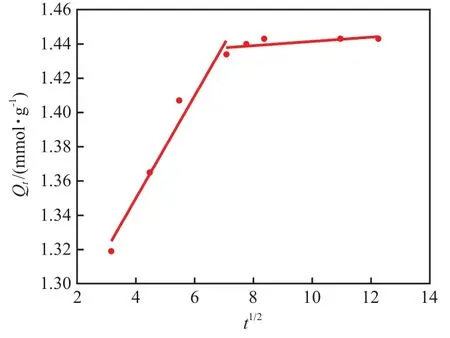
图9 颗粒扩散曲线Fig.9 Particle diffusion curve
在30 ℃吸附条件下对吸附曲线采用Langmuir和Freundlich模型进行数据拟合,结果见表2。Langmuir模型的相关系数较高,并且最大吸附量与实验数据更接近,所以P(AA-AM-St)/Fe3O4@SiO2对Pb2+的吸附主要属于单分子层吸附。

表2 吸附等温模型参数Tab.2 Adsorption isotherm model parameters
对吸附过程进行热力学分析,从表3可以看出:吉布斯自由能(ΔG)小于0,说明P(AA-AMSt)/Fe3O4@SiO2的吸附反应为自发反应[18]。

表3 P(AA-AM-St)/Fe3O4@SiO2吸附Pb2+的热力学参数Tab.3 Thermodynamic parameters of P(AA-AM-St)/Fe3O4@SiO2 to Pb2+
3 结论
a)采用AA,AM,St制备了P(AA-AM-St),再将Fe3O4@SiO2与P(AA-AM-St)复合制备了P(AAAM-St)/Fe3O4@SiO2。
b)P(AA-AM-St)/Fe3O4@SiO2的热稳定性好,平均孔径为3.4 nm,属于介孔材料。
c)P(AA-AM-St)/Fe3O4@SiO2对Pb2+,Cd2+,Cu2+,Ni2+具有较高吸附性,在这四种离子的竞争实验中,对Pb2+有较好的选择性,在pH值为5时对Pb2+的吸附量达484 mg/L。且具有优异的再生能力,10次吸附解吸附后对Pb2+的吸附量仍可达到418 mg/L。
d)P(AA-AM-St)/Fe3O4@SiO2对Pb2+的吸附过程主要为化学吸附,且分为表面吸附与孔道缓慢扩散两个过程。吸附反应为自发反应;吸附模型符合Langmuir模型,为单分子层吸附。
