核苷(酸)类似物停药后对慢性乙型肝炎患者预后的影响
2022-04-02陈尚军谢虎生蒋蒙张继通信作者
陈尚军 谢虎生 蒋蒙 张继(通信作者)
316000中国人民解放军东部战区海军医院感染科,浙江舟山
核苷(酸)类似物(NAs)用于抗乙型肝炎病毒(HBV)治疗已经成为学术界广泛共识,其主要是通过抑制HBV 逆转录和干扰脱氧核糖核酸(DNA)的合成发挥抗病毒作用。但NAs 不能有效地清除共价闭合环状DNA(cccDNA),所以接受NAs 治疗的慢性乙型肝炎(CHB)患者停药后往往会出现病毒学反弹和疾病复发[1]。寻找一种新的血清标志物,优化停药标准是临床医生所共同面临的问题。本研究回顾性分析了乙型肝炎病毒前基因组RNA(HBV pgRNA)对NAs治疗CHB患者停药后疾病转归的影响,现报告如下。
资料与方法
选取2015年6月-2019年6月在中国人民解放军东部战区海军医院感染科门诊及住院的初次接受NAs治疗达到停药标准的CHB 患者98 例,所有病例均符合《慢性乙型肝炎防治指南(2015年版)》[2]的诊断标准,且符合NAs 抗HBV 治疗指征。停药标准:乙型肝炎病毒e 抗原(HBeAg)阳性患者血清乙型肝炎病毒脱氧核糖核酸(HBV DNA)低于检测下限、丙氨酸氨基转移酶(ALT)复常,HBeAg 血清学转换后再巩固治疗至少1年,总疗程超过2年;HBeAg 阴性患者血清HBV DNA 低于检测下限、ALT 复常后再巩固治疗超过1.5年,总疗程超过2.5年。排除合并其他肝炎病毒和(或)合并人类免疫缺陷病毒(HIV)感染者及酗酒、药瘾者。所有病例既往均未接受过干扰素抗HBV治疗。
98例CHB患者中,男58例,女40例;年龄26~61 岁,平均(46.13±3.21)岁;病程6~17年,平均(11.06±5.12)年。HBeAg 阳性57 例(58.16%),HBeAg阴41 例(41.84%)。接受拉米夫定(LAM)治疗者13 例(13.27%)(LAM 组),接受阿德福韦酯(ADV)治疗21 例(21.43%)(ADV 组),接受恩替卡韦(ETV)治疗者64 例(65.31%)(ETV 组)。各组在性别、年龄及病程等方面比较差异无统计学意义(P>0.05),具有可比性。
检测方法:采用OLYMPUS(AU400)全自动生化分析仪测定ALT(正常值<40 IU/L);采用Roche公司提供的Cobas AmpliPrep/Cobas TapMan 平台(罗氏试剂,杭州艾迪康医学检验中心)(检测下限30IU/mL)检测HBV DNA(<30 IU/mL 为阴性);采用酶联免疫吸附测定法(ELISA)检测血清HBV 标志物(广州达瑞生物技术股份有限公司提供试剂)。采用美国Perkin Elmer 公司HBV pgRNA 核酸检测试剂盒(杭州艾迪康医学检验中心)(检测下限200 copies/mL)检测HBV pg RNA(<200 copies/mL为阴性)。
观察指标:观察患者用药后12 周、24 周、48 周的HBV DNA的转阳情况、ALT复发情况。
统计学方法:应用SPSS19.0 统计学软件对数据进行处理,计量资料用(±s)表示,比较采用t值;计数资料用百分比(%)表示,比较采用检验。P<0.05表示差异有统计学意义。
结果
各组HBV DNA 转阳和ALT 复发情况比较:98 例接受NAs 治疗达到停药标准的CHB 患者中,血清HBV DNA 转阳率和ALT 复发率随着停药时间的延长而增加,在停药48 周时HBV DNA 转阳53 例(54.08%,53/98)、ALT复发44例(44.90%,44/98)。LAM组、ADV组和ETV组患者在停药48周时血清HBV DNA转阳率、血清ALT 复发率比较,差异无统计学意义(P>0.05)。见表1。
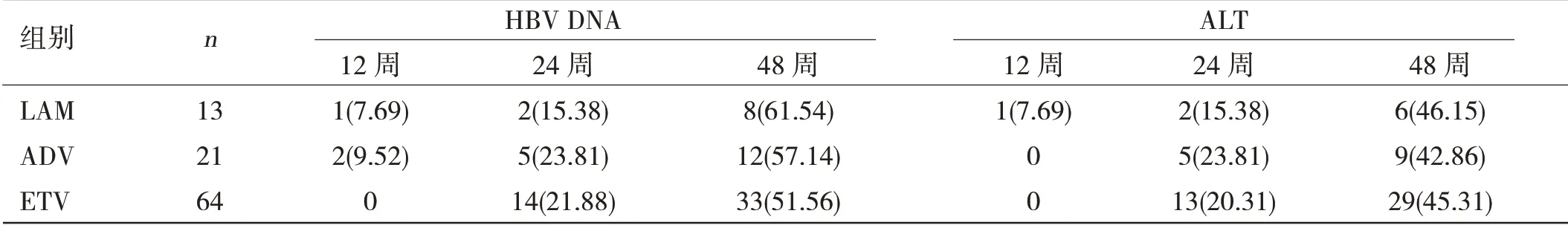
表1 各组患者停药后HBV DNA转阳发生率、ALT复发率比较[n(%)]
血清HBeAg 阳性和HBeAg 阴性患者HBV DNA 转阳和ALT 复发情况比较:98 例接受NAs 治疗达到停药标准的CHB 患者中,HBeAg 阳性与阴性患者停药48 周时血清HBV DNA 转阳率比较,差异无统计学意义(P>0.05)。HBeAg阳性与阴性患者停药48周时ALT复发率比较差异无统计学意义(P>0.05)。见表2。
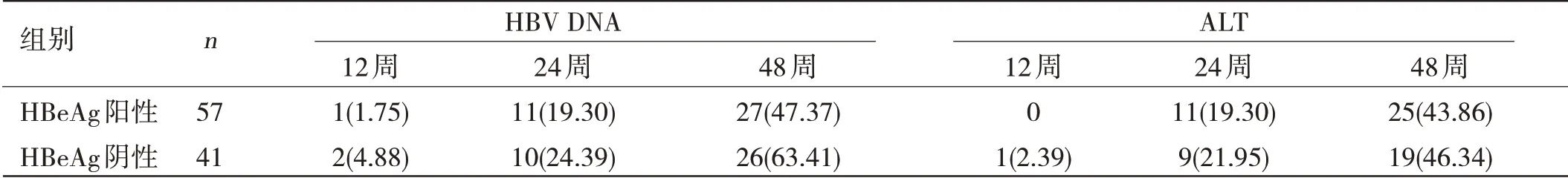
表2 血清HBeAg阳性/HBeAg阴性患者停药后HBV DNA转阳发生率、ALT复发率比较[n(%)]
停药时HBV pgRNA 阳性和HBV pgRNA 阴性患者HBV DNA 转阳情况比较:在98 例CHB 患者中,HBV pgRNA 阳性37 例(37.76%,37/98),HBV pgRNA 阴性61 例(62.24%,61/98)。在停药48 周时,HBV pgRNA阳性和HBV pgRNA阴性患者HBV DNA转阳发生率比较,差异有统计学意义(P<0.01)。见表3。
讨论
CHB 需要长期抗HBV 治疗,这一点在学术界已经达成广泛共识,实现临床治愈、追求停药是临床医生和患者的共同愿望[3]。在停止NAs 治疗后,CHB 患者都存在不同程度的病情复发。临床实践表明,即使按照现行的国内和国外的CHB 管理指南或共识的建议实行临床停药,仍有较高的复发率。NAs 抗HBV治疗理想的停药终点是HBsAg 消失伴(或)不伴血清学转换,HBsAg 既可以由HBVcccDNA 转录表达,也可以由HBV 整合转录表达。通过数学模式推算,患者经过NAs 长期抗HBV 治疗,血清HBsAg 消失可能需要36~52年。所以寻求一个能够预测治疗后疾病复发,且能够便于检测的血清标志物就非常重要。从理论上而言,血清HBV pgRNA 与HBsAg 是不同的检测指标,血清HBV pgRNA 由被感染的肝细胞核内的cccDNA 转录产生,能够很好地反映肝细胞内的cccDNA 的活性,其一定程度上也能够反映HBV 的复制状态[4]。
欧洲肝脏学会《慢性乙型肝炎病毒感染管理临床实践指南(2017 版)》[5]已经将HBV pgRNA 作为一种新的生物学血清标志物。理论上讲,可将血清HBV pgRNA 作为指导NAs 停药的一个新的指标,但其安全性和是否优于血清HBsAg的检测,仍缺少大样本的临床研究数据。如何实现更加安全的停药,减少停药后的复发,则需要通过更多的探索来优化现有的停药标准,从理想和现实标准中做出符合临床实际的选择[6]。
