高效液相色谱法测定蛋白粉中维生素E含量的不确定度评定
2022-04-01薛红玮罗伟敏沈棚
薛红玮 罗伟敏 沈棚



摘 要:为评定高效液相色谱法测定蛋白粉中维生素E含量结果的不确定度,本文按照《食品安全国家标准 食品中维生素A、D、E的测定》(GB 5009.82—2016)测定功能型蛋白粉中维生素E的含量,从标准溶液配制、试样的处理过程、测量重复性等方面分析和量化各不确定度分量,并计算合成标准不确定度和扩展不确定度。结果表明,该功能型蛋白粉中维生素E含量为8.22 mg/100 g,扩展不确定度为0.22 mg/100 g,其中k=2,P=95%。结果表述为(8.22±0.22)mg/100 g。
关键词:不确定度;维生素E;功能型蛋白粉;高效液相色谱
Evaluation of Uncertainty in the Determination of Vitamin E in Protein Powder by High Performance Liquid Chromatography
XUE Hongwei1, LUO Weimin2, SHEN Peng3
(1.Shanghai Yingjia Biotechnology Co., Ltd., Shanghai 201703, China; 2.Inkea Health Technology (Guangdong) Co., Ltd., Dongguan 523808, China; 3.Shanghai Kangnuo Zhixin Food Co., Ltd., Shanghai 201703, China)
Abstract: In order to evaluate the uncertainty of the results of the determination of vitamin E content in protein powder by HPLC, the content of vitamin E in functional protein powder was determined according to GB 5009.82—2016, the uncertainty components were analyzed and quantified from the aspects of standard solution preparation, sample treatment process and measurement repeatability, and the synthetic standard uncertainty and expanded uncertainty were calculated. Results show that the content of vitamin E in the functional protein powder was
8.22 mg/100 g, and the expanded uncertainty was 0.22 mg/100 g, where k=2, P=95%. The result was expressed as (8.22±0.22) mg/100 g.
Keywords: uncertainty; vitamin E; functional protein powder; high performance liquid chromatography
本試验选用的功能型蛋白粉是一种具有增强免疫力作用的保健食品,主要在原有蛋白质组分的基础上增加了维生素、膳食纤维等功能型原料,以提升蛋白粉的综合功效。功能型蛋白粉的主要成分为蛋白质,特别添加了维生素E。蛋白质是构成和修复组织的主要原料,身体的生长发育、衰老组织的更新、疾病和造成创伤后组织细胞的修复,都离不开蛋白质[1]。因此,人体需每天摄入一定量的蛋白质作为构成和修复组织的最重要的材料[2]。维生素E是主要的脂溶性抗氧化物,可阻止大分子发生氧自由基损伤,从而避免很多癌症的发生;维生素E可阻止氧化低密度脂蛋白的形成,从而防止动脉粥样硬化和心血管疾病的发生[3];维生素E还可清除脑组织等细胞的脂褐质并改善皮肤弹性,改善记忆力。将维生素E添加到蛋白粉中,可提高蛋白粉增强免疫力的功效。维生素E作为功能型蛋白粉的主要功效成分,其有效成分的含量对产品质量的评定非常重要[4]。
测量不确定度是与测量结果相关联的参数,表征了可以合理地赋予被测量的量值分散程度[5]。通常由实验室测试得到的单个检测结果并不能代表样品中目标物质的真实含量,需用测量不确定度评估真值分布的范围。为准确地表达出样品中目标物质的含量,本试验通过分析测试过程,找出各不确定度分量,建立一套合理、完整的评定方案,得到更精确的表达测定结果[6-10]。
1 材料与方法
1.1 材料与试剂
功能型蛋白粉,营家健康科技(广东)有限公司;无水乙醇(分析纯);抗坏血酸(分析纯);氢氧化钾(分析纯);石油醚(分析纯);无水硫酸钠(分析纯);甲醇(色谱纯);2,6-二叔丁基对甲酚(分析纯);维生素E标准品(α-生育酚,纯度99.5%)。
1.2 仪器与设备
Agilent 1260高效液相色谱仪(配紫外检测器,安捷伦科技);752G型紫外可见分光光度计(上海仪电分析设备有限公司);AUW 120D分析天平[岛津(中国)有限公司];JA1004电子天平(上海浦春计量仪器有限公司);SHA-B恒温水浴振荡器(上海力辰邦西仪器科技有限公司);LC-RE-201D旋转蒸发仪(上海力辰邦西仪器科技有限公司)。
1.3 试验方法
1.3.1 样品制备
(1)皂化。称取2 g(精确至0.01 g)蛋白粉试样于250 mL具塞三角瓶中,加入20 mL温水,再加入1.0 g抗坏血酸和0.1 g BHT(2,6-二叔丁基对甲酚),加入30 mL无水乙醇,加入10 mL氢氧化钾溶液(50%),边加边振摇,混匀后80 ℃恒温水浴振荡皂化30 min,皂化后立即用冷水冷却至室温。
(2)提取。将皂化液用30 mL水转入250 mL分液漏斗中,加入50 mL石油醚,振荡萃取5 min,将下层转移至另一个250 mL分液漏斗中,加入50 mL石油醚再次萃取,合并醚层。
(3)洗涤。用约100 mL水洗涤醚层,约重复3次,直至将醚层洗至中性(用pH试纸检测下层溶液pH值),去除下层水相。
(4)浓缩。将洗涤后的醚层转移至250 mL圆底烧瓶中,减压浓缩至近干,用甲醇分次将蒸发瓶中残留物转移至10 mL容量瓶中,定容至刻度。溶液过0.22 μm有机系滤膜后供液相色谱测定。
1.3.2 标准溶液配制
(1)标准储备溶液。准确称取维生素E标准品(α-生育酚)50.0 mg,用无水乙醇溶解后,转移至50 mL容量瓶,定容至刻度,溶液的浓度约为1.00 mg/mL,制得标准储备溶液。将溶液转移至棕色试剂瓶中,密封后,在-20 ℃下避光保存,有效期6个月。临用前将溶液回温至20 ℃,并进行浓度校正。浓度校正方法为取维生素E(α-生育酚)标准储备溶液500 μL于10 mL棕色容量瓶中,用无水乙醇定容至刻度,混匀,分别用1 cm石英比色皿,以无水乙醇为空白参比,在292 nm处测定吸光度值。
(2)标准中间溶液。准确吸取维生素E(α-生育酚)标准储备溶液5.00 mL于50 mL容量瓶中,用甲醇定容至刻度,得到100 μg/mL的标准中间溶液。在-20 ℃下避光保存,有效期半个月。
(3)标准系列工作液。准确吸取维生素E(α-生育酚)标准中间溶液0.50 mL、1.00 mL、2.00 mL、4.00 mL和6.00 mL于10 mL棕色容量瓶中,用甲醇定容至刻度,得到标准系列工作液,其中维生素E(α-生育酚)的浓度分别为5.0 μg/mL、10.0 μg/mL、20.0 μg/mL、40.0 μg/mL和60.0 μg/mL,現用现配。
1.3.3 液相色谱仪器条件
色谱柱:Agilent C18柱(150 mm×4.6 mm,5 μm);
柱温:25 ℃;流动相:100%甲醇;流速:
0.8 mL/min;检测波长为:294 nm;进样量:10 μL。
1.3.4 建立数学模型
试样中的维生素E(α-生育酚)的含量计算公式如下:
(1)
式中:X为试样中维生素E的含量,mg/100 g;c为根据标准曲线计算得到的试样中维生素E的浓度,μg/mL;V为定容体积,mL;f为换算因子,为0.001;100为试样中的量以100 g计算的换算系数;m为试样的称样量,g。
1.3.5 不确定度来源分析
参照试验方法及数学模型,影响检测结果的不确定度来源主要有测量重复性、标准溶液配制过程、样品称量、试样定容及加标回收率等。
2 结果与分析
2.1 不确定度分量的评定
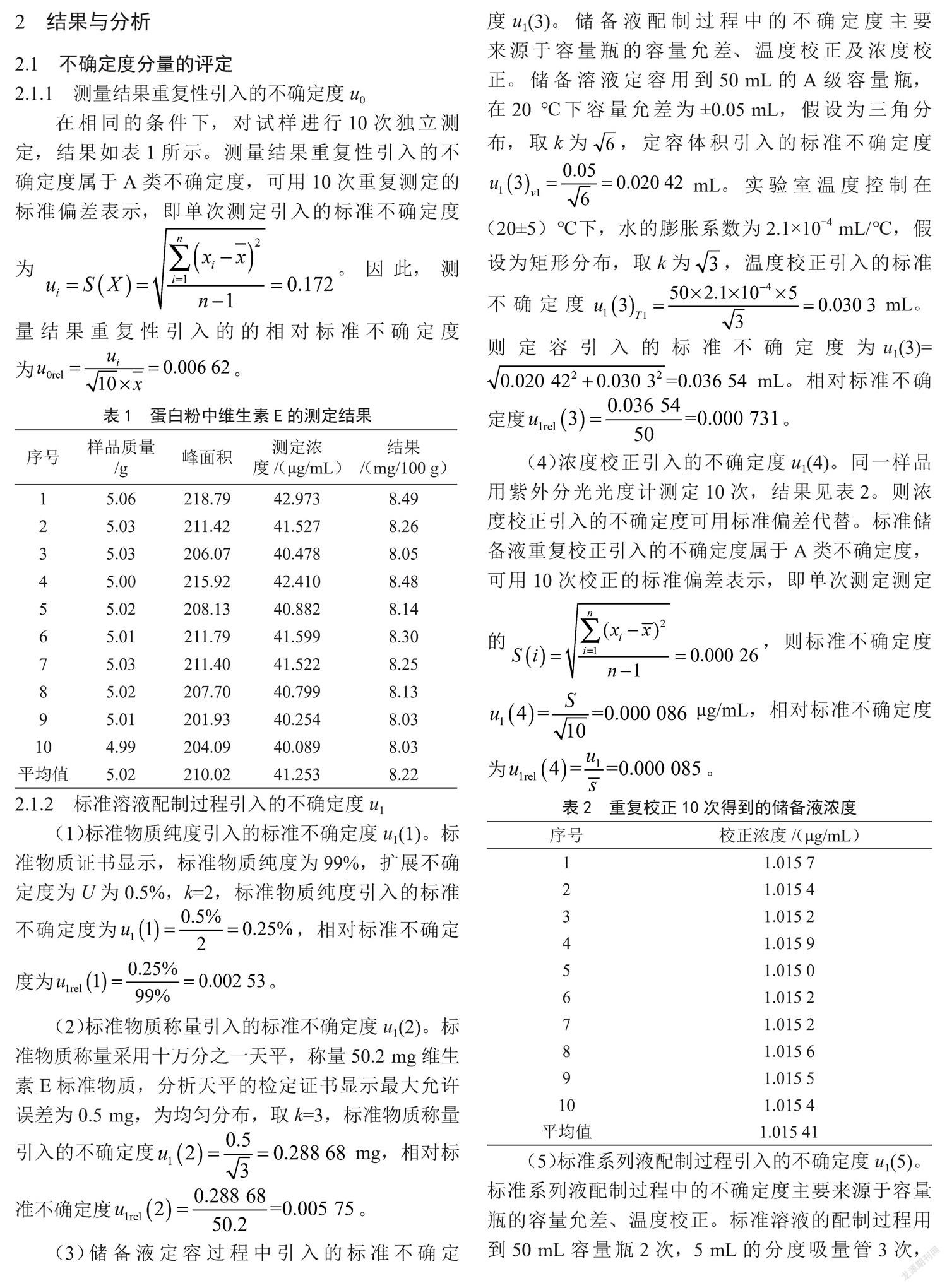
2.1.1 测量结果重复性引入的不确定度u0
在相同的条件下,对试样进行10次独立测定,结果如表1所示。测量结果重复性引入的不确定度属于A类不确定度,可用10次重复测定的标准偏差表示,即单次测定引入的标准不确定度为。因此,测量结果重复性引入的的相对标准不确定度为。
2.1.2 标准溶液配制过程引入的不确定度u1
(1)标准物质纯度引入的标准不确定度u1(1)。标准物质证书显示,标准物质纯度为99%,扩展不确定度为U为0.5%,k=2,标准物质纯度引入的标准不确定度为,相对标准不确定度为。
(2)标准物质称量引入的标准不确定度u1(2)。标准物质称量采用十万分之一天平,称量50.2 mg维生素E标准物质,分析天平的检定证书显示最大允许误差为0.5 mg,为均匀分布,取k=3,标准物质称量引入的不确定度 mg,相对标准不确定度。
(3)储备液定容过程中引入的标准不确定度u1(3)。储备液配制过程中的不确定度主要来源于容量瓶的容量允差、温度校正及浓度校正。储备溶液定容用到50 mL的A级容量瓶,在20 ℃下容量允差为±0.05 mL,假设为三角分布,取k为,定容体积引入的标准不确定度 mL。实验室温度控制在(20±5)℃下,水的膨胀系数为2.1×10-4 mL/℃,假设为矩形分布,取k为,温度校正引入的标准不确定度 mL。
则定容引入的标准不确定度为u1(3)= mL。相对标准不确定度。
(4)浓度校正引入的不确定度u1(4)。同一样品用紫外分光光度计测定10次,结果见表2。则浓度校正引入的不确定度可用标准偏差代替。标准储备液重复校正引入的不确定度属于A类不确定度,可用10次校正的标准偏差表示,即单次测定测定的,则标准不确定度 μg/mL,相对标准不确定度为。
(5)标准系列液配制过程引入的不确定度u1(5)。标准系列液配制过程中的不确定度主要来源于容量瓶的容量允差、温度校正。标准溶液的配制过程用到50 mL容量瓶2次,5 mL的分度吸量管3次,10 mL容量瓶7次,0.5 mL、1.0 mL、2.0 mL和10.0 mL的分度吸量管各1次。《玻璃量器检定规程》(JJG 196—2006)中在温度为20 ℃下不同规格的玻璃量器容量允差及包含因子见表3。假设为三角分布,取k为,体积引入的标准不确定度,计算得到的各相对标准不确定度如表3所示。容量工具引入的合成相对标准不确定度为:
实验室的温度控制在(20±5)℃,水的膨胀系数为2.1×10-4 mL/℃,假设为矩形分布,取k为,使用以上容量工具由温度校正引入的相对标准不确定度,标准系列液配制过程引入的相对标准不确定度u1rel(5)=
。
因此,标准物质引入的相对合成标准不确定度u1rel=
2.1.3 样品称量引入的不确定度u2
用百分之一天平分别称量5.00 g和5.03 g两个平行样,天平的检定证书给出的最大允许误差为0.05 g,属于均匀分布,取k=,样品称量引入的标准不确定度 g,平均称样量 g,则样品称量引入的相对标准不确定度为。
2.1.4 试样定容引入的不确定度u3
样品经皂化、提取、洗涤和浓縮后转移至10 mL容量瓶中,并用甲醇定容至刻度,此过程的不确定度主要由容量瓶的容量允差、温度校正引入。定容用到的10 mL容量瓶为A级,在20 ℃下校正得到的容量允差为±0.02 mL,假设为三角分布,取k=,则 mL,实验室温度控制在(20±5)℃下,有机溶剂的膨胀系数为1.0×10-4 mL/℃,假设为矩形分布,取k为,温度校正引入的标准不确定度 mL。因此,试样定容引入的不确定度为u3=0.00867 mL,相对标准不确定度为u3rel=
。
2.1.5 样品前处理加标回收率引入的不确定度u4
样品的前处理过程烦琐,包含试样制备、皂化、提取、洗涤和浓缩,不确定度难以评定,可通过加标回收试验进行评定,本试验对同一样品进行6次独立的加标回收率测试,试验结果见表4,样品加标回收率的相对标准不确定度。
2.2 合成不确定度的计算
综上所述,高效液相色谱法测定功能型蛋白粉中的维生素E含量的相对标准不确定度由测量重复性不确定度、标准溶液引入的不确定度、样品称量引入的不确定度、样品定容和样品的前处理过程引入的不确定度5个主要不确定度分量组成。合成相对标准不确定度:
蛋白粉中维生素E的平均含量为8.22 mg/100 g,因此合成标准不确定度为u=8.22×0.013 2=0.109 mg/100 g。
2.3 扩展不确定度
本试验的测量结果符合正态分布,取置信概率P=95%,置信因子k=2,则扩展不确定度为U=u×k=0.109×2≈0.22 mg/100 g,蛋白粉中维生素E结果表述为(8.22±0.22) mg/100 g,k=2。
3 结语
本文对高效液相色谱法测定功能型蛋白粉中维生素E含量的不确定度进行了分析评定,研究表明影响检测结果不确定度的因素主要包括测量重复性、标准溶液的配制过程、样品称量、样品定容和前处理过程。其中,标准溶液的配制过程对结果的不确定度影响最大。因此,在测定过程中应选用证书齐全的标准物质,配制过程中使用的器皿应经过检定校准,严格遵守标准溶液配制操作规程,减少测定过程的不确定度,提高检测的准确度。
参考文献
[1]田呈瑞,姚晓玲.现代饮食营养与健康[M].北京:中国计量出版社,2006.
[2]凌育昕.食品中蛋白质的不确定度评定[J].中国食品工业,2021(24):90-92.
[3]凌关庭.保健食品原料手册[M].2版.北京:化学工业出版社,2006.
[4]廖安.复合蛋白粉功能特性的研究[D].湖南农业大学,2013.
[5]中国合格评定国家认可委员会.化学分析中不确定度的评估指南:CNAS—GL006:2019[EB/OL].(2019-04-09)[2022-01-05].https://www.cnas.org.cn/rkgf/sysrk/rkzn/2019/04/896487.shtml.
[6]赵霞,曹改萍,王敏,等.高效液相色谱法测定大豆维生素E方法的优化[J].陕西农业科学,2020,48(4):520-526.
[7]卢慧芳,王文霞,张耀广,等.高效液相色谱法测定灭菌乳中糠氨酸的不确定度评定[J].食品安全质量检测学报,2021,12(2):569-575.
[8]高小春,施小明,许家琦,等.高效液相色谱法测定填充祛斑凝胶中维生素E含量的不确定度评定[J].中国药物经济学,2020,15(9):44-48.
[9]魏帅,吕宁,梁成珠,等.婴幼儿配方乳粉中维生素A、E检测方法的比较研究[J].食品安全质量检测学报,2020,11(24):9083-9092.
[10]罗功才,曾佳艳,雷课,等.一测多评纽斯葆牌多种维生素矿物质片中维生素D3和维生素E的含量[J].现代食品,2020(3):180-184.
