梅毒螺旋体黏附素蛋白TP0136不同亚型重组蛋白在神经梅毒患者血清诊断中的应用
2022-03-31柯吴坚冷欣颖刘雅慧陈嵘祎陈征宇张晓辉王柳苑廖玉英梁春梅陈慧茹龙海莹吴育娇杨立刚杨斌
柯吴坚, 冷欣颖, 刘雅慧, 陈嵘祎, 陈征宇, 张晓辉, 王柳苑, 廖玉英, 梁春梅, 陈慧茹, 龙海莹, 吴育娇, 杨立刚, 杨斌
南方医科大学皮肤病医院,广东 广州 510091
神经梅毒(neurosyphilis, NS)是由梅毒螺旋体(Treponemapallidum, Tp)侵入宿主中枢神经系统所致的一组临床综合征[1-3]。NS在一般人群中的发病率为0.47/10万~2.1/10万,而在梅毒患者中的患病率是一般人群的857~3 830倍[4-6]。NS确诊往往需要行腰椎穿刺术[7-9],该方法不仅有创,且手术成本远高于抽血检测费用。因此是否可以通过血液学检测用于NS诊断,从而减少甚至避免患者接受腰椎穿刺术成为临床研究热点。研究发现:Tp通过多种黏附蛋白(如TP0136)黏附宿主细胞外基质;TP0136蛋白根据是否含有TprK供体区的不同,分为含TprK供体区的Nichols Seattle亚型和不含TprK供体区的Nichols Houston亚型;不同亚型的TP0136在黏附宿主细胞外基质作用中存在差异;不同亚型TP0136在兔皮损中的转录水平和诱导宿主产生的抗体水平存在显著差异[10-16]。结合前期研究成果,本研究分别选用两个具有代表性的TP0136亚型Nichols Seattle TP0136(NST)和Nichols Houston TP0136(NHT)作为研究对象,通过建立NS临床队列,评估两种亚型的TP0136在NS血液中的诊断价值,以期发现潜在的NS血液学诊断标志物,从而实现降低NS患者腰穿率的目的。
1 对象与方法
1.1 研究对象
选取2016年1月—2021年12月南方医科大学皮肤病医院生物样本库中收集的门诊和住院部NS和非神经梅毒的梅毒患者(NNS)血清或血浆样本180例,其中NS血清或血浆样本60例、NNS血清或血浆样本120例。NS和NNS定义参考我国、美国和欧洲梅毒指南[7-9,17]。所有临床实验均经南方医科大学皮肤病医院临床管理及使用委员会批准(GDDHLS-20171004),并参照临床试验管理和使用指南进行操作。
1.2 方法
1.2.1 两种不同亚型TP0136序列分析和引物设计 序列分析和引物设计具体方法[14]如下:应用引物设计软件:Primer 3:WWW primer tool(http://biotools.umassmed.edu/bioapps/primer3_www.cgi)对GenBank查询的NST和NHT的开放阅读框架(open reading frame,ORF)全长分别进行引物设计。用SignalP4.1 Server软件(http://www.cbs. dtu.dk/services/SignalP/)预测NST和NHT信号肽,将NST和NHT ORF引物设计成不含信号肽引物。用Restriction Mapper(http://www.restric-tionmapper.org/)和NEBcutter V2.0. (http://tools.neb.com/NEBcutter2/)预判待扩增的DNA序列不被HindⅢ限制性内切酶酶切。NST、NHT正向引物:5′-ATGACGTGCGATTTCACTGG-3′;NST反向引物:5′-ACTACGTAGATTTTCTGCAC-3′;NHT反向引物:5′-CTCGCGGTTCCAGGAGCACG-3′。NST和NHT的PCR扩增产物大小分别为1 260 bp和1 389 bp。
1.2.2 NST和NHT ORF扩增和鉴定 常规PCR法扩增南方医科大学皮肤病医院生物样本库中经兔睾丸传代培养[16]获得的NST和NHT ORF DNA。50 μL PCR扩增反应试剂含:5 μL待检测DNA样本、200 μM dNTPs、5 μL 10 ×Go Taq PCR缓冲液(Promega)、1.5 mM MgCl2、0.6 μM NST或NHT引物、0.5 U热启动Taq PCR聚合酶(Promega)。扩增条件:95 ℃变性10 min;95 ℃ 1 min、60 ℃ 2 min、72 ℃ 1 min,共45个循环;最后72 ℃延伸10 min。扩增PCR产物经1.5%琼脂糖凝胶电泳鉴定。成功扩增的NST和NHT ORF PCR扩增产物经双向DNA测序法(上海生工)进行测序验证。测序结果用BIOEDIT软件(http://www.mbio.ncsu.edu/bioedit/bioedit.html)与GenBank中的TP0136氨基酸和核苷酸序列进行比对分析。
1.2.3 NST和NHT ORF pEXP-5-CT表达载体的构建 成功扩增并经测序鉴定合格的NST和NHT ORF PCR扩增产物克隆至pEXP-5-CT的表达载体(Invitrogen),将重组质粒转化到TOP10感受态细胞(Invitrogen)。挑选10个菌落,用常规PCR法(同步骤2)验证转化子。取转化正确的转化子摇菌过夜,Plasmid Mini试剂盒(Qiagen)提取质粒。双向DNA测序法(同步骤2)对质粒进行测序验证。
1.2.4 NST和NHT ORF重组蛋白的表达和纯化 将经测序验证正确的NST和NHT 全长ORF pEXP-5-CT表达载体转化到感受态大肠杆菌Rosetta细胞(MerckKGaA)。取转化正确的转化子摇菌过夜。用SDS-PAGE和含6×His标签的Western Blot检测表达蛋白。将不可溶性蛋白NST和NHT分别经超声波处理器GEX130(Cole-Parmer)对重悬沉淀进行超声处理。超声处理后,离心去上清,加 6 M盐酸胍进行重悬。在4 ℃磁力搅拌器上孵育过夜。用Sorvall RC-5B冷冻超高速离心机(Thermo Scientific)离心回收上清液。上清液经含Ni-NTA琼脂糖(Qiagen)的亲和层析柱(Bio-Rad)纯化。将SDS-PAGE验证最纯净的不含污染物洗脱液置于透析盒(Thermo Scientific)透析。透析液为含有逐渐减小浓度的盐酸胍(从3、1.5、1、0.5到0 M)的1×PBS缓冲液。通过离心分离将透析后再次重折叠的可溶性蛋白从沉淀中分离出。NST和NHT ORF重组蛋白经BCA定量测定后储存于-80 ℃。
1.2.5 NS和NNS患者NST和NHT抗体测定 采用ELISA法检测:96孔酶标板分别经NST和NHT重组蛋白包被后,用3%脱脂牛奶封闭。每孔分别加入NS或NNS患者血清或血浆,每个样本重复检测3次。阴性对照为非梅毒感染患者血清,阳性对照为梅毒感染者血清。4 ℃孵育后PBST洗板。每孔加羊抗人IgG碱性磷酸酶结合物二抗(Sigma),室温孵育后PBST洗板。加入显影缓冲液pNPP(Sigma)后,酶标仪MAX250(Molecular Devices)405 nm读板。

2 结果
2.1 NS和NNS患者一般情况比较
由表1可见,60例NS患者与120例NNS患者两组之间年龄、性别、来源地、职业均无统计学差异(均P>0.05);而婚姻状况、神经系统症状、血清或血浆TRUST和TPPA 滴度、血清或血浆TP-IgM阳性率、脑脊液TRUST和TPPA 滴度均有统计学差异(均P<0.05)。
2.2 NST和NHT重组蛋白在NS、NNS患者血清或血浆中TP0136抗体水平比较
NST和NHT ORF重组蛋白经Western Blot检测,分别在46 100 Da和51 700 Da可见NST和NHT全长ORF蛋白。应用ELISA法检测两组重组蛋白在NS和NNS患者血清或血浆的TP0136抗体水平,经独立样本t检验分析(表2),NST在NS组和NNS组抗体水平无统计学差异(t=0.15,P=0.920);NHT在NNS组抗体水平高于NS患者,差异有统计学意义(t=3.68,P=0.021)。

表1 NS和NNS的人口统计学和临床特征Table 1 Demographic and clinical characteristics of the patients with neurosyphilis and non-neurosyphilis
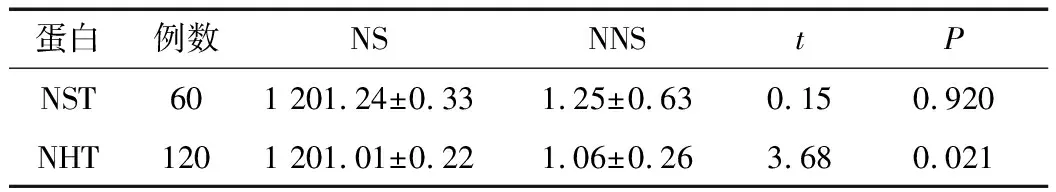
表2 NST和NHT重组蛋白在NS、NNS患者血清或 血浆中TP0136抗体水平比较 (mean±SD)Table 2 Comparison of TP0136 antibody levels of NST and NHT recombinant proteins in the serum or plasma of patients with neurosyphilis and non-neurosyphilis (mean±SD)
3 讨论
TP0136蛋白可与血浆纤连蛋白结合[18-19],还可黏附细胞纤连蛋白,其中TP0136 NH2端作为保守区,是重要的黏附作用区;而在可变的COOH端,Nichols Dallas株和Nichols Seattle株的TP0136氨基酸序列存在TprK插入区[12]。该插入区含可变区V3、V6和V7,在Tp免疫逃逸中发挥重要作用[20],从而提示不同亚型TP0136异质性在Tp免疫逃逸甚至最终形成慢性持续性感染中具有重要作用。因此,本研究选用具有代表性的NST和NHT作为研究对象,经表达纯化后发现,由于NST存在TprK插入区,进而引起阅读框移位和基因编码提前终止,因此其碱基数为1 260 bp,少于不含TprK插入区NHT的1 389 bp。NST ORF最终表达和纯化获得的分子量为46 100 Da,低于NHT的51 700 Da。
为了明确TP0136是否具有免疫原性和免疫反应性,有研究用重组蛋白TP0136对新西兰白兔进行皮下免疫,结果发现TP0136免疫后可产生高滴度抗体[19]。然而不同亚型的TP0136蛋白诱导宿主产生的特异性抗体是否存在差异以及其差异在临床诊断中是否具有不同影响目前仍然未知。本研究首先建立NS研究队列,发现在NS和NNS两组患者的一般信息中,除了婚姻状况存在差异(NS已婚组高于NNS,P<0.05),年龄、性别、来源地和职业等信息均无统计学差异(P>0.05);而两组患者的梅毒或NS相关指标,如有无神经系统症状、血清或血浆TRUST和TPPA 滴度水平、血清或血浆TP-IgM阳性率、脑脊液TRUST和TPPA 滴度水平在NS组均高于NNS组,差异有统计学意义(均P<0.05)。本研究结果与既往以有研究结果[21-23]一致,提示神经系统症状、血液或脑脊液的高TRUST和TPPA 滴度水平、血液TP-IgM阳性等指标都可能是NS的风险因素。
为了探讨TprK供体区在TP0136基因异质性中是否具有临床诊断价值,本研究采用ELISA法检测发现,含有TprK供体区的NST在NS组和NNS组血清或血浆中抗体水平无差异;而不含TprK供体区的NHT在NNS组血清或血浆中抗体水平高于NS患者,差异有统计学意义(P<0.05)。由于目前NS缺乏理想的血清学诊断标志物,比较NS与NNS患者血液中梅毒抗体水平,发现梅毒血清学中TPPA≥1∶10 240可以用于预测NS[24]。然而另一项研究却提示血液中TPPA在识别脑脊液异常的敏感性仅为17.1%~22.2%[25]。以上结果提示,Tp特异性抗体可能具有NS诊断的潜质。但其诊断敏感性不高,或许由于TPPA选用的抗原为Tp的超声裂解物,包含大量Tp蛋白。在早期和晚期梅毒患者中,TP0136抗体水平存在显著差异;进一步采用早期梅毒兔模型证实,与其他Tp黏附蛋白不同,TP0136转录水平分别在一期硬下疳和二期梅毒疹出现前两次高表达[12-16]。以上结果提示TP0136在Tp感染和播散中具有作用。根据是否含有TprK供体区可对TP0136进行分型[15]。Tantalo等[26]通过采用不同Tp菌株感染新西兰白兔,证实不同Tp菌株的神经侵袭性存在差异。本次NS临床队列研究结果也进一步证实该假说,表明不同亚型TP0136蛋白的Tp在神经系统侵袭性方面存在差异,最终可能导致疾病病程或转归的不同,其中不具有TprK供体区TP0136蛋白的Tp可能存在高神经侵袭性作用,因此其诱导产生的特异性血液学抗体或可作为NS诊断的血液学标志物。
综上所述,本研究通过建立NS队列,评估NS患者中Tp黏附素蛋白TP0136的NST和NHT亚型抗体水平,初步发现NHT或可作为潜在NS诊断的血液学标志物,为后续减少NS患者腰穿率或避免腰穿提供血液学检测研究基础,也为进一步研究不同TP0136亚型的神经侵袭性提供临床理论基础。
