地西他滨联合预激方案治疗中高危骨髓增生异常综合征的疗效
2022-03-31张芳芳
张芳芳
平顶山市第一人民医院血液内科 (河南 平顶山 467000)
中高危骨髓增生异常综合征(myelodysplastic syndrome,MDS)是由于患者血细胞发育异常,高风险向急性髓系白血病转化的高度异质性恶性血液疾病[1],地西他滨(decitabine,DAC)联合预激方案是MDS常见的治疗方法。5-氮杂-2′脱氧胞苷(DAC)是一种去甲基化药物,能够激活失活的抑癌基因,从而逆转DNA甲基化过程[2];CAG是其中一种预激方案,主要通过药物阿糖胞苷(cytosine arabinoside,Ara-C)、阿克拉霉素(aclacinomycin,ACLA )、重组人粒细胞刺激因子注射液(granulocyte colony-stimulating factor injection,G-CSF)共同作用对患者进行化疗以杀伤G0期细胞,控制病情,然而单独使用的预后效果较差[3]。本研究对34例MDS患者行DAC联合CAG预激方案治疗,观察其疗效,以期为MDS的临床治疗提供参考。
1 资料与方法
1.1 一般资料选取2017年1月至2019年2月在本院接受治疗的MDS患者66例,采用随机数表法分为观察组和对照组,分别有患者34例、32例。观察组:11例男性患者,23例女性患者;年龄22~80岁,平均年龄(55.64±6.81)岁;病程0.5~4.2年,平均病程(2.74±0.90)年。对照组:11例男性患者,21例女性患者;年龄22~80岁,平均年龄(56.80±6.90)岁;病程0.1~4.0年,平均病程(2.81±0.86)年。上述两组患者的性别、年龄、差异均无统计学意义(P>0.05),本研究经伦理委员会允许。
纳入标准:经诊断,患者实属MDS;患者在此次研究前并未接受过其他治疗;对本次研究所使用的药物不具有抗药性;患者意识清晰,能进行正常交流;患者自愿参与此次研究,并签署知情同意书。排除标准:患者合并有重型感染症状;患者存在重要器官衰竭症;患者患有严重凝血疾病、神经系统或免疫系统的疾病;中途退出研究,或是不能完全配合治疗者。
1.2 方法两组患者在治疗的同时,均需进行抗感染治疗,注意患者生命体征的变化,如体温、血常规、肝肾等脏器的功能,必要时需进行成分输血以及肝、心功能支持治疗。
对照组:采用预激方案单独治疗(此处使用的是CAG方案)。对患者进行皮下静脉注射10mq/m2注射用阿糖胞苷(Ara-C)(生产厂家:Pfizer Italia s.r.l.;生产批号:H20160403;规格:0.1g),每隔12h注射一次,连续14d;12mg/m2注射用不一致(生产厂家:扬州制药有限公司;生产批号:H10920075;规格:20mg),每天一次,连续6~9d;静脉注射200μg/m2欣粒生(G-CSF)[生产厂家:北京四环生物制药有限公司;生产批号:S20020052;规格:300μg/0.9mL/支(预充式注射器)],每天一次,若在治疗过程中患者的白细胞浓度超过20×109个/L,需立即停止用药,若患者完全缓解,则继续使用。一个治疗周期为28d,总共进行2个周期。
观察组:患者采用DAC联合CAG预激方案治疗。预激方案的治疗方法同对照组,另对患者进行MDS药物治疗:静脉注射20mg/m2注射用地西他滨(DAC)(生产厂家:江苏奥赛康药业有限公司;生产批号:H20133080;规格:50mg),每天一次,时间维持在1h左右,连续5d,一个化疗周期为28d,同样进行两个周期。
1.3 观察指标(1)参照IWG疗效标准[4]对两组患者的治疗疗效进行评定。记录患者完全缓解、骨髓完全缓解、部分缓解、未缓解的患者例数,记完全缓解、骨髓完全缓解例数之和为总有效率。(2)治疗前后,抽取患者外周静脉血5mL,利用离心机进行离心(转速:3000r/min)10min,取上层清液,再利用全自动生化检测仪检测患者血清中铁蛋白、维生素B2、叶酸浓度。(3)对患者进行跟踪性调查随访(随访时间为从患者确诊直至患者死亡或截止2020年7月),记录患者的死亡和中位生存期。
1.4 统计学分析采用SPSS 20.0软件处理数据。计数资料以n(%)表示,行χ2检验;计量资料以(±s)表示,两组间行独立t检验,治疗前后行配对t检验。检验水准为α=0.05。
2 结 果
2.1 两组患者治疗效果的比较观察组治疗总有效率为62.50%,高于对照组(34.38%,P<0.05),见表1。
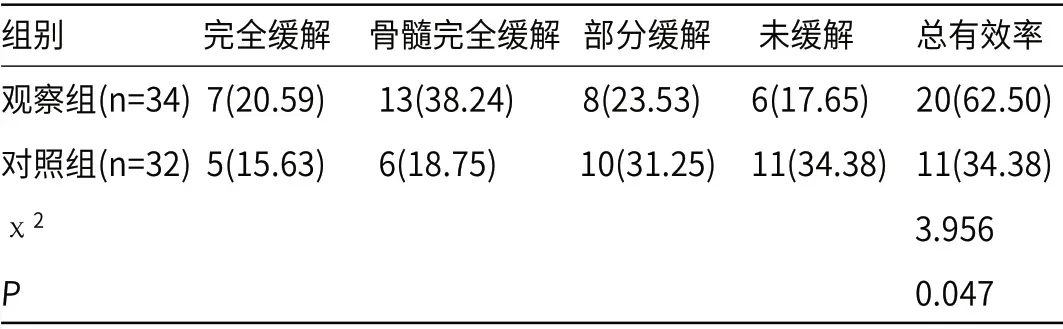
表1 两组患者治疗效果的比较[n(%)]
2.2 两组患者血清铁蛋白、维生素B2、叶酸浓度的比较治疗前,两组患者的铁蛋白、维生素B2、叶酸浓度均无差异(P>0.05);治疗后,两组上述参数均降低(P<0.05);且观察组治疗后的上述参数评分均低于对照组(P<0.05),见表2。

表2 两组患者血清铁蛋白、维生素B2、叶酸浓度的比较
2.3 两组患者生存情况的比较观察组的死亡率低于对照组(P<0.05),中位生存期长于对照组(P<0.05),见表3。
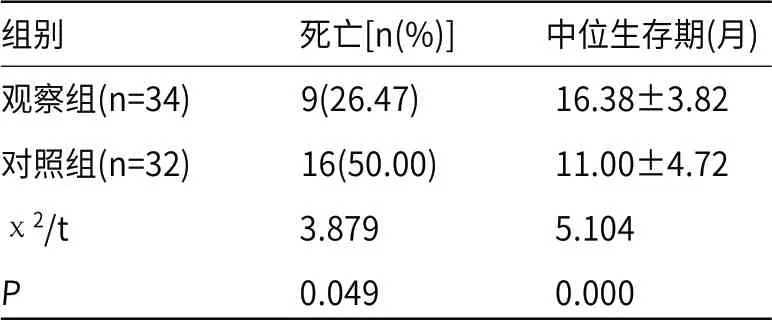
表3 两组患者生存情况的比较
3 讨 论
MDS患者的造血干细胞表现为质量和数量异常,导致不能及时为机体提供足够的正常血细胞,如白细胞、红细胞、血小板等,反而生成大量发育不全的细胞,导致机体功能异常。成熟红细胞的减少会导致患者出现贫血状态;血小板数量不足容易造成患者牙龈、眼底出血,甚至出现便血情况;白细胞较少则直接导致患者的免疫功能异常,消化道、呼吸道等易诱发感染,严重影响患者的生命健康,且病情如若未得到及时控制,会逐渐发展成为急性髓系白血病。MDS最为有效的治疗方式是进行骨髓移植,但常常因患者机体功能低下、医疗费用高、无合适的造血干细胞等条件限制无法实行,而表现基因修饰能够在基因水平延迟MDS向急性髓系白血病发展[5],结合预激方案治疗的有效率往往可达到60%,效率效果显著、价格实惠,是最常见的治疗方法。
本研究对MDS患者实行DAC联合CAG预激方案治疗,预激方案是2000年提出的MDS治疗方案,其临床治疗总效果高达70%左右。在MDS表面具有G-CSF表达受体,能够促进G0期白细胞增殖进入S期,具有增强细胞周期特异性化疗药物杀伤力的作用,同时G-CSF还能显著促进Ara-C对髓系白细胞的分化作用[6]; Acla是蒽环类抗癌药物,能够嵌入癌细胞的DNA中,阻断细胞繁殖的G1晚期和S晚期,能够抑制核酸的形成,但同时也具有一定的心脏毒性;Ara-C是嘧啶类抗代谢药物,就有诱导肿瘤细胞分化的作用,因此可以延缓MDS的发展进度。研究表明,DAC是针对MDS具有很好治疗效果的药物,是目前已知的DNA甲基化最强抑制剂。DAC是一种天然的腺苷类似物,能够有效抑制DNA甲基转移酶、减少DNA的甲基化,但是同时DAC并不影响基因的正常功能,能有效控制细胞的分化和繁殖,临床上常用于MDS的治疗。付海英等[7]的研究中也指出,DAC可以逆转MDS患者DLC-1基因异常甲基化状态,恢复其活性,从而达到治疗MDS的效果,该组患者治疗总有效率也与此有关。机体血清中的铁蛋白是存储铁微量元素的主要方式,铁浓度与机体铁蛋白合成能力呈正相关,治疗后血清中铁蛋白浓度的下降代表着细胞的恶性繁殖受到了抑制;维生素B2、叶酸在造血过程中具有重要意义,是细胞核DNA合成的重要辅助酶,观察组患者以上参数的显著降低,则再次说明了联合方案的有效性。
综上所述,DAC联合预激方案治疗能够有效缓解MDS患者症状,抑制细胞的恶性繁殖,延长患者的生存时间,效果较单独采用预激方案治疗效果更加显著,临床可根据患者的具体情况择优选择。
