水质中硫化物的3种分析方法比对试验研究
2022-03-26邓茂张永江黄晓容王明胜肖艳平姚靖刘蓉王文芳
邓茂,张永江,黄晓容,王明胜,肖艳平,姚靖,刘蓉,王文芳
1.重庆化工职业学院 环境与质量检测学院,重庆 长寿 401220;2.重庆市黔江区生态环境监测站,重庆 黔江 409003;3.重庆市生态环境监测中心,重庆 401147;4.重庆市江津区生态环境监测站,重庆 江津 402260
水质中的硫化物可与人体细胞色素、氧化酶等物质中的二硫键(—S—S—)作用,影响细胞氧化过程,造成细胞组织缺氧,危害人类身体健康.同时水中硫化氢也会消耗水中氧气,导致水生生物因缺氧而死亡[1-2].但温泉中适量的硫化物,有助于身体健康,如以沐浴和健康理疗为主的温泉旅游,符合新兴大众理念,深受人们喜欢[3].因此,准确、快速测定水环境样品中硫化物含量对水质评价具有极其重要的现实意义[4-5].目前,水质中硫化物的测定方法主要包括亚甲蓝分光光度法[6]、气相分子吸收光谱法[7]和流动注射亚甲蓝分光光度法[8].亚甲蓝分光光度法对实验条件要求不高,普通实验室即可进行,该方法易于推广使用,然而由于实验前处理操作繁琐,导致该方法的实验回收率不高且重复性较差[9].气相分子吸收光谱法的实验原理为在5%~10%磷酸介质中将试样中的硫化物瞬间转变成H2S,用氮气将该气体载入气相分子吸收光谱仪的吸光管中,在202.6 nm波长处测得的吸光度与硫化物的浓度遵守朗伯比尔定律[7].流动注射亚甲蓝分光光度法原理与亚甲蓝分光光度法化学反应原理相同,在封闭的管路中,将一定体积的试样注入连续流动的载液中,试样与试剂在化学反应模块中按特定的顺序和比例混合、反应,在非完全反应的条件下,进入流动检测池进行光度检测[8].同时,流动注射亚甲蓝分光光度法更简便,分析速度更快,具有仪器自动处理的优点[10-12].研究环境监测领域亚甲蓝分光光度、气相分子吸收光谱法和流动注射亚甲蓝分光度法测定水质中的硫化物含量,开展3种不同方法的比对研究,可为实验室开展水质中硫化物项目分析测试方法选择提供科学支撑.
1 实验部分
1.1 主要仪器和试剂
紫外可见分光光度计(日本岛津,UV2600);全自动硫化物前处理仪(北京斯珀特,HS-4A).乙酸锌、乙酸钠、抗坏血酸、乙二胺四乙酸二钠、N-二甲基对苯二胺、硫酸铁铵等所用试剂均为分析纯,氢氧化钠、硫酸、磷酸等所用试剂为优级纯.
气相分子吸收光谱仪(苏州北裕,GMA3212).乙酸锌、乙酸钠、等所用试剂均为分析纯.氢氧化钠、硫酸、盐酸和磷酸等所用试剂为优级纯.
连续流动化学分析仪(德国SEAL,AA100).乙酸锌、乙酸钠、抗坏血酸、乙二胺四乙酸二钠、氢氧化钠、N-二甲基对苯二胺、三氯化铁等所用试剂均为分析纯.氢氧化钠、硫酸、盐酸和磷酸等所用试剂为优级纯.
硫化物标准溶液和标准样品均购于生态环境部标准样品研究所,硫化物标准溶液(100±5)mg/L(国标号GSB 07-2733-2019,批号 104421).硫化物标准样品(1.72±0.15)mg/L(国标号GSB 07-1373-2001,批号205540).实验用为水电阻率18.25 MΩ·cm的去离子水.
1.2 实验方法
1.2.1 亚甲蓝分光光度法[6]
取100 mL混匀的水样,或适量样品加水稀释至200 mL,迅速转移至500 mL反应瓶中,再加入5 mL抗氧化剂溶液,轻轻摇动.量取20.0 mL乙酸锌-乙酸钠溶液于100 mL吸收比色管中作为吸收液,导气管下端插入吸收液液面之下,以保证吸收完全.连接好装置,关闭加酸分液漏斗活塞,在分液漏斗中加入10 mL盐酸溶液,开启氮气,调整氮气流量至300 mL/min.5 min后,开启水浴装置使温度升至60~70 ℃.打开活塞,缓慢注入10 mL盐酸于反应瓶中,关闭加酸分液漏斗活塞.连续吹气30 min,关闭气源.断开导气管,用少量水冲洗导气管,冲洗液并入吸收液中,加水至约60 mL.沿比色管壁缓慢加入10 mL N,N-二甲基对苯二胺溶液,立即密塞并缓慢倒转一次.拔塞开小口加1 mL硫酸铁铵溶液,立即密塞并充分摇匀.放置10 min后,用水定容至标线,摇匀.使用10 mm比色皿,以水作参比,在波长665 nm处测量吸光度.
1.2.2 气相分子吸收光谱法[7]
气相分子吸收光谱仪测定参数设置:输入氮气压力为0.30 MPa,载气量为120 mL/min,灯电流为0.8 mA,工作波长为202.6 nm,样品泵转速为50 r/min,试剂泵速为25 r/min,测量时间为15 s,延迟时间为30 s,读数方式为峰高.测定步骤:按仪器规定的顺序开机后,将待测样品放置在自动进样器上,按照与绘制标准曲线相同的条件进行样品的测定,记录信号值(峰高).
1.2.3 流动注射亚甲蓝分光光度法[8]
连续流动化学分析仪测定参数设置:取样速率为60个/h;进样与清洗时间比为3∶1;基线为10%;主峰为75%.测定步骤:按仪器规定的顺序开机后,以纯水代替所有试剂,检查整个分析流路的密闭性及液体流动的顺畅性.待基线稳定后(约 20 min),系统开始泵入试剂,待基线再次稳定后调整基线.量取约10 mL待测样品进行测定,记录信号值(峰面积).
2 结果与讨论
2.1 方法检出限及方法测定下限
按照《环境监测分析方法标准制订技术导则》(HJ 168-2020)[13]附录A的要求,对浓度值或含量为估计方法检出限值2~5倍的样品进行n≥7次平行测定,计算检出限,方法测定下限以4倍检出限计.配制硫化物标准溶液质量浓度为0.02 mg/L的样品,按照实验方法进行测试,相关数据详见表1.
由表1所知,亚甲蓝分光光度法、气相分子吸收光谱法和流动注射亚甲蓝分光光度法测定水中硫化物检出限分别为0.009,0.003,0.004 mg/L,均低于《地表水环境质量标准》(GB 3838-2002)[14]基本项目标准Ⅰ类(≤0.05 mg/L)限值要求.其中气相分子吸收光谱法和流动注射亚甲蓝分光光度法能够满足《地下水质量标准》(GB/T14848-2017)[15]地下水质量常规指标Ⅰ类(≤0.005 mg/L)限值要求.亚甲蓝分光光度法方法由于人工操作,重复性不好等因素,导致检出限不能满足《地下水质量标准》(GB/T 14848-2017)检测要求.
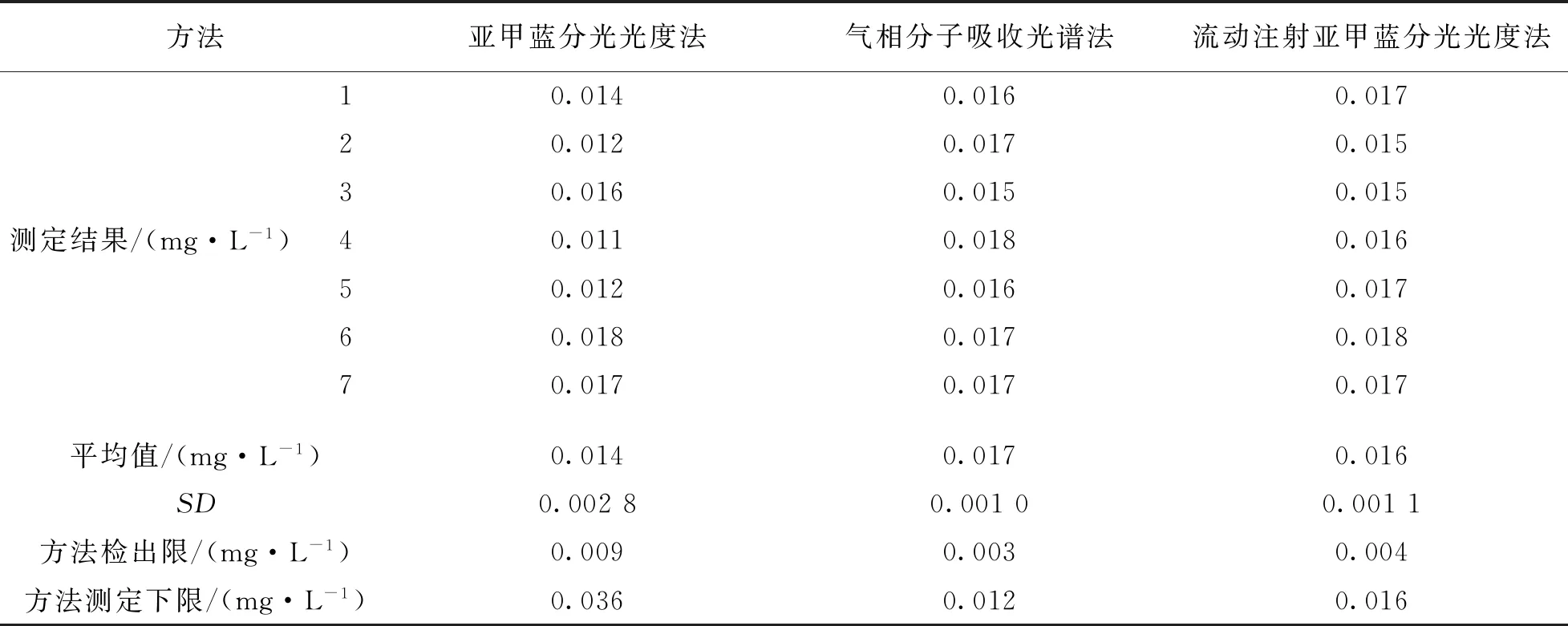
表1 3种方法检出限及测定下限
2.2 方法精密度
准确配置高中低3组硫化物标准溶液,分别用亚甲蓝分光光度法、气相分子吸收光谱法和流动注射亚甲蓝分光光度法各测定7次,结果见表2.由表2可知,亚甲蓝分光光度法的相对标准偏差为4.0%~10.0%,气相分子吸收光谱法相对标准偏差为0.9%~5.2%,流动注射亚甲蓝分光光度法相对标准偏差为5.6%~0.7%.气相分子吸收光谱法和流动注射亚甲蓝分光光度法的相对标准偏差均小于6%,二者重现性相当,均要优于亚甲蓝分光光度法.
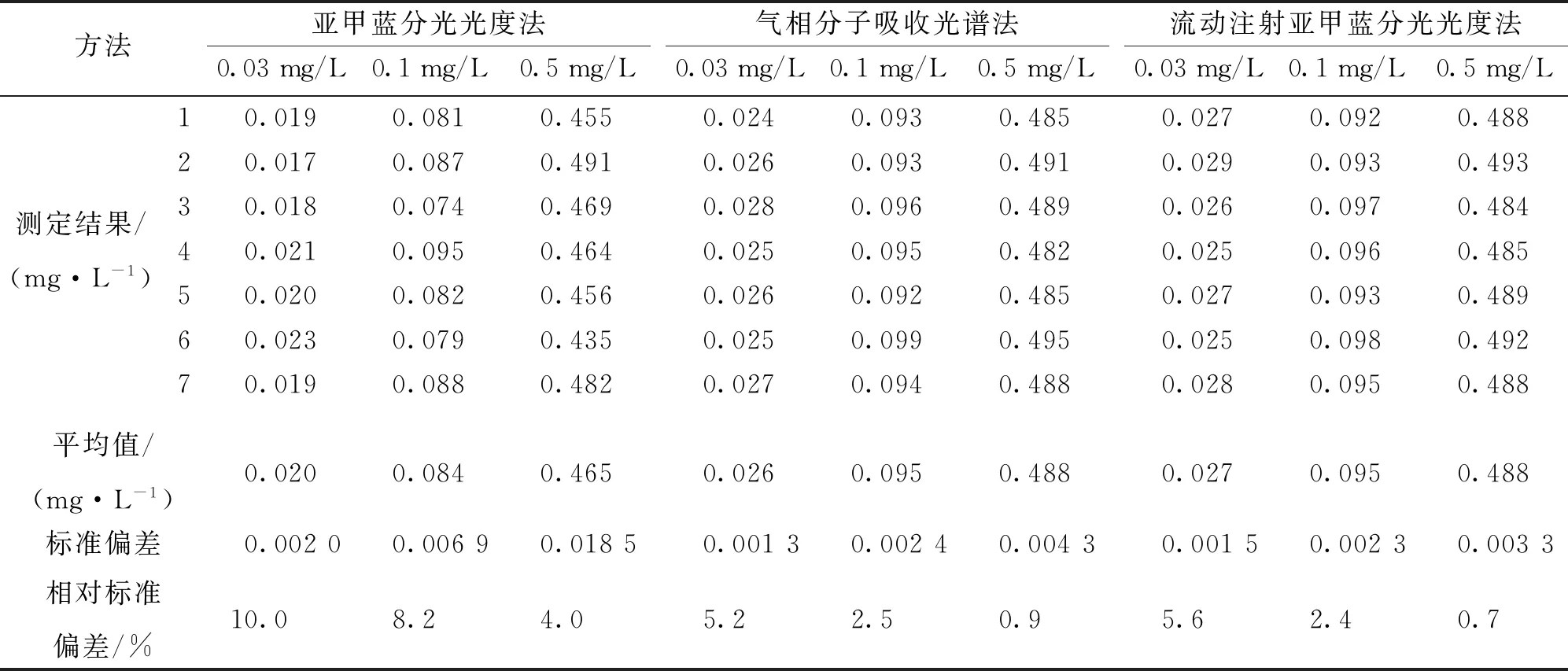
表2 3种方法精密度
2.3 方法准确度
选用生态环境部标准样品研究所研制的标准样品,分别采用3种分析方法进行测定,每个样品平行测定7次,测定值均在标准值范围内,结果见表3.亚甲蓝分光光度法测定值的相对标准偏差为-3.4%,气相分子吸收光谱法的相对标准偏差为0.4%,流动注射亚甲蓝分光光度法的相对标准偏差为-0.4%.气相分子吸收光谱法和流动注射亚甲蓝分光光度法测定硫化物的相对标准偏差均远小于亚甲蓝分光光度法测定硫化物的相对标准偏差.
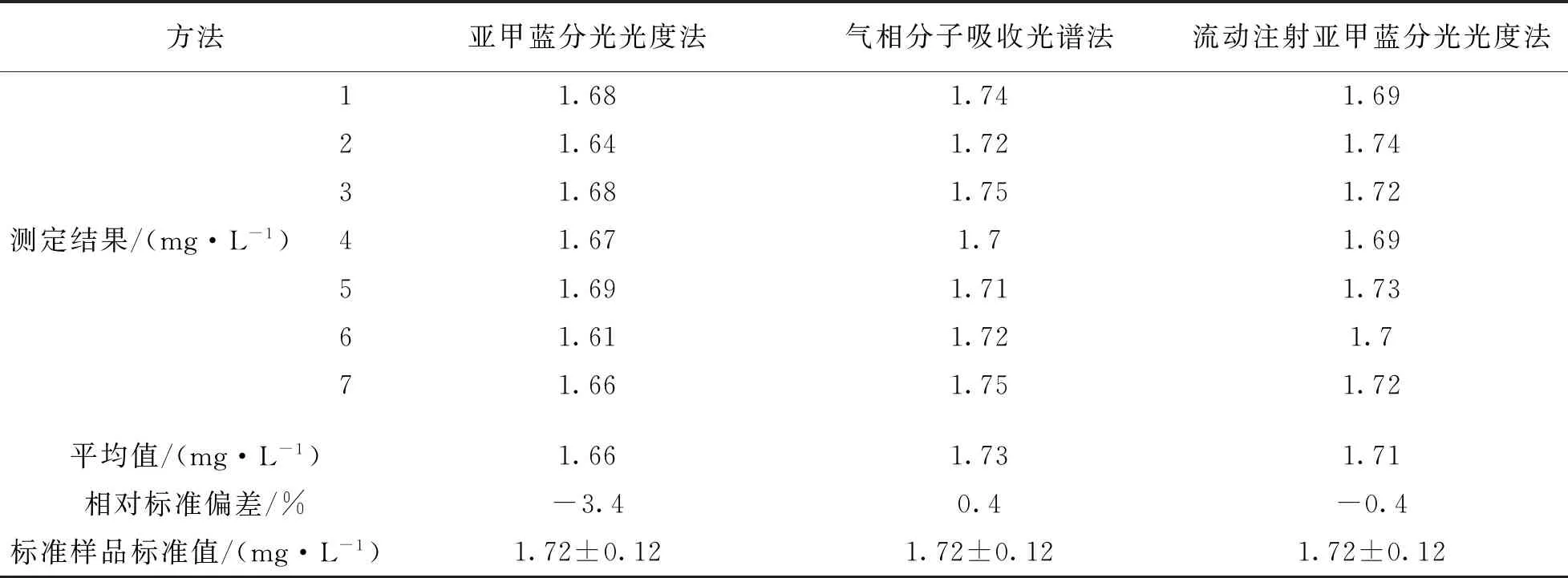
表3 3种方法标准样品测试比对结果
2.4 方法回收率
选取地表水、地下水和生活污水水样进行加标分析,其加标量为0.03 mg/L,对测试结果进行加标回收率计算,结果详见表4.亚甲蓝分光光度法加标回收率为73.3%~83.3%,气相分子吸收光谱法加标回收率为93.3%~96.7%,流动注射亚甲蓝分光光度法加标回收率为90.0%~93.3%.气相分子吸收光谱和流动注射亚甲蓝分光光度测定硫化物的加标回收率均在90%以上.
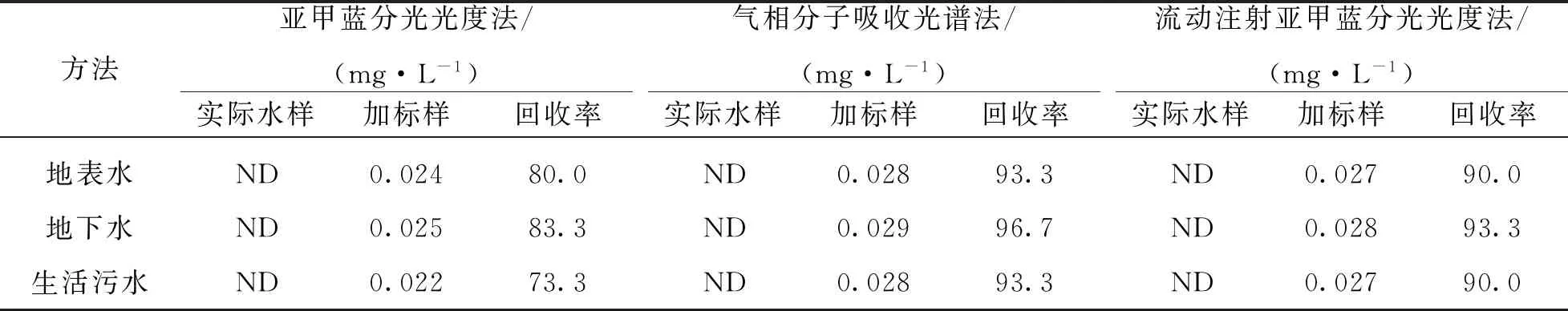
表4 3种方法对实际水样分析比对结果
2.5 比对实验的结果评价
《化学实验室内部质量控制 比对试验》(RB/T 208-2016)[16]规定,对于任何形式的比对试验,当每组检测的平行测量次数n较多(n≥6)时,可先对两组比对数据进行F检验,判断两个均值的精密度差异是否有统计学意义.若差异无统计学意义,即为两组测定结果等精度,继续t检验,对比对试验结果进行评价.
按照《化学实验室内部质量控制比对试验》(RB/T 208-2016)[16]要求,显著性水平α=0.05,对表5比对实验结果进行统计学评价.亚甲蓝分光光度法和气相分子吸收光谱法测定硫化物统计学评价结果:F=2.778,查表得F0.05(6,6)=4.284,F=2.778<4.284,说明亚甲蓝分光光度法和气相分子吸收光谱法测定硫化物的结果精密度差异无统计学意义.t=6.806,查表得t0.05(12)=2.179,t=6.806>2.179,说明亚甲蓝分光光度法和气相分子吸收光谱法测定硫化物的结果差异有统计学意义,表明比对结果不满意.

表5 3种方法对小南海水样分析比对结果
气相分子吸收光谱法和流动注射亚甲蓝分光光度法测定硫化物统计学评价结果:F=1.562,查表得F0.05(6,6)=4.284,F=1.562<4.284,说明气相分子吸收光谱法和流动注射亚甲蓝分光光度法测定硫化物的结果精密度差异无统计学意义.t=1.377,查表得t0.05(12)=2.179,t=1.377<2.179,说明气相分子吸收光谱法和流动注射亚甲蓝分光光度法测定硫化物的结果差异无统计学意义,表明比对结果满意.
亚甲蓝分光光度法和流动注射亚甲蓝分光光度法测定硫化物统计学评价结果:F=1.778,查表得F0.05(6,6)=4.284,F=1.778<4.284,说明亚甲蓝分光光度法和流动注射亚甲蓝分光光度法测定硫化物的结果精密度差异无统计学意义.t=5.292,查表得t0.05(12)=2.179,t=5.292>2.179,说明亚甲蓝分光光度法和流动注射亚甲蓝分光光度法测定硫化物的结果差异有统计学意义,表明比对结果不满意.
2.6 不确定度评定比对
为进行测定实际样品的差异性比较,分析购买的硫化物标准样品,并参考《化学分析中不确定度的评估指南》(CNAS GL006:2019)[17],对亚甲蓝分光光度法、气相分子吸收光谱法和流动注射亚甲蓝分光光度法测定水质中的硫化物含量的不确定度进行评定.置信概率为95%时,包含因子k=2,实际样品及不确定度分别为:亚甲蓝分光光度法(GB/T 16489-1996)的结果为(1.66±0.17)mg/L,气相分子吸收光谱法(HJ/T 200-2005)的结果为(1.73±0.15)mg/L,流动注射亚甲蓝分光光度法(HJ 824-2017)的结果为(1.71±0.12)mg/L.有证标准物质的认定值为(1.72±0.12)mg/L,3种方法分析结果均在证书认定值范围内.
不确定度分量的比对见图1.影响水质中硫化物含量的不确定度主要来源有标准溶液的配置、样品前处理、样品重复测定以及校准曲线的拟合等过程.影响亚甲蓝分光光度法(GB/T 16489-1996)不确定度的主要环节为样品前处理,原因可能为酸化吹气吸收法在前处理过程中样品有损失,回收率不高;影响气相分子吸收光谱法(HJ/T 200-2005)不确定度的主要环节为校准曲线拟合,原因可能为曲线拟合过程中未达到仪器的最佳状态或者硫化物浓度梯度配置不合理;影响流动注射亚甲蓝分光光度法(HJ 824-2017)不确定度的主要环节为标准溶液的配置,影响因素有标准溶液纯度、玻璃器皿的精度和温度等.
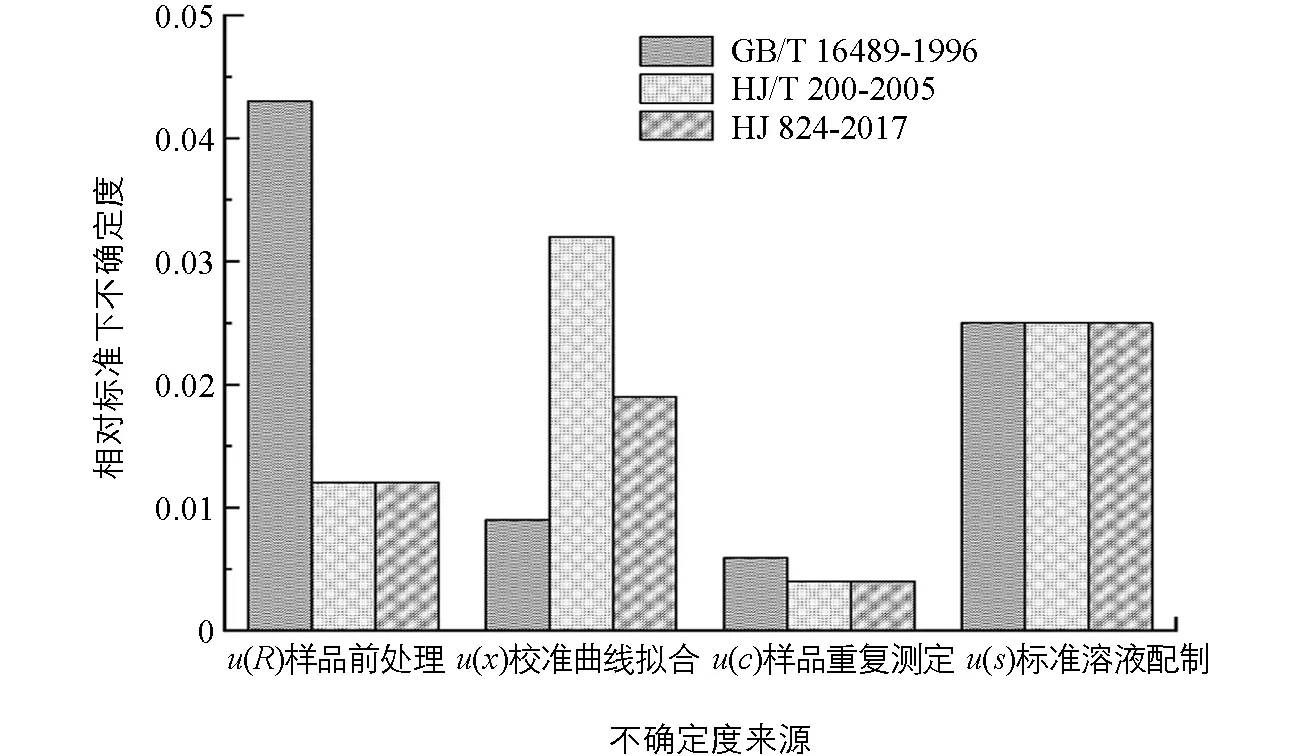
图1 不确定度分量的比对
3 结论
亚甲蓝分光光度法(GB/T 16489-1996)、气相分子吸收光谱法(HJ/T 200-2005)和流动注射亚甲蓝分光光度法(HJ 824-2017)比较研究结果经过统计学评价表明,气相分子吸收光谱法和流动注射亚甲蓝分光光度法的差异无统计学意义.亚甲蓝分光光度法与气相分子吸收光谱法和流动注射亚甲蓝分光光度法的差异有统计学意义.
亚甲蓝分光光度法测定水中硫化物因所需仪器设备简单,在环境监测中得到广泛的应用,但是整个操作过程繁琐,样品前处理复杂,回收率不高,重现性较差.流动注射亚甲蓝分光光度法与气相分子吸收光谱法自动化程度高,分析时间短,灵敏度、精密度和准确度均优于亚甲蓝光度法.
