胸腺肽制剂的质量及安全风险分析
2022-03-24陈小英杨亚婷王嫦鹤刘海静
陈小英,杨亚婷,王嫦鹤,刘海静*
1.陕西中医药大学,咸阳 712046;2.陕西省食品药品检验研究院,西安 710065
胸腺为机体的重要淋巴细胞器官,是T细胞分化、发育、成熟的场所[1]。胸腺肽是从健康猪或小牛胸腺中提取的具有生物活性的多肽类混合物,相对分子质量小于10 000道尔顿[2],其中公认为胸腺肽的有效成分是由28个氨基酸组成的胸腺肽α1(Tα1)。我国从1973年开始研究胸腺肽,在20世纪80 年代末改进并简化了胸腺组分5(TF5)的制备工艺,使制品的相对分子质量控制在10 000道尔顿以下[3]。胸腺肽制剂临床上常用的剂型有肠溶片剂、肠溶胶囊和注射剂。胸腺肽能诱导淋巴细胞分化、增殖与成熟,增强巨噬细胞吞噬和抗原递呈功能,提高白细胞介素应答水平,可以调节机体的免疫功能[4]。胸腺肽制剂常用于各种原发性或继发性T细胞缺陷病、某些自身免疫性疾病、慢性疾病、乙型肝炎、各种细胞免疫功能低下的疾病以及肿瘤的辅助治疗等。
1 国内现有的生产企业和批号
胸腺肽制剂市场需求量大,全国生产胸腺肽制剂的企业较多,通过在国家食品药品监督管理局网查询并统计,我国市场上现有的胸腺肽制剂生产企业和批准文号分别为75家和243个。见表1。
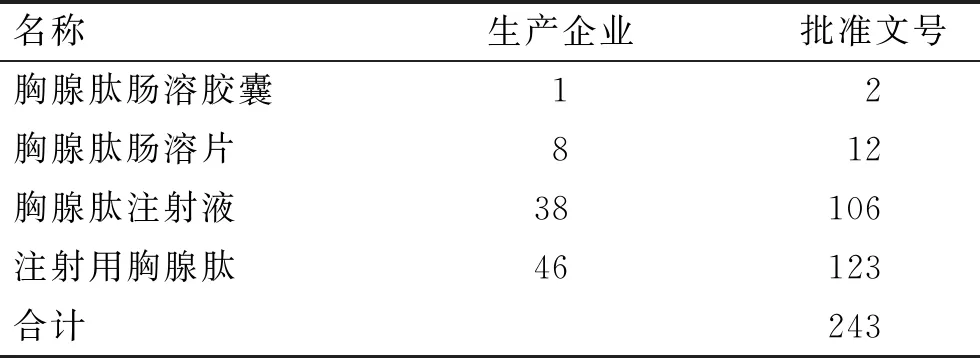
表1 胸腺肽制剂生产企业和批准文号
2 胸腺肽的生产工艺
目前国内生产的胸腺肽制剂是以健康猪或小牛胸腺为原料,提取高活性的多肽混合物。通过查阅文献,胸腺肽提取主要有常规提取法、酸碱提取法和化学酶解法。
常规提取法:胸腺匀浆反复冻融,通过水浴解冻,离心沉淀,取上清液置于水浴中加热80 ℃,调节pH值为中性,超滤,用滞留相对分子质量为1.0×104的超滤膜进行超滤,即得胸腺肽溶液[5-7]。
酸碱提取法:加盐酸调节胸腺匀浆pH值至3.5,反复冻融3次,离心后调节pH值为6.5,超滤,用滞留相对分子质量为1.0×104的超滤膜进行超滤,即得胸腺肽溶液[5-7]。
化学酶解法:胸腺匀浆加入适当的木瓜蛋白酶水解,调节pH值为7.0,在37 ℃水浴中保温数小时,加盐酸调节pH值为3.5,水浴加热,冷却至室温,用氢氧化钠调节pH值为6.8,离心沉淀,超滤,用滞留相对分子质量为1.0×104的超滤膜进行超滤,即得胸腺肽溶液[8]。
常规提取法和酸碱提取法属于物理提取方法,化学酶解法属于化学提取方法。化学提取方法提取的多肽含量大于物理提取法,但是活性低于物理提取方法。物理提取法中,酸碱提取法的多肽含量和活性均大于常规提取法[5-8]。
3 胸腺肽注射剂现行标准及其存在的问题
胸腺肽制剂均属于多组分生化药,成分复杂。现行胸腺肽制剂的质量标准主要是化学药品地方标准上升国家标准第16册、新药转正标准第44册和各企业标准,各标准中具体的检验项目见表2。胸腺肽制剂中的检验项目比较简单,有效性和安全性指标未做出具体的规定。在现有标准中均缺少基原鉴定,无法控制药品原料的动物来源。不同企业中胸腺肽生产工艺不同,导致胸腺肽特征图谱差异较大,表明不同企业的胸腺肽制剂在质量中存在一定的差异,在质量标准中应添加胸腺肽专属性鉴别项目,从而规范胸腺肽生产工艺,在一定程度上可以保证胸腺肽制剂的质量。
胸腺肽制剂的原料为健康猪或小牛胸腺,其原料的特殊性易受致病微生物、病菌等污染,人体过多摄入有害物质,可增加临床不良反应风险。应高度关注胸腺肽制剂中生物胺含量、兽药残留、重金属、病原微生物及病毒等安全性指标,对可能引起不良反应的因素进行控制,增强临床用药的安全性,保证广大患者的利益。

表2 胸腺肽制剂的标准
4 胸腺肽制剂的不良反应
胸腺肽制剂中注射剂的不良反应报道较多, 2007~2013年胸腺肽注射剂的不良反应文献有47篇,不良反应有101例[9]。2003~2011年共收到怀疑与胸腺肽注射剂有关的不良反应报告5 459例[10]。胸腺肽注射剂的不良反应主要有皮疹、心悸、发热、恶心、胸闷、呕吐、呼吸困难、支气管哮喘、严重可导致过敏性休克等[11-12]。胸腺肽注射剂引起不良反应的主要原因为,注射剂具有高风险的特点[13-15],在临床使用上引起的不良反应概率比传统的口服剂型要高[16];胸腺肽是从动物脏器中提取的多肽混合物,在原料提取加工贮存过程中容易产生对人体有害的物质。
5 胸腺肽制剂存在的安全问题
胸腺肽溶液是从健康猪或小牛胸腺中提取的无菌溶液。动物胸腺来源复杂,组成不明确,动物健康状况无法得到保证。胸腺肽制剂在原料和加工过程中易引入有害物质,比如生物胺、兽药残留、重金属、致病微生物和病毒等。应控制这些有害物质,提高胸腺肽制剂的安全性,从而保证临床用药的可靠性。
5.1 生物胺
生物胺是一类具有生物活性的含氮的低相对分子质量有机化合物的总称。生物胺主要包括腐胺、尸胺、精胺、亚精胺、酪胺、苯乙胺、组胺、色胺等[17]。生物胺常存在于动物类中药或以动物为原料的生物药品中。生物胺中组胺毒性最强,主要表现为头疼、胸闷、腹泻、心率增加、血压下降、甚至休克;其次是酪胺可引起血压升高、偏头痛、呼吸困难;尸胺、腐胺可增加组胺和酪胺的毒性,尸胺、腐胺、精胺和亚精胺可与亚硝酸盐反应产生亚硝胺致癌物质[18-19]。
动物源食品中检测生物胺含量的方法比较成熟,常采用柱前衍生反相高效液相色谱法测定生物胺的含量[20-22]。在动物中药材中生物胺的研究也比较普遍,比如对蜈蚣、鹿茸采用柱前衍生化的方法,使用高效液相色谱法(HPLC)测定生物胺的含量[23-24]。以动物为原料的生物制品中生物胺的测定也常用此方法,苏喆等[25]对鹿瓜多肽注射剂中的生物胺应用柱前衍生化反相高效液相色谱法进行测定,该法专属性、精密度、线性关系以及回收率等均良好。徐学平等[26]采用柱前衍生的方法对胸腺中的组胺进行测定,在胸腺中均可测出组胺。可以借鉴文献中生物胺的测定方法,对胸腺肽制剂中生物胺的含量进行测定。
5.2 兽药残留
兽药可用于预防和治疗动物疾病,科学规范地使用兽药,能有效预防动物疾病,促进动物生长,提高产量,改善动物质量。但是,一些饲养户在经济利益的驱使下,为了促进动物生长和提高产量,违规或过多地使用兽药,使过多的兽药残留在动物体内[27]。兽药残留分为4类:抗生素类(四环素类、磺胺类、喹诺酮类、氯霉素等)[28];抗病毒类(美金刚、吗啉胍、金刚烷胺、金刚乙胺等)[29];激素类(己烷雌酚、己烯雌酚、雌酮、雌二醇等)[30];抗寄生虫类[31](苯并咪唑类药物)。其中抗生素类占所有兽药添加剂的60%,是最主要的兽药残留药[32]。动物饲养过程中兽药的滥用,导致在动物源食品和药品中兽药频繁被检出。胸腺肽原料来自健康猪或小牛胸腺,动物来源复杂,生产厂家对动物来源控制薄弱,缺乏统一的监管体系,未对胸腺中兽药残留进行控制。
兽药残留的检测主要使用酶联免疫吸附(ELISA)法、HPLC法、气相色谱-质谱联用法、液相色谱-四级杆-质谱法等[33]。超高效液相色谱-串联质谱法具有高效、灵敏、快速、选择性好等优势,现广泛应用于兽药残留检测[34-35]。兽药残留越来越受到企业和个人的关注,对动物类中药和以动物类为原料的中药制剂中兽药残留进行检测,比如检测梅花鹿鹿茸中兽药残留[36];中药膏剂中蜂蜜的兽药残留用高效液相色谱-串联质谱法,该方法在相应的浓度范围内线性关系良好[37]。胸腺肽制剂原料来源于健康猪或小牛胸腺,在动物生长过程中,养殖户是否过量地使用兽药或使用禁用兽药,提高动物生产繁殖能力和产量,生产企业未对兽药残留进行检测,无法确保原料安全。
5.3 重金属
胸腺肽来自健康猪或小牛胸腺,动物是人工养殖,水、土壤、肥料的使用可能引入重金属[38]。胸腺肽制剂在生产过程中会引进铝、铬、铁、钡等重金属,胸腺肽注射剂内包材常采用玻璃包装,会引入硼、铝、硅等元素[39]。研究表明,重金属对人体的代谢和正常的生理作用会造成明显的损害,当体内重金属过量时会严重危害人体健康[40]。
重金属的检测方法主要有原子吸收光谱法、紫外分光光度法、原子荧光光谱法、电感耦合等离子体质谱(ICP-MS)等[41],其中ICP-MS为重金属常用的检测方法,因其操作简单、结果准确可靠[42-43]。ICP-MS广泛用于动物类中药材中重金属的测定[44],李勇等[45]使用ICP-MS方法对地龙和水蛭中的重金属及有害元素进行测定。胸腺肽注射剂临床用法是皮下或肌肉注射、静脉注射,不经过肝脏的首过效应,直接进入人体,微量的重金属对人体都可能产生很大的危害。为了确保临床安全性,应关注胸腺肽制剂中重金属的含量。
5.4 病原微生物及病毒
动物在饲养过程中很容易被病原微生物污染,比如肉毒梭菌、沙门氏杆菌、巴氏杆菌[46]、布鲁氏菌、副结核分枝杆菌等。检测病原微生物的主要技术有病原学检查、ELISA、胶体金免疫层析技术、聚合酶链式反应(PCR)检测法、生物芯片技术等方法[47]。蔡珠明等[48]采用IS900-PCR分离鉴定得到3株牛型副结核分枝杆菌。何亚鹏等[49]采用多重PCR方法同时检测猪种、牛种、羊种、绵羊种布鲁氏菌,该方法因其特异性强、敏感度高、稳定性好的特点,可用于生物制品污染的布鲁氏菌的快速检测。
国际上现有对生物制品中病毒安全性控制的标准或指导原则主要有:生物技术产品的病毒安全性评价;日本药典(JP17,所列生物技术/生物制品病毒安全的基本要求);美国药典(USP41 1050,人源或动物源细胞系制备的生物技术产品的病毒安全性评价)等。各标准或指导原则虽然都具有科学性和规范性,但是均未涵盖所有相关生物制品。目前国内现有的指导原则有:国家食品药品监督管理总局(CFDA)发布的“血液制品去除/灭活病毒技术方法及验证指导原则”;“生物组织提取制品和真核细胞表达制品的病毒安全性评价技术审评一般原则”。现行药典未对生物制品中通用病毒进行相关的规定[50]。
6 展望
胸腺肽制剂属于多肽类药物,生物活性高和特异性强,但其稳定性差和半衰期短。胸腺肽制剂的生产工艺不同,使其有效性差异较大,导致临床疗效差异性大。胸腺肽制剂在临床上得到广泛的应用,但不良反应报道多,易出现呼吸困难、休克甚至死亡等严重不良反应,应引起高度重视。健康猪或小牛胸腺是胸腺肽制剂的原料,动物在饲养过程中易感染致病微生物和病毒,易摄入过多的重金属,过多地使用兽药。在生产和贮藏的过程中产生对人体有害的生物胺。生物胺、兽药、重金属、致病微生物等,都增加胸腺肽制剂在临床上的安全风险,增加不良反应的概率。
