剑突下入路单孔胸腔镜在前纵隔肿瘤手术中的应用
2022-02-28许彬东黄国忠陈鹏飞蔡茂恩姚金梅
许彬东 陈 豪 黄国忠 张 强 陈鹏飞 蔡茂恩 姚金梅
莆田学院附属医院胸心外科,福建 莆田 351100
纵隔肿瘤是指起源于纵隔的肿瘤,根据肿瘤的部位可分为前纵隔肿瘤、中纵隔肿瘤和后纵隔肿瘤。其中前纵隔肿瘤是所有纵隔肿瘤中最常见的肿瘤。手术仍然是前纵隔肿瘤最主要的治疗方法之一[1]。
患者发病的初期,常常无明显的临床症状,不易被临床医生发现,晚期则常常出现咳嗽、胸痛、呼吸困难、心律失常等,且易出现肿瘤压迫周围脏器或者发生恶变。因此,除恶性淋巴瘤需采取放射治疗和化疗之外,其他类型的纵隔肿瘤均建议尽早外科干预治疗[2]。手术入路主要包括经前正中切口纵行劈开胸骨,常规开胸,胸腔镜下经左胸、右胸或双侧胸腔。尽管伴随着胸腔镜技术的不断成熟,胸腔镜下经肋间胸壁切口的手术方式在临床上逐渐推广[3],但是该手术方式对于对侧纵隔的暴露仍旧不满意。近3年来,剑突下入路行前纵隔肿瘤切除逐渐被临床医师应用[4],但仍未成熟。本研究尝试剑突下入路单孔胸腔镜下行前纵隔肿瘤切除,临床疗效较好,现报道如下。
1 资料与方法
1.1 一般资料
回顾性分析2015年6月至2020年6月,莆田学院附属医院胸心外科收治的前纵隔肿瘤54例患者的临床资料。所有患者均行剑突下入路单孔胸腔镜下前纵隔肿瘤切除术。其中男性39例,女性15例,年龄45~79岁,平均年龄(64.9±7.5)岁。患者的体质量指数(body mass index,BMI)为(20.4±2.8)kg/m2。入住的所有患者中,50例为常规健康体检时发现,无明显临床症状,2例表现为上眼睑下垂,1例表现为咳嗽,1例出现胸痛。前纵隔肿瘤的直径为2.0~5.0 cm,平均(3.2±1.8)cm,见表1。

表1 54例前纵隔肿瘤患者的基线资料
纳入标准:(1)胸部CT直接增强提示:前纵隔肿物,病灶包膜完整;(2)肿瘤最大直径≤5.0 cm。排除标准:(1)肿瘤侵犯邻近的脏器(如无名静脉、上腔静脉、肺动脉主干、心包等);(2)中转开胸;(3)BMI≥28 kg/m2;(4)纵隔肿瘤术后复发。
本研究获得莆田学院附属医院伦理委员会的批准。
1.2 手术方法
患者采用静脉联合气管单腔插管全身麻醉。患者取平卧位,分开双腿,腰背部垫高软枕形成折刀位。术野常规消毒、铺无菌洞巾。主刀医生位于患者两腿之间,扶镜手位于患者的右侧。取剑突下紧贴剑突下缘前正中切口(图1),长度约5.0 cm,常规用电刀切开皮肤、皮下组织及腹白线,钝性游离腹膜外脂肪组织与腹壁后鞘之间的间隙,再沿剑突下,用食指和卵圆钳钝性游离胸骨后与心包之间的间隙,置入单孔保护套(套管穿刺针,康基),连接气腹肌,持续注入CO2,调整CO2压力10.0 mmHg[5]。该单孔保护套有四个管腔,分别置入10.0 mm 30°胸腔镜、气腹肌气体输入管道、超声刀、胸腔镜用胃钳,另外有一排气管道连接胸瓶,便于排气,以减少手术视野模糊。
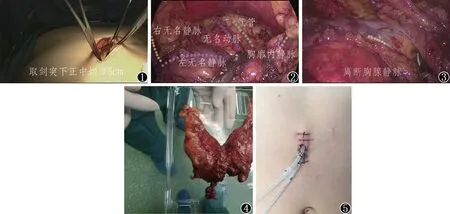
图1 手术部位及手术切口;图2上纵隔结构;图3胸腺静脉;图4肿瘤标本;图5术后切口及引流管
首先,打开左侧纵隔胸膜,以便打开左侧胸腔,沿着左侧膈神经游离胸腺组织和左侧膈神经内侧的脂肪组织,直至暴露左侧胸廓内静脉、左侧无名静脉与左侧锁骨下静脉之间的夹角。然后,打开右侧纵隔胸膜,以便打开右侧胸腔,沿着右侧膈神经游离胸腺组织和右侧膈神经内侧的脂肪组织,直至暴露右侧胸廓内静脉、右侧无名静脉、上腔静脉与左无名静脉之间的夹角(图2)。接着,沿着心包前游离胸腺组织的下极,直至左无名静脉的下缘。最后,切除胸腺组织的上极,直至暴露无名动脉、气管、甲状腺下动脉(图2)。游离胸腺静脉,予以常规处理。一般胸腺静脉有2~4支,对于管径细的胸腺静脉,可以直接用超声刀予以离断,对于管径粗的胸腺静脉(图3),应用钛夹或Hemo-Lock离断。最后,置入标本袋,将前纵隔肿物及周围的脂肪组织从剑突下切口取出(图4)。术后常规留置两根16号颈部负压引流管,均从剑突下切口处引流出(图5)。
1.3 术后处理
术后常规予以心电监护、营养支持、对症处理。术后第1天,复查床边胸部正位片(坐位),若胸片提示双肺膨胀良好,双侧肋膈角清晰,双侧胸管引流液少于100 mL,颜色淡红或淡黄,则拔除双侧胸管。
1.4 观察指标
1.4.1 术后感染情况 观察患者术后感染情况,包括肺部感染、切口感染、泌尿系感染。
1.4.2 术前及术后疼痛应激情况 术前、术后1天及术后7天,取患者晨起空腹外周静脉血3 mL,置入抗凝管内,应用高速离心法分离出血清。应用酶联免疫法检测所有患者的疼痛应激相关指标,包括5-羟色胺(5-HT)、神经肽Y(NPY)、促肾上腺皮质激素(ATCH)和前列腺素E2(PGE2)。项目检测均采用上海润裕生物科技有限公司生产的ELISA试剂盒。
1.4.3 术后视觉模拟量表(visual analogue scale,VAS)评分情况 术后1天和术后7天,对所有患者均采用VAS进行疼痛评分。具体操作方法:在一张白纸上画一直线,其中一头代表0分,另一头代表10分,让患者根据自己的主观感觉来选择分数。0分:患者没有任何疼痛感;1~3分:有轻微的疼痛;4~6分:有明显的疼痛;7~10分:有非常剧烈的疼痛,难以忍受[6]。
1.5 统计学方法
采用SPSS 20.0软件进行统计学分析。计量资料(手术时间、术中出血量、胸液引流量、胸管留置时间、术后住院时间、疼痛应激指标、VAS评分)以±s表示,术后VAS评分、术前与术后疼痛应激指标差异的比较采用重复测量设计资料的方差分析。检验水准α=0.05。
2 结 果
所有患者均顺利完成手术,无中转开胸手术,无死亡病例。手术后病理报告:胸腺囊肿2例,胸腺增生7例,畸胎瘤3例,错构瘤1例,A型胸腺瘤9例,AB型胸腺瘤18例,B1型胸腺瘤3例,B2型胸腺瘤9例,B3型胸腺瘤2例,胸腺癌1例。
2.1 患者术中及术后情况,详见表2。
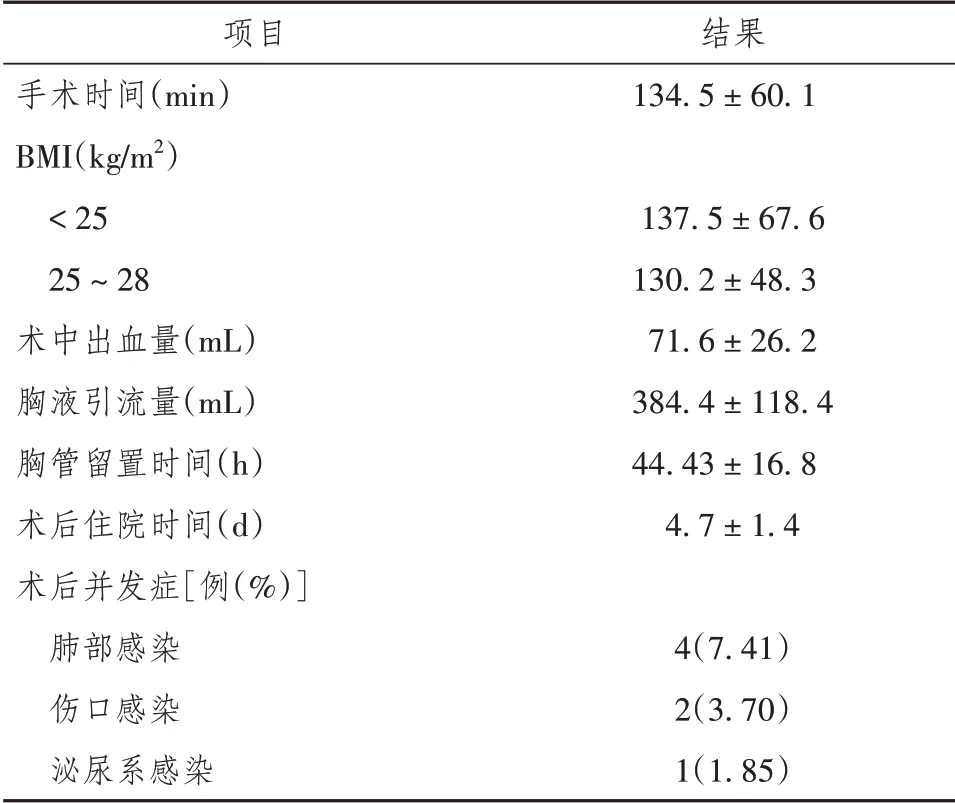
表2 54例前纵隔肿瘤患者术中及术后情况
2.2 术后VAS评分、术前及术后疼痛应激指标的比较,详见表3。
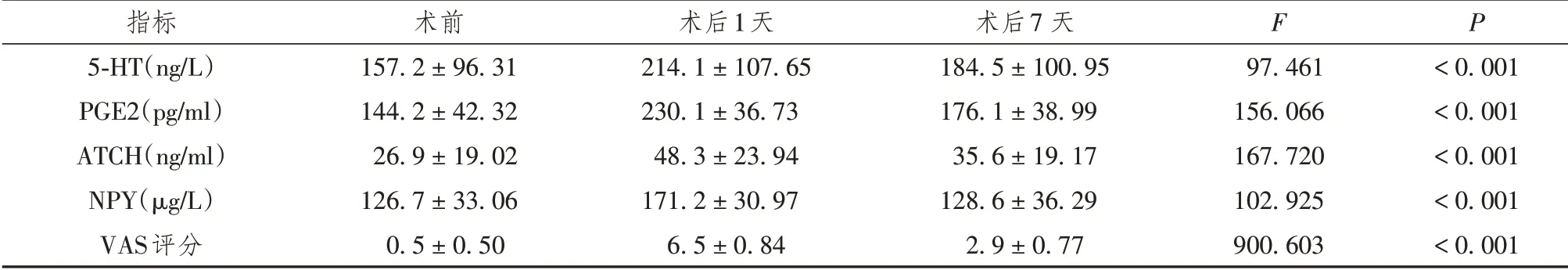
表3 54例前纵隔肿瘤患者术后VAS评分、术前及术后疼痛应激指标的比较
3 讨 论
前纵隔肿瘤大部分为良性肿瘤或者是低度恶性肿瘤。在所有纵隔肿瘤中,前纵隔肿瘤的发病率最高,其中最常见的有胸腺瘤、畸胎瘤、心包囊肿等。该类患者发病初期常常无典型的临床症状,易被患者和临床医生忽略。然而,随着疾病的进展,肿瘤逐渐增大,可以压迫周围脏器而影响心肺功能。另外,前纵隔肿瘤有潜在恶变的可能,因此,一旦发现前纵隔肿物且直径超过2 cm,都主张尽早手术干预治疗[7]。
长期以来,经前正中切口劈开胸骨的手术入路是前纵隔肿瘤手术治疗的标准入路[8]。该入路的主要优点是手术视野暴露清晰,不易损伤左右无名静脉、上腔静脉、双侧膈神经等,而且根据病情的需要还可以同期行大血管置换等复杂的手术。但是该入路也有明显的缺点:手术创伤大,手术后疼痛感剧烈。手术对心肺功能影响较大,手术并发症的发生率高,而且破坏了胸廓的稳定性,增加了胸骨、纵隔及肺部感染的机会,特别是对于老年患者的肺功能影响更大。由于老年患者常常合并骨质疏松,因此,可导致胸骨愈合不良的发生。随着胸腔镜技术的发展和应用,纵隔肿瘤亦成为胸腔镜手术的适应证[9],因此胸外科医师广泛将胸腔镜技术应用于前纵隔肿瘤的切除,进一步提高了纵隔肿瘤患者手术后的生活质量。胸腔镜下经肋间入路的手术方式,具有创伤小、手术视野清晰、术后恢复快的优点,在达到微创治疗的同时,其治疗效果不亚于传统开放手术[10],但该手术入路实际上仍未能完全消除手术引起的疼痛。不管是采用三孔法、单操作孔法或单孔法,所取的观察孔的肋间一般位于第6或第7肋间,此处肌层相对较厚,肋间隙狭窄,因此极易挤压肋间神经,破坏肋间血管,从而出现术后切口疼痛、胸腔出血等并发症,进而影响患者手术后的康复。另外,肋间入路胸腔镜手术,对对侧胸腺组织和其周围脂肪组织的暴露存在一定的困难,有甚者会影响整体的疗效,甚至需要再次手术。虽然有学者提出同期行双侧胸腔镜手术,能很好解决这一问题,但手术过程存在变换体位、双侧胸壁损伤、术后疼痛加剧以及增加麻醉风险等缺点。因此,针对这一系列的问题和不足,临床上需要一种更加简便、有效的手术方式。
2012年,Suda等[11]首次报道了经剑突下胸腔镜下前纵隔肿瘤切除的手术方法。国内学者亦有采用剑突下入路胸腔镜进行纵隔肿瘤切除,但大多数应用三孔法[12],即剑突下为观察孔,左右肋弓下缘和锁骨中线连接处为操作孔,再连接气腹肌制造人工气胸进行手术。但术后切口疼痛会限制呼吸运动,增加去甲肾上腺素的分泌,从而加重围手术期气道反应和炎症反应[13]。
随着微创技术理念的不断革新,本研究探索经剑突下单切口行前纵隔肿瘤切除的手术方式,以求达到减少手术切口长度和数量的目的。经过5年多的手术探索和总结,证实了经剑突下入路单孔胸腔镜手术方式是安全、可行的。特别是术后第7天的疼痛评分即处于较低的水平,而且入组的所有患者中未出现顽固性切口疼痛。提示该手术入路能有效减轻术后切口疼痛的发生。分析原因主要为:(1)单孔剑突下入路进行手术,常规切开剑突下腹壁的皮肤和皮下组织,钝性游离腹直肌,避免腹直肌被完全离断,减少术后腹直肌收缩引起的疼痛,而且不会破坏胸骨剑突组织,特别是不会破坏胸廓骨性结构的完整性,未挤压和牵拉肋间神经,因此,该术式能明显减轻术后切口疼痛;(2)剑突下单孔胸腔镜手术入路,术前及术后的致痛介质(5-羟色胺、缓激肽等)和疼痛相关的应激反应指标(NO、IL-1、IL-6等)水平均明显低于常规的三孔胸腔镜手术[14],与本研究结果相符。因此,该入路的术后疼痛明显减轻;(3)单孔剑突下入路放置的引流管均从胸骨后间隙引流出,由于剑突下区域无肋间神经的分支经过,避免了引流管对肋间神经的过度挤压;(4)与剑突下三孔胸腔镜手术相比,避免了器械对肋弓组织的摩擦和肋弓下缘神经组织的压迫,从而能减轻手术后切口疼痛。
本研究认为,该手术方式具有以下优点:(1)取平卧位即能完成手术的各种操作,术中无需额外更换患者的体位;(2)模拟了常规经胸骨前正中切口开胸的手术视野,能更加清晰暴露双侧膈神经、无名静脉等重要的解剖标志,避免副损伤;(3)麻醉插管只需要普通的单腔气管插管,降低了术后咽喉部疼痛与声音嘶哑的发生率,避免了双腔气管插管带来的额外气道损伤;(4)术中采用人工气胸配合手术,增宽胸骨后脂肪间隙的同时,双肺也得到充分的萎陷,减少呼吸对手术视野和手术操作过程的影响;(5)对于胸腺瘤,特别是合并重症肌无力的患者,该入路手术视野清晰,能更加彻底切除双侧心包前的脂肪组织,从而达到根治的目的;(6)仅有剑突下单一切口,术后切口更加隐蔽、美观;(7)保持了胸膜腔的完整性,减少了术后发生呼吸与循环障碍的风险,术后可以快速康复[15];(8)如果术中出现左无名静脉的损伤而引起大出血,可以立即经胸骨正中切口中转开胸,无需额外变换体位,给手术操作带来安全性的保证;(9)由于剑突下解剖中无骨性结构,更有利于标本的取出,特别是肿瘤直径超过5 cm时,可以避开肋间;(10)对于胸膜腔粘连的患者,该手术方式影响不大,避免了开胸手术带来的创伤。然而,该手术方式亦存在以下缺点:(1)剑突下单一切口,胸腔镜的镜头和各种操作器械均从剑突下进入胸骨后间隙,整个操作空间狭小,手术器械之间极易相互干扰,对手术者的操作技巧要求更高,对扶镜手亦有更高的要求。因此,开展这一手术技术需要完成学习曲线30例[16],方能保证手术的安全性和有效性;(2)由于该入路需经过心包前和胸骨后之间的间隙,整个隧道的距离较长,需要配置相应的超长超声刀头,增加手术耗材费用;(3)剑突下切口,紧贴膈肌的附着处,因此,在游离剑突下胸骨后间隙时,极易误入腹腔而造成损伤;(4)由于整个操作过程手术器械均需经过心包前间隙,极易刺激和压迫心脏,给手术带来损伤,因此,心律失常成为围手术期最常见的并发症[17];(5)前纵隔肿瘤直径较大,特别是超过7 cm,位置较深,或者胸骨下角小于90°时,术中暴露困难,操作风险较大;(6)该手术入路对胸腺的上极区域暴露欠佳,对于胸腺瘤合并重症肌无力的患者,存在无法达到根治的风险;(7)一旦出现血管损伤,几乎无法通过缝合止血,只能通过局部压迫止血,若止血效果欠佳,则只能中转开胸止血。
因此,本研究认为剑突下单孔胸腔镜主要有以下适应证:(1)早期胸腺瘤;(2)除胸腺瘤以外的其他良性前纵隔肿瘤;(3)前纵隔肿瘤未明显侵犯周围脏器或大血管组织[18];(4)直径小于5 cm的前纵隔肿物。禁忌证有:(1)心肺功能欠佳,无法耐受手术;(2)前纵隔恶性肿瘤,而且明显侵犯周围脏器或大血管组织;(3)既往有前纵隔肿瘤手术病史。
总之,剑突下单孔胸腔镜手术技术应用于前纵隔肿瘤是安全、有效、可行的,能够显著减轻术后切口疼痛,值得临床推广应用。但是临床疗效仍需多中心的前瞻性的研究进一步验证。
利益冲突所有作者均声明不存在利益冲突
