滹沱河地下水超采区人工回灌的水岩相互作用模拟
2022-02-28耿新新张凤娥朱谱成马琳娜郭春艳
耿新新,张凤娥,朱谱成,马琳娜,陈 立,郭春艳
(1.中国地质科学院水文地质环境地质研究所,石家庄 050061;2.中国地质大学(北京)水资源与环境学院,北京 100083;3.自然资源部地下水科学与工程重点实验室,石家庄 050061)

1 实验背景与实验方法
1.1 场地概况及含水层特征
回灌试验场地位于石家庄市藁城区梨园庄村东北角(图1),东西宽约400 m,南北长约500 m,由4个回灌井和8个观测井组成。回灌目标含水层为埋深39~60 m处的砂层,产状近水平,岩性由灰白色细砂、灰黄色中粗砂、灰黄色含砾粗砂及少量砾石组成,该含水层横向延伸性好,富水性强,单井涌水量1 000~3 000 m3/d,具有较强的回灌潜力[16]。

图1 回灌场地平、剖面图Fig.1 Plan and section of the groundwater artificial recharge site

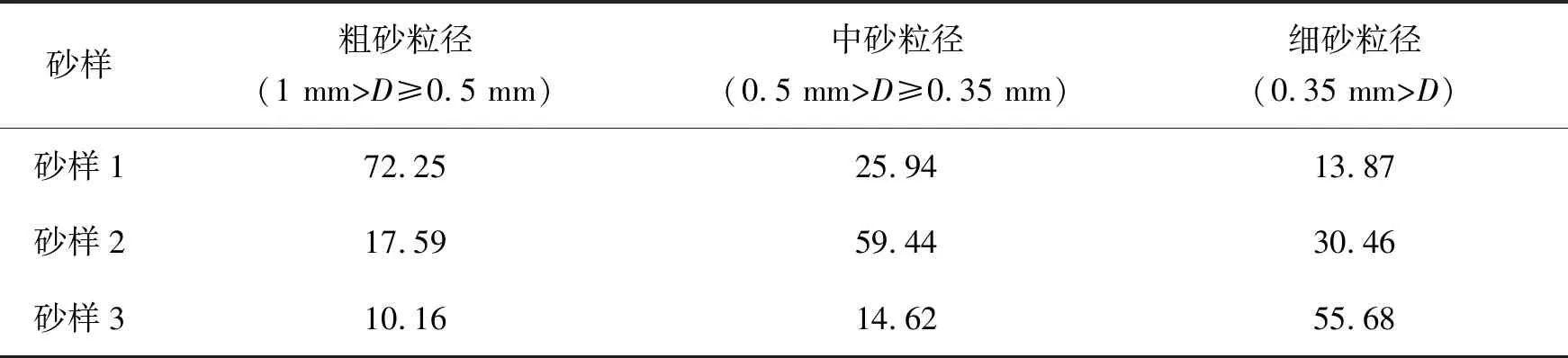
表1 含水介质的粒径占比Table 1 Particle size ratio of aqueous medium %

表2 含水介质可溶盐测试结果Table 2 Test results of soluble salt in aqueous medium mg⋅kg-1
1.2 场地地下水与回灌水水质特征


表3 灌渠水与地下水水质测试结果Table 3 Water quality test results of surface water and groundwater mg/L
1.3 实验方案
实际回灌过程中回灌水源与地下水的混合比随时间不断变化[11],本次实验将灌渠水与场地地下水分别以3 ∶1、1 ∶1及1 ∶3的比例进行混合,并与回灌含水层中的3种不同粒径的介质发生水岩反应,给定不同的实验编号(表4)代回灌水与地下水混合带中不同部位在回灌不同时段的水-岩相互作用过程。
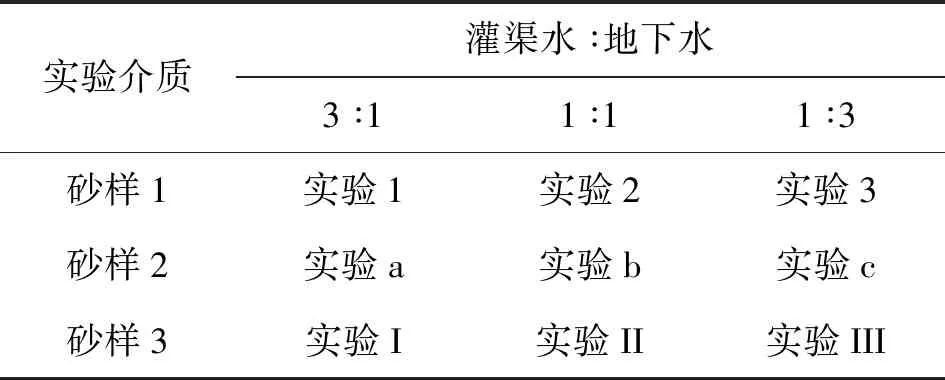
表4 实验方案Table 4 Experimental scheme
实验采用9个规格大小相同的马氏瓶作为反应容器。首先,将回灌目标含水层的代表性岩芯样品各取3份,每份4 kg,放入不同的马氏瓶中;再将3种不同混合比例的水样分别从装有不同介质的马氏瓶底部缓缓注入,使气泡完全从岩样中排出,当注入水样微微淹没实验介质时,即停止注水,并利用橡皮塞封住马氏瓶顶端瓶口。将装有混合水样及实验介质的马氏瓶放置在恒温箱中,恒定温度的设置依据现场测定的地下水温为16 ℃。
2 回灌含水层水质变化规律
2.1 pH、Eh及TDS变化特征
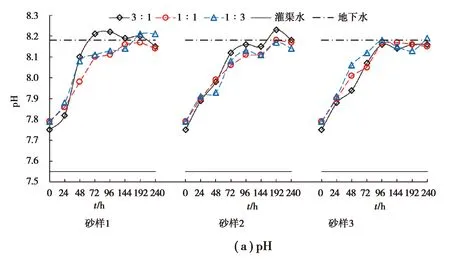
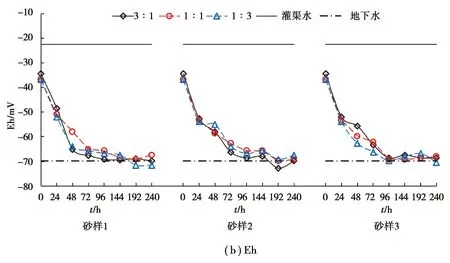
pH、Eh及TDS变化特征如图2所示。实验初始时刻,不同混合水样中的pH值均介于灌渠水和地下水之间,且混合水样之间的pH值差异较小。随着水-岩相互作用时间的增加,混合水样中的pH值的变化特征为均在0~72 h时段内明显升高,在72 h后趋于稳定并与地下水的pH值相当,这说明在0~72 h时段受水-岩作用的影响导致pH值向碱性方向发展,并在72 h后达到了新的酸碱平衡状态(图2(a))。混合水样中Eh值的变化趋势与水的pH变化趋势恰好相反,其变化特征均为在0~72 h时段内明显减小,72 h后趋近地下水的Eh值,说明水-岩相互作用过程中混合水样的还原性逐渐增强(图2(b))。由此可知,随着混合水与含水介质相互作用时间的增长,混合水中的pH与Eh值会逐渐恢复到原有地下水的大小。
不同占比的混合水与含水介质作用后总溶解固体的(TDS)质量浓度均呈先增大后减小的变化特征,但不同混合比的水样与不同粒径含水介质反应后,TDS变幅表现为:在同种粒径含水介质中,混合水中地表水占比越大,则TDS变幅越大;在同一混合比例条件下,粒径越小的含水介质中混合水的TDS变幅越大(图2(c))。
2.2 主要离子变化特征

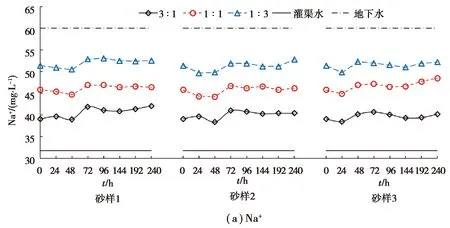





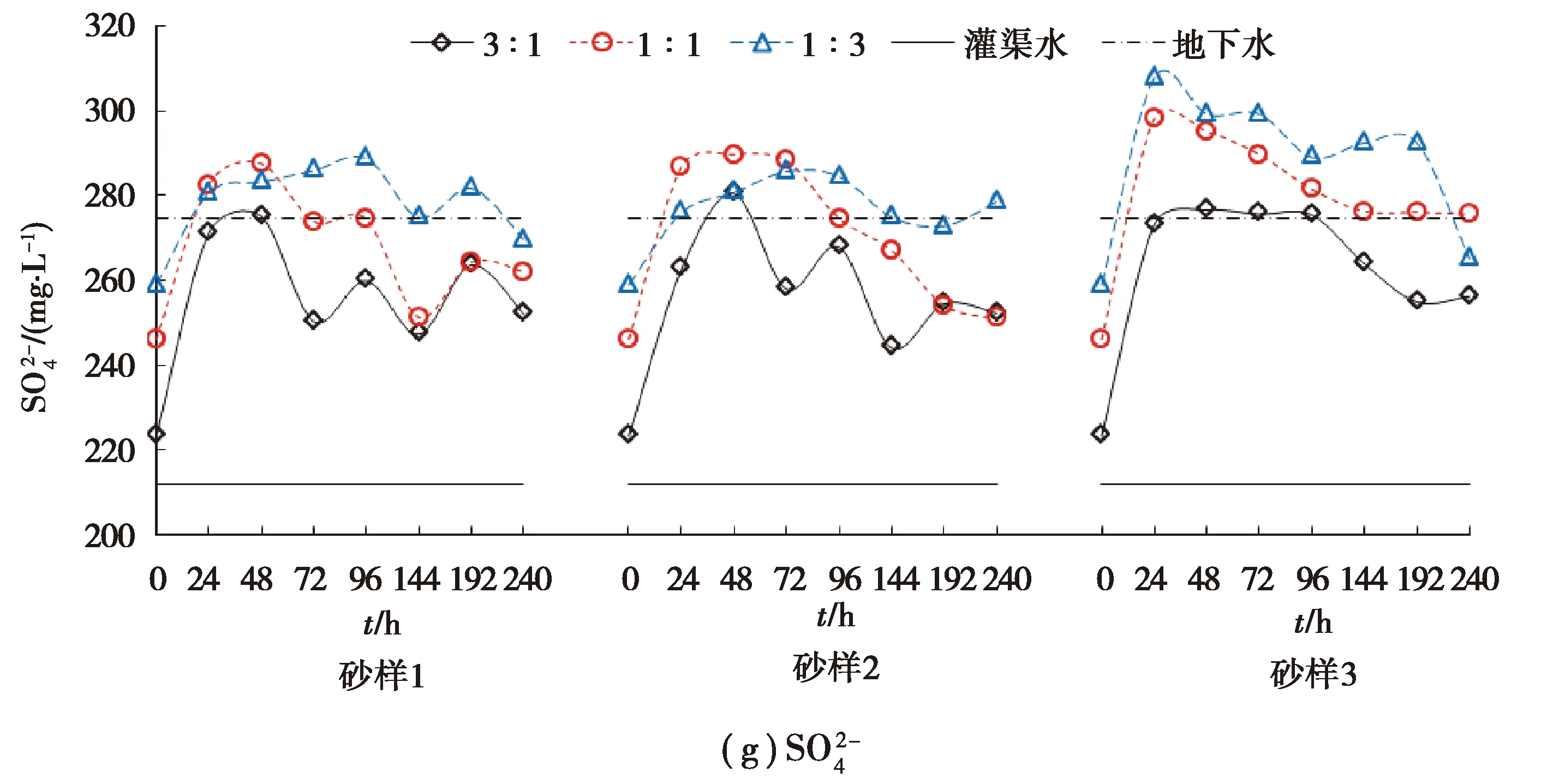
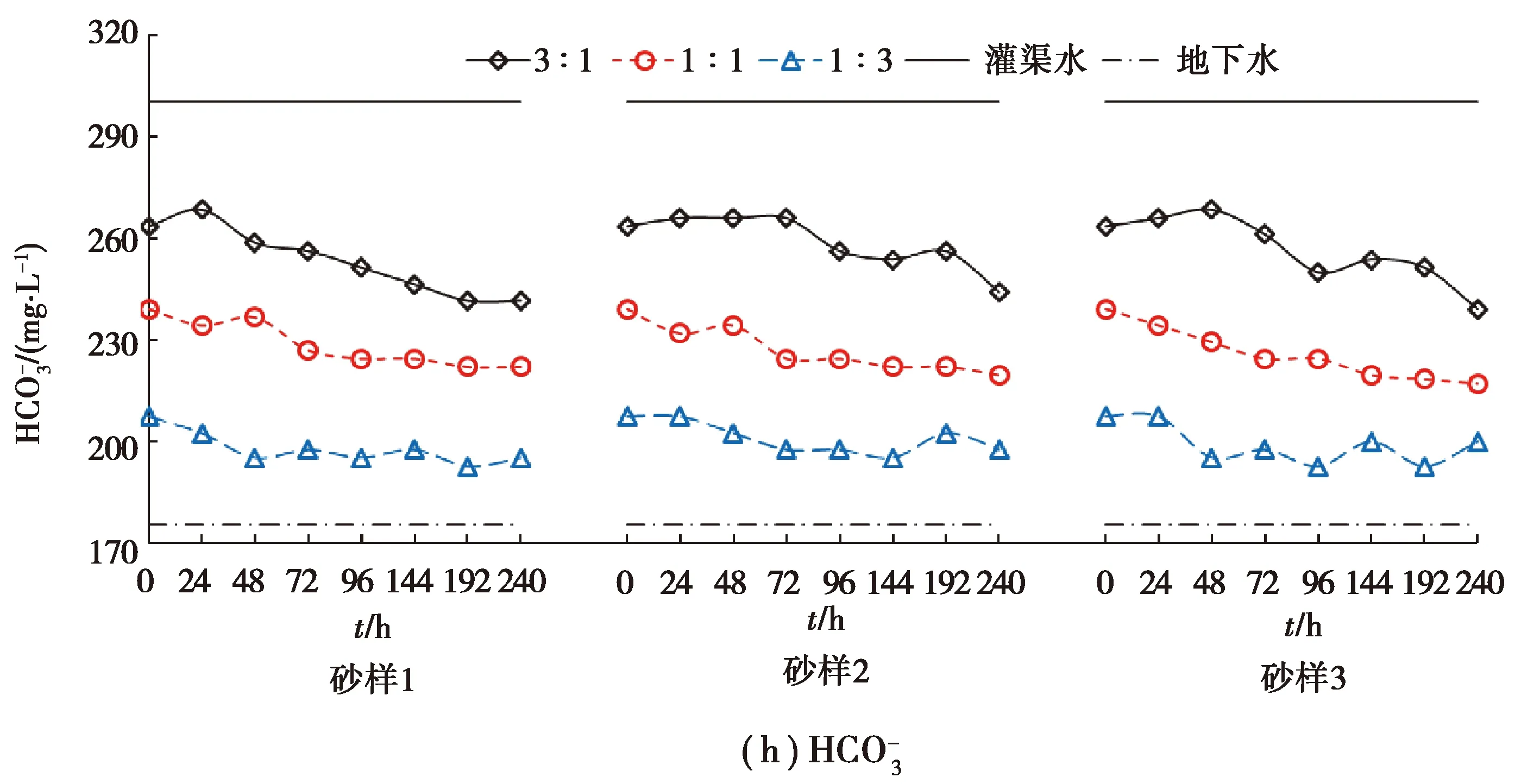
图3 回灌含水层中主要离子质量浓度随时间变化特征Fig.3 Time-varying characteristics of the concentration of major ions in the recharged aquifer
3 结果分析与讨论
3.1 混合作用

3.2 碳酸平衡作用

图离散点图Fig.4 Discrete point diagram of and pH
3.3 溶解沉淀作用
利用Na+与Cl-毫克当量γ(meq/L)的比值可判断水-岩相互作用过程中Na+、Cl-的矿物来源[17]。实验起止时刻不同混合比水样中γ(Na+)、γ(Cl-)离散点均分布于直线的上方(图5),图中黑色直线为γ(Na+)/γ(Cl-)=1,且实验过程中γ(Na+)、γ(Cl-)离散点向右上方漂移,表明水-岩相互作用过程中Na+、Cl-质量浓度升高受盐岩和硅铝酸盐矿物溶解控制。此外,结合含水介质特征可知水-岩反应过程中K+质量浓度升高受含水介质可溶盐中的钾盐和钾长石的溶解控制。


图5 γ(Na+)/γ(Cl-)的离散点图Fig.5 Discrete point diagram of γ(Na+)and γ(Cl-)

图的离散点图Fig.6 Discrete point diagram of γ(Ca2++Mg2+)
朗格利尔指数(LSI)可反映水-岩作用过程中方解石是否产生沉淀[21]。实验过程中LSI随时间变化曲线(图7)显示,不同混合比水样中的LSI值大小次序均为3 ∶1>1 ∶1>1 ∶3>0(灌渠水 ∶地下水)。随着水-岩相互作用时间的增长,混合水样中的LSI值均逐渐增大在t=48 h时均大于0.5,并在72 h后趋于稳定,而当LSI>0.5时表明水中可产生方解石沉淀。由此可知,利用灌渠水回灌地下水的混合带中可产生方解石沉淀。


图7 LSI随时间变化曲线Fig.7 Time-varying curves of LSI
3.4 硝化作用

表5 混合水样在0~96 h内的质量浓度增量一览表Table increment of mixed water samples within 0-96 h mg/L
3.5 反向水文地球化学模拟

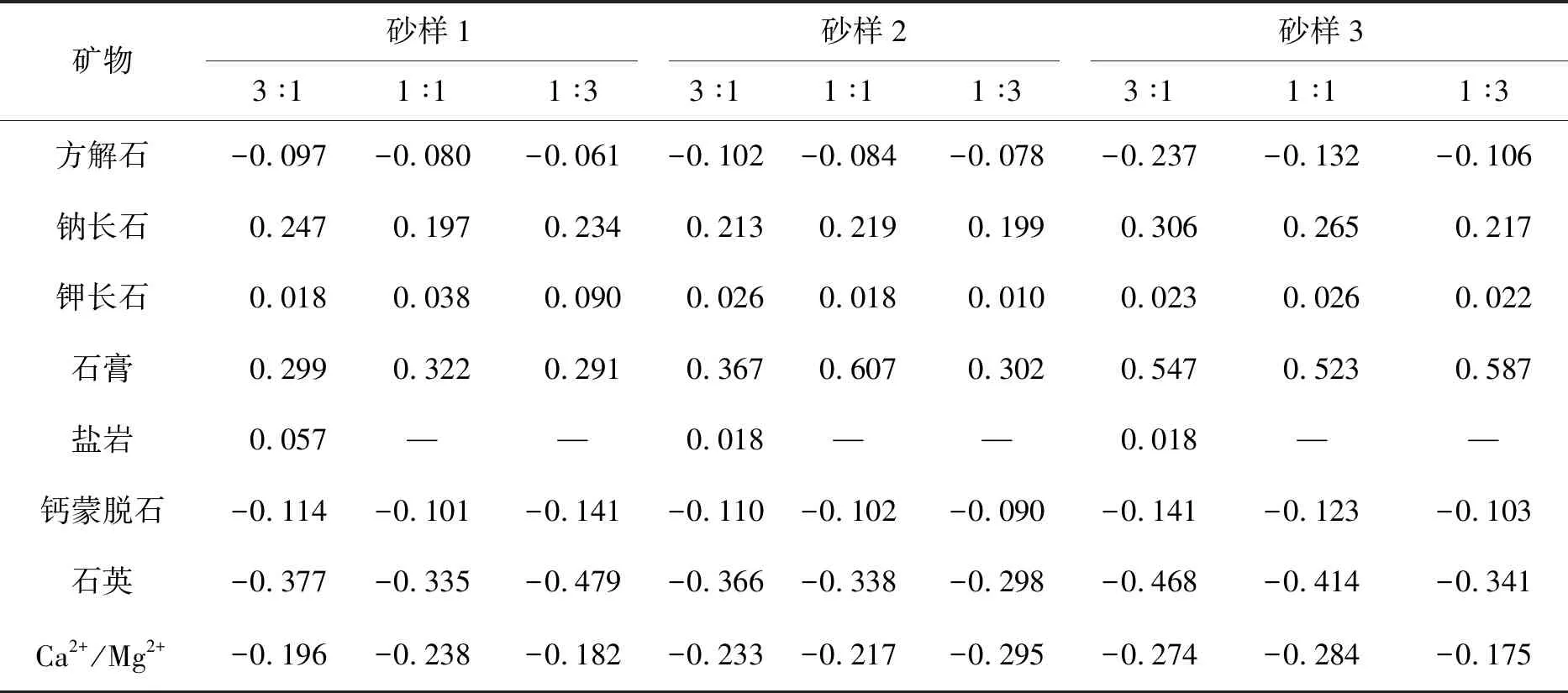
表6 反向水文地球化学模拟结果Table 6 The results of inverse hydrogeochemical models mmol/L
结合实验过程中主要离子浓度的变化特征和反向水文地球化学模拟结果,可将混合带中水-岩相互作用过程归结为如下化学反应:
NaCl→Na++Cl-,
(1)

(2)
Mg2+(lq)→ Ca2+(sd),
(3)
2KAlSi3O8+4H2O→2Al(OH)3+6SiO2+2K++2OH-,
(4)
2NalSi3O8+4H2O→2Al(OH)3+6SiO2+2Na++2OH-,
(5)

(6)
(7)
0.165Ca2++ 2.33Al(OH)3+3.67SiO2+7.34H2O→Ca0.165Al2.33Si3.67O10(OH)2+0.33H++9.67H2O。
(8)

3.6 讨 论
1)碳酸岩盐沉淀是地下水人工回灌过程中导致化学堵塞的主要因素之一[23],但回灌过程中水化学演化导致的化学堵塞的时间尺度跨度非常大,因此通常采用水文地球化学模型开展矿物沉淀风险的评估[24,25]。对比表5中反向水文地球化学模拟结果可知,在相同介质不同混合比条件下水中的方解石沉淀量大小依次均为3 ∶1>1 ∶1>1 ∶3,相同混合比水样与不同粒径的介质作用后方解石沉淀量大小依次均为砂样3>砂样2>砂样1,表明地表水占比越大、含水介质粒径越细方解石的沉淀量越高。由此可推断在场地回灌过程中,长期利用当地地表水通过回灌井补给地下水时,在井壁附近粒径较细的含水层位发生碳酸岩盐类型化学堵塞的风险较高。
4 结 论
1)随着回灌层位混合带水-岩相互作用时间的增长,混合水的pH与Eh值会逐渐恢复到与原地下水一致,TDS变化特征表现为先增大后缓慢降低,且地表水占比越大、含水介质粒径越细,则其变幅越大。

3)水-岩相互作用过程中溶解的矿物有石膏、钾长石、钠长石及盐岩,析出的矿物有方解石、钙蒙脱石及石英,且地表水占比越大、含水介质粒径越细方解石的沉淀量越大。回灌过程中在地表水占比大且粒径较细的含水层中发生碳酸岩盐化学堵塞的风险较高。
