高原湖泊溶解甲烷浓度空间异质性研究—以阳宗海秋季为例
2022-02-25郑祥旺肖尚斌王圣瑞王雪竹许浩霆
郑祥旺,陈 敏,3*,肖尚斌,3,王圣瑞,王雪竹,陈 巍,刘 佳,许浩霆
高原湖泊溶解甲烷浓度空间异质性研究—以阳宗海秋季为例
郑祥旺1,2,陈 敏1,2,3*,肖尚斌1,2,3,王圣瑞4,5,王雪竹2,陈 巍2,刘 佳2,许浩霆2
(1.三峡库区生态环境教育部工程中心,湖北 宜昌 443002;2.三峡大学水利与环境学院,湖北 宜昌 443002;3.三峡水库生态系统湖北省野外科学观测研究站,湖北 宜昌 443002;4:北京师范大学水科学研究院,北京 100875;5.云南省高原湖泊流域污染过程与管理重点实验室,云南 昆明 650034)
以西南典型高原湖泊阳宗海为研究对象,于2020年11月应用新型快速水-气平衡装置(FaRAGE)及便携式温室气体分析仪,开展了表层水体和垂向剖面溶解CH4浓度的高分辨率监测,揭示了溶解CH4浓度空间分布特征及影响因素.结果表明,阳宗海表层水体溶解CH4浓度为0.02~0.97μmol/L,表现为大气甲烷的源.空间上呈现出南北高、中部低的分布特征,与水生植物分布、入湖河流输出和水深等因素密切相关.湖泊不同区域垂向剖面溶解CH4浓度分布较为一致,湖心区CH4氧化消耗最为明显.自展分析表明,基于少量样点监测的CH4排放估算具有较大不确定性,准确估算阳宗海CH4扩散通量所需最小采样点数量约为3.7个/km2,高空间分辨率的监测对于湖库碳排放的准确估计十分必要.
温室气体;溶解浓度;空间分布;通量;阳宗海
湖泊作为淡水生态系统的重要组成部分,是CH4的重要排放源之一[1].Bastviken等[1]估计全球湖泊CH4年排放量为71.6Tg,远高于2004年估计的6~36Tg[2].这种巨大差异不仅存在于全球尺度,单一湖泊的碳排放估计也存在较大不确定性[3-4].
目前估算单个湖泊水-气界面CH4扩散通量通常采用薄边界层法[5],CH4扩散通量主要受控于表层水体溶解CH4浓度和气体传输速率,风速作为气体传输速率的主控因子较容易监测,表层水体溶解CH4浓度的准确获取是CH4通量估算的关键.现有研究多基于有限样点溶解CH4浓度计算的CH4扩散通量均值乘以水域面积估算总扩散通量,但该方法缺乏对溶解CH4浓度分布空间异质性的考虑[6-7]. Xiao等[8]基于太湖29个采样点的监测发现,藻类大量生长的梅梁湾溶解甲烷浓度高达0.13μmol/L,而中心湖区仅为0.02μmol/L.Yang等[9]监测研究则发现,通量计算中剔除排污区域监测点溶解CH4浓度数据,总CH4扩散通量将被低估69%,可见基于少数监测点的通量估算具有很大的潜在误差.尽管部分研究者尝试按照水深等自然地理特征对湖泊进行分区[10],通过分区面积加权平均估算扩散通量,但由于观测点数量有限,某一分区内的实测均值很可能无法表征该区域的扩散通量真实水平.事实上,为评估溶解CH4浓度分布空间异质性对甲烷排放估算的影响,已有部分学者在水库的研究中尝试加密监测点和革新监测技术以获得高空间分辨率的CH4浓度.例如,Yang等[9]基于传统顶空平衡法在面积为5.2km2的文武砂水库进行了108个样点溶解CH4浓度加密监测,Paranaíba等[11]基于膜平衡器对巴西3个水库溶解CH4浓度进行了高空间分辨率的走航式监测,两项研究均表明,高空间分辨率的CH4浓度数据是准确估算CH4扩散通量的关键.
中国西南云贵高原湖泊众多,在全球气候变化的背景下,其碳排放问题成为国内外关注的焦点[12].本文以云贵高原湖区典型湖泊阳宗海为研究对象,应用新型快速水-气平衡装置(FaRAGE)[13-14]及便携式温室气体分析仪原位高频监测表层水体及垂向剖面中的溶解CH4浓度,并估算扩散通量,探讨阳宗海溶解CH4浓度的分布规律和影响因子,通过将空间异质性因素纳入考虑,以期为湖库水域CH4排放更准确的估算提供参考.
1 材料与方法
1.1 研究区概况
阳宗海(102°59'~03°02' E、24°51'~24°58' N)地处云南省昆明市东南,湖面面积31.9km2(水位1770m时),平均水深19.5m,蓄水量6.04×108m3,换水周期13a[15].流域内有阳宗大河、七星河、摆衣河等河流汇水入湖,出水河道仅有汤池河.阳宗海流域地处亚热带高原季风气候区域,多年平均降水量824.7mm,多年平均湖面蒸发量1161.7mm,多年平均温度16.2℃[16].研究区域及监测点位置如图1所示.
1.2 样品采集与分析
于2020年11月9日白天在阳宗海进行走航监测,监测船以10km/h的速度航行并采用自吸泵连续取水,取水口位于水面以下20cm处,共设3个监测点进行垂向剖面监测.
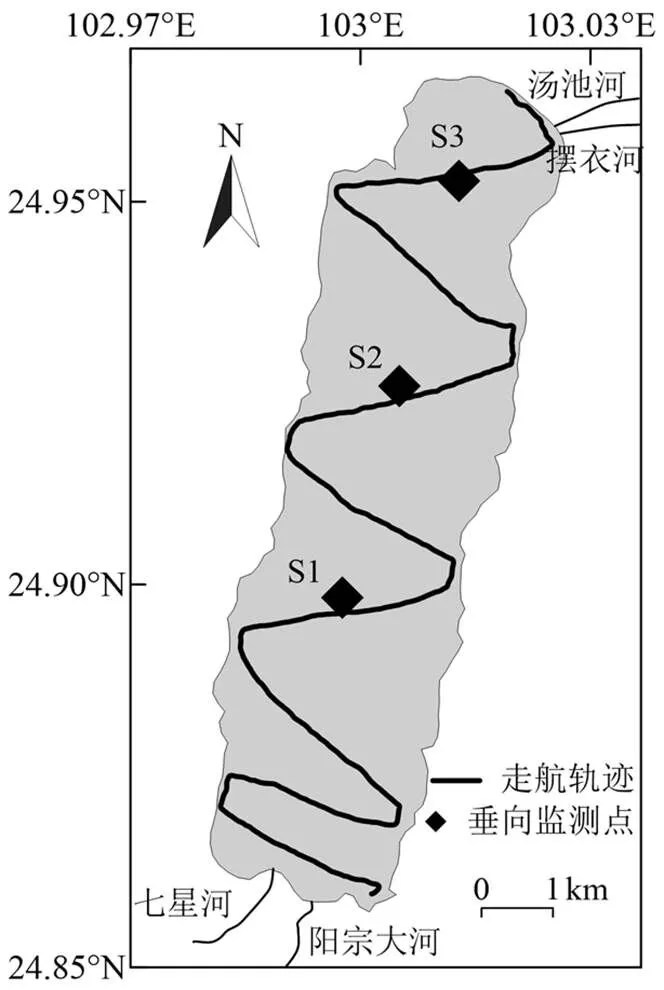
图1 走航轨迹及监测点分布
利用手持式气象站(YGY-QXY,中国)监测风速和气温等气象要素.溶解氧饱和度、电导率、叶绿素a、水温、pH值和水深采用多参数水质分析仪(YSI- EXO,美国)进行测定.走航水深使用声学多普勒流速剖面仪(RDI RiverRay ADCP,美国)测定,并同步记录船只移动过程的地理坐标.
水体溶解CH4浓度及其稳定碳同位素监测分为表层水体和垂向剖面2个部分.水体溶解CH4浓度及其稳定碳同位素采用新型快速水-气平衡装置(FaRAGE)[13-14]及便携式温室气体分析仪(Picarro G2301,美国)连续测定,待测水体和载气(氮气)以恒定流量进入水-气平衡装置,载气形成的微气泡与待测水体发生水气交换并达到动态顶空平衡,该装置具有响应时间短(12s)、测量精度高(误差小于0.5%)的优点.选取S1、S2和S3共3个监测点进行垂向剖面监测,垂向剖面溶解CH4浓度及其稳定碳同位素监测使用潜水泵从水体表层到底层分层抽取水,采用相同方法测定不同深度水体溶解CH4浓度,且与多参数水质分析仪监测同步.
1.3 数据处理与统计分析
淡水中溶解氧饱和度计算公式为[17]:
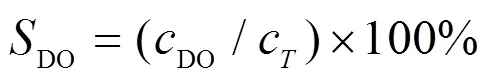
式中:DO为溶解氧饱和度,%;DO为实测溶解氧质量浓度,mg/L;c为观测温度下的饱和溶解氧质量浓度,mg/L.计算公式为:
c=477.8/(+32.36) (2)
式中:为实测水温,℃.
稳定碳同位素的组成利用公式(3)计算.

式中:sa和s1分别表示待测样品和标准样的同位素比值,13C/12C对应于国际标准ViennaPDB.
薄边界层法计算水-气界面气体通量利用公式(4)计算:
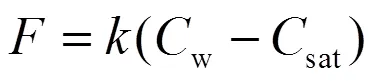
式中:为水-气界面扩散通量,mol/(m2·h);为气体交换系数,cm/h;sat为该气体相对于上方空气而言平衡时表层水体中的浓度,mol/L;W为该气体在表层水体中的浓度,mol/L.
为便于不同气体传输速率的比较,采用式(5)对进行标准化[18]:
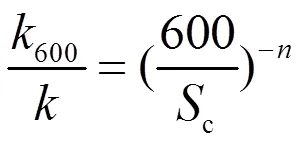
式中:c为给定气体在相应温度下的CH4的Schmidt数,本研究利用Wanninkhof等[19]提出的方法计算c;600是当Schmidt数为600时的气体传输速率;是与风速相关的系数,由于所有10m高度的风速均小于<3.7m/s,本文中取值为2/3[20].
气体传输速率600使用风速模型[21]计算:
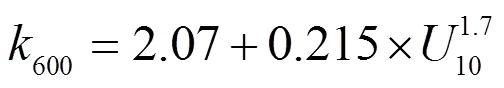
式中:10为水面10m高处的风速,m/s,可由实测风速和观测高度计算[22].
采用Spearman相关性分析探求表层溶解CH4浓度与各理化因子的相关性,使用自展分析进行重抽样,评估数据样本量大小对通量估算的影响.
2 结果与分析
2.1 环境因子
如表1和图2所示,表层水体溶解氧饱和度为52.17%~75.93%,表现为南部湖区大于北部湖区;电导率为421.82~427.56mS/cm,湖泊北部大于南部;表层水体水温为18.56~20.18℃,湖泊北部高于南部;叶绿素a浓度为1.82~12.37mg/L,空间上呈现南北高、中部低的特征;pH值为8.23~8.55,呈现弱碱性,南部湖区大于北部湖区,整个湖泊差异较小.

表1 层水体理化性质及溶解甲烷浓度(n=1554)
如图3所示,受秋季气温、光照等气象因素的影响,垂向上水温均存在分层现象,但温跃层深度和厚度有所差异.3个监测点溶解氧饱和度在0~6.0m先增大后减小,S1和S2监测点溶解氧饱和度在2.5m水深处达到最大值,S1监测点为71.71%,S2监测点为75.92%,而S3监测点在3.8m水深处达到最大值(73.50%),各监测点氧跃层以下溶解氧饱和度均维持一个稳定的低值(<15.01%).3个监测点垂向剖面中叶绿素a浓度最大值均位于3m水深附近,底部叶绿素a浓度均接近0,S2监测点叶绿素a浓度表现出双峰现象.3处监测剖面电导率变化趋势一致,在0~18.0m水深处保持稳定,而在18.0~20.0m快速上升.
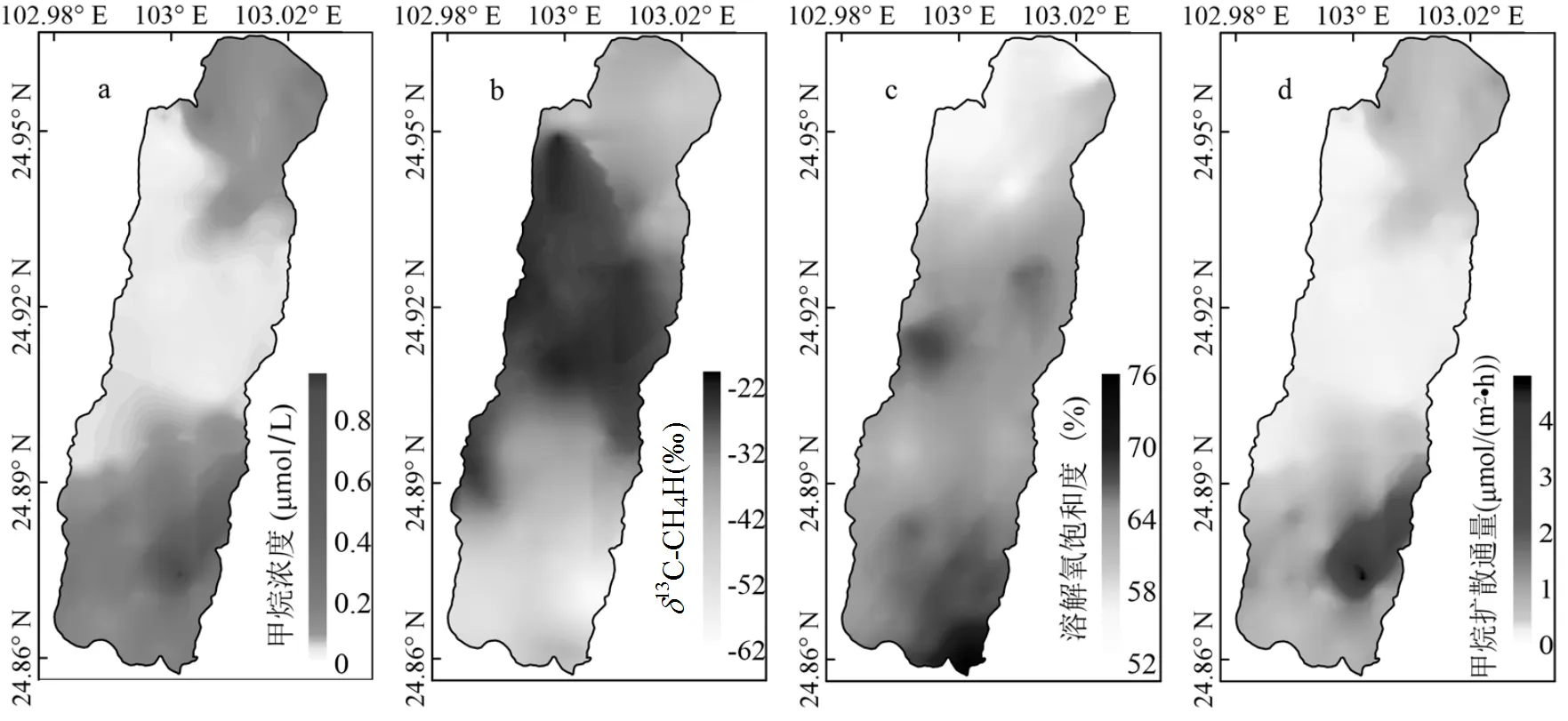
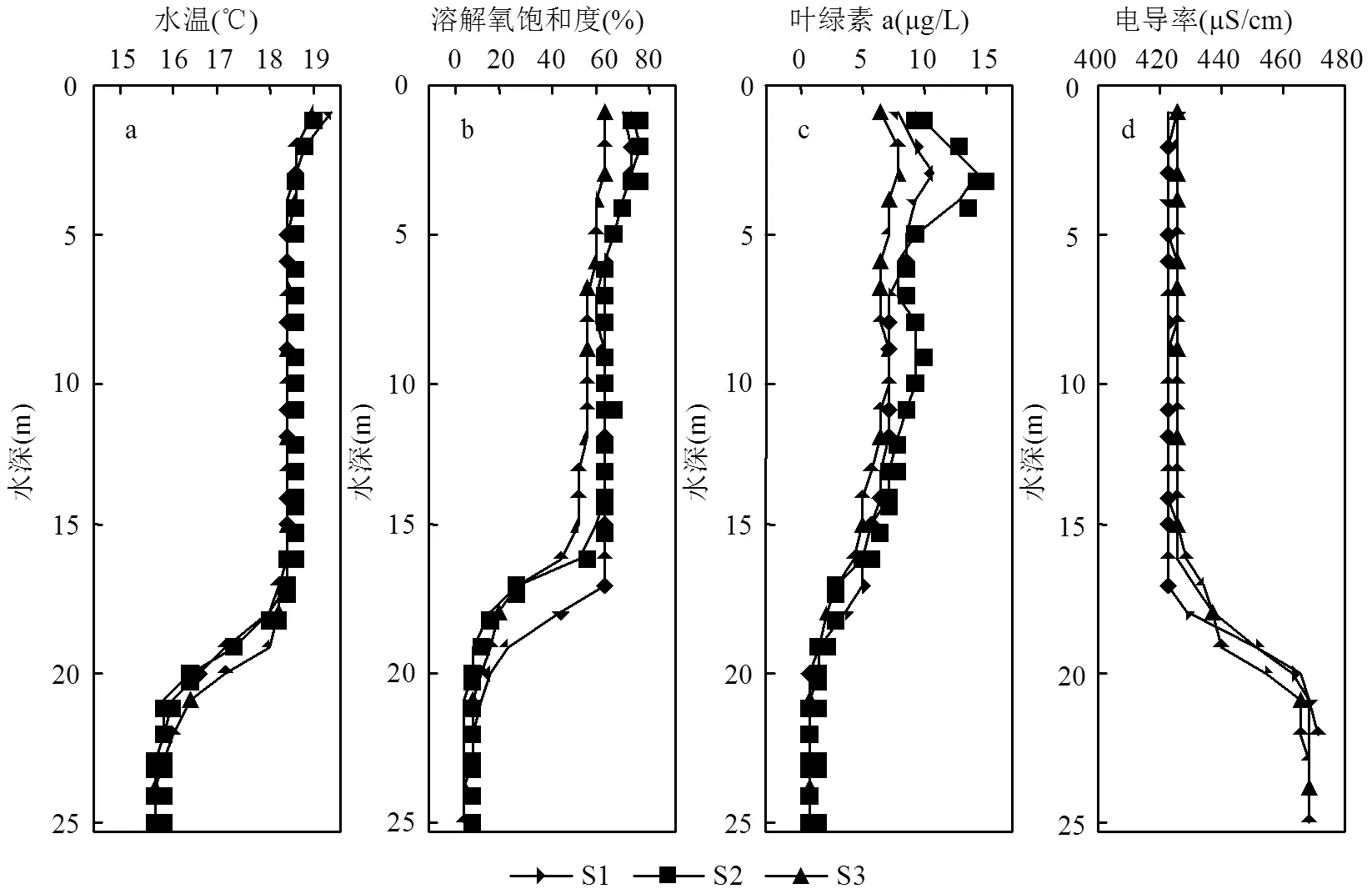
图3 垂向剖面中各水环境因子分布
2.2 CH4扩散通量和水体溶解CH4浓度分布
CH4扩散通量为0.61~4.85μmol/(m2×h),平均值为(1.38±1.03)μmol/(m2×h).表层水体溶解CH4浓度为0.02~0.97μmol/L,平均值为(0.14±0.15)μmol/L.CH4扩散通量和表层水体CH4浓度空间分布十分相似,均表现为南北高、中间低的特点(图2a、2d).如图4所示,各监测点垂向剖面溶解CH4浓度分布特征相似,但数值上存在较大差异.S1监测点表层水体溶解CH4浓度为0.43μmol/L,在0~18m水深处表现为先降低后增加,7m水深处达到最低值0.13μmol/L,18m水深以下溶解CH4浓度快速增加,在底层达到最大值104.98μmol/L.相较于其他监测点,S2监测点表层水体溶解CH4浓度最低(0.04μmol/L),在0~18m水深处溶解CH4浓度变化较小(0.04~0.03μmol/L),20m水深以下溶解CH4浓度快速增加,在底层达到最大值94.71μmol/L.S3监测点表层到底层溶解CH4浓度先降低后增加,表层水体溶解CH4浓度为0.12μmol/L, 0~3.0m水深处快速下降,最低值出现在5m水深处(0.07μmol/L),15m水深以下溶解CH4浓度快速增加,在底层达到最大值107.67μmol/L.
2.3 表层水体和垂向剖面中δ13C-CH4分布
表层水体13C-CH4为-60.75‰~-20.12‰,平均值为(-37.99±10.70)‰, 如图2b所示,空间分布表现为南端和北端偏负,中部偏正.如图4所示,3个监测点垂向剖面中13C-CH4表现出相似的变化趋势.S1监测点13C-CH4为-31.07‰~-68.49‰,0~16m水深处13C-CH4变化较小(-31.07‰~-41.64‰),16~21m水深处13C-CH4快速下降,21m水深处13C-CH4为-67.28‰,底部21~22m水深处变化较小.S2监测点13C-CH4为-31.27‰~-66.73‰,0~15m水深处13C-CH4变化较小.15m水深以下13C-CH4快速下降,21m水深处13C-CH4为-66.67‰,21~25m水深处变化较小.S3监测点0~16m水深处13C-CH4变化较小(-31.27‰~-39.03‰),16~20m水深处13C-CH4快速下降,底部20~25m水深处13C-CH4保持稳定((-66.78±0.87)‰)
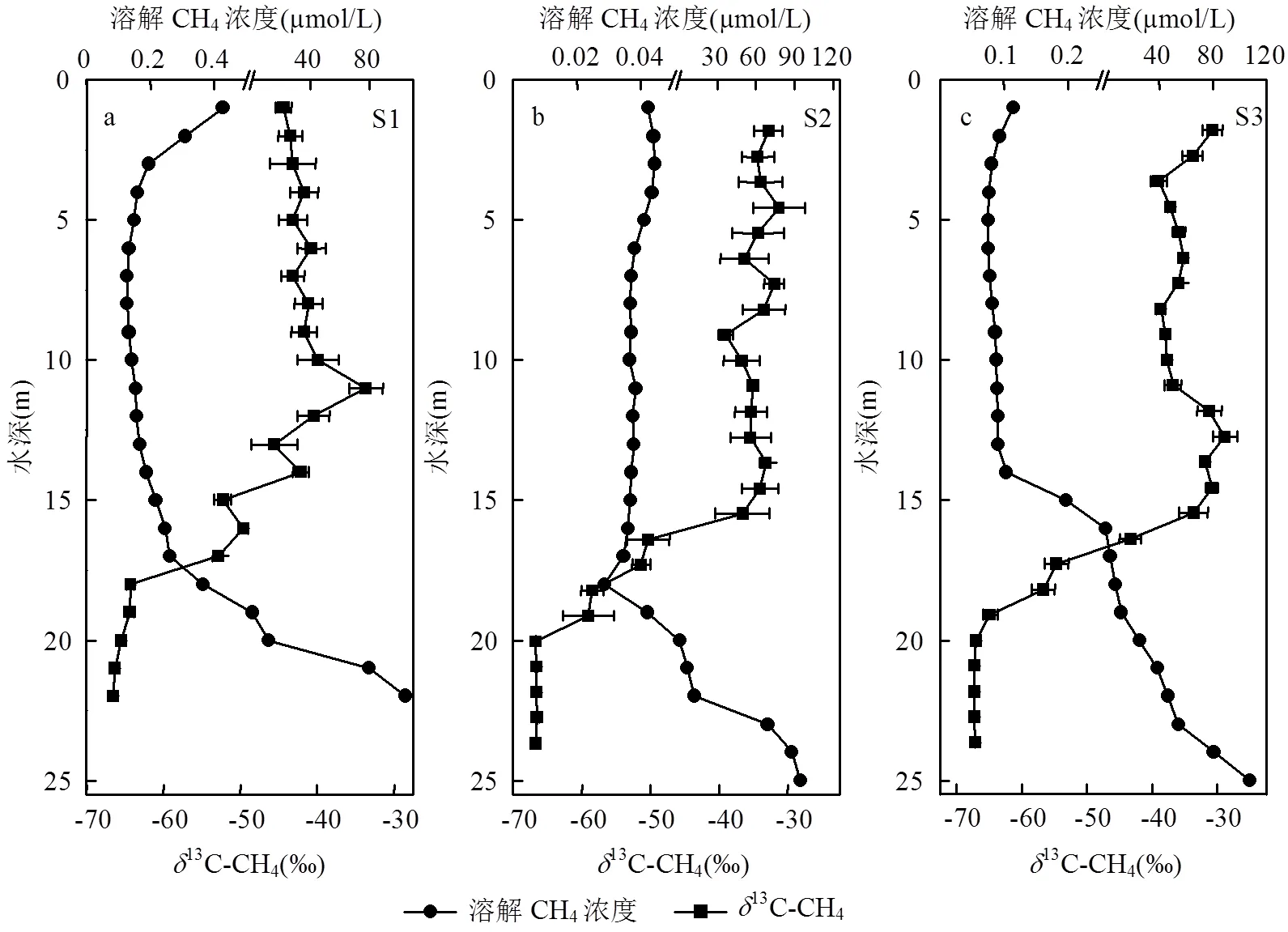
图4 垂向剖面中溶解CH4浓度及13C-CH4分布
3 讨论
3.1 溶解CH4浓度分布规律及主要影响因素
如图2所示,溶解CH4浓度空间分布表现为南北高、中间低的特点.表层水体溶解CH4浓度与水深表现出极显著负相关关系,因为水深是影响湖泊CH4氧化消耗和传输的重要因素.浅水区CH4浓度更高,原因在于风浪扰动更容易传递到湖泊底部.一方面,波浪引起强烈的压力振荡[23],增强沉积物孔隙水-上覆水的交换[24],减小沉积物-水界面扩散边界层的厚度,导致沉积物扩散通量增加[25].另一方面,波浪引起颗粒再悬浮,导致孔隙水中的CH4直接向上覆水中释放[26].
水温是影响湖泊CH4分布的重要因素之一.一方面,水温升高通过增加产甲烷菌和甲烷氧化菌活性提高甲烷产率和消耗速率[27-29],例如张成[30]的室内培养试验表明,25℃时甲烷产率为15℃时的近10倍,15℃甲烷消耗速率为0℃时的1.77倍.另一方面,水温升高会降低CH4在水体中的溶解度.由观测结果可知, S1~S3 3个监测点垂向剖面中水温分布基本一致(图2),湖域表层水体水温变化范围为18.56~20.18℃(图2f),而表层水体CH4浓度为0.02~0.97μmol/L(图2a),虽然表层水体水温与溶解CH4浓度表现出负相关(表2),但较小的水温差异对CH4溶解度及CH4产生和消耗速率的影响十分有限,水温并不是造成阳宗海溶解CH4浓度空间异质性的主要原因.
室内培养试验表明,沉积物生成的CH4稳定碳同位素13C-CH4约为-70‰,CH4氧化伴随着强烈的同位素分馏,较轻的12CH4优先被氧化,导致13C-CH4偏正[31].本次监测结果显示,13C-CH4空间分布表现为南端和北端浅水区偏负,中部深水区偏正,表明中部深水区产自沉积物的CH4向表层水体传输路径长,更多的CH4被氧化消耗,到达表层水体CH4较少[32],降低了表层水体溶解CH4浓度.由图4可知, S1~S3三个监测点底层水体溶解CH4浓度远高于中上层,且底层水体13C-CH4明显偏负,表明大量产生于沉积物的CH4积累在底层.温跃层附近CH4浓度快速下降,13C-CH4快速上升,表明CH4在温跃层附近发生氧化,消耗了大量CH4并导致13C-CH4偏正.虽然S2和S3监测点水深相差较小,但S3监测点更靠近湖泊北部的浅水区,S2监测点则位于中心湖区,高浓度CH4由浅水区向中心湖区侧向扩散传输的距离远,CH4氧化消耗路径加长使得更多的CH4被氧化,导致S2监测点中上层水体溶解CH4浓度远低S3监测点.
湖泊水体分层是影响水体溶解CH4浓度的重要因素.湖泊水体分层结构的打破往往出现在季节性混合期.此期间积累在温跃层以下的高浓度CH4由于水体的快速掺混而向上迁移,形成甲烷的快速排放期.Fernández等[33]在德国南部Mindelsee湖的研究发现,夏季水温分层期间水体底部存储的甲烷约46%在秋季湖水混合期被释放,占到全年CH4扩散通量的80%.大风和降雨事件对水温分层的扰动更为迅速[34],Mindelsee湖在秋季大风时期,浅水区底层储存CH4快速进入混合层,而深水区受影响较小.由图4可知,温跃层之上垂向剖面中溶解CH4浓度虽然远低于底层,但依然为过饱和,表现为S1>S3>S2监测点,其原因在于水体的垂向掺混导致底层高浓度CH4向中上层水体的迁移[23,35].本次监测正值湖泊水温分层的消退期,随着气温的降低,表层水温持续下降,水体垂向掺混加剧,底层积累的部分CH4通过冷却对流进入混合层,混合层内CH4的消耗量低于深层CH4的补给量,导致了混合层内CH4的过饱和.相较于S2和S3监测点,S1监测点水深小,表层扰动可传递到有着高浓度CH4的底层,促进底层储存的CH4进入上层水体,提高混合层内溶解CH4浓度.
靠近岸边的浅水区通常直接接收污水排放、降雨径流和河流汇入,新鲜有机物的增加可能提高沉积物CH4产量[8].事实上污染物中新鲜有机碳的输入可刺激表层沉积物中的CH4生成,也通过溶解的不稳定有机物(如乙酸盐、丙酸盐)的扩散刺激深层沉积物中的CH4生成[36].阳宗海北部入流河流为摆衣河,南部入流为阳宗大河和七星河(图1),入流河流可能携带居民区的大量污水进入阳宗海.梅涵一等[37]对阳宗海流域农村水污染的调查研究表明,农村污水对阳宗海造成很大的污染风险.李楠[38]研究发现,阳宗海南部湖区表层沉积物总有机碳含量最高,指示南部入流可能携带大量有机物进入阳宗海,在南部湖区沉积,成为促进CH4产生的重要因素.
水生植物的生长对CH4的生成和传输有重要影响:一方面,水生植物气孔组织可促进CH4从沉积物向水体的释放[8];另一方面,水生植物生长和死亡带来丰富的碳积累,促进沉积物CH4的产生[39].潘义宏[40]在阳宗海南部和北部电厂附近采集到金鱼藻、黑藻、小叶眼子菜等水生植物,本次监测过程中在浅水区可观察到大量沉水植物和水藻.阳宗海表层水体溶解CH4浓度与叶绿素a浓度呈现极显著正相关关系(表2),与Wang等[41]在太湖的研究结论相似.新近研究表明,CH4可在湖泊有氧水体中产生,有氧水体缺氧微环境中的产甲烷古生菌产甲烷[42]、藻类的直接产生[43]和甲基膦酸酯脱甲基化[44]可能是产生此现象的原因.Gunthel等[45]在Stechlin湖进行的野外监测和室内培养试验表明,蓝细菌和硅藻等浮游植物可促进甲烷的生成,并伴随着13C-CH4的偏正.本次监测结果显示,中上层水体叶绿素a浓度的高值出现在3m水深处,但上层水体溶解CH4浓度的高值并未出现在这一水深处.S3监测点表层水体13C-CH4偏正,与上层水体溶解CH4浓度的高值位于同一水深处,但S1和S3监测点并未表现出相似特征.溶解CH4浓度、叶绿素a和13C-CH4的分布特征表明,阳宗海表层水体溶解CH4过饱和是否与有氧CH4产生有关,尚需要进一步的研究.

表2 阳宗海表层溶解CH4浓度与理化参数皮尔逊相关系数(N=1554)
注:*为<0.05,**为<0.01.
3.2 溶解CH4高空间分辨率监测的意义
薄边界层法是一种被广泛使用的水-气界面扩散通量估算方法[46],而精确的表层水体溶解CH4浓度是进行通量估算的重要前提.现有研究中,多采用少数点位的监测代表湖泊整体水平[6-7],但是湖泊表层水体溶解CH4浓度往往具有很大的空间异质性[47].例如本次高空间分辨率的走航式监测发现,阳宗海表层水体溶解CH4浓度为0.02~0.97μmol/L,相差近48倍,这种空间分布上的巨大差异给水-气界面扩散通量的估算带来了巨大的潜在误差.为进一步评估这种误差,本研究采用自展分析进行了模拟采样,探究采样点数量的大小对通量估算的影响.本次走航式监测共获得1554个表层水体溶解CH4浓度数据,采用薄边界层法求得1554个扩散通量数据,自展分析即基于1554个通量值进行.以采样点数量为5的第一组为例,从1554个通量数据中随机提取5个不重复的数据并计算其平均值5,重复此过程1000次,得到1000个5,第2~6组的采样点数量分别为10, 50, 100, 500和1000,计算方法与第1组一致.模拟采样结果表明,平均CH4扩散通量的标准差从5个采样点数量时的0.24μmol/(m2·h)持续下降到1000个采样点数量时的0.01μmol/(m2·h)(图5).由此可见,增加采样点数量可以有效降低整个湖泊排放量估算的不确定性,高空间分辨率的表层水体溶解CH4浓度监测对于准确估算CH4扩散通量十分重要.
基于少数采样点浓度监测的扩散通量估算在未来很长一段时间内仍然是不可缺少的,考虑到溶解CH4浓度的空间异质性,通量的准确估算往往需要大量采样点的浓度数据,时间和人力等因素限制了采样点数量的增加,如何通过最少的采样点数量得到相对准确的通量估算成为亟待解决的问题.Paranaíba等[11]在大量监测数据的基础上对巴西3个热带水库进行了模拟采样,发现水库面积是影响单位面积所需最小采样点数量的重要因素,这是因为初级生产力、营养状态、汇流和浅水区沉积物CH4输入的异质性对小型水库扩散通量影响更大.然而针对湖泊最小采样点数量的定量分析尚未见报道,本研究进一步采用自展分析进行模拟采样,探讨单位面积所需最小采样量.自展分析数据为本次走航式监测结合薄边界层法计算获得的1554个扩散通量数据,且假定1554个扩散通量数据的均值为真实通量,模拟采样将每平方公里所需最小采样点数量设置为0.1~5公差为0.1的50个数,若模拟采样计算所得95%通量值落在真实通量±20%范围内,则认为满足通量估算的精度要求.结果表明,相对准确估算阳宗海扩散通量所需最小采样点数量约为3.7个/km2(图6).虽然不同湖泊的空间异质性特征存在差异,但该结果能够为湖库水域甲烷浓度监测及通量估算提供科学参考.
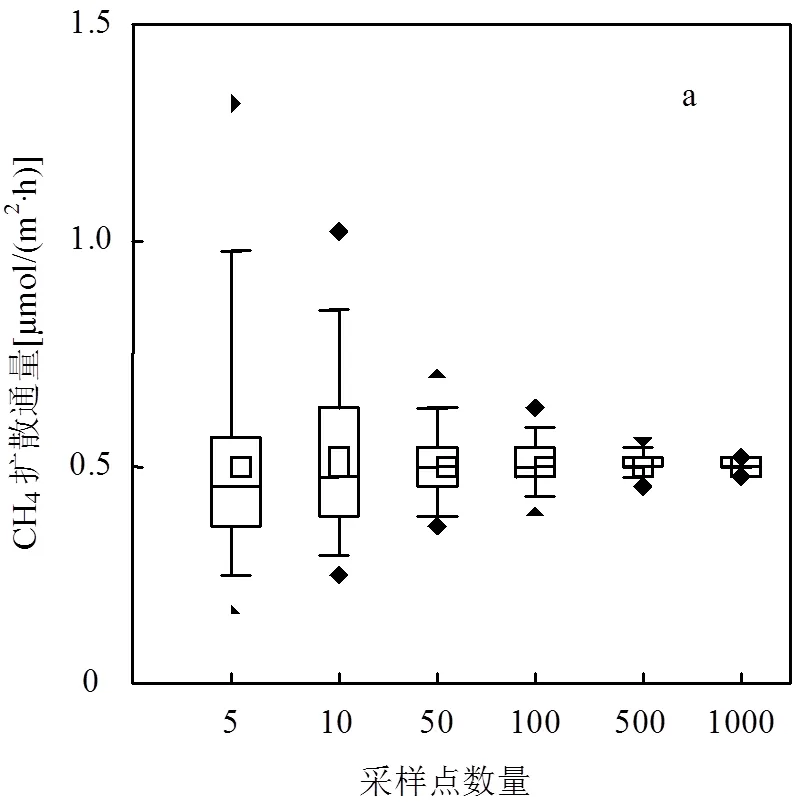
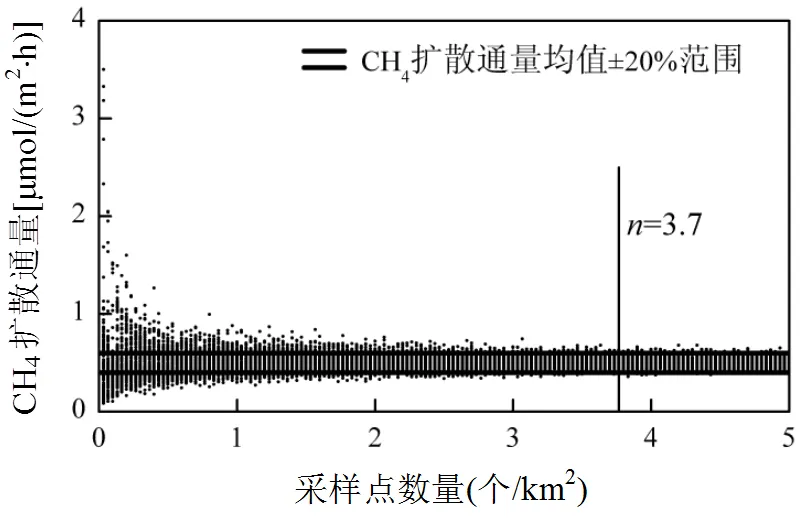
图6 相对准确估算阳宗海扩散通量所需的最小采样点数量
4 结论
4.1 2020年11月10日阳宗海表层水体溶解CH4浓度为0.02~0.97μmol/L,表现为大气甲烷的源.空间上呈现出南北部高,中部低的分布特征,与水生植物分布、入湖河流输出和水深等因素密切相关.
4.2 监测期间存在水温分层现象,湖泊不同区域垂向剖面溶解CH4浓度分布形式一致,高浓度的CH4积累在缺氧的底层水体中,底层CH4在向上扩散的过程中,氧化消耗作用明显,上部混合层溶解CH4浓度受垂向掺混和侧向输移影响显著.
4.3 基于1554个扩散通量数据进行的模拟采样表明,采样点数量的增加可以有效降低整个湖泊排放量估算的不确定性,基于少量采样点监测数据进行CH4排放估算具有较大不确定性,相对准确估算阳宗海CH4扩散通量所需最小采样点数量约为3.7个/km2,高空间分辨率的监测对于湖库碳排放的准确估计是必要的.
[1] Bastviken D, Tranvik L J, Downing J A, et al. Freshwater methane emissions offset the continental carbon sink [J]. Science, 2011,331 (6013):50-50.
[2] Bastviken D, Cole J, Pace M, et al. Methane emissions from lakes: dependence of lake characteristics, two regional assessments, and a global estimate. Global Biogeochem Cycles [J]. Global Biogeochemical Cycles, 2004,18(4):GB4009.
[3] 张 佩,王晓锋,袁兴中.等.中国淡水生态系统甲烷排放基本特征及研究进展[J]. 中国环境科学, 2020,40(8):3567-3579.
Zhang P, Wang X F, Yuan X Z, et al. General characteristics and research progress of methane emissions from freshwater ecosystems in China [J]. China Environmental Science, 2020,40(8):3567-3579.
[4] 龚琬晴,文帅龙,王洪伟,等.大黑汀水库夏秋季节温室气体赋存及排放特征 [J]. 中国环境科学, 2019,39(11):4611-4619.
Gong W Q, Wen S L, Wang H W, et al. Characteristics of greenhouse gas occurrence and emission in summer and autumn of Daheiting Reservoir [J]. China Environmental Science, 2019,39(11):4611-4619.
[5] Pighini S, Ventura M, Miglietta F, et al. Dissolved greenhouse gas concentrations in 40lakes in the Alpine area [J]. Aquatic Sciences, 2018,80(3):1-13.
[6] Zhang L, Liao Q, Gao R, et al. Spatial variations in diffusive methane fluxes and the role of eutrophication in a subtropical shallow lake [J]. Science of the Total Environment, 2021,22:1674–1682.
[7] Li B, Gu Q, Miao Y, et al. Methane distribution patterns along a transect of Lake Fuxian, a deep oligotrophic lake in China [J]. Environmental Science and Pollution Research, 2020,27(21):25848- 25860.
[8] Xiao Q, Zhang M, Hu Z, et al. Spatial variations of methane emission in a large shallow eutrophic lake in subtropical climate [J]. Journal of Geophysical Research-Biogeosciences, 2017,122(7):1597-1614.
[9] Yang P, Yang H, Sardans J, et al. Large spatial variations in diffusive CH4fluxes from a subtropical coastal reservoir affected by sewage discharge in southeast China [J]. Environmental Science & Technology, 2020,54(22):14192-14203.
[10] 张 斌.金沙江下游梯级水库水体CH4、CO2分布与源汇特征研究[D]. 重庆:中国科学院大学(中国科学院重庆绿色智能技术研究院), 2019.
Zhang B. Rolubility and air-water fluxes of CH4and CO2of cascade reservoirs in lower reaches of Jinsha River [D]. Chongqin: University of Chinese Academy of Sciences, 2019.
[11] Paranaíba J, Barros N, Mendonça R, et al. Spatially resolved measurements of CO2and CH4concentration and gas-exchange velocity highly influence carbon-emission estimates of reservoirs [J]. Environmental Science & Technology, 2017,52(2):607–615.
[12] Li B, Gu Q J, Miao Y Q, et al. Methane distribution patterns along a transect of Lake Fuxian, a deep oligotrophic lake in China [J]. Environmental Science and Pollution Research, 2020,27(21):25848- 25860.
[13] Xiao S, Liu L, Wang W, et al. A fast-response automated gas equilibrator (FaRAGE) for continuous in situ measurement of CH4and CO2dissolved in water [J]. Hydrology and Earth System Sciences, 2020,24(7):3871-3880.
[14] 王 炜,肖尚斌,雷 丹,等.快速监测水体溶解痕量气体浓度的装置及方法:中国[P]. 2018-07-09.
[15] 张玉玺,向小平,张 英,等.云南阳宗海砷的分布与来源[J]. 环境科学, 2012,33(11):3768-3777.
Zhang Y X, Xiang X P, Zhang Y, et al. Distribution and sources of arsenic in Yangzonghai Lake [J]. Environmental Science, 2012,33(11): 3768-3777.
[16] 邓丽仙,孔桂芬,杨绍琼,等.阳宗海湖泊水质与来水量的关系研究[J]. 水文, 2008,28(4):43-45.
Deng L X, Kong G F, Yang S Q, et al. Study on the relationship between water quality and water quantity of Lake Yangzong [J]. Journal of China Hydrology, 2008,28(4):43-45.
[17] 杨 凡,纪道斌,王丽婧,等.三峡水库汛后蓄水期典型支流溶解氧与叶绿素a垂向分布特征 [J]. 环境科学, 2020,41(5):2107-2115.
Yang F, Ji D B, Wang L J, et al. Vertical distribution characteristics of dissolved oxygen and chlorophyll a in typical tributaries during the impoundment period of the Three Gorges Reservoir [J]. Environmental Science, 2020,41(5):2107-2115.
[18] Jähne B, Libner P, Fischer R, et al. Investigating the transfer processes across the free aqueous viscous boundary layer by the controlled flux method [J]. Tellus B, 1989,41(2):177-195.
[19] Wanninkhof R. Relationship between wind speed and gas exchange over the ocean [J]. Limnology and Oceanography: Methods, 1992, 12(6):1541-5856.
[20] Liss P, Merlivat L. The role of air-sea exchange in geochemical cycling [M]. Netherlands: Springer, 1986:113-127.
[21] Cole J, Caraco N. Atmospheric exchange of carbon dioxide in a low-wind oligotrophic lake measured by the addition of SF6 [J]. Limnology and Oceanography, 1998,43(4):647-656.
[22] Amorocho J, Devries J J. A new evaluation of the wind stress coefficient over water surfaces [J]. Journal of Geophgsical Research: Oceans, 1980,85(C1):433-442.
[23] Hofmann H, Lorke A, Peeters F. The relative importance of wind and ship waves in the littoral zone of a large lake [J]. Limnology and Oceanography, 2008,53(1):368-380.
[24] Precht E, Franke U Polerecky L, et al. Oxygen dynamics in permeable sediments with wave-driven pore water exchange [J]. Limnology and Oceanography, 2004,49(3):693-705.
[25] Lorke A, Peeters F. Toward a unified scaling relation for interfacial fluxes [J]. Journal of Physical Oceanography, 2006,36(5):955-961.
[26] Nielsen P. Coastal bottom boundary layers and sediment transport [Z]. World Scientific, 1992:343-345.
[27] Gudasz C, Bastviken D, Steger K, et al. Temperature-controlled organic carbon mineralization in lake sediments [J]. Nature, 466 (7305):478-481.
[28] Liikanen A, Flöjt L, Martikainen P. Gas dynamics in eutrophic lake sediments affected by oxygen, nitrate, and sulfate [J]. Journal of Environmental Quality, 2002,31(1):338-349.
[29] Segers R. Methane production and methane consumption: A review of processes underlying wetland methane fluxes [J]. Biogeochemistry, 1998,41(1):23-51.
[30] 张 成.富营养化池塘甲烷排放过程与机制研究[D]. 武汉:中国地质大学, 2018.
Zhang C. On the process and mechamism of methane emission from eutrophic ponds [D]. Wuhan: China University of Geosciences, 2018.
[31] Barker J F, Fritz P. Carbon isotope fractionation during microbial methane oxidation [J]. Nature, 1981,293(5830):289-291.
[32] Lei D, Liu J, Zhang J, et al. Methane oxidation in the water column of Xiangxi Bay, Three Gorges Reservoir [J]. Clean-Soil Air Water, 2019,47(9):1863-0650.
[33] Fernandez J E, Peeters F, Hofmann H. Importance of the autumn overturn and anoxic conditions in the hypolimnion for the annual methane emissions from a temperate lake [J]. Environmental Science & Technology, 2014,48(13):7297-7304.
[34] Peter F, Bernward T, Ralf C. Oxidation of methane in the oxic surface layer of a deep lake sediment (Lake Constance) [J]. Fems Microbiology Ecology, 1990,73(2):149-158.
[35] Hofmann H, Federwisch L, Peeters F. Wave-induced release of methane: Littoral zones as a source of methane in lakes [J]. Limnology and Oceanography, 2010,55(5):1990-2000.
[36] Schwarz J I K, Eckert W, Conrad R. Response of the methanogenic microbial community of a profundal lake sediment (Lake Kinneret, Israel) to algal deposition [J]. Limnology and Oceanography, 2008,53 (1):113-121.
[37] 梅涵一,刘云根,梁启斌,等.阳宗海流域冬季典型农村污水污染特征及水质评价[J]. 水资源保护, 2017,33(2):67-73.
Mei H Y, Liu Y G, Liang Q B, et al. Pollution characteristics and water quality evaluation of typical rural sewage in winter in Yangzonghai Lake Basin [J]. Water Resources Protection, 2017,33(2):67-73.
[38] 李 楠.阳宗海表层沉积物有机质的空间分布特征分析与环境评价[D]. 昆明:云南师范大学, 2017.
Li N. Analysis of spatial distribution characteristics and environmental assessment of organic matter in surface sediments of Lake Yangzong [D]: Kunming: Yunnan Normal University, 2017.
[39] Raghoebarsing A A, Smolders A J P, Schmid M C, et al. Methanotrophic symbionts provide carbon for photosynthesis in peat bogs [J]. Nature, 436(7054):1153-1156.
[40] 潘义宏.阳宗海大型水生植物对砷的吸收、富集特征及机理[D]. 昆明:昆明理工大学, 2011.
Pan Y H. Arsenic uptake, accumulation and possible mechanism in macrophytes growing in Yangzong Lake, Yunnan Province [D]. Kunming: University of Science and Technology, 2011.
[41] Wang H J, Lu J W, Wang W D, et al. Methane fluxes from the littoral zone of hypereutrophic Taihu Lake, China [J]. Journal of Geophysical Research-Atmospheres, 2006,111(D17):D17109.
[42] Bii-Ionescu M, Ionescu D, Günthel M, et al. Oxic methane cycling: New evidence for methane formation in oxic lake water [M]. Biogenesis of Hydrocarbons, 2019:379-400.
[43] Gunthel M, Donis D, Kirillin G, et al. Contribution of oxic methane production to surface methane emission in lakes and its global importance [J]. Nature Communications, 2019,10:5497.
[44] Carini P, White A E, Campbell E O, et al. Methane production by phosphate-starved SAR11chemoheterotrophic marine bacteria [J]. Nature Communications, 2014,5(1):1-7.
[45] Gunthel M, Klawonn I, Woodhouse J, et al. Photosynthesis-driven methane production in oxic lake water as an important contributor to methane emission [J]. Limnology and Oceanography, 2020,65(12): 2853-2865.
[46] Cole J, Caraco N F. Atmospheric exchange of carbon dioxide in a low-wind oligotrophic lake measured by the addition of SF6 [J]. Limnology & Oceanography, 1998,43(4):647-656.
[47] Hofmann H. Spatiotemporal distribution patterns of dissolved methane in lakes: How accurate are the current estimations of the diffusive flux path [J]. Geophysical Research Letters, 2013,40(11):2779-2784.
Spatial heterogeneity of dissolved methane in a plateau lake: a case study in Yangzonghai Lake in autumn.
ZHENG Xiang-wang1,2, CHEN Min1,2,3*, XIAO Shang-bin1,2,3, WANG Sheng-rui4,5, WANG Xue-zhu2, CHEN Wei2, LIU Jia2, XU Hao-ting2
(1.Engineering Research Center of Eco-environment in Three Gorges Reservoir Region, Yichang 443002, China;2.College of Hydraulic and Environmental Engineering, China Three Gorges University, Yichang 443002, China;3.Hubei Field Observation and Scientific Research Stations for Water Ecosystem in Three Gorges Reservoir,Yichang 443002, China;4.College of Water Sciences, Beijing Normal University, Beijing 100875, China;5.Yunnan Key Laboratory of Pollution Process and Management of Plateau Lake-Watershed, Kunming 650034, China)., 2022,42(2):834~842
Near-surface and vertical profiles of dissolved CH4concentrations were measured at a high resolution using the new fast-response automated gas equilibrator (FaRAGE) connected to a greenhouse gas analyzer at Yangzonghai Lake in November 2020, to investigate the spatial pattern of dissolved CH4and its driving factors. Results showed that dissolved CH4concentrations of surface water ranged between 0.02 and 0.97μmol/L, indicating a net source of atmosphere CH4. The dissolved CH4was relatively higher in the north and south parts of the lake, but lower in the middle area, which was mainly influenced by aquatic plants distribution, discharge from inflow rivers and topographical conditions. Vertical profiles of dissolved CH4at different spots of the lake exhibited relatively consistent pattern, while CH4was more significantly oxidized in the middle section. The bootstrap analysis suggested that estimates of CH4emission derived from fewer measurements were subjected to potentially large biases, and the minimum number of sampling sites that guaranteed an accurate estimation of diffusive CH4flux at Yangzonghai Lake was 3.7per km2. It was necessary to perform high-resolution observations of CH4concentration for an accurate estimation of carbon emission from lakes or reservoirs.
greenhouse gas;dissolved concentration;spatial distribution;flux;Yangzonghai Lake
X524
A
1000-6923(2022)02-0834-09
郑祥旺(1996-),男,湖北宜昌人,三峡大学硕士研究生,主要从事淡水生态系统碳循环研究.发表论文2篇.
2021-06-21
国家自然科学基金资助项目(41807513,51979148);湖北省自然科学基金创新群体项目(2019CFA032)
* 责任作者, 副教授, minchen@ctgu.edu.cn
