Y型双支架取栓治疗急性大脑中动脉M1段分叉部闭塞脑梗死7例
2022-02-23李水仙陈星宇阳清伟郑维红陈中杰陈良义朱仁敬金首跃
李水仙, 陈星宇, 阳清伟, 郑维红, 陈中杰, 陈良义, 朱仁敬, 金首跃,林 威
急性大血管闭塞缺血性脑卒中病情重,自然病程预后差,静脉溶栓血管再通率低、疗效欠佳[1],2015年以来机械取栓,尤其是支架取栓逐渐成为首选治疗方案[2-3]。大动脉分叉部闭塞由于血管形态、血栓负荷等介入再通困难、耗时长、疗效差[4],目前文献报道多为颈内动脉末端分叉部闭塞行双支架取栓[5],对大脑中动脉(middle cerebral artery,MCA)M1段分叉部急性闭塞再通研究较前者少[6-7]。因此,本研究探讨Y型双支架取栓技术治疗急性MCAM1段分叉部闭塞患者的有效性、安全性及预后,为将来更好地治疗提供依据。
1 材料与方法
1.1 研究对象
收集2017年5月至2020年9月在厦门大学附属中山医院接受Y型双支架取栓治疗的连续7例急性MCA-M1段分叉部闭塞脑梗死患者临床资料。其中男2例,女5例;年龄为(58.6±12.7)岁(36~70岁),入院时美国国立卫生研究院卒中量表(NIHSS)评分为(17.7±3.9)分(13~23分)。入选标准:①DSA造影证实M1段分叉部闭塞累及上下干,大脑前动脉或大脑后动脉通过脑膜支代偿供血;②发病至股动脉穿刺时间<6 h 6例,15 h 1例[入院多模态MRI示MCA闭塞、弥散加权成像(DWI)<70 mL、动脉自旋标记(ASL)/DWI>1.8]。排除标准:①CT示颅内出血;②CT或MRI示大面积脑梗死;③既往严重残疾。
1.2 Y型双支架取栓治疗
2例发病至股动脉穿刺时间<4.5 h患者取栓前接受重组组织型纤溶酶原激活剂(rt-PA)(0.9 mg/kg)静脉溶栓治疗。
手术在局部麻醉下进行,DSA确定MCA-M1段分叉部闭塞累及上下干;将8 F导引导管送至颈内动脉颈段,6 F Navien中间导管顺0.014英寸微导丝、导引导管上行至海绵窦段;Rebar18微导管顺微导丝、中间导管上行通过M1闭塞处至M2段上干,撤出微导丝,微导管造影确认在真腔内、远端血管通畅;Solitaire FR自彭式支架(6 mm×30 mm)经微导管送至闭塞段远段,回撤微导管打开支架远端,释放支架,造影确定支架位置正常、远端血管通畅;支架锚定下中间导管上行至M1闭塞近心端,5 min后负压维持下中间导管抽吸,同时回撤微导管,行颅内支撑导管辅助Solitaire FR支架机械取栓术(Solitaire FR with intracranial support catheter for mechanical thrombectomy,SWIM)(若海绵窦段迂曲明显、中间导管上行不能,仅予支架取栓),复查造影MCA-M1段仍闭塞,可重复上述步骤,在M1段上干或下干取栓1~2次,否则予以双支架取栓:微导丝导引下将Rebar18微导管送至MCA-M1段上干,撤出微导丝造影显示远端血流通畅,取Solitaire FR支架(6 mm×30 mm)置于微导管内,另取微导丝和Rebar 18微导管送至MCA-M2段下干,撤出微导丝,造影显示远端血流通畅,取Solitaire FR支架(4 mm×20 mm)置于微导管内,先后释放6 mm×30 mm支架、4 mm×20 mm支架,呈Y型;造影显示血流通畅,MCA-M2段上下干显影后静置5 min,同时回撤双微导管和双支架并取栓,再次造影观察血管再通情况。术后24 h复查CT排除出血和大面积脑梗死,予双联抗血小板治疗,根据脑梗死面积进行脱水治疗,必要时去骨瓣减压。
1.3 观察指标
①血管再通情况:术毕采用改良溶栓治疗脑梗死(mTICI)血流分级评估,2b或3级为再通。②手术情况:发病至股动脉穿刺时间、穿刺至血管再通时间、取栓次数、血栓逃逸。③神经功能及预后判定:术前、术后1周评估NIHSS评分,术后90 d评估改良Rankin量表(mRS)评分。④不良事件:颅内出血转化、90 d内死亡。
2 结果
7例患者一般临床资料见表1。7例中6例M1段上干和下干单支架各取栓1~2次(其中3例应用SWIM技术),均未再通,遂以Y型双支架取栓均1次再通,其中5例mTICI血流分级为3级,1例为2b级,股动脉穿刺至血管再通时间为(120.6±18.2)min(97~141 min);1例直接接受双支架取栓1次再通,mTICI血流分级为3级,动脉穿刺至血管再通时间为97 min,手术过程影像见图1。
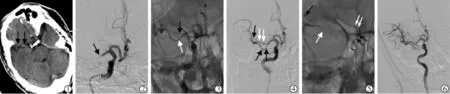
图1 双支架取栓治疗急性MCA-M1段分叉部闭塞性脑梗死患者手术过程影像
7例患者中5例术后1周NIHSS评分为(10.0±1.6)分(8~40分),术后90 d mRS评分为1~3分(表1);例4患者取栓术前2 d曾接受冠状动脉支架植入术,取栓术后5 d心源性猝死;例6患者既往因风湿性心脏病接受二尖瓣机械瓣置换术(术后口服华法林,未监测凝血功能),取栓术前国际标准化比值(INR)为1.9,单支架取栓时血栓逃逸至下干M3段,术后2 h复查CT示脑出血转化,术后8 d脑疝死亡。
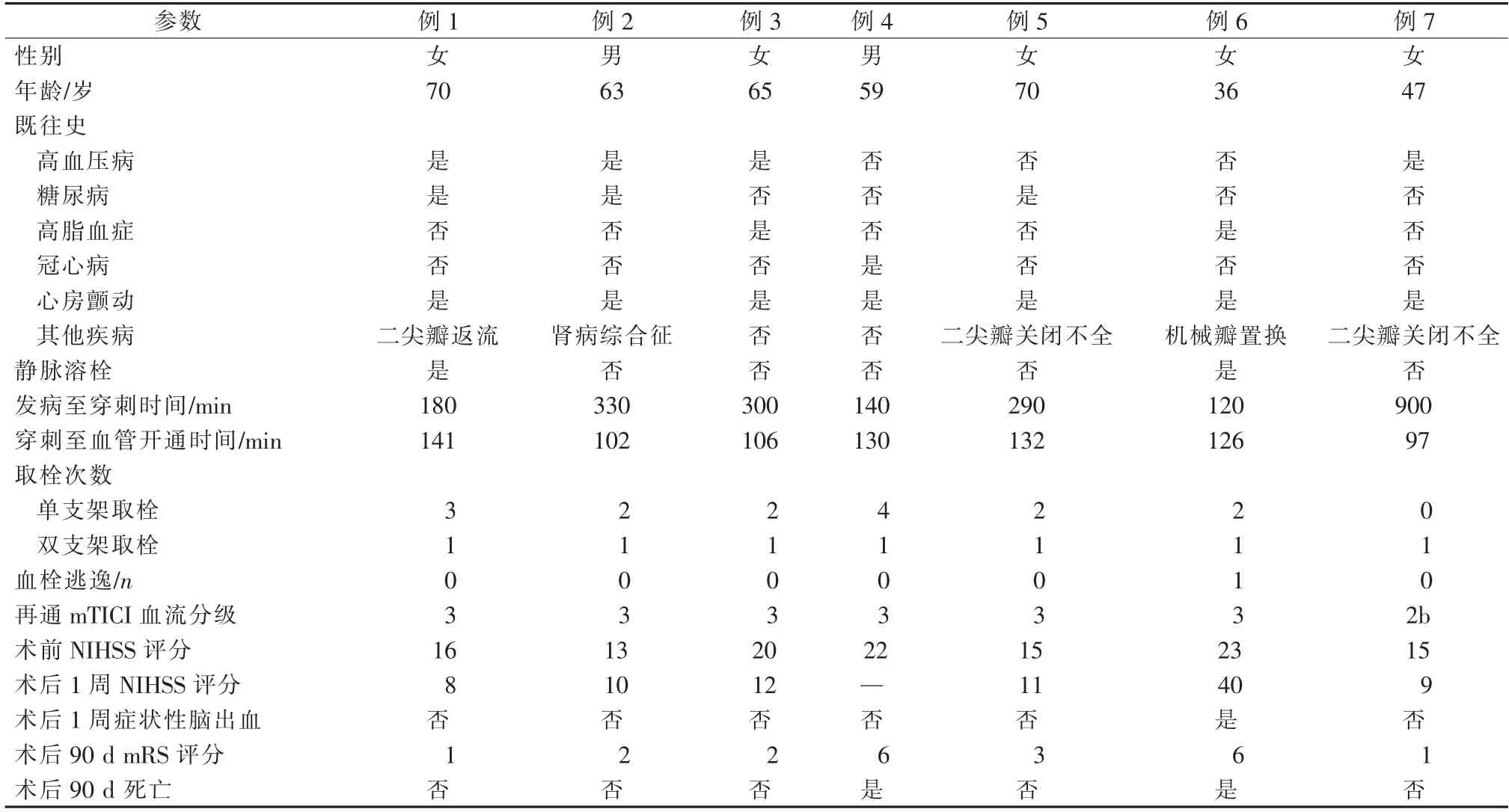
表1 7例急性MCA-M1段分叉部闭塞性脑梗死患者一般临床资料
3 讨论
急性大血管闭塞缺血性脑卒中,自然病程病死率高,存活者常重度致残,静脉溶栓效果差[1]。随着近年介入技术进步,支架取栓在这类患者中已取得较好疗效,中国卒中学会、美国卒中学会均将其作为颅内大血管再通的Ⅰ级推荐(A证据)[2-3]。心房颤动引起的心源性脑栓塞,是急性大血管闭塞缺血性脑卒中最常见病因之一[8]。由于这种心源性血栓负荷常较大[9],往往需要多次取栓,致再通时间延长,影响预后。
MCA血流量大、血流速度最快,心源性栓子最易进入该血管而成为心源性脑栓塞最常见部位[10]。有研究显示MCA闭塞经单纯支架取栓的再通率为66.7%,33.3%不能再通[11]。SWIM技术系支架取栓联合导管抽吸取栓,可提高支架取栓效率、增加血管再通率,逐渐成为国内外颅内大血管急性闭塞再通的主流技术[12]。邢鹏飞等[13]研究显示,Solumbra技术(支架取栓联合导管抽吸取栓)治疗MCA主干闭塞后血管再通率为90.5%。但本研究中部分患者颈内动脉颈段和海绵窦段常弯曲明显,中间导管无法到达M1段尤其是M1分叉,影响SWIM技术在M1分叉闭塞患者应用,7例中仅3例应用SWIM技术,且均未再通。
由于解剖结构影响,脑动脉分叉部闭塞介入取栓时易出现血栓位移、取栓不完整,多次取栓仍不易完全再通,一直是介入治疗中的难题,相关研究较少且多涉及颈内动脉末端闭塞研究[5]。M1分叉部易卡顿大负荷心源性血栓,关于该处取栓研究目前仅见个案报道[6-7,14]。本研究显示,即便采用SWIM技术多次取栓,仍未能再通MCA-M1段分叉部闭塞,并易出现血栓位移,而采用Y型双支架取栓1次再通,取栓时间缩短,且未出现血栓逃逸;认为这与M1段分叉部急性闭塞由心源性栓塞、血栓负荷重并呈Y型分叉嵌顿有关。由于该处血栓负荷重并存在分叉,单支架不能接触、结合整个血栓,常造成血栓切割,并易使分叉处另一血管内剩余血栓位移或逃逸,而Y型双支架可增大血栓接触面积、增加血栓缠绕结合力、限制血栓在分叉处移位、减少血栓逃逸,从而提高再通率并缩短再通时间。
心房颤动所致心源性脑栓塞与无心房颤动脑梗死相比,栓子突然堵塞脑血管,对血管内皮细胞损伤重,缺血脑组织不能及时形成有效的侧支循环,低灌注与神经功能障碍更重,梗死面积更大,出血转化较重[15],因此尽早尽快再通闭塞血管显得尤为重要。再通时间是良好预后的预测因素,再通时间延长则为结局不良的影响因素。研究显示,起病至再灌注时间延长1 h,良好预后获益降低6%~10%,随后每延迟1 h,良好预后获益则降低20%[16-18]。本组7例患者中5例术后NIHSS评分改善明显、90 d时结局良好,可能与Y型双支架取栓缩短再通时间有关;例4患者单支架取栓4次,术后出现症状性脑出血、脑疝,5 d后死亡,再通时间长可能是主要原因。
术后脑出血是支架取栓最严重并发症,伴心房颤动时脑出血率增加,甚至导致术中死亡[19-20]。Singh等[21]研究报道单支架取栓后症状性脑出血发生率为8.1%。部分研究认为,双支架取栓时支架与血管内膜接触面积增加,支架重叠部分径向支撑力增大,可增加血管牵拉损伤风险,可能导致血管壁损伤甚至撕裂,引起脑出血[22]。本研究中仅1例患者出现症状性脑出血,其既往心脏机械瓣置换术后长期口服华法林,取栓术前INR为1.8,脑出血可能主要与凝血异常有关;提示对凝血异常患者应慎用Y型双支架取栓。
Y型双支架取栓存在增加费用、可能出现支架相互铰链而取出困难等不足。动脉硬化严重患者需慎用该技术,因其有可能导致动脉夹层,一般仅推荐用于心源性栓塞[22]。本研究为回顾性研究,样本量有限,以后应扩大样本量并进行前瞻性对照研究。
综上,采用Y型双支架取栓治疗急性MCA-M1段分叉部闭塞脑梗死1次再通率高,可缩短取栓时间,预后较好。
