助剂对生物法去除疏水性VOCs性能的影响
2022-02-22杨菊平杜佳辉窦晓娜祁弘毅
刘 佳, 杨菊平, 杜佳辉, 窦晓娜, 祁弘毅, 李 坚
(北京工业大学区域大气复合污染防治北京市重点实验室, 北京 100124)
近几十年来,随着经济和工业的不断发展,以及人口的不断增加,各种气态污染物被大量排放[1-3],使得进入大气的挥发性有机物(volatile organic compounds,VOCs)越来越多,其排放严重影响了环境的清洁和人类的健康[4]以及环境中动植物的生存. VOCs是一类常压下沸点低于260 ℃或室温时饱和蒸气压大于71 Pa的有机化合物的总称[5],在中国《“十三五”挥发性有机物污染防治工作方案》中规定,VOCs是指参与大气光化学反应的有机化合物,包括非甲烷烃类(烷烃、烯烃、炔烃、芳香烃等)、含氧有机物(醛、酮、醇、醚等)、含氯有机物、含氮有机物、含硫有机物等[6-8],是形成臭氧(O3)和细颗粒物(PM2.5)污染的重要前体物. 根据《大气挥发性有机物源排放清单编制技术指南(试行)》,VOCs排放源可划分为溶剂使用源、工艺过程排放源、化石燃料燃烧源、生物质燃烧源和移动源五大类,而其中溶剂使用源是我国工业VOCs排放最主要的贡献源[9],包括涂料制造[10]、家具喷涂[11]、制鞋[12]、印刷[13]等行业,都会向大气中排放苯、甲苯、二甲苯、环己烷、乙酸乙酯等物质. 因此,为了应对这些化学物质所带来的有害健康风险和潜在的环境问题,有关VOCs排放控制的法律法规也越来越严格[14]. 近年来相继出台了《中华人民共和国大气污染防治法》《大气污染防治行动计划》《重点行业挥发性有机物综合治理方案》《重点行业挥发性有机物削减行动计划》等法规政策及治理计划,说明减排和治理VOCs已经刻不容缓.
气态污染物的去除主要有2类技术:一是物理化学技术,二是生物技术. 物理化学技术包括吸收、吸附、焚烧、冷凝和等离子体等[15-17],而生物技术包括生物过滤(biofiltration)、生物滴滤(biotrickling)和生物洗涤(bioscrubber)等方法,广泛应用于VOCs、温室气体(greenhouse gases,GHGs)和恶臭气体的去除[18-19]. 目前去除VOCs应用的反应器主要包括生物过滤器(biofilter,BF)和生物滴滤器(biotrickling filter,BTF),在处理过程中,微生物以生物膜的形式固定或附着在诸如泥炭、木屑、陶粒、聚氨酯海绵、硅藻土等多孔介质上[20-23],当污染气体通过填料层时,其中的污染物被生物膜中的微生物捕获进而转化为CO2、H2O和生物质等无害的产物[24]. 与物理化学的方法相比,生物法具有操作简单、无二次污染、净化效果好、投资运行费用低等优点[25]. 杨竹慧[26]、兰善红等[27]分别将生物法运用于石化和喷漆行业,研究发现其对苯、甲苯、乙酸乙酯、乙酸丁酯等均具有良好的去除效果.
根据VOCs在25 ℃时的亨利常数(H)可划分为亲水性VOCs和疏水性VOCs[28]. 一般H<0.1被归类为亲水性VOCs(如醇类、酮类、醛类等),H≥0.1则被归类为疏水性VOCs(如烷烃、烯烃和芳香烃等)[29-30]. 在利用传统生物法处理有机废气的过程中,污染物的转移过程是从气相到液相再到生物膜中被微生物降解,而疏水性污染物在水相中的溶解度小,气液传质阻力大,传质速率低[31], 故对疏水性污染物的处理效果并不理想. 为了提高生物反应器对疏水性污染物的去除效果,众多研究者尝试了多种方法,如污染物预处理、接种真菌、添加助剂等[32]. 研究表明添加助剂可有效改善疏水性污染物的去除效果,提高生物降解效率[33-34]. 近年来,研究较多的助剂主要有三大类. 1) 物理化学类助剂:如臭氧、硅油、吐温-20(Tween-20)、吐温-80(Tween-80)等;2) 生物表面活性剂:如皂角苷、鼠李糖脂等;3) 金属离子:如Zn2+、Fe3+等.
本文列举了目前应用较多的助剂及其使用效果,并综述了不同助剂对生物反应器去除疏水性VOCs性能的影响,包括降解效率、生物量的积累与压降、微生物群落与生物膜、矿化率等方面,为进一步研究助剂对反应器性能的影响及其作用机理提供基础理论依据. 另外,由于目前少有对添加助剂影响反应器性能的机理研究,故文章中也对今后在生物法中添加助剂的研究方向进行了展望.
1 助剂在生物反应器中的应用及影响
1.1 常用的助剂种类
生物法处理有机废气时,污染物一般是从气相到液相再到生物膜被微生物吸收降解,如图1所示. 其中污染物从气相到液相的传质速率与污染物的H有关,H越大,溶解度越小,传质也越受限制. 疏水性VOCs向液相的低传质限制了微生物对污染物的降解,导致疏水化合物的生物利用度低,生物降解效率低[35]. 另一方面,生物反应器中微生物活性的高低也会影响污染物质的去除效率,所以提高VOCs的生物利用度或提高微生物活性,都有利于微生物对其降解[28,36]. 为了解决这些问题,目前研究者们在各式反应器中尝试添加了多种多样的助剂,包括物理化学类助剂、生物表面活性剂、金属离子等,都取得了较好的效果. 助剂的选取需要考虑多方面的因素,包括水溶性、对微生物的毒性、与目标污染物是否发生反应以及经济成本等. 表1列举了已有研究中常用的助剂种类及其对去除效率的影响.

图1 污染物质传质示意图Fig.1 Mass transfer of pollutant
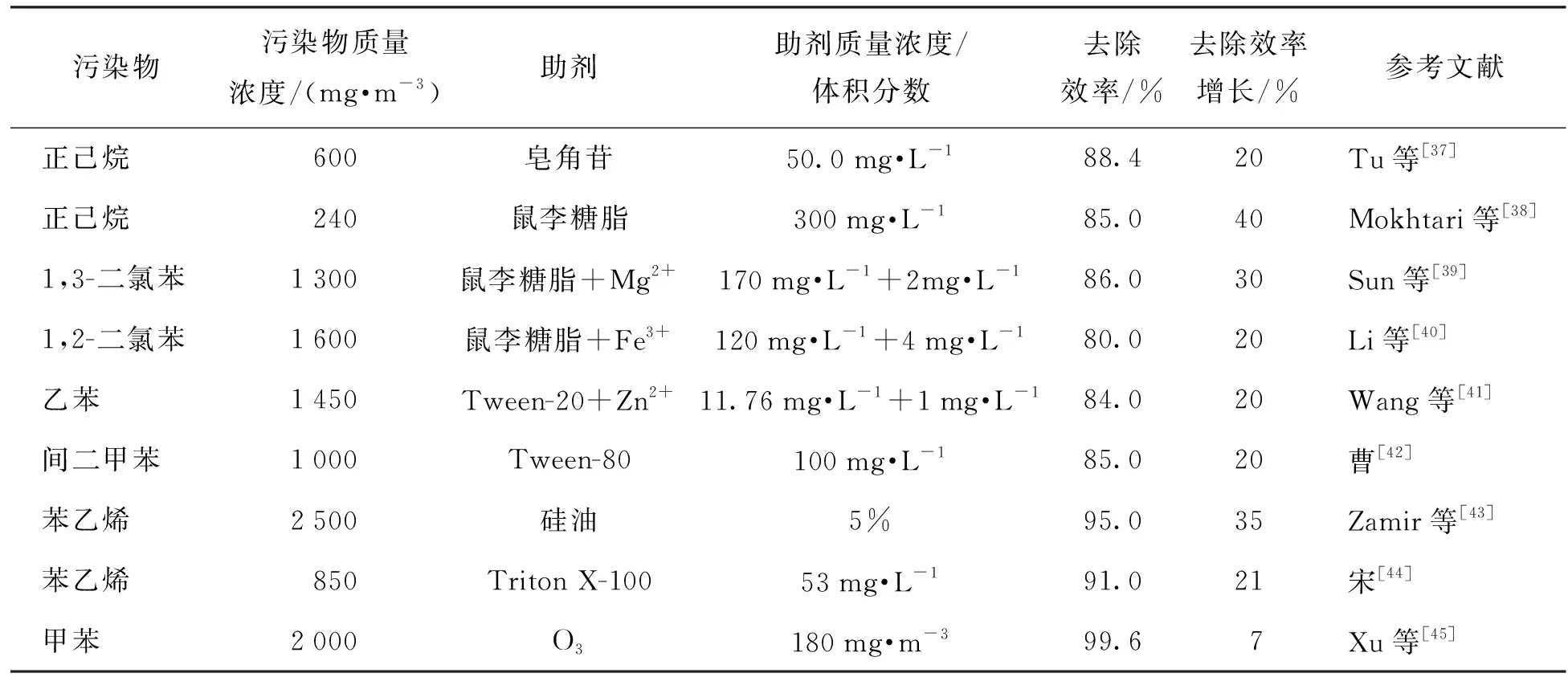
表1 常见的助剂种类及其使用效果Table 1 Types of frequently-used additives and their effects
1.2 助剂对降解效率的影响
导致疏水性VOCs在生物反应器中去除效率较低的主要原因之一是,VOCs从气相转移到生物膜相的传质速率较低,从而限制了其被微生物捕获并降解的效率[46-48]. 而添加具有增溶作用的表面活性剂可以增大污染物质在液相中的溶解度. 因为表面活性剂的分子结构具有两亲性,一端为极性的亲水基团,另一端为非极性的疏水基团[49]. 表面活性剂分子分布在气液两相界面,能降低液相的表面张力,有效降低气液两相间的传质阻力,使疏水性污染物更易溶于液相中,进而增加污染物与微生物的接触,增大生物反应器的降解效率[50-51].
吴超等[52]在BTF中添加了体积比为5%的二甲基硅油构成双液相体系,在二甲苯进气质量浓度保持在1 200~1 600mg/m3、停留时间为30 s时去除效率仍能达到90%以上,比同运行条件下的单液相体系高出20%左右. 周学霞[53]在反应器中添加了Tween-60,当Tween-60质量浓度为100 mg/L时邻二甲苯的去除效率比不添加Tween-60时可提高20%. Tu等[37]在降解正己烷的生物反应器中添加了生物表面活性剂皂角苷,与未添加皂角苷的反应器相比,去除效率大幅度提高,最大提高了27%. Sun等[39]添加生物表面活性剂鼠李糖脂到处理1,3-二氯苯的BTF中,发现添加鼠李糖脂后,BTF性能提高了30%.
但众多研究结果表明并非助剂浓度越高降解效率就越好. 程燕[54]考察了不同浓度的十二烷基硫酸钠(SDS)对BTF去除正己烷的降解效率的影响. 实验结果显示当SDS浓度由低到高增加时,去除效率表现出先增高后降低的趋势. 可能是由于SDS本身具有一定的生物降解性,低浓度时主要作为增溶剂来提高污染物的溶解度,从而提高污染物的生物利用度,而高浓度的SDS则可成为与目标污染物竞争的碳源,从而对污染物在生物反应器中的生物降解产生不利影响. 同样出现了高浓度助剂与污染物质存在碳源竞争情况的还有Tween-80和Tween-20. 许锐伟等[5]在研究中考察了3种不同浓度的Tween-80对间二甲苯降解效率的影响,发现初期3种助剂浓度下间二甲苯的降解效率相当,但随后高浓度助剂条件下的降解效率增长比低浓度的缓慢. Wang等[55]在降解乙苯的研究中添加Tween-20,降解效率也随着Tween-20浓度增大出现先增加后降低的现象. 此前也已经有研究人员证明SDS、Tween-80等确实可以作为碳源被微生物降解[56-57]. SDS为醇的衍生物,Tween-80和Tween-20为酯类物质,都具有生物可降解性. 当其浓度较低时,生物反应器中存在的微生物为降解目标污染物的优势菌种,能高效降解目标污染物. 而当其浓度较高时,生物反应器内微生物群落可能已经随着表面活性剂浓度的升高逐渐演变成SDS、Tween-80和Tween-20等的优势降解菌种,导致目标污染物的降解效率降低.
除了添加化学和生物表面活性剂作为起增溶作用的助剂外,还有研究者把金属离子作为添加剂加入去除污染物的生物反应器中. 许多研究者发现一些金属离子对微生物活性有促进作用[58-59],因为金属离子可以与微生物细胞壁上的含氧或含氮基团络合[60],增大微生物活性,进而提高污染物的去除效率.
Li等[40]比较了单独添加鼠李糖脂、Fe3+以及同时添加鼠李糖脂和Fe3+三种情况下的去除效率,比不添加任何助剂的对照组分别高出约15%、20%、30%,可以看出Fe3+的添加对去除效率有非常积极的影响. Wang等[55]把不同浓度的Zn2+作为助剂添加到反应器中时,发现其作用与添加Tween-20有类似的变化趋势,在低浓度时促进生物降解,而浓度继续增大时降解效率甚至低于未添加Zn2+的反应器. Mg2+也有类似的效果[38]. 可能是由于高浓度的金属离子使污染物降解所必需的蛋白质变性或重要酶类失活,导致微生物的生命代谢活动受阻,从而降低了污染物的降解效率[61-62].
除此之外,Rezaei等[63]在去除苯乙烯的BTF中添加了氧化性物质H2O2,而H2O2是微生物产生过氧化物酶和过氧化氢酶的主要诱因之一[64]. 过氧化物酶是一种能降解碳碳键的胞外酶[65],过氧化氢酶是一种能直接氧化有机污染物的氧化性胞外酶[64],它们的存在能有效促进污染物质的生物降解. 同时,作者还测定了运行期间反应器中生物表面活性剂鼠李糖脂、脂肽等的产量,发现在H2O2存在时,生物表面活性剂的产量能有所提高,进一步增加了苯乙烯的溶解度,加速了苯乙烯从气相到液相再到生物膜的传质,从而提高了其生物利用度,增大了降解效率. Shekoohiyan等[66]也有相似的结果.
1.3 助剂对生物量积累及压降的影响
生物反应器的另一个限制是运行过程中生物量过度积累. 微生物是生物法处理污染气体的关键因素[15],其在反应器中的生长是最难控制的因素之一. 生物膜的形成和生长是一个动态过程,受到多个因素的影响,包括pH、温度、氧浓度、营养物质和微量元素[67]以及填料表面性质等. 生物膜的厚度,可能从几微米到几毫米不等. 反应器运行期间生物膜在填料中过多的积累和分布不均,可能导致反应器运行出现各种问题,如堵塞、压降增大、增加空气流动阻力、在填料床层内形成沟流等[68-69],从而抑制O2、养分和污染物的转移. 此外,生物膜厚度的增加还可能会导致生物膜内厌氧区的形成,从而对生物降解产生不利影响[70]. 而一系列研究发现助剂的加入可以很好地改善这些问题.
Woertz等[71]在降解甲苯的生物反应器中分别添加了SDS和Tween-20,实验结果显示Tween-20和SDS的添加均能有效减少生物量的积累,但对生物反应器降解效率的影响却相反. 添加Tween-20可以提高降解效率而添加SDS却使降解效率降低了,这可能是因为高浓度的SDS可以破坏蛋白质中的离子键和氢键等非共价键甚至蛋白质的构象,导致某些具有重要功能的蛋白质变性. García-pérez等[72]的研究发现向反应器中添加适当浓度的臭氧作为助剂也能克服生物量过度增长导致生物反应受限的问题. Covarrubias-García等[73]在去除乙酸乙酯的研究中得到,在其他条件相同时,用臭氧进行协同处理的BF去除效率更高,去除负荷更大,而生物量积累却相对较小. Zhou等[74]在处理甲苯的研究中发现添加臭氧的BTF中生物量一直低于未添加臭氧的BTF,且臭氧浓度越高生物量越少,分布也更均匀. Saingam等[75]也有类似结论,添加臭氧的BF的生物量积累一直低于未添加臭氧的BF. 但研究也发现去除效率并非臭氧浓度越高越好,超过某个值后就会逐渐下降. 因为有研究表明,具有强氧化性的臭氧可以与细胞外聚合物(EPS)发生反应,有助于清除生物膜中的死细胞[76-78]. 故高剂量臭氧可能会使BTF的生物量含量下降到生物降解速率受生物量限制的水平,从而降低了污染物的去除效率. 另一种原因可能是臭氧的添加影响了微生物的代谢途径,增大了污染物的矿化率,使污染物更多地转化为CO2而不是生物质. 除此之外,一些研究在处理蒎烯、氯苯等污染物时将UV与生物反应器结合,也能较好地控制生物量的过量生长,因为UV处理能产生臭氧等产物发挥作用[61,79-80].
也有研究者通过监测生物反应器压降的变化间接监测生物量的变化. 生物质的过度积累、分布不均以及生物膜黏性过大等都可能导致气体在反应器中的流通受阻,从而造成压降增大. 控制压降的措施很多,机械方法包括反冲洗和床层搅拌,生物方法包括设置饥饿期和生物捕食者的应用[81-82],化学方法包括控制营养物质和水分以及表面活性剂的应用等.
宋甜甜[44]研究了Triton X-100对生物滴滤塔压降的影响,发现在反应器运行前期尤其是挂膜驯化阶段,是否添加表面活性剂对BTF压降的影响相差不大,但在后期污染物浓度增大后添加表面活性剂的BTF1压降却明显低于未添加表面活性剂的BTF2. 说明表面活性剂的使用一定程度上可以缓解BTF在高负荷运行时发生的生物质积聚造成的填料堵塞现象. Tu等[37]在实验中观察到皂角苷也有同样的效果,添加皂角苷的生物反应器的压降在同样长的运行时间内增量小于未添加的反应器. Saingam等[75]研究发现,在BF中添加一定浓度的臭氧也可以降低压降,长时间运行后,注入臭氧的BF1压降明显低于未添加臭氧的BF2,这一结果也与以前的研究结果相似[83]. 由以上对生物量的监测与对压降的监测结果可以看出,添加适当浓度的助剂可以有效减少生物反应器运行过程中生物量的过度积累,缓解填料堵塞现象的发生,减小压降.
1.4 助剂对微生物群落和生物膜的影响
生物反应器对VOCs降解性能的有效性取决于微生物对污染物的生物降解能力[84]. 生物反应器中的微生物群落组成受多种因素的影响,包括接种源、污染物组成、环境条件、氧气利用率等. 以往对生物反应器中微生物群落的研究发现,细菌、真菌和原生动物多种多样[85-86],这些微生物的代谢活动和功能对VOCs的去除效果有很大的影响. 助剂的加入往往会引起微生物生长微环境的改变,继而使反应器中的微生物种类发生演变,微生物活性也会受到影响.
Covarrubias-García等[73]研究发现,在利用BF处理乙酸乙酯时,添加臭氧的体系中生物多样性较不添加臭氧的对照组低,可能是添加臭氧导致了生物量减少,从而消除了一部分微生物种类,也可能与添加臭氧使反应器中pH明显低于对照组,导致只有耐酸的微生物才能在其中生存有关. Saingam等[75]的研究中对细菌群落结构的分析表明,在臭氧的作用下,活性优势菌种没有明显的变化,但某些耐臭氧属菌种得到了增强,与未加臭氧的反应器相比,注入臭氧的反应器中发现有更多的变形菌和更少的放线菌. 也有使用2种BF处理甲苯的研究表明,在连续添加臭氧的情况下,革兰氏阳性菌比革兰氏阴性菌更丰富. 因为革兰氏阳性菌的细胞壁较厚,肽聚糖含量较高,故而可能对臭氧更耐受[78]. Han等[87]研究发现,在其他条件相同的情况下,添加了硅油的双液相生物反应器中微生物的活性高于未添加硅油的生物反应器,因为硅油的加入可能改变了生物膜的特性. 20 ℃时硅油的氧溶解度高于水[88],因此,氧更容易被转移到生物膜内较深的位置. 在以好氧微生物为主的生物反应器中生物膜内氧浓度和VOCs浓度的变化可能会导致2种生物膜的微生物群落和代谢活性的差异[89]. 表2简要总结了添加助剂前后生物反应器内微生物种类的变化情况.
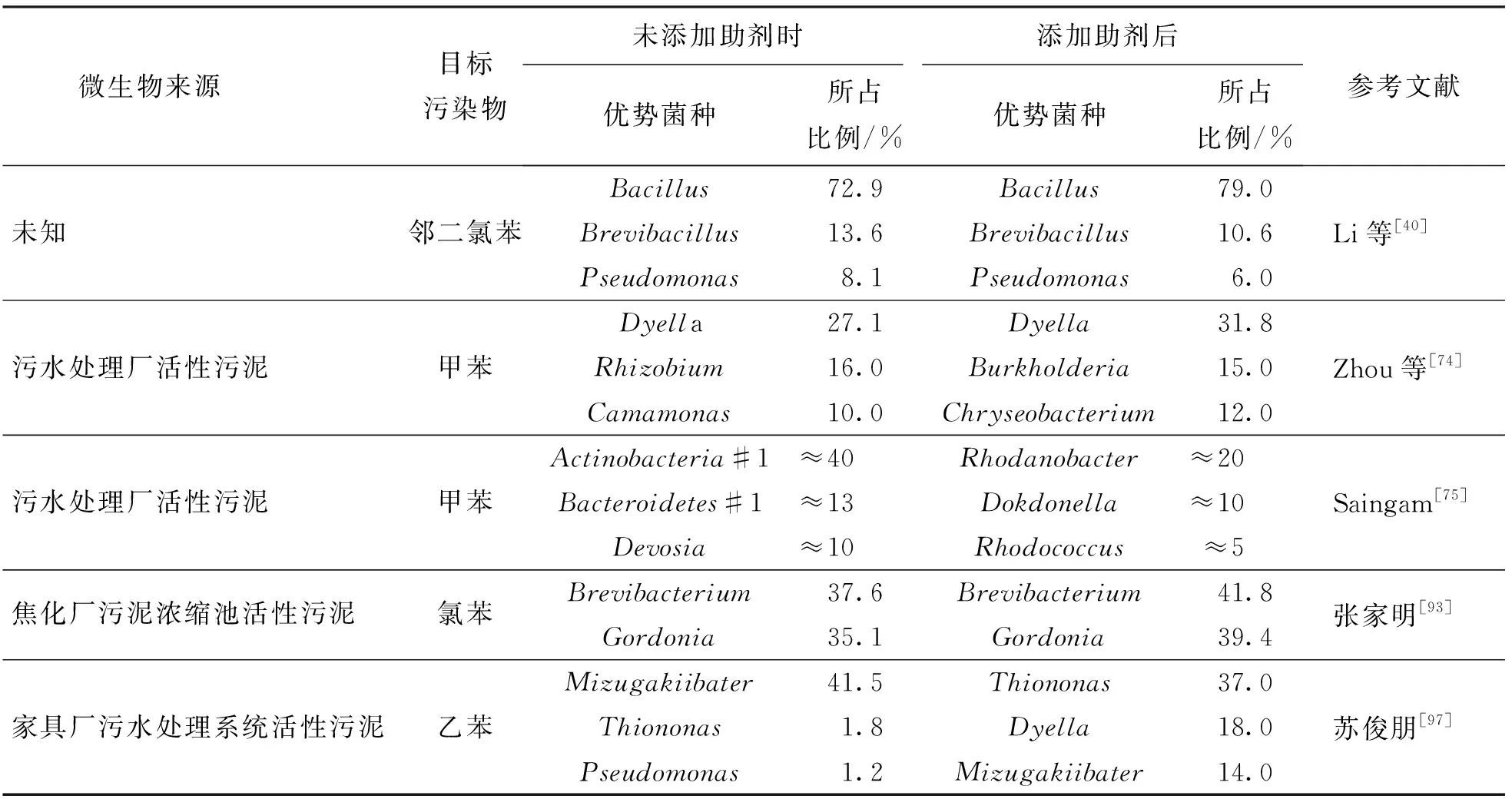
表2 助剂添加前后微生物种类变化情况Table 2 Changes of microbial species before and after additive addition
生物膜干重中EPS约占80%,主要由蛋白质(PN)和多糖(PS)组成,在调节生物膜形态等方面起着重要作用[90]. 生物膜的孔隙度、密度和疏水性等重要性质均与EPS有关. EPS还会影响污染物的传质效率,因为污染物必须通过EPS层才能与细胞接触并相互作用[91]. Li等[92]的研究表明,过量的EPS会阻止O2和营养物质进入生物膜. 有研究者考察了助剂的加入对生物膜中EPS的影响. Li等[40]在研究中发现添加了鼠李糖脂和Fe3+的BTF中的微生物群落多样性与接种时差距更小,并表现出了更强的黏附性,EPS测定结果显示添加助剂的BTF中的生物膜中含有更多的PS和PN. 可能是由于鼠李糖脂和Fe3+的存在促使微生物分泌了更多的PN和PS,进而提高了生物膜中EPS的含量. 张家明[93]在降解氯苯的研究中添加了鼠李糖脂、Fe3+和Zn2+,并得到了与Li等相似的结论. 以往研究发现富含EPS的菌株的细菌黏附能力比常规菌株强得多[90],不仅可以促进微生物有效地附着在填料上,还可以维持生物膜结构的完整性,从而保持生物膜中微生物群落的整体稳定性,使反应器的性能稳定且对污染物的去除效率有效提高.
而Zhou等[74]的研究却发现添加臭氧的反应器中生物膜的EPS含量明显低于不添加臭氧的反应器,但其中微生物的代谢活性却相对较高,与Maldonado-Diaz等[94]得到的结论相似,臭氧减小EPS含量和厚度的同时却不影响生物膜活性. 说明EPS含量较少的生物膜中却可以具有更多的活性细胞. 也就是说臭氧可以与EPS发生反应,使细胞连接松散,EPS层变薄[95],也可以提高微生物的活性[96],即臭氧具有通过改善生物反应器中微生物氧化还原反应来提高微生物代谢活性的能力. 因此,虽然臭氧的存在减少了生物膜中EPS的含量,但由于微生物的活性变得更高,故对反应器的性能仍然有着积极的影响.
以上研究结果表明,不同种类的助剂由于对微生物及EPS的作用机理不同,故对生物反应器中生物膜的影响结果各不相同,但殊途同归的是,不管是增强微生物群落的稳定性还是生物膜中微生物的活性,都可以使生物反应器处理污染物的性能更好. 研究者可以根据自己对反应器性能和参数的需求选择添加合适的助剂,以得到期望的效果.
1.5 助剂对污染物矿化率的影响
污染物在生物膜中被微生物吸收,通过各种生化反应将污染物质转化为生物质和对环境无害的H2O和CO2等. 通常认为有机污染物中碳的去向主要包括CO2、生物质和EPS. 其他可能少量存在于可溶性代谢物[98]、CO等挥发性物质[99]中. 而CO2产量是评价污染物质降解程度的重要参数,以矿化率表征. 一般矿化率计算式为

(1)
在Han等[87]的研究中可以看到,二氯甲苯在添加了硅油的生物反应器中更多地被转化为CO2(72.47%),而较少一部分转化为生物量(27.53%),对比未添加硅油的生物反应器中,二者的比例分别为56.22%和43.66%. Valero等[100]在实验中测得,在同样的条件下运行,添加硅油的生物反应器矿化率为73%,而此时未添加硅油的反应器中矿化率为58%. 付妍[101]在去除二氯甲烷的研究中也得出了类似结论,添加硅油与不添加硅油的矿化率分别为61%、51%. Saingam等[75]在研究中测得,添加臭氧的BF中甲苯的矿化率为91.29%,而未添加臭氧时低大约9%,为82.58%. 前文提到硅油的氧溶解度大于水,氧分子更容易进入生物膜较深处发挥作用,而臭氧的加入可以提高微生物的活性,这些原因可能使微生物对污染物的降解更彻底,得到更高的矿化率.
然而与之相反的是, Yousefinejad等[102]做图表示去除负荷与相应的甲苯矿化和细胞呼吸产生CO2的速率之间的相关性发现,单液相(OLP-BTFs)的斜率(0.667)大于添加硅油的双液相(TLP-BTFs)的斜率(0.317). 与双液相条件下相比,在不加硅油的单液相条件下真菌呼吸产生更多的CO2,换句话说,在有硅油的情况下微生物的生长得到了增强. Zamir等[103]也有类似的结果,OLP-BTFs和TLP-BTFs的斜率分别为2.1和1.1. Rene等[104]也有相似的结论. 产生这种与前文所述相反结果的原因可能是不同菌种的生命代谢活动和对污染物的降解能力有差异,不同的代谢降解路径可能使污染物转化为生物质和CO2的比例不同,故而有不同的矿化率. 但目前虽然已经有研究者注意添加助剂后的矿化率如何变化,却还极少有人对助剂是如何影响矿化率的原因和机理进行准确地探究和解释,因此这也是未来研究助剂对生物法去除VOCs性能影响的一个新的方向.
2 结论与展望
制约生物反应器性能的因素很多,如温度、pH、传质、生物量等,众多研究者开发了很多方法改善反应器的运行环境,试图尽最大可能提高反应器对污染物的去除性能,而这其中添加助剂被广泛研究. 由以上所述可知,添加适合种类适当浓度的助剂有助于生物反应器去除效率的提高,同时也可以控制微生物的过度生长不至于出现填料层堵塞、气流分布不均、压降增大等问题. 另外,助剂的添加还会引起反应器中微生物群落发生相应变化,以适应发生改变的生存环境. 微生物通过各类生命代谢活动将污染物质转化为生物质、H2O和CO2等,不同的微生物群落对污染物有不同的代谢途径,所以对污染物质的矿化率也会产生很大的影响.
但目前对于助剂的研究大多集中在宏观层面考察助剂对去除效率、生物量、矿化率等方面的影响,却很少有对影响机理方面的研究,尤其是助剂的添加对矿化率的影响机制. 同时值得注意的是,助剂在去除VOCs和其他废气的过程中虽然有一系列积极影响,但也存在一些问题. 有些助剂本身就是水和空气的污染物,有些对人体和微生物有毒害作用,助剂的加入在促进了VOCs降解的同时却产生了新的污染,可能会导致一些严重的疾病[105].
另外,目前在生物法中添加助剂以改善反应器性能的研究还停留在实验室模拟阶段,几乎没有运用在实际工程中. 但在工程中风量一定的情况下,助剂对降解效率的改善可以使停留时间缩短,进而缩小生物反应器的体积,在工程应用中可以进一步缩减经济成本和空间占用,具有良好的应用前景.
综上,未来对助剂与生物法的研究方向包括:1) 添加不同类型的助剂引起生物量、微生物群落及生物膜成分等变化的原因及机理;2) 助剂的添加对微生物产生的酶类及降解路径的变化解析;3) 助剂对污染物质矿化率的影响机理;4) 着力于开发新型助剂,更高效地提升反应器性能并对环境更友好;5) 在中试反应器中进一步研究添加助剂对反应器性能等各方面的影响.
