丙硫菌唑原药中脱硫丙硫菌唑和甲苯的液相色谱通用分析方法研究
2022-02-21张叶明
张叶明
(上海晓明检测技术服务有限公司,上海 201612)
1 前言
丙硫菌唑,化学名称为2-[2-(1-氯环丙基)-3-(2-氯苯基)-2-羟丙基]-1,2-二氢-3H-1,2,4-三唑-3-硫酮,是一种新型广谱三唑硫酮类杀菌剂,主要用于谷物、大豆、油菜、水稻、花生、甜菜和蔬菜等,杀菌谱广。该剂不仅能高效防治小麦赤霉病,而且能有效抑制赤霉病菌产生毒素。同时还表现出良好的保绿防衰作用,增产效果明显。
脱硫丙硫菌唑是丙硫菌唑产品中的相关杂质,甲苯是残留溶剂,目前有关这两个杂质的分析方法有团体标准T/CCPIA 026-2020丙硫菌唑原药,分别采用液相外标法测定脱硫丙硫菌唑含量和气相内标法测定甲苯含量,但对于同时检测两个杂质的分析方法尚少报道。本文旨在建立一种可对丙硫菌唑原药中脱硫丙硫菌唑和甲苯同时进行分离和定量的高效液相色谱法。该方法分离效果好,操作简单快速,适用于丙硫菌唑产品中脱硫丙硫菌唑和甲苯的定量分析。
2 试验部分
2.1 仪器和试剂 高效液相色谱仪,具可调波长的DAD检测器:安捷伦1260液相色谱仪;MS205DU型电子天平;2200T型超声波清洗仪;Direct 8纯水超纯水一体机。
乙腈:色谱纯;磷酸:分析纯;脱硫丙硫菌唑标样:已知质量分数97.4%;甲苯标样:已知质量分数99.9%;试样:98%丙硫菌唑原药。
2.2 色谱条件 色谱柱:采用Agilent SB-Aq(150mm × 4.6mm,1.8μm);检测波长:216nm;流动相:

流动相时间水(0.05%磷酸)乙腈0.00min475316.00min475316.10min109022.00min109022.10min4753
流速:0.25mL/min;柱温:30±2 ℃;进样体积:5μL。在上述色谱条件下,甲苯的保留时间约为15.9min,脱硫丙硫菌唑的保留时间约为18.0min。典型的高效液相色谱图(图1)。
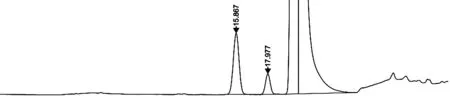
图1 丙硫菌唑试样的高效液相色谱图
2.3 溶液的配制
2.3.1 标样溶液的配制 分别称取约0.025g(精确至0.000 01g)脱硫丙硫菌唑标样和约0.05g(精确至0.000 1g)甲苯标样于同一个50mL容量瓶中,用乙腈溶解并稀释至刻度,摇匀得标样溶液储备液。移取0.5mL标样溶液储备液于25mL容量瓶中,加入乙腈稀释至刻度,摇匀。
2.3.2 样品溶液的配制 称取约0.5g(精确至0.000 1g)丙硫菌唑原药的样品于25mL容量瓶中,加入乙腈溶解并稀释至刻度,摇匀。
2.4 测定 在上述操作条件下,待仪器稳定后,连续注入数针标样溶液,直至相邻2针脱硫丙硫菌唑(甲苯)峰面积相对变化<10%后,按照标样溶液、试样溶液、试样溶液、标样溶液的顺序进行测定。
2.5 计算 试样中脱硫丙硫菌唑(甲苯)的质量分数X按式(1)计算:
(1)
式中:X—脱硫丙硫菌唑(甲苯)的质量分数,%;
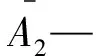
m1—脱硫丙硫菌唑(甲苯)标样的质量,g;
P —脱硫丙硫菌唑(甲苯)标样的质量分数,%;
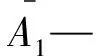
m2—试样的质量,g。
3 结果和讨论
3.1 方法与讨论
3.1.1 检测波长的选择 本方法检测波长的选择,参照了T/CCPIA 026-2020[5]中脱硫丙硫菌唑的检测方法,另外甲苯的紫外光谱图(图2),从图中可以看出甲苯的最大吸收波长约为206nm,考虑到甲苯的紫外吸收不太强,为提高检测灵敏度,故选择210nm为检测波长,在该波长处干扰较少,同时能够满足分析要求。

图2 甲苯的紫外光谱图
3.1.2 流动相的选择 色谱柱选择常用的Agilent SB-Aq柱,根据丙硫菌唑的物化性质和溶剂的紫外吸收波长,选择乙腈作为溶剂溶解样品。以乙腈和水作为流动相,为了得到更好地分离效果,在1 000mL水中加入0.5mL磷酸,使用梯度洗脱的方式,流速选择0.25mL/min。
3.2 分析方法特异性 试验采用HPLC-DAD峰纯度分析法来鉴别脱硫丙硫菌唑和甲苯。脱硫丙硫菌唑标样、甲苯标样、试样溶液,它们的HPLC-DAD峰纯度均>999,未检测到不纯物,即该分析物处无其它物质干扰,符合定量分析要求。峰纯度色谱图如(图3~6)。
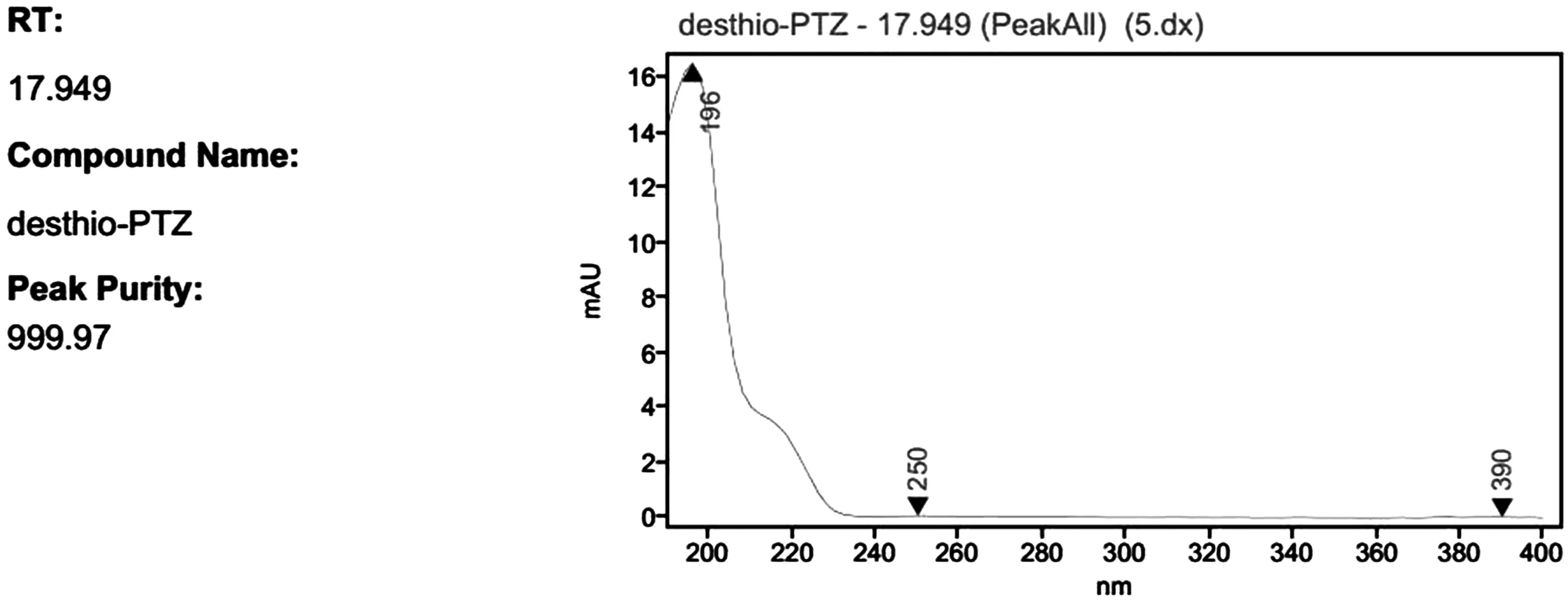
图3 标样中脱硫丙硫菌唑的峰纯度图
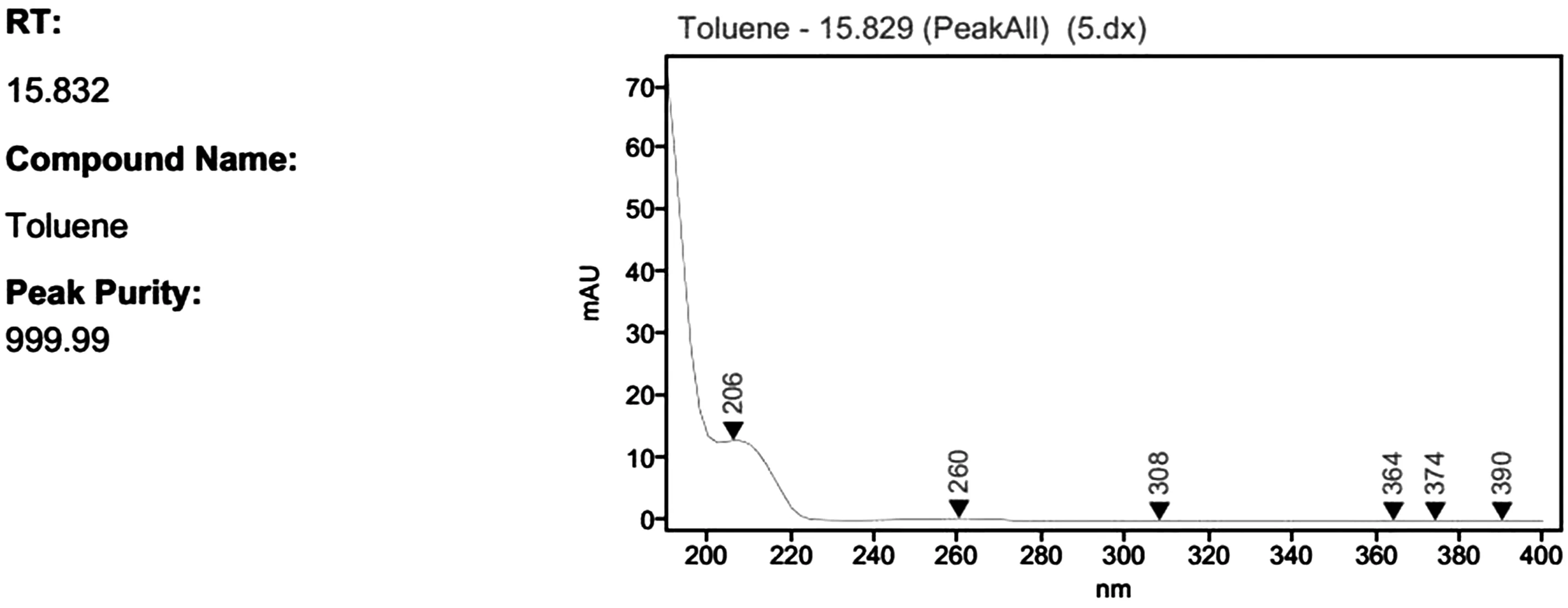
图4 标样中甲苯的峰纯度图
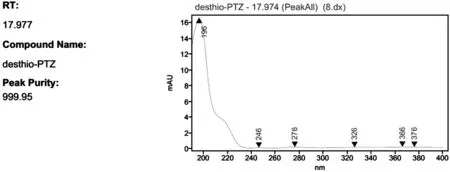
图5 试样中脱硫丙硫菌唑的峰纯度图

图6 试样中甲苯的峰纯度图
3.3 分析方法线性相关性 按1.3.1标样溶液的配制方法,准确制备6个质量浓度递增的脱硫丙硫菌唑和甲苯线性相关溶液。按标准规定的操作步骤进行分析,测定线性溶液中脱硫丙硫菌唑和甲苯的峰面积,取2次测定的平均结果,结果(表1~2)。以脱硫丙硫菌唑(甲苯)质量浓度为横坐标,峰面积为纵坐标绘制标准曲线,从而得到脱硫丙硫菌唑和甲苯的线性相关曲线(图7~8)。
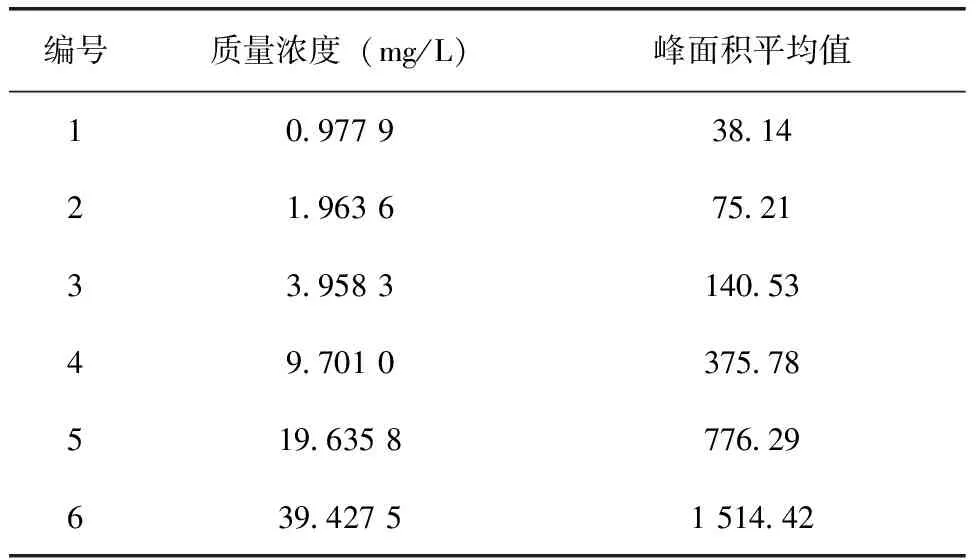
表1 脱硫丙硫菌唑线性范围的测定
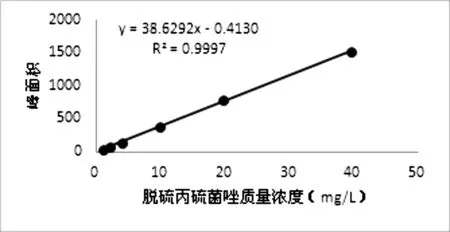
图7 脱硫丙硫菌唑峰面积与质量浓度线性关系图
图7中,当脱硫丙硫菌唑质量浓度0.977 9 ~ 39.427 5mg/L,线性回归方程为y=38.629 2x-0.413 0,相关系数R2= 0.999 7,符合要求。
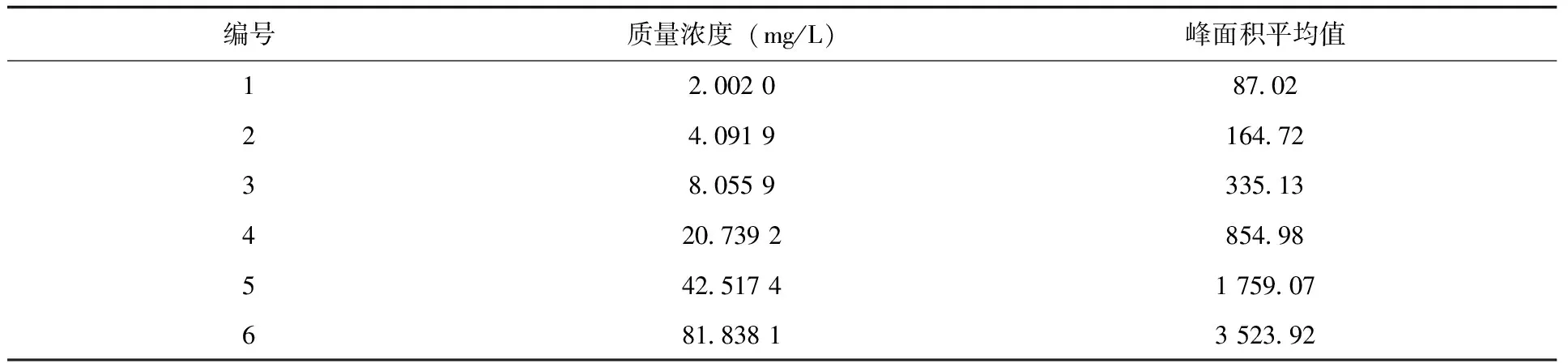
表2 甲苯线性范围的测定
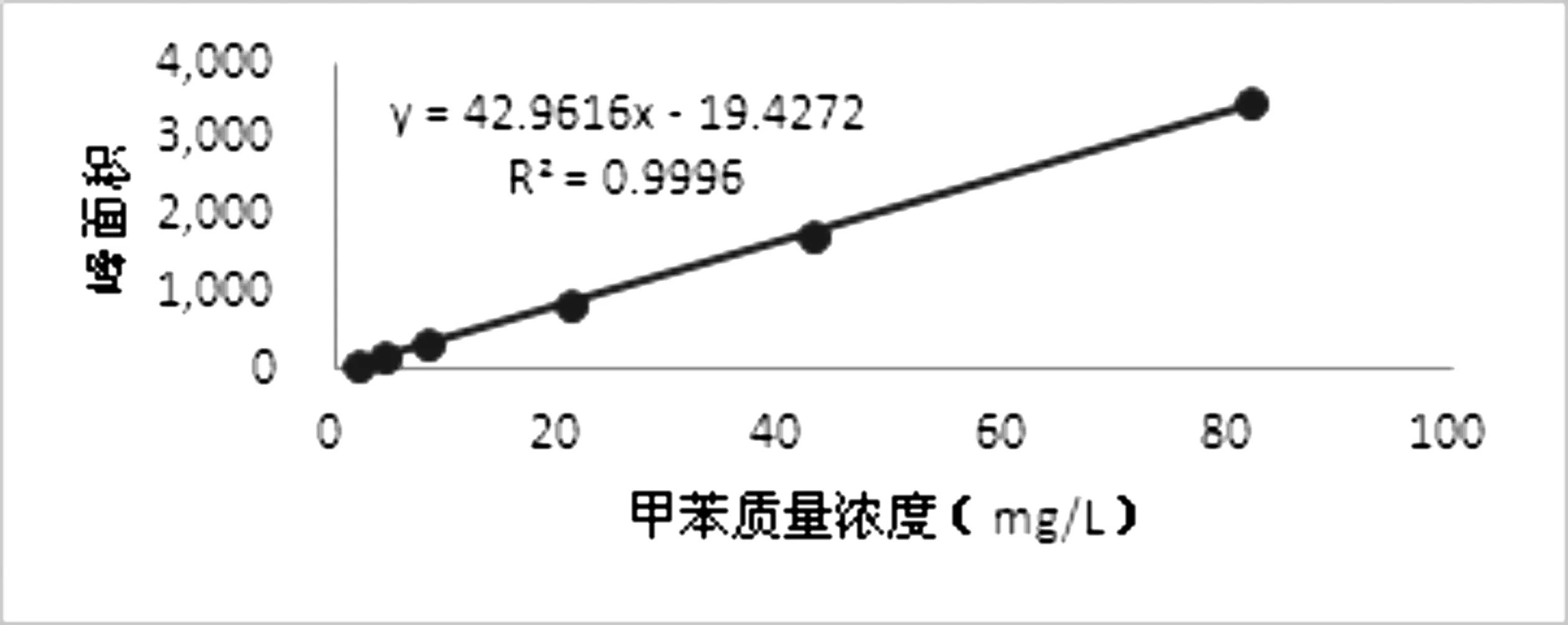
图8 甲苯峰面积与质量浓度线性关系图
图8中,当甲苯质量浓度2.002 0 ~ 81.838 1mg/L,线性回归方程为y = 42.961 6x - 19.427 2,相关系数R2= 0.999 6,符合要求。
3.4 分析方法精密度 按1.3.2试样溶液的制备方法配制6个丙硫菌唑原药的样品溶液。在前述色谱操作条件下,对样品平行测定。脱硫丙硫菌唑的标准偏差为0.000 5,变异系数为1.61%(表3)。小于修改的Horwitz公式2(1-0.5logC)×0.67=4.52%,脱硫丙硫菌唑分析方法精密度的测定结果符合要求。

表3 丙硫菌唑原药中的脱硫丙硫菌唑精密度实验结果
甲苯的标准偏差为0.000 8,变异系数为0.56%(表4)。小于修改的Horwitz公式2(1-0.5logC)×0.67=3.60%,甲苯分析方法精密度的测定结果符合要求。
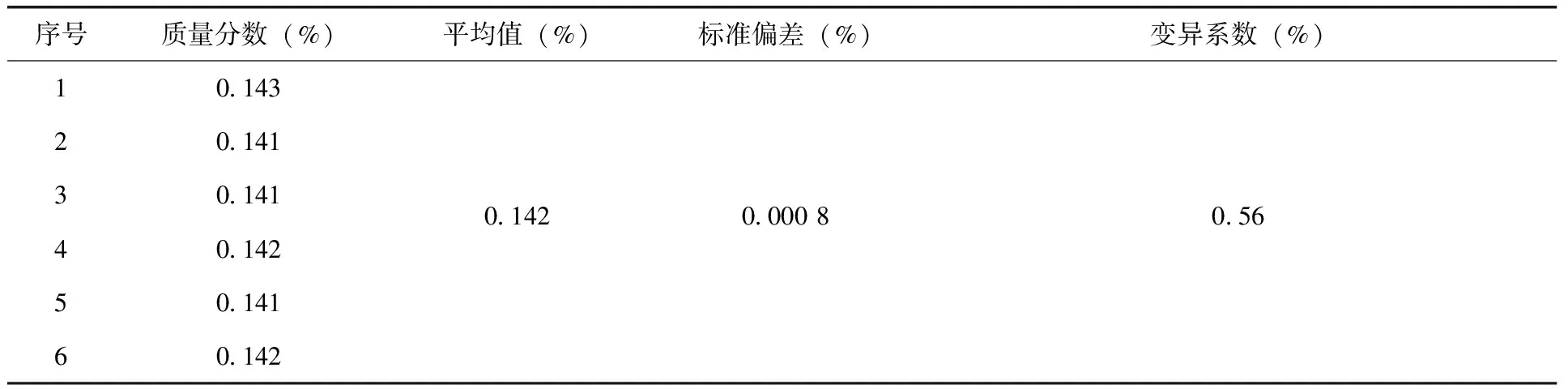
表4 丙硫菌唑原药中的甲苯精密度实验结果
3.5 分析方法准确度 称取约0.25g丙硫菌唑的样品于25mL容量瓶中,再分别移入1.3.1中标样储备液0.25mL(含脱硫丙硫菌唑约0.125mg、甲苯约0.25mg),按1.3.2试样溶液的制备方法配制6个样品溶液,用作准确度试验。在前述操作条件下进行测定,脱硫丙硫菌唑平均回收率94.6%,结果(表5),具有良好的准确度。

表5 丙硫菌唑原药中脱硫丙硫菌唑回收率试验结果
甲苯平均回收率102.1%,结果(表6),具有良好的准确度。
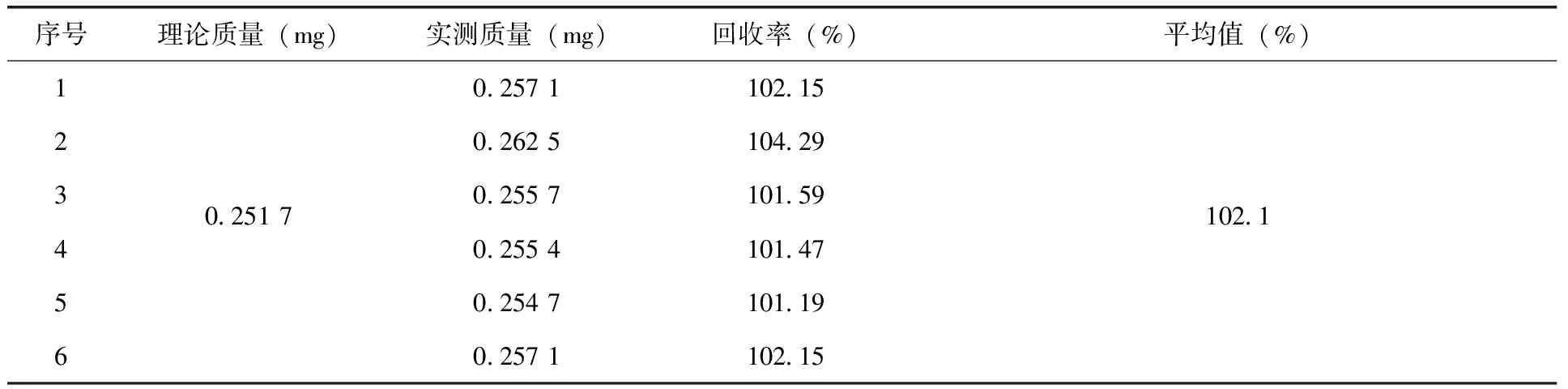
表6 丙硫菌唑原药中甲苯回收率试验结果
3.6 分析方法定量限 2.3中线性最低点标样溶液中脱硫丙硫菌唑浓度为0.977 9mg/L,甲苯浓度为2.002 0mg/L,它们的信噪比数据分别为10.8和11.9,该溶液浓度可用来计算分析方法的定量限,计算得到脱硫丙硫菌唑定量限为0.005%,甲苯定量限为0.01%。
4 结论
本文建立了同时测定丙硫菌唑产品中测定脱硫丙硫菌唑和甲苯的分析方法。此方法具有高精密度和高准确度的特点,其分离效果、线性关系良好,定量限符合相关产品标准中相关杂质的限量要求,实验操作简便,是进行该类产品中相关杂质检测较理想的分析方法。
