自身免疫性胃炎的临床及内镜下表现(附31例报告)
2022-02-17曾丽妮吴伟东雷延昌
曾丽妮,吴伟东,雷延昌
(柳州市人民医院消化内科,广西柳州 545006)
自身免疫性胃炎又称为A型胃炎,是自身免疫机制导致的慢性萎缩性胃炎,主要表现为胃底、胃体黏膜萎缩及胃窦黏膜正常,血清存在自身抗体,部分患者还可合并贫血及自身免疫性疾病。欧美的发病率明显高于亚洲[1]。随着我国消化内科技术的发展,这类疾病的发现率逐年增加。本研究回顾性分析31 例自身免疫性胃炎患者的临床资料,旨在提高临床对自身免疫性胃炎的诊断水平。现报道如下:
1 资料与方法
1.1 一般资料
回顾性分析2019年1月-2020年12月柳州市人民医院消化内科31 例经血清学抗体测定确诊为自身免疫性胃炎患者的临床资料。其中,男8 例,女23例,男女比为1.0∶2.9,年龄29~78 岁,平均(40.78±11.53)岁。纳入标准:胃底、胃体黏膜萎缩及胃窦黏膜正常者;血清中存在抗胃壁细胞抗体或/和内因子抗体者。
1.2 研究方法
收集患者的临床病例资料,进行整理、归纳、总结。分析患者的临床表现、胃镜检查、病理检查、合并症、胃蛋白酶Ⅰ/Ⅱ比值及胃泌素-17等资料,并对患者进行随访。
2 结果
2.1 临床表现
31 例自身免疫性胃炎患者中,纳差14 例,上腹胀12 例,偶有上腹不适症状10 例。12 例贫血患者中,缺铁性贫血7 例,巨幼红细胞贫血5 例。合并胃神经内分泌肿瘤4例,合并脊髓亚联综合征2例。
2.2 内镜特点
内镜下特征为在胃底腺区域(胃体部和胃底部)高度萎缩,表现为:黏膜变薄,血管纹理透见,胃窦部没有明显萎缩。患者早期出现红色结节样的多发性假息肉,部分患者可见胃体、胃底区域黏膜下隆起。见图1。
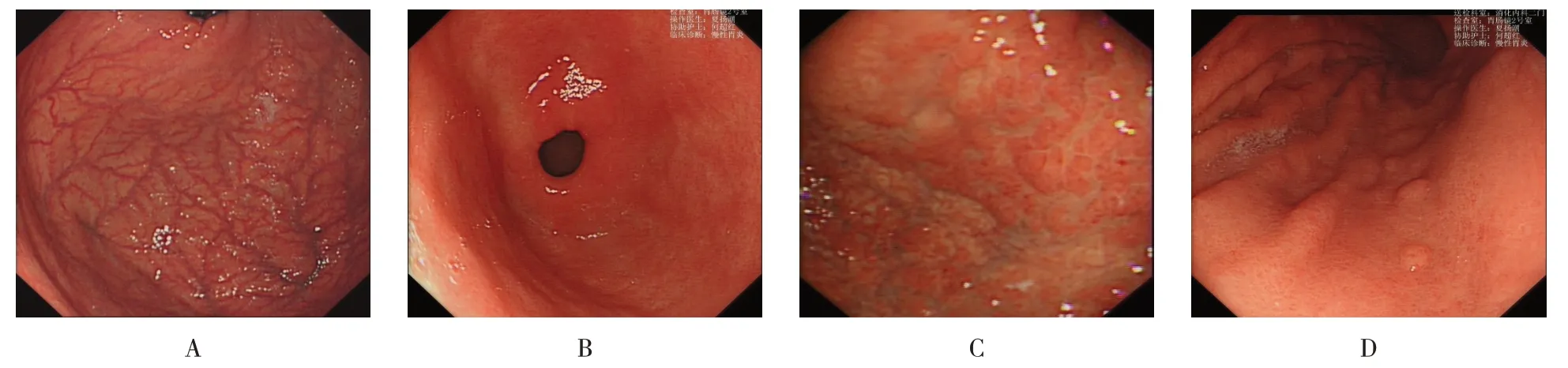
图1 自身免疫性胃炎的内镜特点Fig.1 Endoscopic characteristics of autoimmune gastritis
2.3 病理特点
组织病理为胃体/胃底具有不同程度的固有腺体萎缩,固有层弥漫性淋巴细胞、浆细胞浸润,伴有不同程度的肠上皮化生及假幽门腺化生。黏膜下隆起病理为神经内分泌肿瘤。见图2。
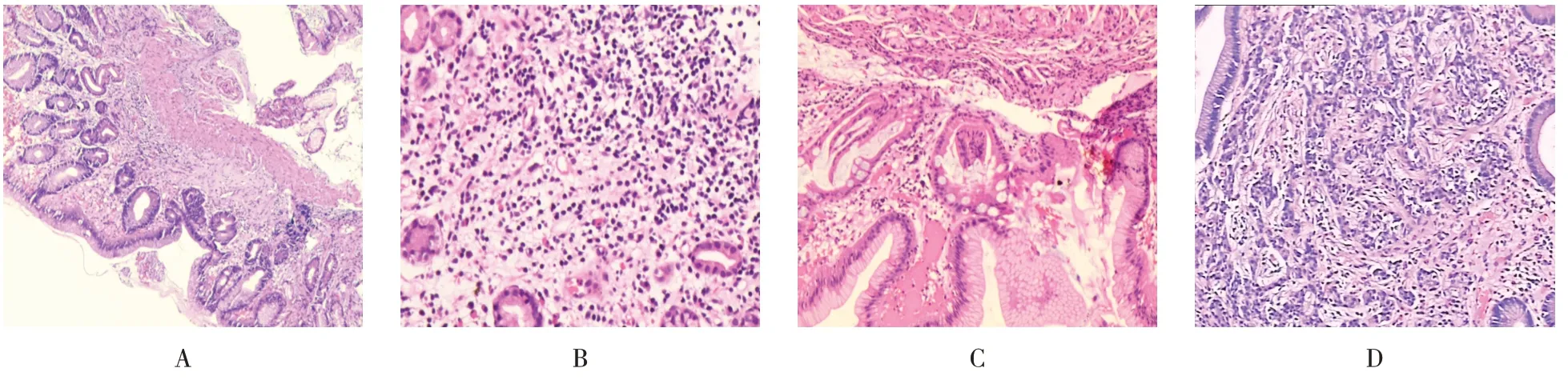
图2 自身免疫性胃炎的病理特点Fig.2 Pathological characteristics of autoimmune gastritis
2.4 实验室检查
单纯壁细胞阳性28 例,单纯内因子抗体阳性3例,抗胃壁细胞抗体及内因子抗体均阳性6例。有13例患者行胃泌素-17 和胃蛋白酶原检查,8 例出现胃泌素-17升高,胃蛋白酶原Ⅰ/Ⅱ比值下降。幽门螺旋杆菌抗体测定10 例阳性。合并自身免疫性疾病:Ⅰ型糖尿病1例,自身免疫性甲状腺炎1例。
2.5 随访
4例合并神经内分泌肿瘤患者采用氩气刀及内镜下黏膜切除术治疗,完整切除肿物。其中,2例随访1年余,2 例随访3~8 个月,均无复发。合并脊髓亚联综合征患者补充维生素B12后,神经系统症状改善。巨幼红细胞贫血及缺铁性贫血患者分别补充维生素B12及二价铁后,血红蛋白较前上升。
3 讨论
国外有研究[2]显示,自身免疫性胃炎的发病率为2%,且随年龄增长而增加。亚洲国家发病率低于西方国家[1]。有研究[3]显示,每年门诊胃镜检查中自身免疫性胃炎的检出率为0.9%。本研究共纳入6 000例胃镜检查患者,共检出31 例,检出率为0.5%,低于文献[3]报道,考虑原因为:自身免疫性胃炎症状无特异性,本院医师对本病认知度不够。
自身免疫性胃炎的发病机制是:CD4+T细胞介导胃壁细胞分泌小管膜上的H+/K+ATP 酶产生自身免疫反应,导致壁细胞破坏,从而出现临床症状[4]。本院31 例病例中,10 例患者幽门螺杆菌抗体呈阳性。自身免疫性胃炎中,幽门螺杆菌感染征象阳性;幽门螺杆菌胃炎中,自身免疫血清标志物阳性,提示:幽门螺杆菌在胃黏膜自身免疫诱导和/或维持过程中起着重要作用[5-6],推测幽门螺旋杆菌可能是自身免疫反应的感染性触发因素。幽门螺旋杆菌感染引起上皮细胞受损,H+/K+ATP 酶暴露于抗原呈递细胞;幽门螺旋杆菌蛋白肽含有与壁细胞质子泵相似的序列,通过分子模拟,使CD4+T 细胞交叉识别H+/K+ATP 酶和各种幽门螺旋杆菌蛋白抗原,产生免疫反应[7]。
目前,诊断自身免疫性胃炎主要依据为:内镜下胃黏膜萎缩部位、组织病理及自身抗体。在疾病初期,胃镜下表现可能与正常胃黏膜没有区别,随着酸分泌障碍加重导致胃黏膜巢状破坏[8],可能会出现假性息肉。有研究[9]发现,红色结节为多发性假息肉,是早期自身免疫性胃炎的特征性内镜表现。随着萎缩的进展,胃黏膜皱襞逐渐变平,黏膜下血管透见。如未合并幽门螺旋杆感染,患者胃窦黏膜一般正常[10]。自身免疫性胃炎病理特征以局限胃体的萎缩性胃炎为表现,伴有不同程度的肠上皮化生、假幽门腺化生、胰腺腺泡化生和肠嗜铬样细胞增生。自身免疫性胃炎患者抗胃壁细胞抗体和/或内因子抗体阳性,但临床表现缺乏特异性,部分患者表现为纳差、上腹胀症状,与胃酸分泌减少有关。贫血是自身免疫性胃炎的主要临床表现之一,自身免疫性胃炎使胃体胃底的壁细胞被破坏,导致内因子缺乏,从而引起维生素B12吸收障碍,患者晚期出现恶性贫血和脊髓亚急性联合变性。铁是主要的造血原料,人们进食时,含铁食物在胃酸的作用下释放出铁离子,与肠内容物中某些糖和氨基酸形成络合物,在十二指肠吸收。胃酸缺乏时,食物中的三价铁不能还原为二价铁,使铁的吸收变困难,从而引起缺铁性贫血。因此,慢性铁缺乏患者,尤其是对于口服铁效果不佳的患者,应考虑是否存在自身免疫性胃炎[11]。
低胃蛋白酶原Ⅰ/Ⅱ比值和高胃泌素-17水平是自身免疫性胃炎典型的实验室表现。发生自身免疫性胃炎时,T 细胞分泌胃蛋白酶原Ⅰ的胃体壁细胞是靶标,而分泌胃蛋白酶原Ⅱ的胃窦腺体未受影响,但胃蛋白酶原Ⅰ下降,会导致胃蛋白酶原Ⅰ/Ⅱ比值下降。壁细胞受损导致缺酸状态,促使胃窦G细胞持续产生胃泌素,且没有壁细胞对其反馈抑制,导致高胃泌素血症,进一步刺激肠嗜铬样细胞增生。在长期升高的胃泌素作用下,肠嗜铬样细胞增殖进展为胃神经内分泌肿瘤(Ⅰ型)[12]。MAGRIS等[13]研究报道,15.4%的自身免疫性胃炎患者同时观察到胃神经内分泌肿瘤,受试者操作特征曲线分析显示:胃蛋白酶原Ⅰ/Ⅱ比值<2.3、胃泌素-17水平>29.6 pmol/L是区分自身免疫性胃炎患者是否合并胃神经内分泌肿瘤的基线。
综上所述,自身免疫性胃炎起病隐匿,早期缺乏特异性,常以贫血为首发表现,并合并其他自身免疫疾病,如:Ⅰ型糖尿病、自身免疫性甲状腺炎、白癜风、重症肌无力和自身免疫性肝炎等。巨幼红细胞贫血或慢性缺铁性贫血补铁效果欠佳者,要考虑是否合并自身免疫性胃炎。内镜检查发现逆向萎缩表现时,应在胃底、胃体和胃窦进行多点活检病理,完善抗胃壁细胞抗体和内因子抗体检查,以排除自身免疫性胃炎。目前无根治自身免疫性胃炎的方案,应注意随访。如果检测到幽门螺旋杆感染,应及时治疗并根除。维生素B12、叶酸及铁缺乏者要进行相应补充。对于合并神经内分泌肿瘤的患者,视浸润深度及淋巴结转移情况行内镜下治疗或者外科手术。但本研究病例数有限,今后仍需大样本数据进行研究,以提供更多的参考依据。
