123例替罗非班致药物不良反应文献分析
2022-02-15孙牧新原永芳
孙牧新,原永芳
(1.上海交通大学医学院附属第九人民医院药剂科,上海 201900;2.上海交通大学医学院附属第九人民医院,上海 201900)
盐酸替罗非班是一种血小板糖蛋白Ⅱb/Ⅲa受体的可逆性拮抗剂,该受体是与血小板聚集过程有关的主要血小板表面受体[1]。血小板激活、黏附和聚集是粥样斑块破裂表面动脉血栓形成的关键性起始步骤,盐酸替罗非班阻止纤维蛋白与糖蛋白Ⅱb/Ⅲa受体结合,从而阻断血小板的交联及聚集。临床上,盐酸替罗非班尤其在经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)以及急性冠状动脉综合征(acute coronary syndrome,ACS),即冠心病中急性发病的临床类型中被广泛应用[2-3],ACS包括急性ST段抬高型心肌梗死、非ST段抬高型心肌梗死和不稳定型心绞痛。随着替罗非班的在临床上广泛应用,有关其药物不良反应(adverse drug reaction,ADR)的个例报道也逐渐增多。替罗非班说明书中记录的常见不良反应有出血、血小板减少、过敏反应、寒战等。本文通过文献检索对2010年1月至2020年12月的替罗非班ADR病例报道进行回顾性分析,旨在提高临床替罗非班的用药安全性,降低临床用药过程中ADR的发生率。
1 资料与方法
1.1 资料来源
检索中国知网数据库、万方数据库、维普数据库、中国生物医学文摘数据库、中华医学会期刊、PubMed和Web of Science,中文检索词为“替罗非班”“不良反应”或“致”;英文检索词为“tirofiban”“adverse”“induced”“associated”或“related”,检索时间均为2010年1月至2020年12月。文献排除标准:资料完整性及翔实性较差;同一病例重复报道;同期对照临床研究或观察报道、综述及无法判断ADR相关性的报道。共筛选出该药的ADR案例报道英文12篇和中文86篇,98篇文献案例报道中共报道123例替罗非班ADR。
1.2 判定标准
替罗非班诱导的血小板减少症(tirofiban-induced thrombocytopenia,TIT):应用替罗非班24 h内血小板计数下降至<100×109/L,分为轻度(血小板计数<100×109/L)、重度(血小板计数<50×109/L)、极重度(血小板计数<20×109/L)[4]。
1.3 方法
采用回顾性分析方法,详细阅读检索出的98篇文献,用Excel记录发生替罗非班ADR的患者性别、年龄、临床诊断及既往史、不良反应名称、不良反应发生时间、累及器官/系统及临床表现、治疗和转归等有效信息,并进行详细的归纳和分析。累及器官/系统及临床表现参照国家ADR监测中心编译的《WHO ADR术语集》[5],关联性评价标准参照我国《ADR报告和监测管理办法》[6]。
1.4 统计学方法
采用SPSS 19.0统计学软件进行数据分析,计量资料以均数±标准差(x±s)表示,组间比较采用t检验或单因素方差分析,计数资料以率(%)表示。P≤0.05为差异有统计学意义。
2 结果
2.1 患者性别与年龄分布
123例替罗非班ADR中,男性99例,女性24例,平均年龄(63.02±11.30)岁,其中71~80岁年龄段ADR发生率最高,占26.8%,见表1。

表1 123例替罗非班ADR患者性别与年龄分布
2.2 替罗非班ADR累及器官/系统及临床表现
123例替罗非班ADR中,共出现303例次ADR。根据《WHO ADR术语集》,对替罗非班所致ADR累及系统/器官进行分类,总共累及10个系统,其中累及血液系统的损害最多(50.8%),其次为累及皮肤及其附件的损害(17.4%),见表2。

表2 替罗非班ADR累及器官/系统及临床表现
2.3 替罗非班ADR的处理、关联性评价及转归
123例替罗非班ADR患者中,应用14种处理方法(单独或者联合应对替罗非班产生的药物不良反应),其中51例(41.5%)停药后未予特殊处理自行恢复,13例(10.6%)停药后给予糖皮质激素和输血小板治疗后恢复,9例(7.4%)停药后给予糖皮质激素后恢复,9例(7.4%)停药后输血小板治疗后恢复,见表3。根据《ADR报告和监测管理办法》中ADR关联性评价标准对123例ADR进行评价:描述为“肯定”10例,“可能”18例,“很可能”95例;对患者发生ADR后的转归情况进行统计:115例痊愈,4例好转,4例死亡,见表3。
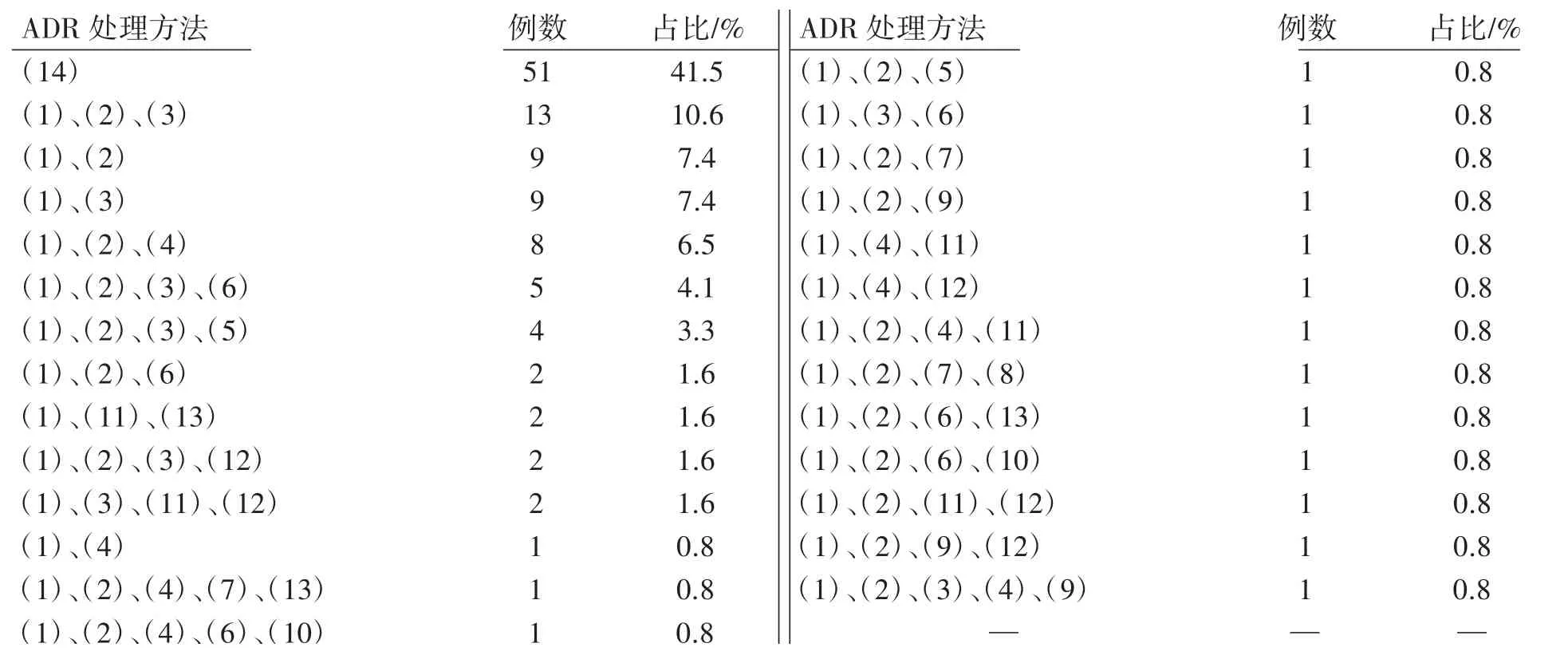
表3 替罗非班ADR的处理方法
2.4 首次监测替罗非班致血小板计数下降及其恢复时间
首次监测替罗非班致轻度、重度、极重度血小板下降平均时间呈现延长趋势,但组间比较,差异无统计学意义(F=0.897 8,P=0.410 8);此外,轻度、重度、极重度血小板下降后平均恢复时间增加(F=3.934,P=0.022 7),见表4。
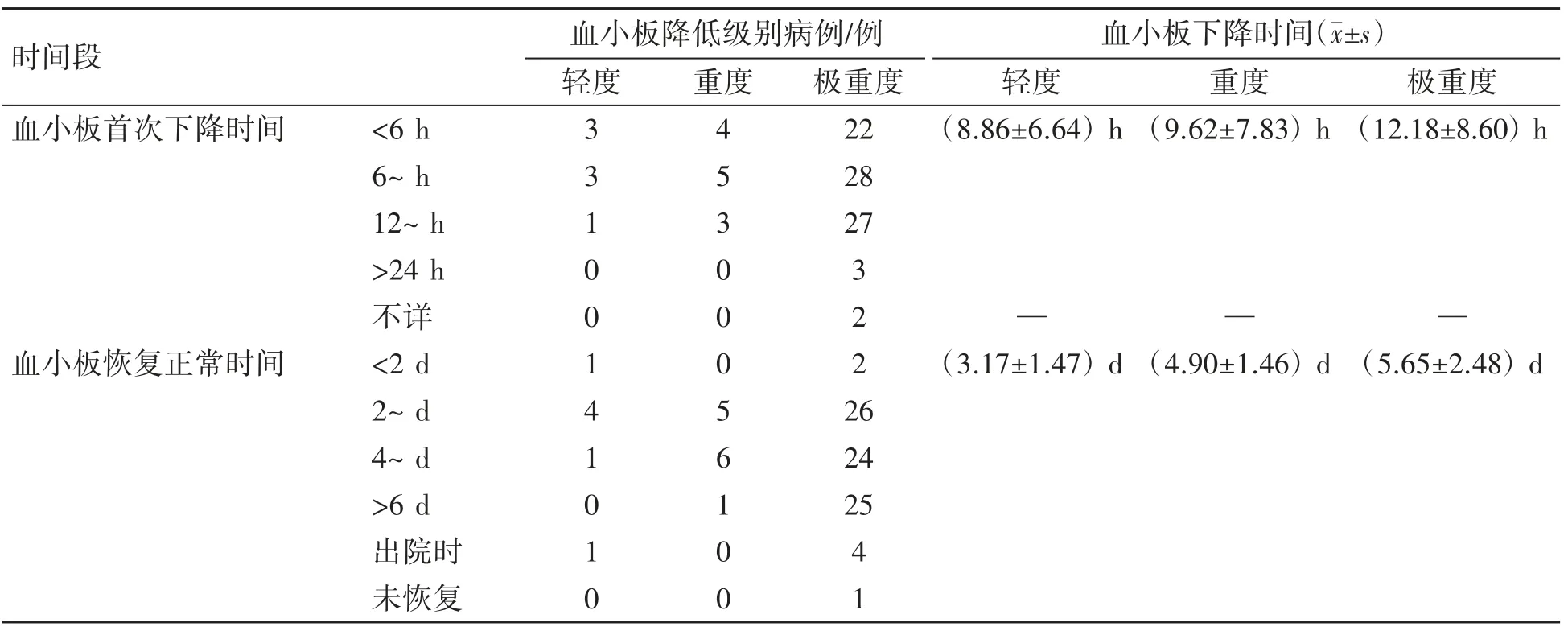
表4 首次监测替罗非班致血小板计数下降及其恢复时间
2.5 替罗非班用药前后血小板恢复水平情况
检索出的替罗非班ADR中轻度、重度、极重度血小板下降病例数分别为7例、12例、82例;替罗非班用药前与用药后相比较,极重度血小板平均下降值最低,其次是重度,见表5。

表5 替罗非班用药前后血小板计数及停用处理后时间情况变化(x±s)
3 讨论
替罗非班ADR发生病例数男性高于女性,这与关于替罗非班致ADR研究[7-8]结果相一致。检索出的123例患者中,90%以上患者患有ACS或ACS合并其他疾病,可能与替罗非班在临床上主要用于ACS疾病本身有关。据研究[9-10]报道,ACS患者中,男性发病率明显高于女性。性别差异造成ADR发生率的不同可能与男性和女性体内激素水平不同有关联,但还需要进一步研究证实。本研究结果显示,随着年龄的升高,替罗非班ADR的发生率也升高,说明替罗非班临床应用中患者年龄也是其临床应用的风险因素之一,患者年龄越高,则越要注意替罗非班ADR事件的发生。
替罗非班所致ADR累及系统/器官共分为10类,其中以替罗非班累及血液系统的ADR位居首位,临床表现以出血和血小板减少最为常见。目前,替罗非班致血小板减少的机制尚不明确,很可能与替罗非班的作用机制有关。有一种免疫介导的假说机制:替罗非班主要作用于血小板,与血小板膜糖蛋白Ⅱb/Ⅲa受体结合使后者构象发生改变,阻止纤维蛋白与糖蛋白Ⅱb/Ⅲa受体结合,形成新的抗原决定簇,最终被肝脏或血液中预存的抗体识别、清除[11];还有一种血小板的再分布机制假说:替罗非班与血小板膜糖蛋白Ⅱb/Ⅲa受体结合,使血小板的受体发生空间构象改变,产生新的抗原决定簇,该抗原决定簇被肝脏识别后被肝脏摄取。替罗非班与血小板是可逆性结合,随着血液中替罗非班药物浓度的降低,被肝脏摄取的血小板可再重新回到血液循环中[12]。
123例患者中有41.5%停用替罗非班后ADR可自行恢复。糖皮质激素治疗、输血小板、质子泵抑制剂、输血浆、静注人免疫球蛋白、凝血酶冻干粉溶于生理盐水后漱口、口服或输注血液凝固药物、口服或输注升血小板药物、注射多巴胺等升血压治疗,都是针对替罗非班产生血小板减少和出血的应对方法。尽管替罗非班诱导的TIT的发生率很低,为1%~2%[13-15],然而一旦发生TIT,出血并发症的风险极大,严重时甚至危及生命。因此,一旦发现血小板减少,应立即停用所有替罗非班等抗血小板和抗凝药物,多数患者的血小板在短期内可以恢复[16],必要时输注新鲜血小板、应用激素、注射丙种球蛋白[17-19]都是可选择的治疗手段。
本研究结果显示,首次监测血小板下降平均时间:轻度TIT、重度TIT、极重度TIT分别是8.86 h、9.62 h、12.18 h;血小板恢复正常时间:轻度TIT、重度TIT、极重度TIT分别是3.17 d、4.90 d、5.65 d。TIT常发生在用药后2~24 h,停药后恢复较快,多数于停药1~6 d后即可恢复至正常范围,与相关研究[20-21]结果一致。TIT通常分为5种类型:1)第一次接触后的12 h内急性严重TIT(血小板<10×109/L);2)第二次接触后的12 h内急性TIT;3)延迟TIT(治疗后57 d);4)第一次或第二次接触后出现过敏反应;5)假性TIT[22]。本研究显示,轻度、重度、极重度血小板下降恢复平均时间增加。因此,应用替罗非班的临床患者应当密切监测血小板计数,及时发现血小板减少情况,避免或减少重度TIT和极重度TIT所致ADR的发生,提高用药安全性。
针对替罗非班所致的不良反应采取的临床防治措施有:1)用药前评估患者应用替罗非班的风险和药物使用的必要性[23];2)临床药师应该对应用替罗非班的患者进行用药宣教,告知患者密切观察自身有无皮疹、牙龈出血、黑便、皮肤瘀点瘀斑、寒战等早期症状,如有上述症状应立即告知医生和护士,以便及时处理和治疗。这样不仅可以避免患者产生ADR带来的恐慌、焦虑、紧张情绪,而且可以起到ADR预警作用[24];3)应主动监测应用替罗非班患者的血小板计数,建议用药前和用药后1 h、2 h、4 h、6 h、24 h内复查患者的血小板计数,以便尽早发现血小板的变化[25];4)如发生TIT,正确评估患者出血及血栓的风险至关重要,应及时停用替罗非班,结合患者临床表现及血小板计数,适时加用其他抗栓治疗,防止血栓形成;一旦发生重度或极重度TIT,停用替罗非班等血小板糖蛋白Ⅱb/Ⅲa受体拮抗剂,同时进行血栓弹力图检查显示最大振幅[26],或者进行血液凝固常规检查,以明确出血风险。必要时可考虑输入血小板、输血浆、静注人免疫球蛋白等治疗,避免血小板减少引起严重不良反应事件的发生。
综上所述,临床应加强对使用替罗非班患者的用药安全性监测,做好药物警戒工作,特别是谨慎替罗非班造成的TIT、出血等并发症的风险。一旦出现ADR,应立即停药,加强临床观察并及时对症治疗,保证临床用药安全性。
