基础疾病负担对药物性肝损伤严重程度及预后的影响
2022-02-15武亭王艳刘立伟李柯鑫王昱欧晓娟贾继东赵新颜马红
武亭 王艳 刘立伟 李柯鑫 王昱 欧晓娟 贾继东 赵新颜 马红
药物性肝损伤(drug-induced liver injury,DILI)的发病率逐年升高,国外发病率为2.3~19.1/10万[1],我国发病率为23.8/10万[2]。绝大多数DILI患者肝功能可恢复正常,约13%的DILI患者迁延不愈转变为慢性药物性肝损伤,10%的患者2年内需要肝移植或死亡[2-3]。
DILI可发生在合并有多种基础疾病的患者中,也可发生在无基础疾病的患者中,合并基础疾病负担重的患者损伤重、预后差[3-4]。中国人群遗传背景及肝损伤药物种类与西方国家存在较大差异,基础疾病是否对中国DILI患者有类似影响,需要进一步研究验证。为此,根据国际通用标准[5],本研究将各类基础疾病进行量化分组,以明确基础疾病负担对中国DILI患者严重程度及预后的影响,为DILI的诊疗及预后评估提供参考依据。
资料与方法
一、研究对象及纳入排除标准
筛选2016年1月1日至2019年12月31日于北京友谊医院肝病中心出院诊断为DILI的患者。纳入标准:①符合中华医学会肝病学分会药物性肝病学组2017年发表的《药物性肝损伤诊治指南》[6]诊断标准,RUCAM因果评分≥3分;②符合以下条件之一[7]:ALT≥5正常值上限(ULN);ALP≥2 ULN;ALT≥3 ULN 且 TBil≥2 ULN。排除标准:①合并非药物因素导致的肝损伤,如病毒性肝炎、自身免疫性肝病、酒精性肝病、脂肪性肝炎、遗传代谢性肝病、肝细胞癌等;②资料不完整;③失访。
二、资料收集
采集入组患者的年龄、性别、体重指数、住院天数、用药种类、伴随的基础疾病及实验室指标(ALT、AST、碱性磷酸酶、谷氨酰转肽酶、总胆红素、直接胆红素、胆汁酸、胆碱酯酶、白蛋白、球蛋白、肌酐、尿酸、血糖、国际标准化比值、白细胞、嗜酸性粒细胞百分比、血红蛋白、血小板、免疫球蛋白G)以及临床预后等。
三、分组
使用查尔森合并症指数对目前出现的基础疾病进行量化,CCI根据伴随或不伴随以下基础疾病而建立:心肌梗死、充血性心衰、周围血管疾病、脑血管病、痴呆、慢性阻塞性肺病、结缔组织病、消化性溃疡、肝脏疾病(轻度或重度)、糖尿病、晚期肾脏疾病、实体肿瘤(伴或不伴转移)、白血病或淋巴瘤以及获得性免疫缺陷综合征等。每种疾病根据其预后赋值于不同的分值(1~6分),这些分数之和构成最终的CCI值。参考CCI在药物性肝损伤及心功能衰竭等不同疾病中的研究[3,8],将患者分为无或轻度基础疾病负担组(CCI≤2)和显著基础疾病负担组(CCI>2),本研究肝脏疾病仅包括脂肪肝(影像学诊断)。
四、临床分型、严重程度及预后判断标准
DILI临床分型参照国际临床分型标准[9],分为肝细胞损伤型(R≥5)、混合型(5>R>2)和胆汁淤积型(R≤2);R=(ALT实测值/ULN)/(ALP实测值/ULN)。
严重程度参考文献[6]分为5级。
临床预后主要包括恢复正常、慢性化及肝移植或者死亡。恢复正常:1年内临床症状完全消失或显著好转,转氨酶、胆红素、碱性磷酸酶、胆碱酯酶等血生化指标完全恢复正常;慢性化:参考欧洲指南[10],1年时仍存在肝脏生化持续异常或发展为肝硬化。肝移植或者死亡:因肝功能衰竭行肝移植术或者死亡,以及非肝脏原因死亡。
五、统计学分析
结 果
一、无或轻度与显著基础疾病负担组患者基础疾病构成
313例DILI患者纳入本研究,包括CCI 0分的患者134例,1分88例,2分50例,3分23例,4分14例,5分3例,6分1例。无或轻度基础疾病负担患者272例(87%),显著基础疾病负担患者41例(13%),与无或轻度基础疾病负担组相比,显著基础疾病负担组合并脂肪肝、外周血管疾病、糖尿病、冠状动脉粥样硬化性心脏、实体肿瘤及脑血管疾病比例显著增高,差异均有统计学意义(均P<0.01),见表1。本研究涉及的实体肿瘤包括食管癌、肺癌、肾癌、前列腺癌各1例。
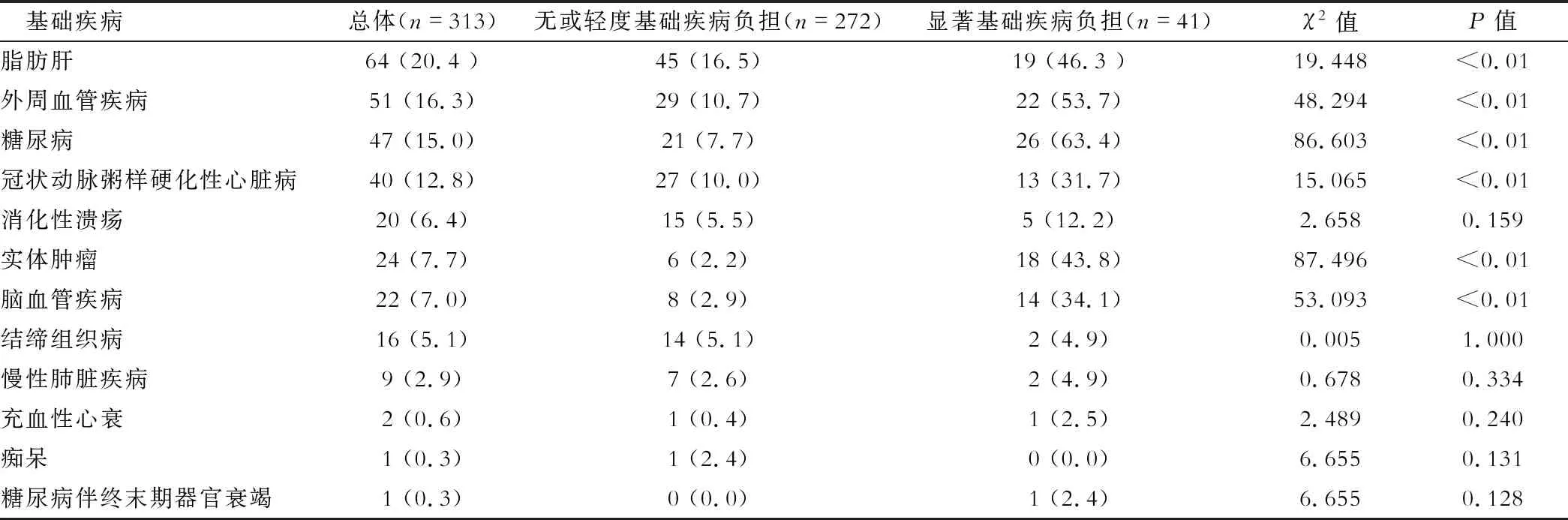
表1 无或轻度与显著基础疾病负担患者基础疾病比较[例(%)]
二、无或轻度与显著基础疾病负担组患者临床特征比较
两组临床特征比较见表2。显著基础疾病负担组发病年龄及体重指数、GGT发病初始值及峰值、肌酐、葡萄糖值均显著高于无或轻度基础疾病负担组(均P<0.01)。性别、临床分型、凝血功能、IgG等两组差异无统计学意义(均P>0.05)。
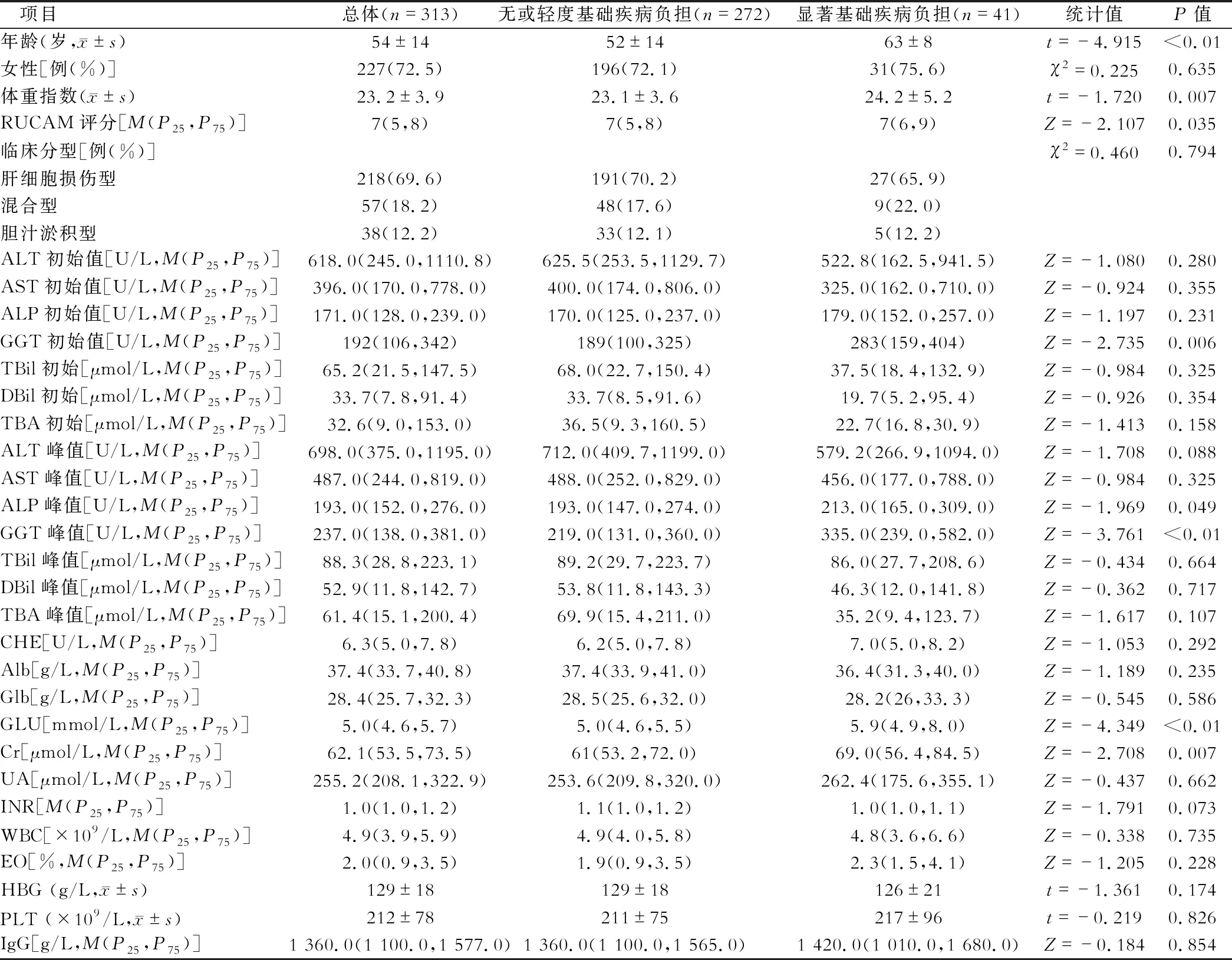
表2 无或轻度与显著基础疾病负担组临床特征比较
三、无或轻度与显著基础疾病负担组致病药物种类比较
本研究中引起肝损伤的药物以中药最为常见,其次为西药及复合药(中药+西药),中药诱导的DILI在无或轻度基础疾病负担组所占的比例较显著基础疾病负担组高,西药、复合药在显著基础疾病负担组所占的比例较无或轻度基础疾病负担组高,但差异无统计学意义(χ2=4.518,P=0.376),见表3。

表3 无或轻度与显著基础疾病负担组致病药物种类比较[例(%)]
四、无或轻度与显著基础疾病负担组患者严重程度及临床结局比较
显著基础疾病负担组和无或轻度基础疾病负担组相比,严重程度分级、住院天数、入住ICU比例、MELD评分差异均无统计学意义(均P>0.05)。
本队列随访的中位数时间为2.35年,79.9%DILI患者恢复正常,13.1%发展为慢性DILI,7.0%接受肝移植或者死亡,其中1.9%的DILI患者因食管癌、肺癌、肾癌、前列腺癌、阵发性睡眠性血红蛋白尿、慢性阻塞性肺疾病等慢性病死亡。显著基础疾病负担组全因病死率及非肝脏相关病死率高于无或轻度基础疾病负担组,差异有统计学意义(P<0.01),肝病相关死亡/肝移植率差异无统计学意义(P>0.05),见表4。
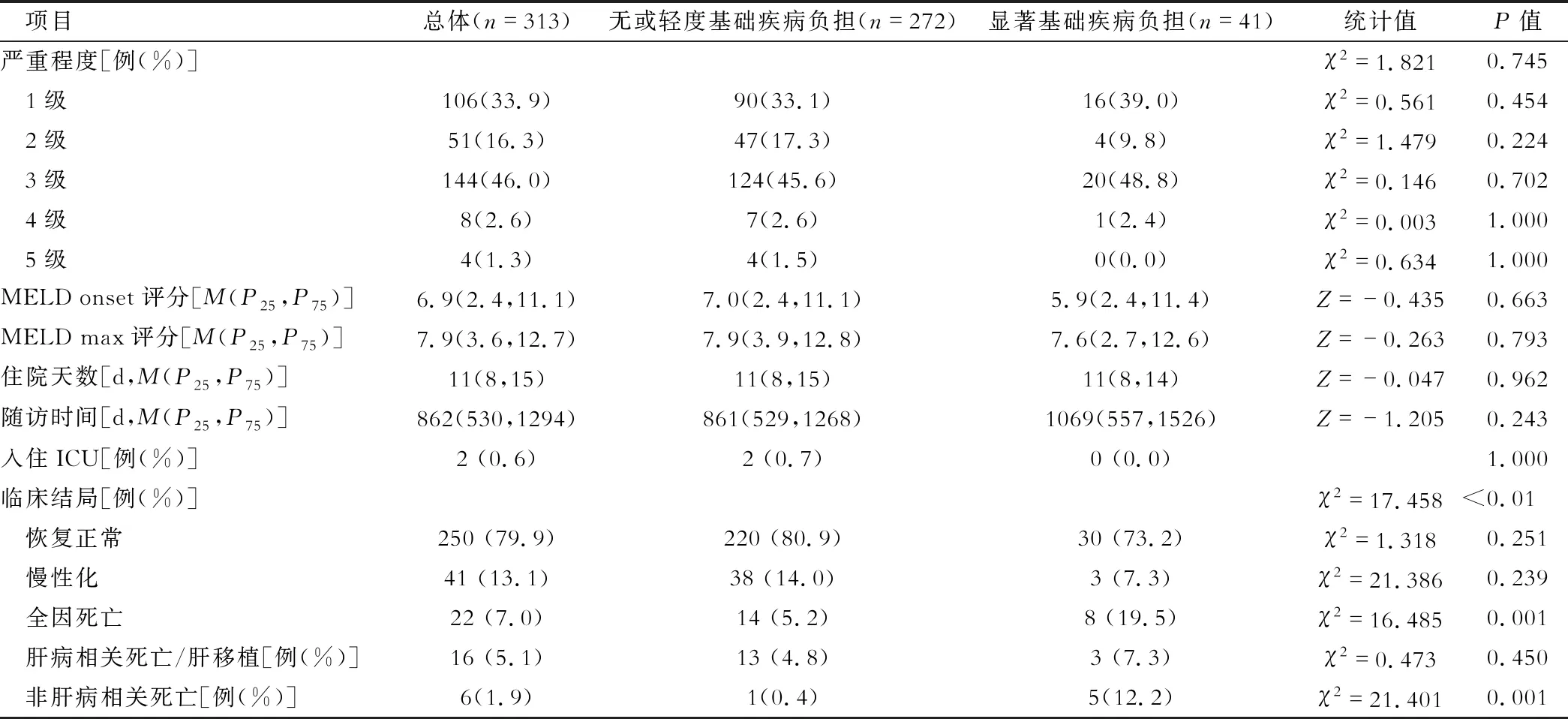
表4 无或轻度与显著基础疾病负担组患者严重程度及临床结局比较
讨 论
本研究结果显示,与无或轻度基础疾病负担组相比,显著基础疾病负担组年龄大,用药种类多,与其他研究结论一致[11,12]。文献报道DILI患者年龄越大,CCI指数越大,即年长的患者随着基础疾病种类增加,服用药物种类也增多,临床分型以肝细胞损伤型为主[13],与本研究结论一致。此外,显著基础疾病负担组体重指数及血糖更高,考虑与合并脂肪肝、糖尿病等代谢综合征相关。
本研究发现,基础疾病负担与DILI患者临床预后相关,显著基础疾病负担组较无或轻度基础疾病负担组的DILI患者全因病死率及非肝脏相关的病死率显著增高。Ghabril等[3]报道,DILI患者总病死率10.8%,显著基础疾病负担组较无或轻度基础疾病负担组全因病死率高(26.7%比4.8%P<0.01),其死亡原因绝大多数与肝脏无关,可能与潜在基础疾病负担相关。在现有的预测模型中加入基础疾病负担可提高预测药物性肝损伤6个月病死率的准确性,其ROC曲线下面积为0.89。西班牙前瞻性研究也表明6个月内死亡的患者基础疾病负担显著高于存活的DILI患者(CCI为2.25比0.6,P<0.01)[13]。美国研究发现合并丙型肝炎病毒感染、非酒精性脂肪性肝病等基础肝病的DILI患者损伤更重、病死率更高[4]。因此,基础疾病负担在预测全因死亡中发挥一定作用,以非肝脏相关死亡为主。对于肝脏相关的死亡或肝移植,显著基础疾病负担组也高于无或轻度基础疾病负担组,但差异无统计学意义,具体原因值得进一步研究。2020年昆明医院研究了基础疾病对预后的影响,发现肝脏、肾脏、高血压、高脂血症、糖尿病等单一基础疾病与预后无关[14]。在分析DILI患者预后时,应将基础疾病量化,综合分析。
本研究提示基础疾病负担与DILI损伤的严重程度无关,表现为肝脏合成功能及凝血功能指标差异均无统计学意义。有研究表明,糖尿病、基础肝病与DILI严重程度无关,重度损伤的DILI患者合并糖尿病的比例虽然高于轻中度损伤的DILI患者,但差异无统计学意义(37%比25%,P=0.07)[15]。Li等[16]的研究认为,糖尿病及基础肝脏疾病与DILI严重程度无关,但血脂异常是肝脏损伤程度的独立危险因素(AOR3.926 95%CI:(1.282~12.026),P=0.017)。
综上所述,显著基础疾病负担DILI患者预后差,全因死亡及非肝脏相关死亡显著高于无或轻度基础疾病负担DILI患者,具有显著基础疾病负担的DILI患者更应重视。但本研究为单中心回顾性研究,尚待多中心前瞻性研究进一步验证。
