肝切除术与TACE治疗原发性肝癌破裂出血疗效的倾向评分匹配分析
2022-02-15万文武张瑜丁兵张勇凌俊方程何攀谢飞蒋辉
万文武,张瑜,丁兵,张勇,凌俊,方程,何攀,谢飞,蒋辉
(1.四川省内江市第二人民医院肝胆外科,四川内江641000;2.西南医科大学附属医院肝胆外科,四川泸州646000;3.四川省内江市第一人民医院肝胆外科,四川内江641000)
原发性肝癌(primary liver cancer,PLC)是世界上第6 位常见的恶性肿瘤,也是全球范围内第三大致命的恶性肿瘤[1],由于乙肝病毒的流行,PLC在世界范围内的发病率一直居高不下[2]。自发性破裂是PLC 危及生命的并发症,其发病率为5%~26%,急性期病死率高达25%~75%[3-4]。PLC 破裂出血的病理机制至今尚未完全阐明,有研究[5]认为随着病情发展,肿瘤局部可出现缺血坏死及软化,在外力或腹内压升高的情况下发生破裂出血,另外可能与肿瘤恶性程度高、肿瘤增长过快或凝血功能异常有关。PLC 破裂出血的治疗原则是及时有效控制出血,同时兼顾肿瘤的综合治疗[6]。目前,对于PLC 破裂的治疗主要包括手术和非手术治疗,前者包括肝切除术(liver resection,LR)和手术探查止血,后者包括介入和保守治疗。临床上,对于PLC破裂出血患者,LR 及经导管动脉栓塞化疗术(transcatheter arterial chemoembolization,TACE)治疗应用最为广泛。LR 能兼顾止血及根治肿瘤的目的,但其主要适用于患者一般情况良好,肝功能良好,肿瘤存在半肝,无远处转移等情况。TACE 主要适用于出血急性期的治疗,可避免全麻和手术的双重打击,可重复操作,可最大限度保护正常肝组织,可为进一步手术切除肿瘤做准备。但TACE 后肿瘤再出血风险较高,同时癌组织中血管内皮生长因子的高表达促进了微血管生成,进而增加了PLC 转移和复发的风险。LR 和TACE 都广泛应用于PLC 破裂出血的治疗,但疗效结果相关报道仍有较大差异[7-8]。一般来说,能行LR 的患者往往具有更好的实验室及影像学指标,因此对于采取不同治疗方式的患者,基线特征之间不免存在一些选择偏倚。为此,本研究旨在通过倾向性评分匹配(propensity score matching,PSM) 的方法,探讨在PLC 破裂出血的患者中,包含LR 的综合治疗相比较于单纯TACE 治疗是否可以获得更好的预后,并探索影响长期预后的危险因素,以期为临床工作提供合理的治疗决策。
1 资料与方法
1.1 一般资料
本研究回顾性分析了2013年6月—2018年6月期间,在西南医科大学附属医院、四川省内江市第一人民医院、四川省内江市第二人民医院接受治疗的PLC 破裂出血患者的数据。纳入标准:⑴腹部增强CT/MRI 提示PLC 破裂出血或腹腔穿刺抽出不凝血;⑵肿瘤无远处转移。排除标准:⑴入院经抗休克治疗后休克不能纠正;⑵仅行保守治疗、TACE 或开腹止血手术者;⑶肝功能Child-Pugh C 级;⑷BCLC 分期为D 期。收集的资料包括:⑴一般情况:年龄,性别,常见合并症、肝功能Child-Pugh 分级、BCLC 分期、有无失血性休克。⑵实验室检查:乙肝两对半,国际标准化比值(international normalized ratio,INR)、凝血酶原时间(prothrombin time,PT)、活化部分凝血活酶时间(activated partial thromboplastin time,APTT)、甲胎蛋白(alpha fetoprotein, AFP)、 血红蛋白(hemoglobin,HGB)、血小板(platelets,PLT)、总胆红素(total bilirubin,TBIL)、天门冬氨酸氨基转移 酶(aspartate aminotransferase, AST)、 白蛋白(albumin,ALB)。⑶影像学检查:肿瘤部位、大小,是否有门脉高压、门静脉癌栓及腹腔积液。⑷治疗情况:治疗方式、手术并发症、术后复发模式、随访时间和结果。实验室检查以入院后第1 次检查结果为准,肿瘤标志物以治疗前最近一次检查结果为准。PLC 是根据美国肝病研究协会发布的诊断指南和中国临床肿瘤学会编写的《原发性肝癌诊疗指南》[9-10]进行诊断的。PLC 破裂出血的初步诊断依靠患者基本状况、症状、体征,随后通过动态增强CT/MRI 来证实,部分患者通过腹腔穿刺术来明确诊断。研究经四川省内江市第二人民医院伦理委员会批准(批件号20210301)。
1.2 治疗
三所医疗中心关于PLC 破裂出血的总体治疗原则如下:入院后首先通过静脉补液和支持治疗进行液体复苏和保持血流动力学的稳定,如有输血指征则给予输血治疗。在血液动力不稳定的患者或持续腹腔内出血的患者中,介入或保守治疗是第1 次干预。如果介入或保守治疗失败,则在入院后48 h 内对可切除肿瘤并且残余肝脏功能足够的患者进行LR。在其他患者中,使用包括肝周围纱布填塞、肝动脉结扎及微波消融的手段来止血。在血流动力学状态稳定时,患者接受了完整的临床评估,以制定明确的治疗计划,包括血清学,Child-Pugh 分级,腹部CT,肝血管造影以及15 min时吲哚菁绿保留率的测量。根据测试结果评估LR的可行性。对于可切除的患者行LR,而对于无法进行手术的患者则采取TACE 等非手术治疗,TACE 是无法进行手术的患者的首选疗法。具体的治疗取决于患者的肝功能状态、全身状况、肿瘤相关情况等,并且在实施前征求患者和家属的知情同意。
1.2.1 TACE 采用Seldinger 方法经皮股动脉穿刺,将导管插入肿瘤供血动脉,DSA 造影后经导管注入化疗药物和栓塞剂的混悬液。化疗药物选用盐酸多柔比星40 mg+洛铂40 mg+碘化油10~30 mL(按肿瘤直径1~2 mL/cm3计算)。栓塞后行DSA 检查以确认栓塞效果。术后给予护肝、抑酸、止吐等对症治疗。
1.2.2 LR 采用开腹或腹腔镜两种方式,探查腹腔内有无局部及远处转移等情况。游离肝脏,采用Pringle 法阻断入肝血流。术中B 超明确肿瘤位置,标注切肝线。使用双极电凝及超声刀断肝,显露大部分脉管结构,丝线结扎中、小血管,大血管及胆管予以结扎后缝闭,蒸馏水冲洗腹腔,肝断面缝扎止血并覆盖止血纱。放置硅胶引流管于肝断面。术后行常规抗感染、止血、抗病毒、保肝等对症处理。
1.3 随访
电话、门诊及再住院随访至2021年1月。所有患者术后半年内每1 个月复查肝功能、AFP、病毒载量及胸腹部CT,以后每3 个月复查1 次。术后复发患者,根据复发模式,肝功能储备和患者的一般情况制定治疗方案。对复发患者采用多学科方法,包括再切除,局部消融治疗,TACE,免疫治疗或索拉非尼治疗。研究终点为患者术后总生存期(overall survival,OS),OS 被定义为从治疗后到任何原因死亡的时间或直到随访结束。术后并发症采用了Clavien-Dindo 分类[11]。
1.4 统计学处理
采用SPSS 24.0 进行数据分析,正态分布的计量资料以均数±标准差(±s)表示,比较采用独立样本t检验,非正态分布的计量资料以中位数(四分位间距)[M(IQR)]表示,比较采用非参数秩和检验;计数资料以例数和百分数表示,比较采用χ2检验,小样本则使用Fisher's 确切检验;等级资料比较采用秩和检验,术后生存率用Kaplan-Meier 法,组间生存差异用Log-rank 检验,使用Cox多因素分析方法探寻影响生存的独立危险因素,P<0.05 有统计学意义。用PSM 的方法来矫正两组基线特征的差异。PSM 采用最近邻匹配法进行1∶1匹配。
2 结 果
2.1 患者治疗情况
在本研究中,共有286 例新诊断PLC 破裂出血的患者在3 个医疗中心接受治疗。排除首次入院时有远处转移者11 例,排除30 d 内失访或资料不齐者18 例,排除仅行保守治疗者45 例,排除仅行开腹止血手术者17 例,最终有195 例纳入研究。其中LR 组64 例,22 例入院后急诊行LR,33 例经TACE 治疗后延期行LR,9 例经保守治疗后再延期行LR,TACE 组131 例。
2.2 PSM前后基线特征比较
在PSM 分析前,两组患者入院时在有无休克、HGB、AST、TBIL、有无门静脉侵犯、有无腹水、肿瘤数目、Child-Pugh 分级、BCLC 分期等方面差异有统计学意义(均P<0.05)。将患者的上述变量纳入PSM 分析后,获得了29 例LR 病例以及与之匹配的29 例TACE 病例。经过对比,匹配后的LR 组和TACE 组患者的基线特征差异均无统计学意义(均P>0.05)(表1)。
2.3 PSM后生存分析
从短期病死率看,LR 组30 d 病死率为3.4%(1/29),TACE 组30 d 病死率为10.3% (3/29),两组差异无统计学意义(χ2=1.074,P=0.611)。从总体生存(OS)来看,LR 组和TACE 组患者的1、2、3年OS 率分别 为75.9%、41.4%、12.9% 与55.5%、14.4%、0;中位生存期分别为18.5(95%CI=12.9~24.1)个月和12.5(95%CI=10.4~14.6)个月,两组差异有统计学意义(χ2=4.843,P=0.028)(图1)。
2.4 PSM后预后的危险因素分析
单因素分析显示,门静脉侵犯、门脉高压、腹水、肿瘤多发、肿瘤直径>10 cm、Child-Pugh 分级、BCLC 分期、AFP>400 ng/mL、治疗方式是影响PLC 破裂出血患者OS 的危险因素(均P<0.05);多因素Cox 分析显示,肿瘤多发,Child-Pugh 分级、AFP>400 ng/mL、治疗方式是影响PLC 破裂出血患者OS 的独立危险因素(均P<0.05)(表2)。
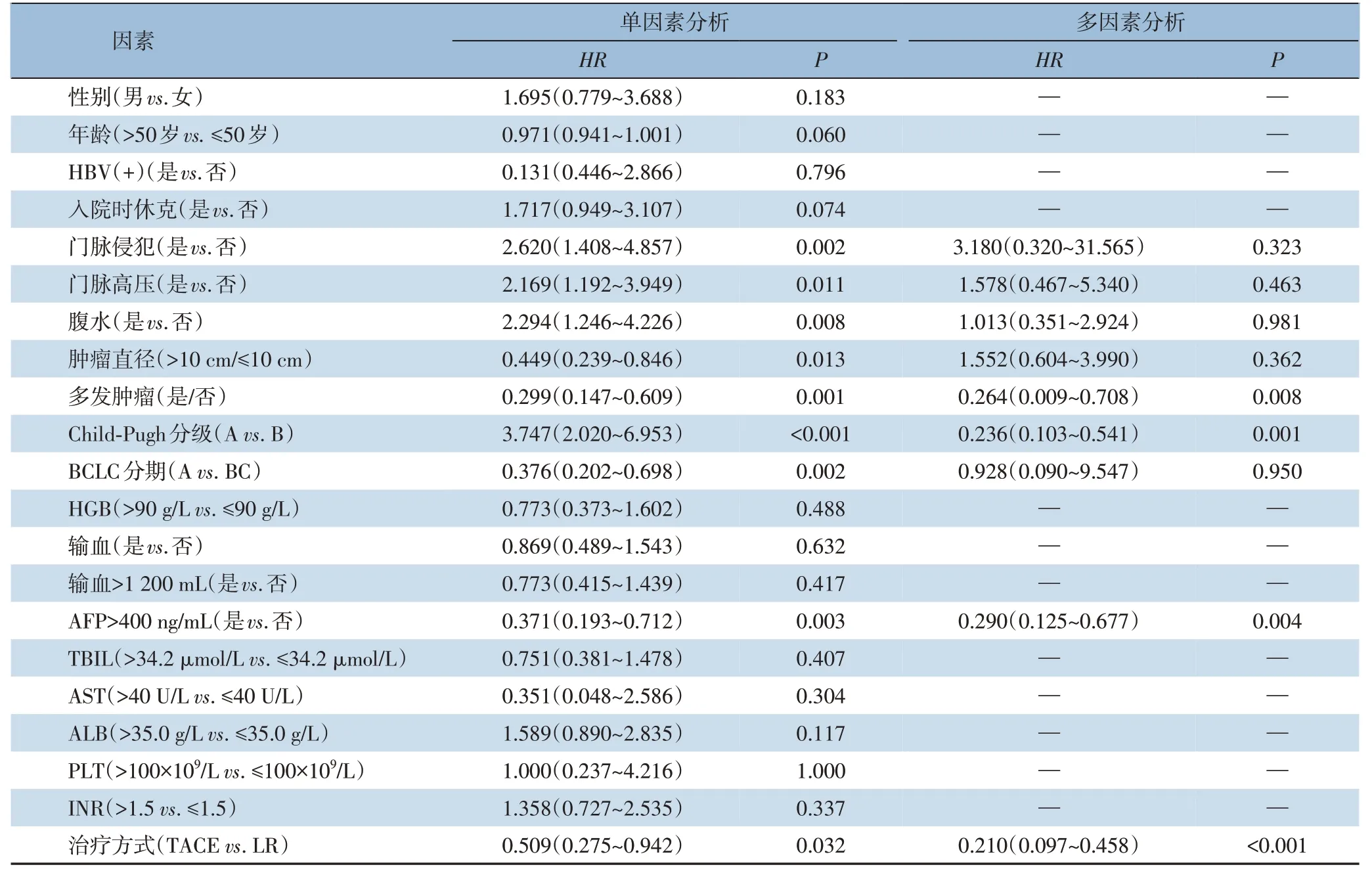
表2 PSM后预后危险因素分析Table 2 Analysis of prognostic factors after PSM
3 讨 论
PLC 破裂出血是一种罕见但危及生命的并发症,患者的病死率高达6%~10%[12]。自发性破裂的机制尚未完全阐明,可能相关的因素有高血压、肿瘤外生性生长、肿瘤较大以及血管功能障碍等[13-14]。
PLC 破裂出血的治疗仍然是一个复杂的问题,止血是初始治疗的主要目的。据报道[15-16],TACE是破裂出血急性期实现止血的一线方法,止血成功率>90%。此外,TACE 既能通过栓塞肝动脉控制出血,也能通过局部化疗和栓塞控制肿瘤,使临床医师有时间完成肿瘤的术前评估,这有助于在PLC 破裂患者中选择可手术切除病例,并提高二期手术切除率。然而,经TACE 治疗后,肿瘤仍然有再次破裂出血的风险。据报道[6,17],这些再次破裂出血的患者预后极差。LR 的优点是可以在一次手术中实现止血和切除肿瘤的目标,然而,它可能与短期内高病死率有关[18]。
从近年的文献报道来看,对于PLC 破裂出血最佳的治疗方式仍有许多争议[7-8,19-20]。遗憾的是,目前临床常用的两种分期方法(BCLC 分期和TNM分期)均未将PLC 破裂出血纳入其中。为此,日本肝癌研究小组(LCSGJ)建立的《原发性肝癌临床病理研究的基本规范》认为,不管肿瘤的大小、数量以及有无血管或胆管的侵犯,应直接将PLC破裂出血列为T4 期,即肿瘤晚期[21-22]。这导致许多医疗机构在选择治疗方式时倾向于非手术治疗[23-24]。但在之前的一些研究中,这种分类方法受到质疑,有学者[4,25]认为PLC 破裂出血的影响不足以抵消其他所有肿瘤因素的影响,该影响仅仅将肿瘤向晚期推进了0.5~2 个级别,这表明将所有的破裂的PLC 患者都划分到T4 期可能无法准确反映真实的预后。
Aoki 等[3]报道了一项来自日本的全国性调查,它是迄今为止关于PLC 破裂出血的最大临床研究。在该研究中,根据主要治疗方式分类的OS 分析显示, LR 后1、 3、 5年 的OS率分别为76.0%、48.6%、33.9%,而TACE 后1、3、5年的OS 率分别为39.7%、14.1%、6.0%。这与本研究的结果相似,即包含LR 的综合治疗相比单纯TACE 可以让PLC破裂出血患者有更多的生存获益。但与以往研究不同的是,本研究在PSM 后TACE 组患者30 d 病死率稍高,但总体并无显著差异(10.3%vs.3.4%,P=0.611)。分析原因可能是:⑴TACE 组比LR 组患者的肿瘤分期更晚,一般情况更差,肝功能更差;⑵PSM后仅获得29 对数据,统计分析受限于样本量大小。
近年来,PLC 破裂出血的长期生存率较以往显著升高[26],但总体预后仍未令人满意。因此,有必要分析其预后的影响因素。在一项多中心研究中,Kirikoshi 等[27]报道,最大肿瘤直径不超过7 cm是决定长期生存的独立危险因素。还有研究[28-29]表明,包括肿瘤相关因素(肿瘤负荷,位置,PVTT和甲胎蛋白水平)和宿主相关因素(肝功能状态)都是PLC 破裂患者长期存活的重要预测因子。近来,LR 手术细节与患者预后的相关性越来越受到关注,如术中联合5-FU 腹腔灌洗、TACE 后二期切除以及解剖性LR 都被认为是影响患者OS 的独立危险因素[30]。与之前的报道相似,本研究发现肿瘤多发、Child-Pugh 分级、AFP>400 ng/mL 和治疗方式为影响OS 的独立危险因素。肿瘤多发可能意味着肿瘤侵及不同范围的门静脉系统,与术后高复发密切相关[31]。Child-Pugh 分级较高反应了肝细胞损害程度严重和肝脏储备功能较低,进而影响患者术后恢复和长期生存。AFP 是PLC 最重要的生物标志物,其与PLC 的发生、增殖、转移密切相关[32]。AFP 的高表达会促进PLC 干细胞的活性及抑制机体的免疫应答,从而促进肿瘤的复发[33]。而治疗方式的选择尤其重要,本研究显示LR 预示着相对良好的预后,分析其原因:⑴LR 兼具止血和切除肿瘤的优势;⑵避免了介入术后再次出血可能;⑶术中蒸馏水冲洗、浸泡腹腔减少了肿瘤腹腔种植转移的几率。
当然,本研究仍然存在不足之处。首先,本研究为回顾性病例对照研究,病例选择不免存在一些选择偏倚;第二,TACE 组患者没有进行术后病理检查,所以无法对微血管侵犯及肿瘤分化程度进行统计和分析;第三,PLC 破裂出血的病例极其罕见,即便综合了三所医疗中心的数据,在PSM 后的病例数仍然不多,这限制了进一步的亚组分析;第四,本研究样本中存在大部分复发病例,不同的后续治疗可能会对OS 产生不同影响。
总之,通过PSM 后的研究结果表明,对于肝功能可耐受和肿瘤可切除的PLC 破裂出血患者,以LR 为主的综合治疗应该被视为实现肿瘤控制和患者长期生存的主要方法。而TACE 治疗可能最适用于术前的止血治疗或因手术效果不佳、其他合并症而无法进行手术的患者。其预后与门静脉侵犯、门脉高压、腹水、肿瘤多发、肿瘤直径>10 cm、Child-Pugh 分 级、BCLC 分 期、AFP>400 ng/mL、治疗方式存在相关性;其中肿瘤多发,Child-Pugh 分级、AFP>400 ng/mL 和治疗方式是影响患者长期预后的独立危险因素。不过对于LR 手术时机、不同分期患者的不同组合治疗策略仍然需要进一步的研究。
利益冲突:所有作者均声明不存在利益冲突。
