儿童炎症性肠病微量营养素缺乏研究进展及治疗建议*
2022-02-02周丹丽林琼倪竹梦凌菁菁岳园园陈艳华
周丹丽,林琼,倪竹梦,凌菁菁,岳园园,陈艳华,王 燕
无锡市儿童医院,无锡214023
炎症性肠病(inflammatory bowel disease,IBD)是一种多因素导致的肠道慢性炎症,包括克罗恩病(Crohn's disease,CD)和溃疡性结肠炎(unlcerative colitis,UC),目前新诊断病例中儿童炎症性肠病占比25%[1]。营养不良是IBD 最常见的并发症,大约有85%的IBD 患儿合并营养不良,营养状况已被证明是决定IBD 预后的关键因素[2]。营养治疗分为宏观营养素治疗和微量营养素治疗,前者包括蛋白质、碳水化合物和脂肪;后者包括微量元素和维生素。宏观营养素缺乏常常发生在IBD 初期及活动期,临床关注较多;而微量营养素缺乏即使是轻度活动的IBD 及疾病缓解期也可能发生但却常被忽略。维生素和矿物质是天然存在的化合物,人们从食物中获取以满足各种生理功能需求。在正常情况下,95%维生素和矿物质都在近端小肠被吸收,通常是在空肠的中部[4]。微量营养素缺乏与IBD 患者并发症如贫血、骨病及生活质量密切相关[2],导致儿童IBD 发生微量营养素缺乏的风险则包括摄入不足、肠道丢失增加、吸收不良、代谢增加和药物不良反应[3,4]等。现就儿童IBD 并发症及疾病相关微量营养素缺乏情况进行综述,总结IBD 不同微量营养素缺乏的治疗策略,以引起IBD 治疗团队的关注,共同全方位的规范管理IBD 患儿。以此为IBD 患儿的治疗提供参考。
1 贫 血
贫血是炎症性肠病最常见的并发症。IBD 患者的贫血通常是多因素导致的,包括缺铁、失血、炎症、维生素B12和叶酸的缺乏、药物毒性作用等[5]。研究发现,儿童IBD 贫血的发生率在诊断时为44%~74%,随访一年后发生率为25%~58%[6,7]。Pels LP 等[8]研究表明,新诊断IBD 儿童贫血发生率为78%,有58%为缺铁性贫血,且有三分之一的患儿在随访的一年期间存在持久性贫血。多项研究表明,儿童贫血的发生率高于成人[6,7,9]。
IBD 患者贫血分为缺铁性贫血、慢性贫血及混合型贫血。根据2015 年《ECCO 关于炎症性肠病缺铁和贫血诊断治疗共识》[10],IBD 贫血的诊断基于实验室筛查、转铁蛋白饱和度、血清铁蛋白和C 反应蛋白水平。贫血诊断:根据WHO 不同年龄段血红蛋白水平诊断贫血,未合并炎症时,血清铁蛋白<30 μg·L-1;合并炎症时,血清铁蛋白<100 μg·L-1,诊断为缺铁性贫血;当合并炎症时,血清铁蛋白>100 μg·L-1,转铁蛋白饱和度(TfS)<20%,考虑慢性贫血;转铁蛋白为30~100 μg·L-1时,考虑为混合型贫血。
IBD 患儿及时纠正贫血能够有效改善生活质量,因此需监测IBD 患儿贫血状态,根据贫血类型积极予以纠正。2020 北美儿科胃肠病学/肝病学和营养学会年会(NASPGHAN)关于儿童贫血的管理指南[11]参考2015 ECCO 成人贫血的管理指南,提出IBD 患儿的贫血监测管理意见:应在初始诊断IBD时评估贫血状态,疾病活动期每3 个月重复评估,疾病缓解期6~12 个月重复评估。所有患者应每年进行叶酸和维生素B12水平筛查,而对于维生素缺乏高风险人群(肠切除、广泛回肠疾病)每3~6 个月重复评估。
IBD 患儿贫血相关微量营养素缺乏的治疗意见:
1.1 铁
IBD 患儿缺铁性贫血治疗的铁制剂选择需基于疾病活动度、贫血程度、病人的耐受程度。根据2015年ECCO 共识,静脉铁剂用于以下情况:临床活动期IBD,不能耐受口服补铁,Hb 低于10 g·dL-1,需要促红细胞生成素(Erythopoietin,EPO)治疗;口服铁剂用于以下情况:轻度贫血,非临床活动期,能够耐受口服铁剂[10]。一项调查儿童静脉铁剂使用的安全性和有效性的研究指出静脉铁剂使用标准:①不能耐受口服铁剂的不良反应;②口服铁剂3 个月仍不能解决的缺铁性贫血;③医生评估IBD 严重程度不能耐受口服铁剂[13]。2018 年欧洲儿科胃肠肝病和营养学会(ESPGHN)在儿童IBD 营养共识[12]中推荐口服铁剂用于以下情况:轻度贫血(Hb>10 g·dL-1),炎症标记物阴性。因此,目前儿童IBD 缺铁性贫血静脉铁剂和口服铁剂的选择标准与成人基本相同。
我国静脉铁剂有右旋糖酐铁和蔗糖铁(见表1),由于右旋糖酐铁的不良反应发生率比较高,目前临床主要使用蔗糖铁。口服铁剂含有不可吸收铁,在活动性炎症时口服补铁可诱导氧化应激,有增加IBD 活动度的风险[14]。口服铁剂对肠道黏膜有刺激,不利于IBD 患儿肠道黏膜修复,而多糖铁复合物中铁元素含量高,其与多糖合成复合物,在消化道以分子形式被吸收,减少肠道刺激。研究显示,3 mg·kg-1·d-1铁元素的补充量为儿童口服铁剂的安全耐受量,故以此作为IBD 患儿口服补铁剂的推荐剂量[10]。
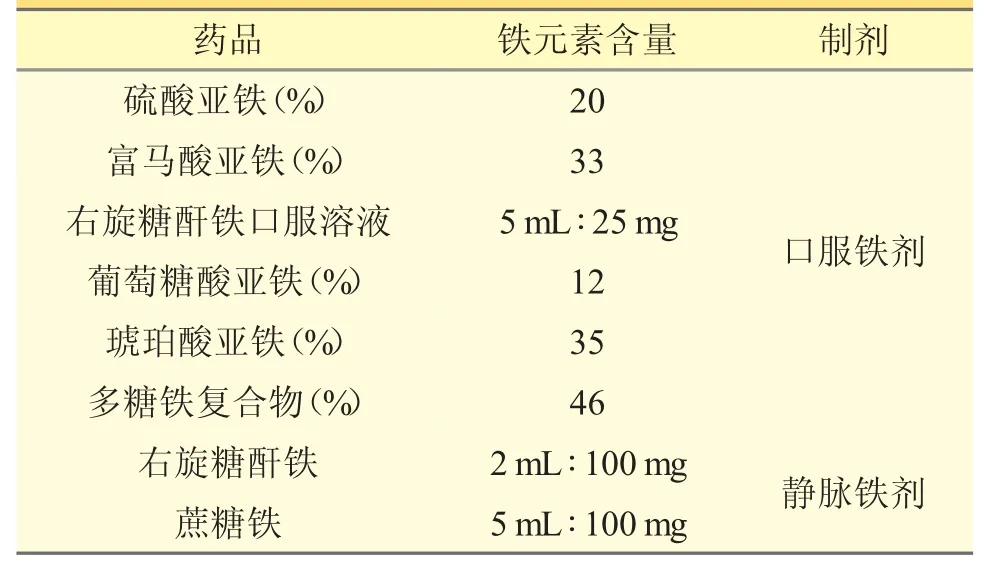
表1 国内不同铁制剂特点
1.2 叶酸
叶酸缺乏通常与IBD 患者的贫血相关,临床上罕见IBD 患儿存在叶酸显著缺乏的情况,然而考虑到相较于健康儿童,IBD 患儿的叶酸缺乏风险增加,建议每年至少一次检测血清或红细胞的叶酸水平,或在没有使用巯嘌呤的情况下出现巨幼红细胞贫血亦需检测[10]。目前叶酸补充剂量尚不明确,每天服用1 mg 或每周服用5 mg 似乎都可以[15,16];ECCO 指南建议使用柳氮磺吡啶或甲氨蝶呤的患者,每年至少检测一次叶酸水平,缺乏时以叶酸1 mg·d-1治疗2~3周[17]。目前儿童的叶酸缺乏治疗参考成人治疗方法。
1.3 维生素B12
维生素B12对多种营养素代谢、DNA 合成及神经功能发育至关重要[18],其缺乏通常与IBD 患儿的巨幼红细胞贫血相关。回肠末端切除>20cm 的CD 患者,维生素B12缺乏的风险增大;回肠远端切除>60 cm的患者,需终生补充维生素B12。针对广泛回肠远端切除者或临床筛查维生素B12缺乏的IBD 患儿,推荐每隔一天肌肉注射维生素B121 g,持续一周,后每周一次,直到临床症状好转,以后根据尿液和血液中甲基丙二酸水平决定维生素B12的注射剂量[10]。
2 骨 病
炎症因子、吸收不良、维生素D 和钙缺乏,以及类固醇激素治疗是影响IBD 患者骨健康的重要因素[19]。IBD 患儿处于骨骼发育的关键时期,忽视IBD患儿骨健康将导致其成年后发生严重骨病,其骨折风险会增加约40%[20]。骨密度是评估骨健康的重要指标,骨密度Z 值介于SD~2SD,且处于IBD 活动期,需引起重视,当低于SD 时应转至专科医院评估骨健康状态[21]。建议具有风险因素的IBD 患儿(如使用类固醇激素、生长迟缓、营养不良及维生素D 缺乏者)定期监测和筛查骨密度[10]。
IBD 患儿骨病相关微量营养素缺乏治疗意见:
2.1 维生素D
维生素D 缺乏的流行病学研究广泛开展,多达62%的IBD 患儿25-OH-D 水平不足30 ng·mL-1[22],尤其是CD 患儿,只有9.5%的CD 患儿25-OH-D水平达到维生素D 充足[23]。维生素D 在调节钙磷稳态,特别是骨矿化中发挥重要作用,除了对骨骼的作用外,还参与其他多种疾病的病理过程,包括感染性疾病、自身免疫性疾病、炎症性肠病等[24,25]。成人和儿童研究发现,IBD 患者血清25-OH-D 浓度与疾病严重程度成正比[26,27]。越来越多的证据支持维生素D参与了IBD 的发病机制,有临床研究使用维生素D作为CD 轻症的治疗药物或者是联合治疗药物[28,29]。
目前关于维生素D 缺乏的定义国内外学者达成共识:25-OH-D<10 ng·mL-1为维生素D 严重缺乏;25-OH-D<20 ng·mL-1为维生素D 缺乏;25-OH-D>30ng·mL-1为维生素D 充足;25-OH-D>100 ng·mL-1为维生素D 中毒[24]。无论是成人还是儿童,对于IBD 患者均推荐监测和额外补充维生素D[10]。关于IBD 患儿维生素D 的推荐:诊断时及以后至少每年检测25-OH-D 水平,最好在冬末早春期间;维生素D 的常规补充,推荐高于同年龄段的补充量(1000~1500 IU·d-1);维生素D 缺乏的治疗量为2000 IU·d-1或50000IU·w-1,至少6周,继而以1000~1500 IU·d-1维持[10,25]。
临床使用的维生素D 制剂包括维生素D2、维生素D3、阿法骨化醇和骨化三醇。导致IBD 患者维生素D 缺乏主要原因是摄入和吸收障碍,肝肾功能正常的儿童推荐使用原型维生素D 制剂,也就是维生素D2和维生素D3,无需使用活性维生素D 制剂,易引起高钙血症。
2.2 钙
大约13%的克罗恩病成年患者存在钙吸收不良,IBD 患者钙缺乏也普遍存在[30]。对于IBD 患者、尤其是儿童,推荐在诊断及确诊后每年监测一次钙浓度,对于摄入量不足患者,积极补充钙制剂[10]。儿童和成人IBD 患者钙元素的推荐量与一般人群相同:1~3 岁为700 mg·d-1;4~8 岁为1000 mg·d-1;9~18 岁为1300 mg·d-1。考虑到中国人群的饮食结构和生活习惯,尤其是学龄期儿童学业任务重,户外活动少,处于生长发育时期,建议额外补充钙制剂。
目前钙制剂可分为无机钙、有机钙和新型钙(见表2),主要有碳酸钙、枸橼酸钙、醋酸钙、葡萄糖酸钙等;不同钙制剂钙元素含量不等,碳酸钙的钙元素含量最高为40%,而葡萄糖酸钙的钙元素含量最低为9%。对于IBD 患者,钙制剂推荐枸橼酸钙和碳酸钙,这两种钙制剂能够提供碳酸氢盐前体,纠正IBD 患者持续腹泻引起的代谢性酸中毒,并降低尿石症的倾向[31]。

表2 国内不同钙制剂特点
3 其他微量营养素缺乏的治疗
3.1 锌
锌缺乏常见于腹泻、吸收不良以及高代谢疾病如烧伤。大约15% IBD 患者合并锌缺乏。锌是催化活化100 多种金属酶的重要必需矿物质,在生长、免疫系统调节中具有多种生理作用[32]。但是IBD 患者锌缺乏常常处于亚临床阶段,有临床意义的锌缺乏并不多。严重缺乏常见于接受造瘘术、存在瘘管或者剧烈腹泻的IBD 患者,出现锌缺乏的皮肤改变如肢端皮炎。
建议严重腹泻(每天大便量>300g)成人,可每天给予葡萄糖酸锌20~40 mg 锌元素治疗[33]。若为了促进伤口愈合,建议每天给予硫酸锌元素锌40 mg 补充,疗程10 天。患儿IBD 不推荐常规监测和补充锌制剂,只在有严重或长期腹泻(腹泻时间大于4 周)时短期补充20~40 mg 锌元素[10]。不建议长期大剂量补充,因过量的锌会干扰铁和铜的吸收。
3.2 镁
镁是人体必需的阳离子,参与人体能量代谢和蛋白质合成。IBD 患者常常伴有腹泻,因此镁缺乏也是IBD 常见的微量元素缺乏之一,超过有13%的IBD 成年患者合并镁缺乏[34]。评价儿童镁缺乏是比较困难的,人体肾脏镁排泄减少通常是镁缺乏的首选生化指标。研究发现,IBD 病人并没有明显的尿镁排泄量减少,因此认为IBD 患者的镁缺乏可能是轻微的[35]。
一般而言,在急性复杂情况下静脉补充镁制剂,对于慢性镁缺乏可选择口服镁制剂或以饮食强化。IBD 患者肠外镁需求量至少为120 mg·d-1[36]。IBD 患儿不推荐常规监测和补充镁制剂,若存在持续腹泻(超过4 周)考虑检测镁含量。当镁缺乏时,短疗程(2~4 周)口服镁制剂通常可以使血清镁恢复至正常[10]。口服镁制剂有氧化镁、左旋乳酸镁、门冬氨酸钾镁(国内仅有本品,11.8 mg 镁元素/片)。
4 小 结
本文综述了IBD 患儿微量营养素缺乏的诊疗,明确微量营养素对IBD 患儿,尤其是合并有并发症的CD 患儿具有重要作用。微量营养素缺乏不仅与并发症相关,还能提示疾病的活动度。多种微量营养素参与了IBD 的发生发展过程。因此,关注IBD患儿微量营养素状况,合理监测和补充微量营养素水平,才能做到全方位管理IBD 患者。对于IBD 患儿,应重点关注铁、钙、维生素D、叶酸和维生B12水平,接受甲氨蝶呤和柳氮磺吡啶药物治疗者,宜重点监测体内叶酸水平。