基于比值失衡法对利拉鲁肽上市后安全信号的检测与评价*
2022-01-15季欢欢霍本念张妮宋林贾运涛
季欢欢,霍本念,张妮,宋林,贾运涛
(重庆医科大学附属儿童医院药学部,儿童发育疾病研究教育部重点实验室,国家儿童健康与疾病临床医学研究中心,儿童发育重大疾病国家国际科技合作基地,儿科学重庆市重点实验室,重庆 400014)
新型胰高糖素样多肽-1(glucagon-like peptide-1,GLP-1)类似物降糖药利拉鲁肽(liraglutide)通过与全身GLP-1受体结合,促进胰岛素合成与分泌。研究证实,利拉鲁肽可显著改善胰岛β细胞功能,延缓糖尿病进程,疗效确切,降糖持久,为糖尿病的治疗带来了新的希望。近年来,评价利拉鲁肽心血管的试验(liraglutide effect and action in diabetes:evaluation of cardiovascular outcome results,LEADER)取得突破性进展,证实利拉鲁肽可有效改善2型糖尿病患者的心血管结局[1]。
然而,涉及利拉鲁肽的安全性信息上市后研究较为欠缺,安全性特征与前期临床研究及潜在安全性问题尚未可知。作为新型降糖药,利拉鲁肽在国内应用逐步扩大,且其价格较传统降糖药物高,有必要对其进行安全性监测与评价。为全方位了解利拉鲁肽相关不良事件分布状况,本研究拟在报告比值比(reporting odd ratio,ROR)和比例报告比值比法(proportional reporting ratio,PRR)数据挖掘算法与统计检验的基础上,对美国食品药品管理局(FDA)不良事件报告系统(FDA adverse event reporting system,FAERS)中利拉鲁肽的不良事件进行信号检测,从国际医学用语词典(Medical Dictionary for Regulatory Activities,MedDRA)的首选语(preferred term,PT)、高位语(high level term,HLT)、标准MedDRA 分析查询(standardized MedDRA queries,SMQ)3个维度进行信号分析。通过上市后大样本数据以发现和评价利拉鲁肽在真实世界中的安全性特征,实施药物警戒安全性监测,以期为降糖治疗安全合理用药提供参考。
1 资料与方法
1.1数据来源 本研究数据来源于FDA公共数据开放项目(openFDA)数据库,其ADE原始数据由FAERS导入。所有ADE数据采用MedDRA术语进行编码。FAERS数据库每季度进行更新,截止到2021年第1季度已收集超过1000万份不良事件个例报告,信息量极大,可有效支持药品上市后安全性风险监测及评价。
本研究数据提取采用OpenVigil,该站点通过对接API应用程序接口直接提取Open FDA数据库中结构化的ADE报告信息。为保证数据提取的完整性,结合药物上市时间,在“Drug检索模块”以目标药物“Liraglutide”进行自动映射匹配检索,提取FAERS数据库2010年1月25日—2021年第1季度期间的数据,对利拉鲁肽为首要怀疑药物的报告进行挖掘分析。
1.2数据分析 比值失衡测量法在国内外药品不良反应信号挖掘中被广泛应用。本研究采用比例失衡法中的PRR和ROR信号挖掘方法,其算法基于四格表[2](表1),信号数值越大表示信号越强,即利拉鲁肽与目标不良事件之间的关联越强。

表1 比值失衡测量法四格表Tab.1 Fourfold table of disproportionality measurement
ROR=(a/c)/ (b/d),95%CI=eln (ROR)±1.96√(1/a+1/b+1/c+1/d),a≥3,ROR≥ 2,95%CI下限>1,提示产生信号;PRR=[a/(a+c)]/[b/(b+d)],a≥3,PRR≥ 2且χ2≥4,提示产生信号[3-4]。
1.3信号筛选 HLT为PT的上级术语,属于概括性术语;而SMQ是若干MedDRA术语的集合及在该集合基础上建立的查询策略,术语通常在PT层级。SMQ的产生源于MedDRA用户对采用标准查询工具获取安全性数据的需求。用户通过MedDRA获取某一疾病的数据,可直接以疾病名称为检索术语进行检索;为了全面获取可能病例,有时会以该疾病相关症状、体征或实验室检查等术语为查询条件。SMQ能够提高ADE病例报告检索的准确性和全面性,为找出极有可能代表所关注的目标事件,本研究采用狭义SMQ术语,以提高信号挖掘分析的可信度。
考虑到基于比例失衡算法的ROR与PRR法均有很强的灵敏性,PT层级检测结果易出现假阳性信号。结合信号的颗粒度与准确度关系,为得到高频出现且与利拉鲁肽关联性密切的信号,本研究将通过MedDRA术语的映射关系对信号结果进行二次筛选与规整。即数据挖掘得到的所有事件PT术语将被映射规整到现行MedDRA23.0版本的106个SMQ及1856个HLT术语组,再次进行信号检测。
2 信号检测结果
共纳入24 957份利拉鲁肽不良事件报告,经PRR及ROR检测,分别得到53个HLT信号,12个SMQ信号,包括胰腺恶性肿瘤(不包括胰岛细胞瘤和类癌瘤)、胰腺肿瘤、急性及慢性胰腺炎、各种消化酶检验及各种甲状腺良性肿瘤等显著信号,其中10个信号事件说明书未收录(表2、表3)。

表2 高位语信号检测结果Tab.2 Signal detection results of HLT
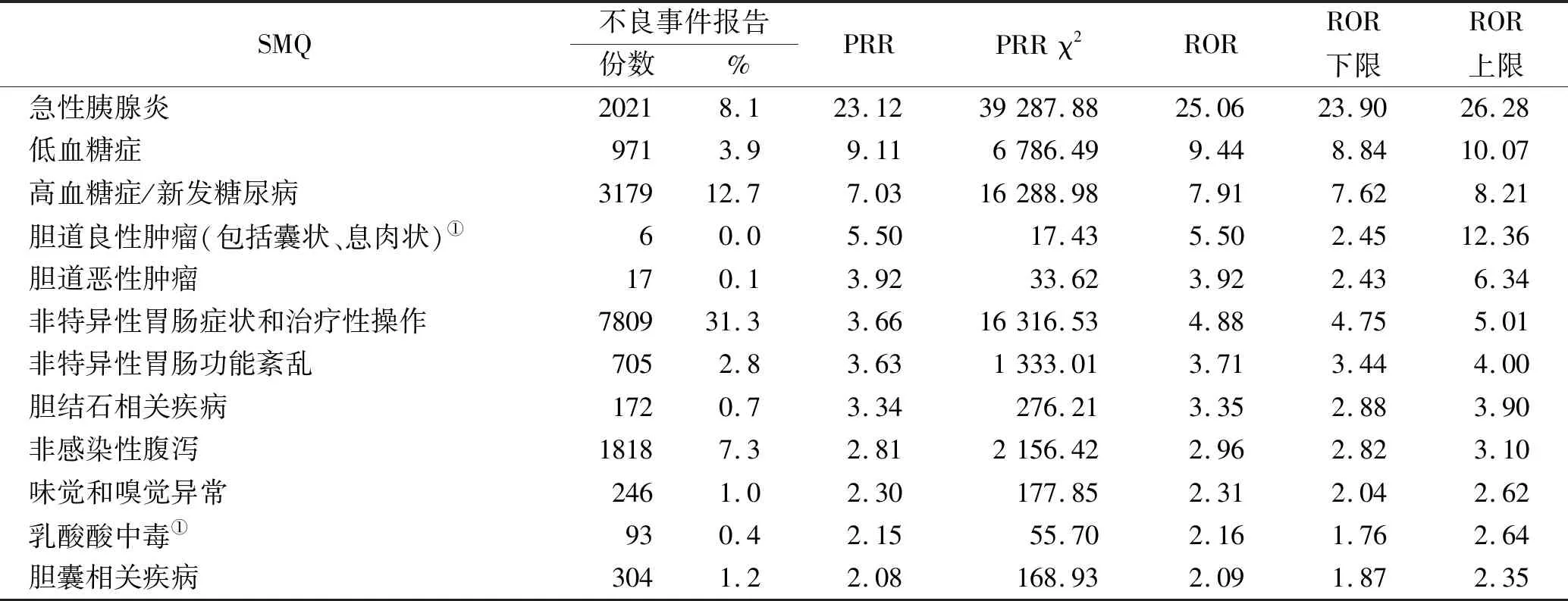
表3 SMQ信号检测结果Tab.3 Signal detection results of SMQ
为直观展示高频上报事件的信号及分布状况,本研究将PT/HLT/SMQ层级上报频数前30位不良事件进行信号挖掘,结果显示PT层级事件多数为信号,达到21个,SMQ层级事件少数显示为信号,仅9个,与HLT层级事件信号结果分布基本一致(表4)。
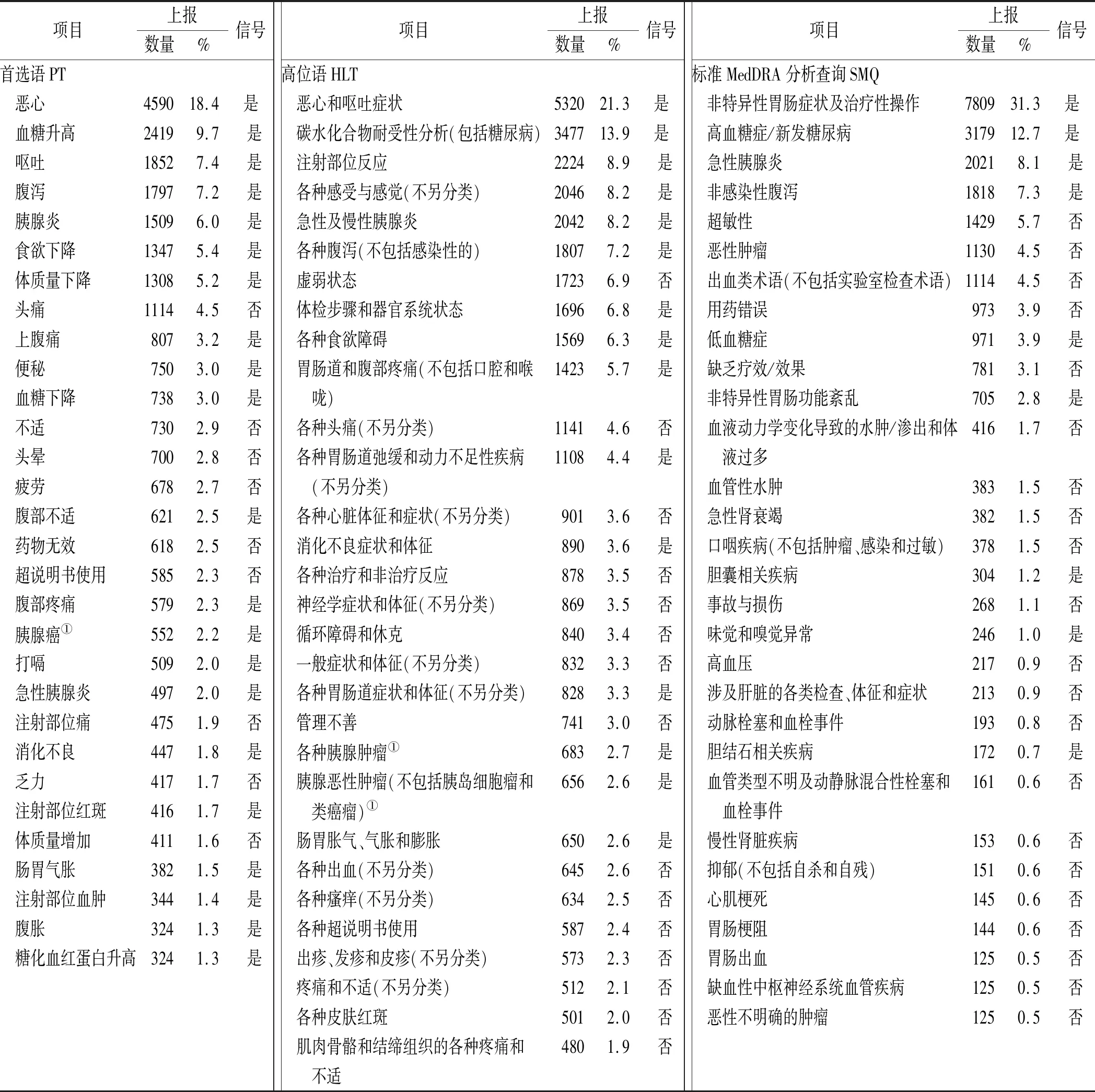
表4 PT/HLT/SMQ上报频数前30位不良事件信号结果Tab.4 The top 30 adverse event signal results reported in PT/HLT/SMQ
3 讨论
本研究对利拉鲁肽进行上市后安全性数据库大样本分析,多维度探索性地分析了其在真实世界的安全性。信号检测结果显示其安全性事件分布与说明书已知的安全性信息描述基本一致,主要表现为胃肠道不良反应、急性和慢性胰腺炎、急性胆囊疾病和低血糖等事件。此外,ROR法和PRR法检出的信号结果一致性高,从侧面证实了本研究基于数据挖掘方法在信号检测的可用性及可信度,可为利拉鲁肽临床用药提供大样本数据参考。
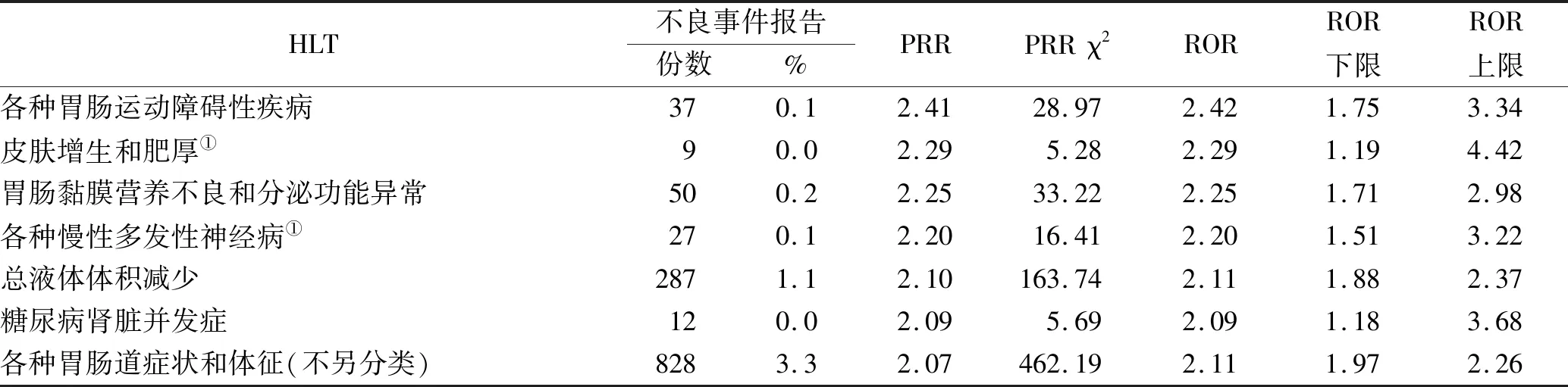
续表2 高位语信号检测结果Tab.2 Signal detection results of HLT
利拉鲁肽较强的安全信号主要集中在胰腺及甲状腺,例如HLT层级的胰腺恶性肿瘤(n=656,PRR=33.81,ROR=34.70)、胰腺肿瘤(n=683,PRR=31.10,ROR=31.94)、急性和慢性胰腺炎(n=2042,PRR=22.75,ROR=24.69)、各种甲状腺良性肿瘤(n=25,PRR=14.58,ROR=14.59)、各种甲状腺肿瘤(n=204,PRR=12.77,ROR=12.86)、各种甲状腺恶性肿瘤(n=124,PRR=12.32,ROR=12.38)等;SMQ层级的急性胰腺炎(n=2021,PRR=23.12,ROR=25.06)。研究表明,在胰腺癌患者中,肿瘤GLP-1受体水平降低与预后不良相关;利拉鲁肽可抑制胰腺癌细胞生长、迁移及侵袭,提示GLP-1具有抑制胰腺癌的效应[5-6]。Meta分析证实利拉鲁肽不增加胰腺炎风险,但胰腺癌数据太少尚无法得出结论[7-8]。基于人群的大样本观察性研究表明,利拉鲁肽暴露与急性胰腺炎、胰腺癌风险的增加无关,但涉及甲状腺癌的研究太少,无法得出确切的结论[9]。利拉鲁肽说明书黑框警示其在临床相关的暴露水平可能导致啮齿类动物甲状腺C细胞肿瘤。尚不清楚利拉鲁肽能否导致人类甲状腺C细胞肿瘤,包括甲状腺髓样癌,因为临床或非临床研究均无法确定其与人类的相关性[10]。本研究信号结果显示利拉鲁肽各种甲状腺肿瘤信号明确,包括良性及恶性肿瘤,建议既往有甲状腺疾病,如甲状腺肿的患者应慎用利拉鲁肽。
此外,在SMQ层级低血糖症(n=971,PRR=9.11,ROR=9.44)及高血糖症/新发糖尿病(n=3179,PRR=7.03,ROR=7.91)信号显著。说明书指出临床试验中低血糖事件大多为轻度,单药治疗未观察到重度低血糖事件[11]。LEADER试验结果表明,利拉鲁肽存在严重低血糖不良反应风险,但低于安慰药组[1.0vs1.5事件/100患者年;风险比为0.69(0.51-0.93)][1]。临床联合应用降糖药(如磺脲类)应密切关注患者血糖变化。高血糖症/新发糖尿病信号,考虑为原发病或适应证。
值得注意的是,本研究检出10个说明书未收录的安全信号,在PT/HLT/SMQ层级均有体现,如各类胰腺、胆管肿瘤、乳酸酸中毒、恶性肾盂和输尿管肿瘤、小肠恶性肿瘤、各种视网膜病、前列腺和精囊腺感染和炎症等。既往研究表明,利拉鲁肽相关胆囊疾病主要表现为胆囊炎和结石病[12],在本研究中得以信号重现,但胆管胆道肿瘤新信号尚未有明确记录。利拉鲁肽相关乳酸酸中毒信号,考虑为二甲双胍合并用药影响。恶性肾盂和输尿管肿瘤、小肠恶性肿瘤、各种视网膜病、前列腺和精囊腺感染和炎症上报数较少,信号结果有待后续报告数据积累加以确认。信号结果警示临床工作者应关注患者是否出现此类不良事件,并及时采取相应的临床干预。
利拉鲁肽胃肠道事件最为常见,PT/HLT/SMQ层级上报数均为首位,分别表现为恶心、恶心和呕吐症状,非特异性胃肠症状及治疗性操作等信号。此外腹泻、上腹痛、便秘和消化不良等常见不适事件均显示为信号且上报占比较高。研究表明,利拉鲁肽胃肠道不良反应发生率为剂量依赖性,剂量越大胃肠道不良反应的患者比例越高[13]。临床实践中,应合理调整剂量,降低胃肠道不良反应风险,以期提高患者的依从性。
考虑到临床试验的周期或者病例数等局限性,上市后大样本数据的信号挖掘可为药物安全性概况提供参考,本研究对FAERS数据库进行信号挖掘,探索性分析和评价了利拉鲁肽上市后安全信号概况。需要注意的是,数据挖掘产生的信号不代表药物与事件存在必然的因果关联,个例报告中的不良事件可能是联合用药或患者自身疾病进展或其他并发症等因素影响的结果,同时数据库中部分报告带有偏倚和随意性,低报漏报、内容不完整性等也会对信号结果造成影响。因此,利拉鲁肽相关信号风险需要进一步的临床及实践用药观察加以评估和验证。综上所述,本研究为利拉鲁肽用药提供了真实世界研究的安全性数据补充,提示临床关注其相关不良反应,并采取预防措施,以更多元化的医学数据支持临床用药,保证患者用药安全。
