光催化与微藻耦合快速去除水中铬离子
2022-01-13罗宏扬袁吉林钟兰兰向文浩肖川宝贺媛媛常海星钟年丙
罗宏扬,袁吉林,钟兰兰,向文浩,肖川宝,贺媛媛,常海星,钟年丙,3
(1.重庆理工大学 光纤传感与光电检测重庆市重点实验室 重庆市现代光电检测技术与仪器重点实验室,重庆 400054;2.重庆理工大学 化学化工学院,重庆 400054;3.重庆理工大学 两江国际学院,重庆 401135)
铬是一种重要的环境污染物,具备良好的电子层结构,被广泛运用于制革、冶金、电镀、燃料、纺织等领域[1]。含铬废水中主要包含六价铬(Cr(Ⅵ))及三价铬(Cr(Ⅲ)),Cr(Ⅵ)以铬酸盐和重铬酸盐的形式存在,具有较高的迁移率、溶解性和毒性,它可以通过消化道、呼吸道、皮肤和粘膜侵入人体,引起炎症,过量摄入将会致癌;Cr(Ⅲ)是人体必须的微量元素,但是过量摄入会导致一些慢性氧化性疾病[2-3]。因此,中国及欧美各国都将铬列为水中优先控制的污染物。
含铬废水的处理方法包括电化学法[4]、生物法[5]、光催化法[6]、光催化-生物耦合法[7-10]等。光催化-生物耦合法是将光催化剂和微生物置入同一反应器内,其中光催化能快速将高生物顽抗性、高毒物质降解为低毒物质,光催化降解产物可为微藻提供生长所需的碳源或无机物;与此同时,微生物代谢产物可反向促进光催化反应,如微生物代谢产生的有机物可综合光催化产生的空穴,进而促进光生电子空穴对的分离,提高光催化活性[7]。可见,光催化与微生物相互影响又相互作用,从而促使废水中有毒物质的快速去除及转化。因此光催化与生物耦合技术被认为是一种具有前景的废水治理技术,并被广泛应用于有毒有机废水治理及其资源转化领域。
当前国内外关于光催化与生物耦合技术用于去除铬的研究极少,去除率较低[8-10],其主要原因在于:① 当光催化剂与微生物耦合在同一多孔载体内部及其表面时,微生物细胞及其代谢产生的液相产物会强吸收紫外-可见光,导致光催化反应过程受光限制严重,进而降低光催化活性及去除有毒物质的效率[11];② 直接将微藻完全暴露于高毒铬溶液时,微生物细胞会快速死亡或萎缩,导致微生物细胞表面处理铬离子的活性位点降低,进而导致铬的去除速率降低[12];③ 部分微生物与光催化剂接触时会吸收电子,导致光催化剂表面电荷密度降低,进而影响到光催化还原铬的效率[11]。
为了突破光催化与生物耦合技术在去除铬研究方面的限制,实现快速去除铬的目标,构建了一种新型光催化-微藻耦合化学反应器。反应器分为上下2层:上层为悬浮微藻区,下层为固定化光催化区。上下2层由多孔导光核孔滤膜隔离并实现物质与光能传递。反应器中,光催化区光传输不受微藻及其代谢产物吸收的限制,N掺杂TiO2涂覆的石英光纤束快速地将铬溶液中高毒Cr(Ⅵ)还原为低毒的Cr(Ⅲ),并由核孔膜传递至微藻区,从而降低了高毒Cr(Ⅵ)对微藻的毒性,微藻高效还原部分Cr(Ⅵ)成为Cr(Ⅲ),并通过离子交换和络合吸附进一步去除Cr(Ⅲ)。同时,微藻与光催化剂的分区使光催化剂表面的电子不再被微藻吸收,微藻代谢产生的有机物通过核孔膜反向传输至光催化区,消耗催化剂表面产生的空穴和·OH,促进光催化反应。光催化与微藻相互耦合、相互促进,可高效去除铬。
1 材料与方法
1.1 材料与试剂
重铬酸钾(≥99.8%,成都科隆化学品有限公司,中国)、二苯氨基脲(≥97%,阿拉丁,中国)、高锰酸钾(≥99.5%,成都科隆化学品有限公司,中国)、浓硫酸(≥95.0%,川东化工,中国)、氢氟酸(≥40%,成都科隆化学品有限公司,中国)、磷酸(≥85%,川东化工,中国)、氢氧化钠(≥97.0%,阿拉丁,中国)、氨水(25%~28%,阿拉丁,中国)、钛酸异丙酯(≥99.0%,阿拉丁,中国)、乙二醇(≥99.0%,阿拉丁,中国)、一水柠檬酸(≥99.5,阿拉丁,中国)、介孔二氧化硅(511 m2/g,平均孔径6.31 nm)、核孔滤膜(孔径=1 μm,膜厚=11 mm,武威科技,中国)、小球藻(中国科学院水生生物研究所,武汉)。
1.2 N-TiO2涂覆光催化光纤的制备
为了获得高性能N-TiO2涂覆光催化光纤光催化剂,首先采用湿法制备锐钛矿型N-TiO2纳米颗粒[13],制备步骤如下:
步骤1 将100 mL含氨28%的氨水滴加到25 mL纯度为95%的钛酸异丙酯中,常温下搅拌8~10 h,蒸发水分获得沉淀;将沉淀以1 ℃/min的升温速率加热至400 ℃并煅烧6 h;用研磨钵将其研磨6 h,获得N-TiO2纳米颗粒。
步骤2 取3.34 mL乙二醇,加热至60 ℃;然后边搅拌边加入0.75 mL钛酸异丙酯,并加热至90 ℃;加入3.15 g一水柠檬酸,继续搅拌,直至溶液澄清;向澄清的溶液中加入3.34 g研磨好的N-TiO2纳米颗粒,搅拌1 h后避光静置24 h,得到稳定的N-TiO2溶胶凝胶。
选用空心毛细石英光纤(optical hollow-fibers,OHFs)(内径0.8 mm,外径1.5 mm,长度 200 mm)作为光催化剂的载体。首先,依次用丙酮、异丙醇、乙醇溶液对OHFs进行超声清洗并在氮气下干燥;依次使用氢氟酸、氢氧化钠对光催化光纤进行腐蚀预处理,每次处理时间0.5 h,使其表面粗糙(用于增强N-TiO2纳米颗粒与光催化光纤间的附着强度),并用去离子水清洗、干燥备用;最后,将制备好的NT光催化溶胶用提拉法涂覆在清洗后的OHFs表面;每涂覆一层溶胶之后,在温度为60 ℃的干燥箱中干燥15 min,涂覆3层即得到光催化光纤样品;最后,把制得的光催化光纤样品在400 ℃下煅烧8 h,得到高性能紫外-可见光催化光纤[14],干燥后N-TiO2光催化剂质量为70 mg。
1.3 微藻培养
选择小球藻(chlorella,FACHB-31)作为实验藻种。小球藻购自中国科学院武汉水生生物研究所淡水藻种库。通过将BG11营养液与小球藻种混合,并在光照下通入CO2对藻种进行激活和扩大化培养,从而获得成熟小球藻[15],以下是具体步骤:
步骤1 将实验所需的容器及配置好的培养液通过120 ℃的高压灭菌锅进行20 min灭菌;将冷却后的培养液与小球藻按照9∶1的比例于锥形瓶中混合接种,并将导气管密封于瓶口,导入体积浓度为10%的CO2,为提供小球藻必须的碳源。
步骤2 将培养瓶放入恒定25 ℃和光照强度4 000 lx的光照培养箱(GXZ-260B,宁波东南仪器,中国)中进行7~15 d扩大化培养,得到生长活性旺盛的小球藻。
步骤3 取成熟藻液,经培养液稀释,通过海洋光学光纤光谱仪(QEPRO-FL,海洋光学,中国)于680 nm测定小球藻吸光度,从而配制不同生物量的小球藻溶液。
1.4 反应器系统构建及其工作原理
图1为光催化与微藻耦合反应器(长140 mm,宽59 mm,高27 mm,体积66 mL)。反应器分为上下2层,上层是微藻区(体积为12 mL),下层是固定化光催化区(体积为54 mL),中间由平均孔径为300 nm,厚度为20 μm的导光核孔滤膜隔开。生物膜区和光催化区的能质可通过核孔膜进行传递,从而实现光催化-微藻耦合。
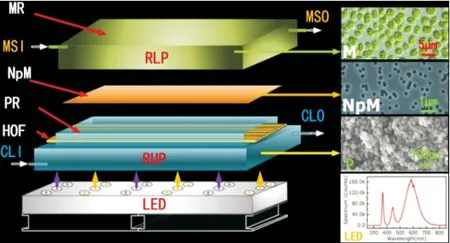
MR:微藻区;MSI:藻液入口;MSO:藻液出口;RUP:反应器盖板;NpM:核孔膜;PR:光催化区;CLI:Cr(Ⅵ)溶液入口;CLO:铬溶液出口;RLP:反应器底板;LED:发光二极管面阵光源;M:小球藻;P:催化剂;HOF:光催化光纤
微藻区由悬浮的小球藻(OD680 nm=0.8、小球藻干重为60 mg)及其培养基构成。光催化区由N-TiO2涂覆光催化光纤和Cr(Ⅵ)溶液构成,光催化光纤有2 层,每层18 根,催化剂重量为70 mg。光催化剂激发光源为自制可见-紫外LED面阵光源,LED光源由6个紫外LED灯珠(辐射中心波长365 nm、单个灯珠功率5 W)、6个可见光灯珠LED(光谱辐射范围420~780 nm、单个灯珠功率为5 W)构成;蠕动泵用于反应废液和藻液循环;恒温水浴用于控制废水和藻液温度(温度变化≤0.5 ℃);PC显示系统用于连接温度电极(DO-958-BF,雷磁,中国)从而控制废液温度变化。
耦合系统工作原理:涂覆有N-TiO2的光催化光纤受到紫外-可见光激发后,Cr(Ⅵ)被快速还原为Cr(Ⅲ)。Cr(Ⅲ)及未还原的Cr(Ⅵ)通过核孔膜传递进入微藻区,小球藻对Cr(Ⅵ)进一步还原,同时吸附Cr(Ⅲ)。小球藻产生的有机物通过核孔膜传递到光催化剂表面,消耗光催化剂表面产生的空穴和·OH,进一步提高光催化对Cr(Ⅵ)的去除率。
1.5 Cr(Ⅵ)去除实验
单独光催化实验:实验体系由N-TiO2涂覆光催化光纤(催化剂重量为70 mg)、Cr(Ⅵ)废水(体积为54 mL)构成,在(35±0.5)℃、铬溶液流速为3 mL/min条件下研究pH及初始Cr(Ⅵ)浓度对光催化还原Cr(Ⅵ)效率的影响。
单独微藻实验:通过核孔滤膜(孔径=1 μm,膜厚=11 mm)将小球藻溶液(体积为12 mL)与Cr(Ⅵ)溶液(体积为54 mL)置于同一反应中。在(35±0.5)℃、小球藻流速为6 mL/min,铬溶液流速为3 mL/min的条件下,研究pH与Cr(Ⅵ)浓度对微藻还原Cr(Ⅵ)效率的影响、小球藻生物量对Cr(Ⅵ)还原速率及总铬去除率的影响。
光催化耦合微藻实验:实验系统由N-TiO2涂覆光催化光纤(催化剂为70 mg)、小球藻液(体积为12 mL、小球藻干重为60 mg)、Cr(Ⅵ)废水(浓度为5 μmol/L、体积为54 mL)构成。实验在温度为(35±0.5)℃、pH=2.0、藻液流速6 mL/min、铬溶液流速为3 mL/min的条件下,定时采集Cr(Ⅵ)及总铬浓度的变化信息。
1.6 Cr(Ⅵ)及总铬浓度及其去除率分析方法
采用二苯碳酰二肼分光光度法[16]测定Cr(Ⅵ)浓度:在硫酸和磷酸1∶1混合配置的酸性条件下,Cr(Ⅵ)将与二苯碳酰二肼生成紫红色络合物,通过在540 nm处测定其吸光度确定Cr(Ⅵ)浓度。
采用高锰酸钾氧化-二苯碳酰二肼分光光度法[17]测定总铬浓度:在硫酸和磷酸1∶1混合配置的酸性条件下Cr(Ⅲ)将被高锰酸钾氧化为Cr(Ⅵ),Cr(Ⅵ)将与二苯碳酰二肼生成紫红色络合物,通过在540 nm处测定其吸光度确定总铬浓度。其中过量高锰酸钾用亚硝酸钠分解,过量亚硝酸钠用尿素分解。
将总铬浓度减去Cr(Ⅵ)浓度,所得值为Cr(Ⅲ)去除的浓度。
单独光催化对Cr(Ⅵ)的去除率(Rp)及单位质量光催化剂在单位时间内对Cr(Ⅵ)的去除速率(Rps)的计算表达式为:
Rp=Ct/C0
(1)
Rps=(C0-Ct)/(t×Mp×C0)
(2)
式中:C0和Ct分别表示初始Cr(Ⅵ)浓度和反应t小时后的Cr(Ⅵ)浓度。式(2)中Mp表示光催化剂干重。
单独微藻对Cr(Ⅵ)的去除率(Rm)及单位质量微藻在单位时间内对Cr(Ⅵ)的去除率(Rms)的计算表达式为:
Rm=Ct/C0
(3)
Rms=(C0-Ct)/(t×Mm×C0)
(4)
式(4)中Mm表面反应体系中微藻生物量总干重。
光催化与微藻耦合对Cr(Ⅵ)的去除率(Rc)及单位时间内光催化与微藻耦合体系对Cr(Ⅵ)的去除速率(Rcs)的计算表达式为:
Rc=Ct/C0
(5)
Rcs=(C0-Ct)/(t×C0)
(6)
光催化与微藻耦合对总铬的去除率(Rg)及单位时间内光催化与微藻耦合体系对总铬的去除率(Rgs)的计算表达式为:
Rg=Cg/C0
(7)
Rgs=(C0-Cg)/(t×C0)
(8)
式(7)(8)中Cg表示反应t小时后的总铬浓度。
1.7 光催化剂及小球藻的表征
利用场发射扫描电镜SEM(sigma-HD,MERCK,Germany)对光催化光纤、N-TiO2、小球藻表面形貌进行分析。利用X射线光电子能谱XPS(ESCALAB250Xi,Thermo Scientific,USA)和X射线衍射XRD(D/max 2 500PC,Rigaku Corporation,Japan)对N-TiO2光催化剂成分进行表征。利用X射线能谱分析EDS(X-MaxN,Oxford Instruments,China)对小球藻表面元素进行分析。采用光纤光谱仪表征光催化光纤及N-TiO2光谱吸收特性、LED面阵光源光谱发射特性。
2 结果与讨论
2.1 光催化材料物理光学特性
图2(a)显示初始光催化光纤具有光滑的表面结构,经过氢氟酸和氢氧化钠溶液腐蚀后的光催化光纤表面具有不规则凹坑,该凹坑有助于增大光催化光纤的比表面积、提高催化剂负载量与附着强度、提高光催化的整体效率与光催化剂的可重复利用性。图2(b)显示光催化剂被均匀的涂覆在光催化光纤表面,放大图显示N-TiO2具有纳米尺度,平均直径约为25 nm。

图2 扫描电子显微镜图像
图3为XRD图谱中,2θ=25.26°、38.01°、48.09°、53.91°、55.07°、62.7°、68.8°、70.23°、75.09°处的9个特征峰,分别对应锐钛矿TiO2正方晶体的(101)(004)(200)(105)(211)(204)(116)(220)和(215)反射面。XPS图谱中,406.45 eV为N 1s 的特征吸收峰,表明光催化剂中含有Ti-N键;458.25、464.1 eV对应Ti 2p 的特征吸收峰峰;529.5 eV对应O1s的特征吸收峰峰。图3为成功制备的N-TiO2光催化剂的图谱。
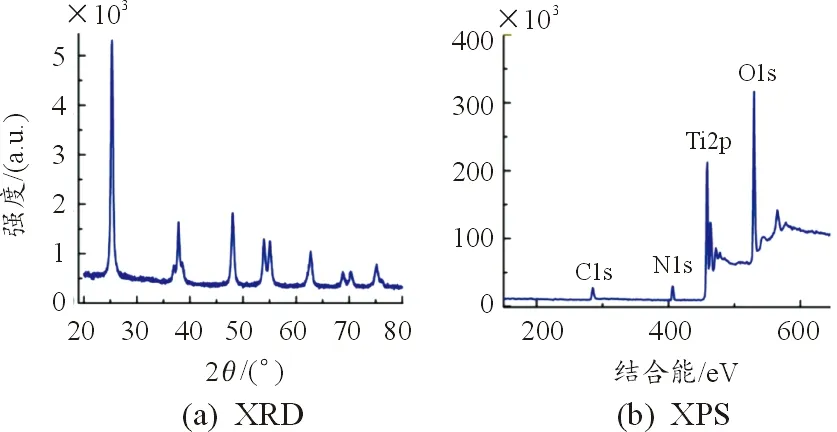
图3 N-TiO2光催化材料的图谱
图4(a)显示光催化光纤对光吸收率低,表明光催化光纤适宜作为固定N-TiO2光催化剂的载体。当光催化光纤表面涂覆厚度约为10 μm的光催化剂时,透射光谱质量显著减弱,表明光催化剂对光产生了强吸收。图4(b)进一步显示固定化N-TiO2膜具有显著的紫外-可见光吸收特性,其可见光吸收边带延长至525 nm,原因在于N掺杂剂减小了TiO2禁带宽度[14],N-TiO2良好的可见光响应特性将有助于提高TiO2光催化活性,实现对Cr(Ⅵ)的快速还原。
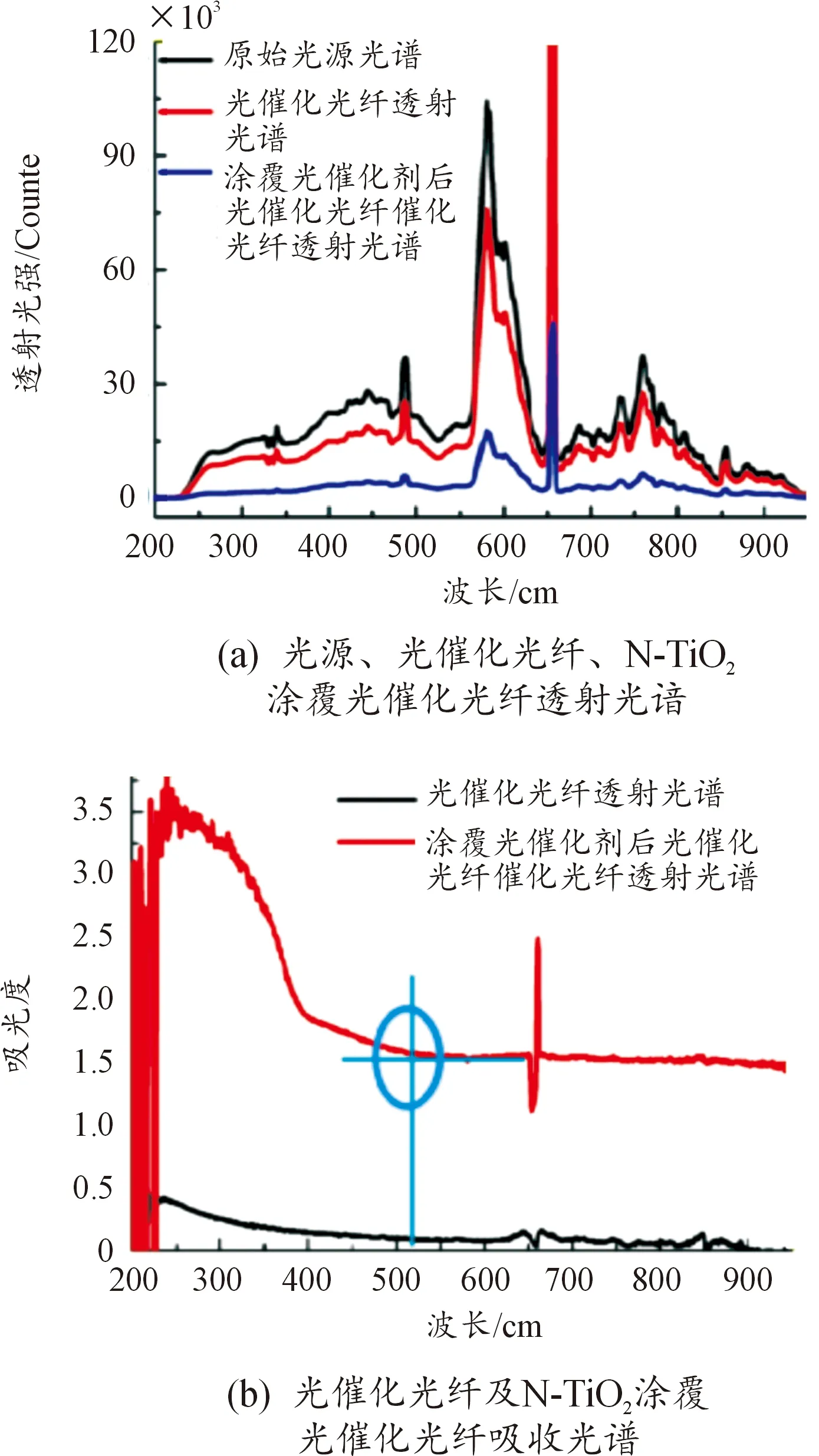
图4 光谱传输及吸收特性曲线
2.2 pH值及初始Cr(Ⅵ)浓度对单独光催化及单独微藻去除Cr(Ⅵ)性能的影响

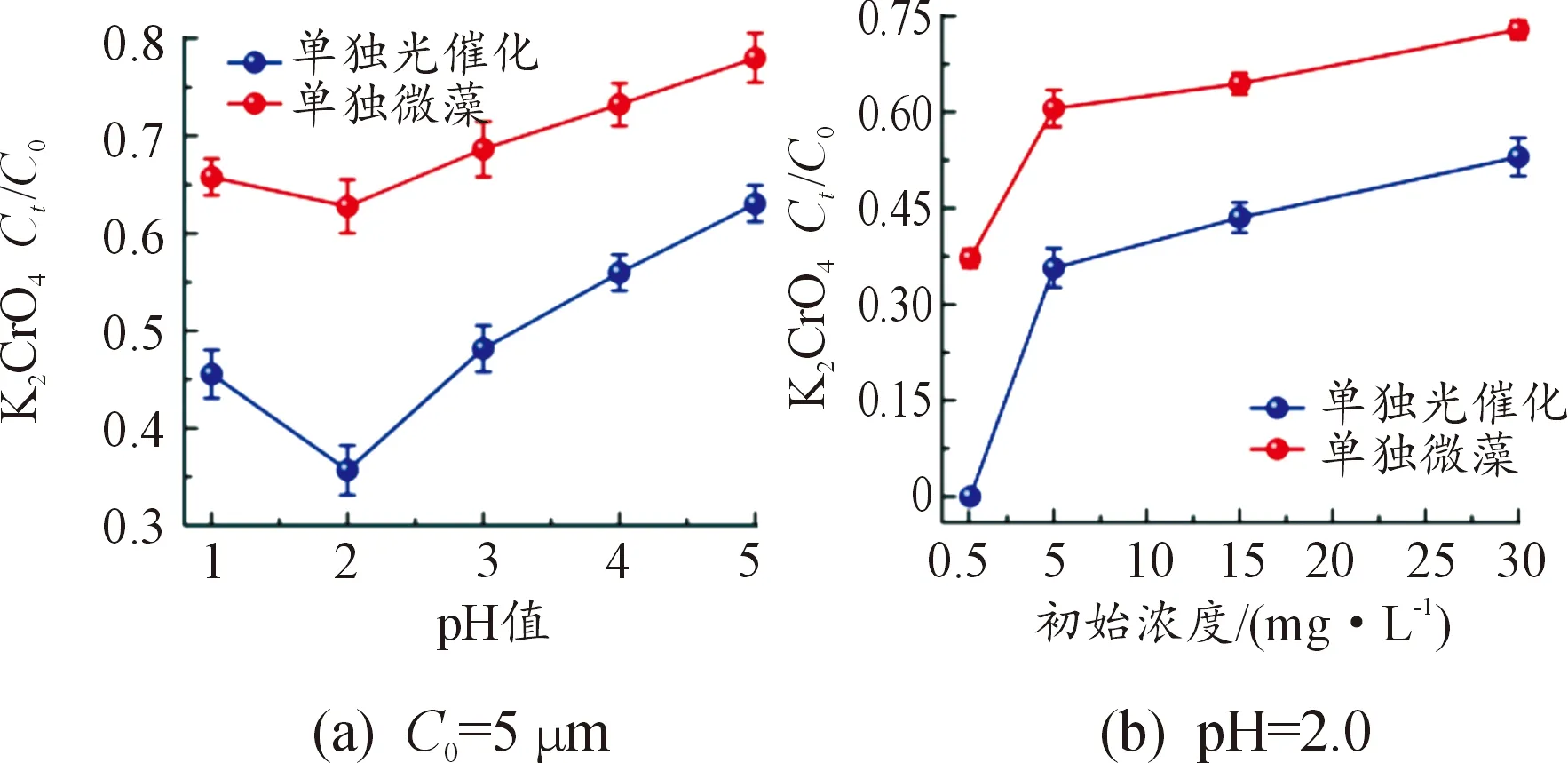
图5 初始pH和初始Cr(Ⅵ)浓度对Cr(Ⅵ)去除性能的实验结果曲线
图5(b)显示:随着初始Cr(Ⅵ)浓度的增加,单独光催化与单独微藻对Cr(Ⅵ)的去除率逐步降低;原因在于光催化剂与小球藻表面的活性位点有限,高浓度Cr(Ⅵ)会在光催化剂及小球藻表面产生竞争吸附,导致光催化及微藻去除率降低;尤其是小球藻的生长代谢过程受高浓度Cr(Ⅵ)抑制,导致小球藻失活、细胞变形或破碎,进一步削弱小球藻对Cr(Ⅵ)的去除。因此,在后续的实验研究过程中,将选择pH=2.0和初始浓度为5 μmol/L的Cr(Ⅵ)进行研究。
2.3 单独光催化及单独微藻去除Cr(Ⅵ)及总铬性能
N-TiO2催化剂在10 g光催化光纤表面负载量及小球藻生物量对液相中Cr(Ⅵ)及总铬去除性能的影响,如图6所示。
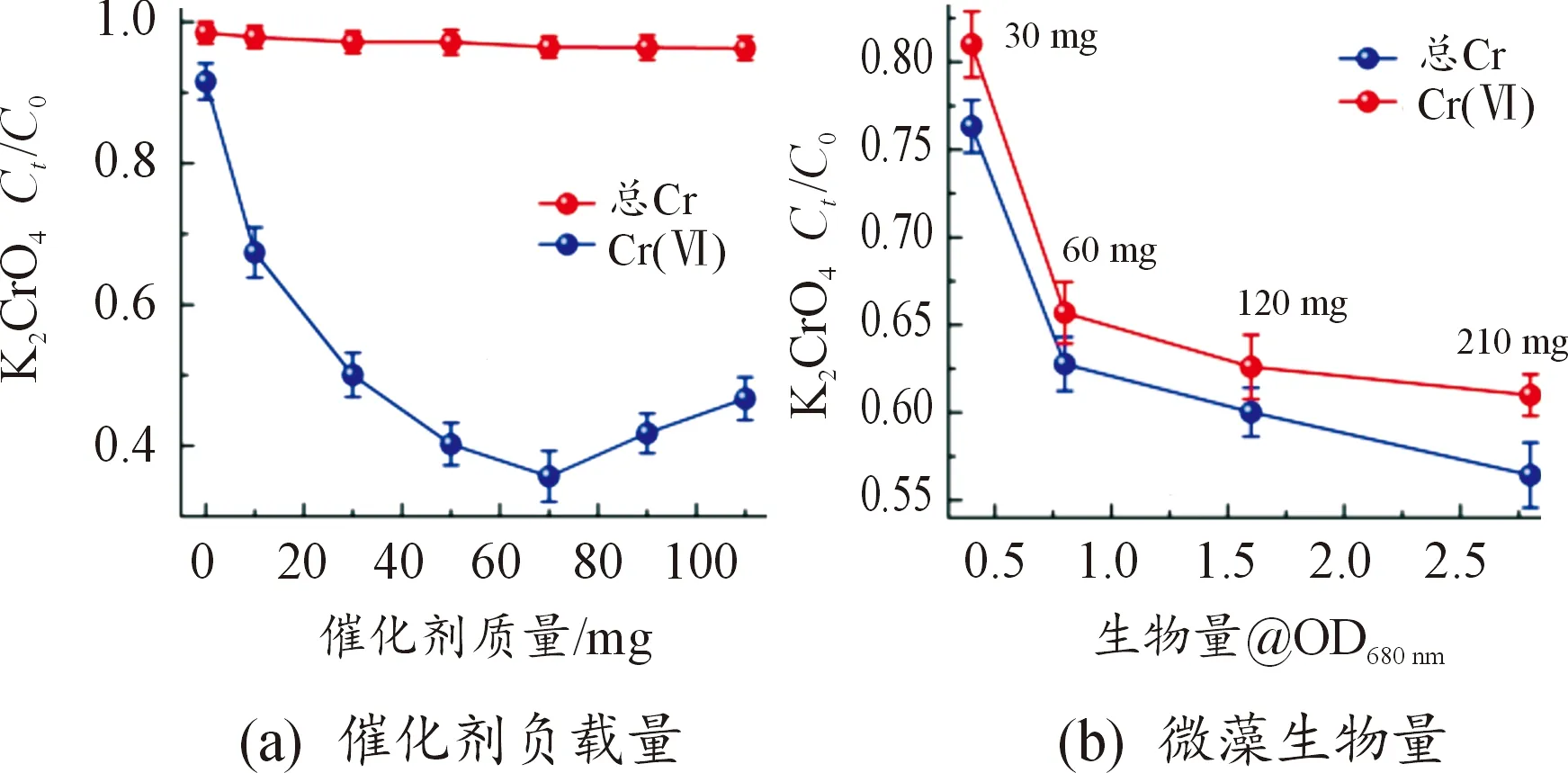
图6 单独光催化及单独微藻对Cr(Ⅵ)及 总铬去除性能(去除时间3 h)曲线
图6(a)显示:随着光催化剂质量的增加,Cr(Ⅵ)去除率先增大后减小,当质量为70 mg时,Cr(Ⅵ)去除率达到最大,原因在于:当光催化剂负载量较少时,光催化膜较薄有利于光传输及表面电子转移,但光催化活性受光催化剂负载量限制;而当N-TiO2负载量较大时,催化层较厚,催化层内光传输受限且分布不均,导致光电转换性能降低,光生电子-空穴对复合率提升,光催化层活性降低,Cr(Ⅵ)去除性能降低[18]。同时,图6(a)显示:液相中总铬浓度基本不受光催化剂负载量的影响,原因在于单独光催化将Cr(Ⅵ)还原为Cr(Ⅲ),无法进一步将Cr(Ⅲ)还原为更低价的Cr或金属铬[18],因此液相中总铬保持恒定。
图6(b)显示,当生物量从OD680 nm=0.5(干重30 mg)增加到OD680 nm=0.8(干重60 mg)时,Cr(Ⅵ)和总铬去除率显著增加,随后Cr(Ⅵ)和总铬去除率随着生物量的增加缓慢提升。液相中小球藻生物量增加后,会提供更多的活性位点还原Cr(Ⅵ)并吸附Cr(Ⅲ),因此去除率增加。当小球藻生物量超过一定限度时,小球藻的活性位点已经能去除一定浓度的Cr(Ⅵ),此时继续增加小球藻的生物量的作用降低,因此去除率增加趋势逐渐减缓。
虽然单独光催化和单独微藻可实现对液相中高毒Cr(Ⅵ)的去除,但去除率低,尤其是受生物量的限制,微藻难以完全去除Cr(Ⅵ),如图7所示。单位质量光催化剂在单位时间内对Cr(Ⅵ)的去除速率(Rps)为0.001 6 μmol/L(h·mg)-1,单位质量微藻在单位时间内对Cr(Ⅵ)的去除率(Rms)为0.001 12 μmol/L(h·mg)-1。
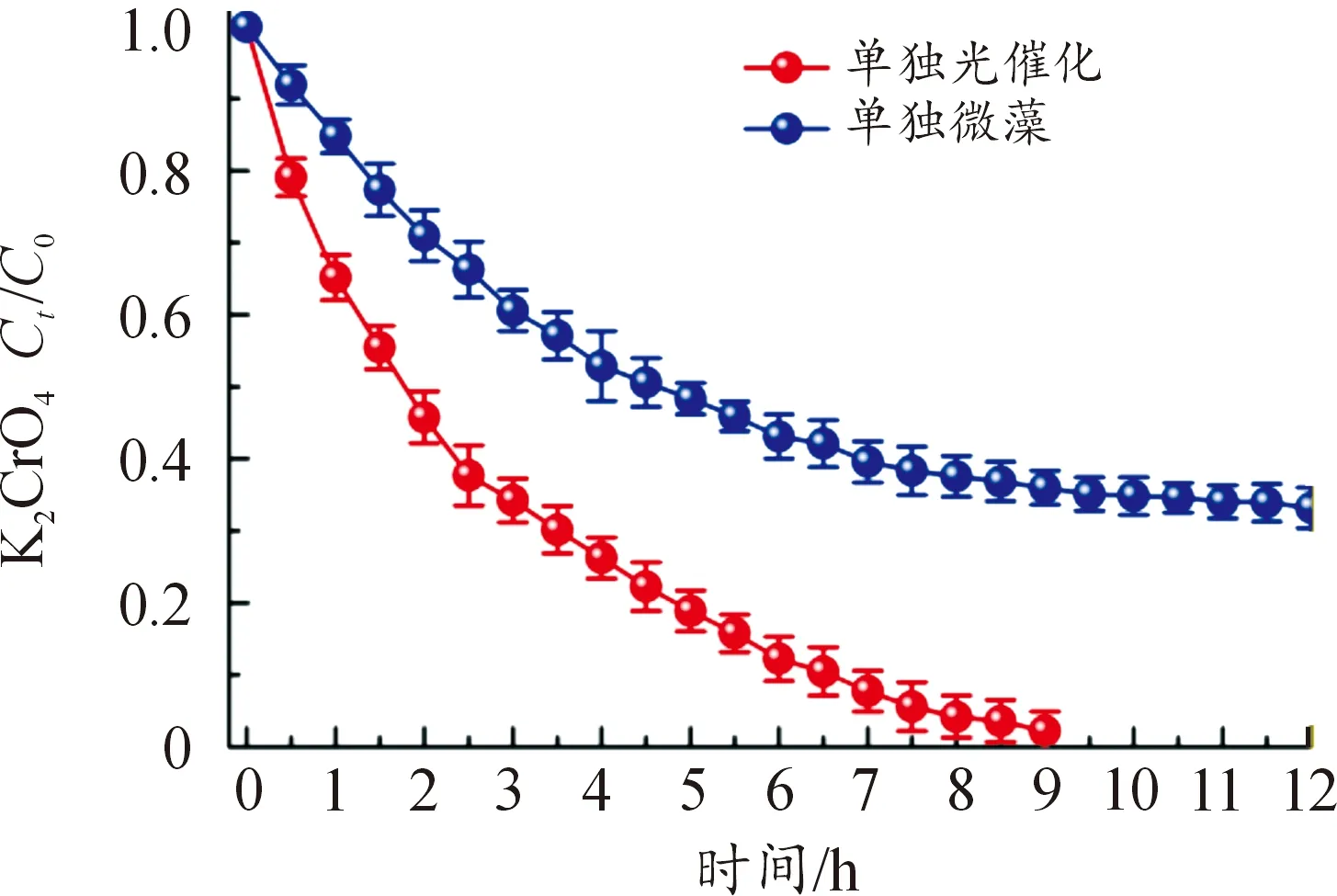
图7 不同时间下单独光催化和单独微藻对Cr(Ⅵ)的去除性能曲线(光催化剂负载量为70 mg,微藻生物量OD680 nm=0.8,生物量干重60 mg)
2.4 耦合系统去除Cr(Ⅵ)及总铬性能
为了提高Cr(Ⅵ)及总铬除去效率,进一步研究耦合系统对Cr(Ⅵ)及总铬除去性能,实验结果如图8所示。实验条件:pH=2.0,C0=5 μmol/L,光催化剂负载量为70 mg,小球藻生物量OD680 nm=0.8(干重为60 mg)。
图8(a)显示3 h内,光催化与微藻耦合系统对Cr(Ⅵ)的去除率达到100%,高于单独光催化与单独微藻去除率之和96%(图6),原因在于光催化与微藻相互耦合,相互促进,提高了去除Cr(Ⅵ)的效率。单位时间内光催化与微藻耦合体系对Cr(Ⅵ)的去除率(Rcs)达0.334 μmol/(L·h-1)。图8(a)还显示在光催化与微藻耦合系统中总铬含量等于Cr(Ⅲ)与Cr(Ⅵ)含量之和,间接证实光催化还原的Cr(Ⅲ)被微藻吸附。
图8(b)显示耦合系统在3 h内对总铬的去除率为44.2%,高于单独微藻系统对总铬去除率34.3%和单独光催化系统对总铬的去除率3.9%之和(图6)。单位时间光催化与微藻耦合体系对总铬的去除率(Rgs)到达0.148 μmol/(L·h-1)。综合图8(a)和图8(b)可知,光催化与微藻耦合系统能实现对Cr(Ⅵ)及总铬的快速去除。
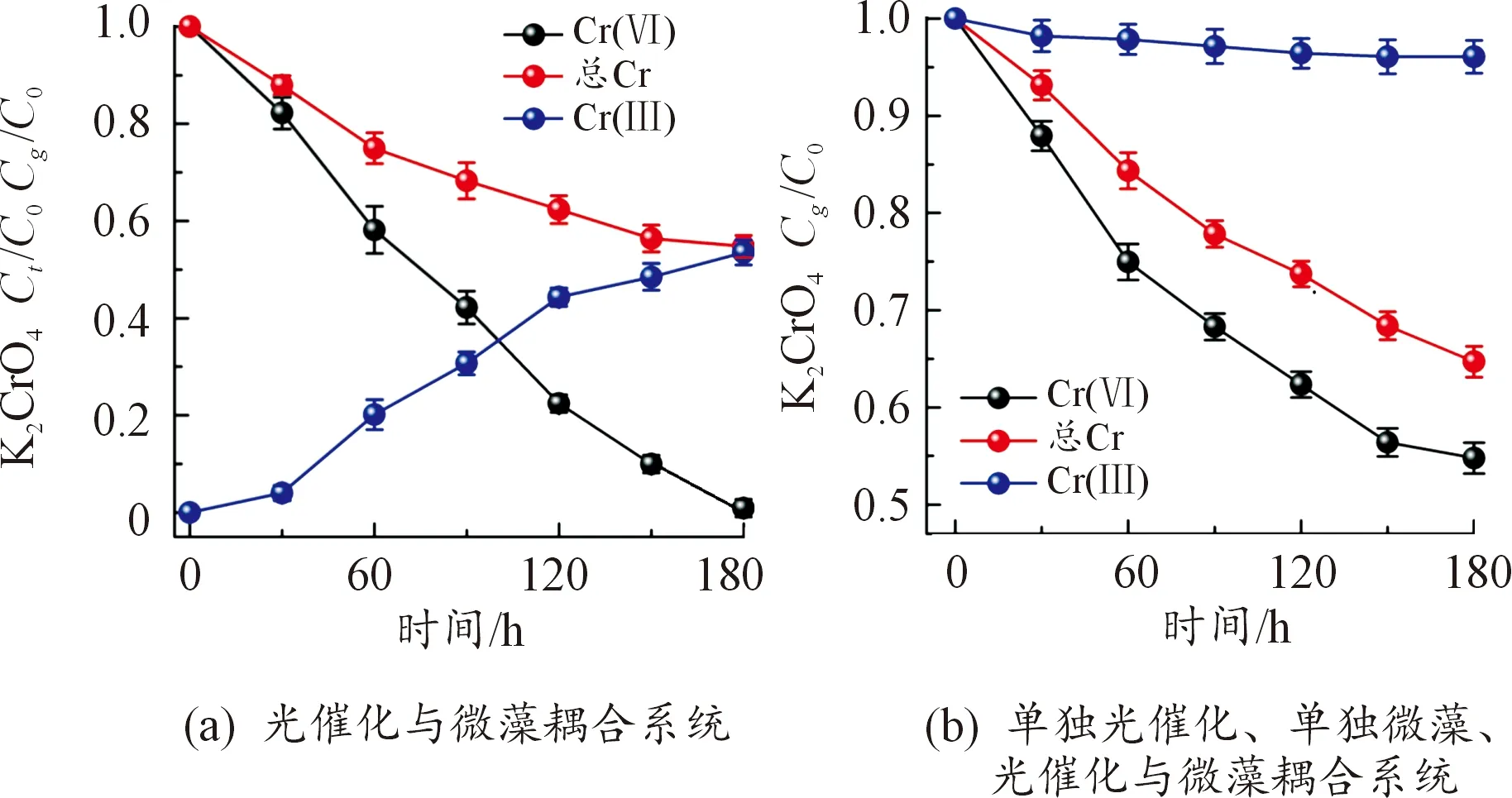
图8 耦合系统对Cr(Ⅵ)及总铬除去性能的实验结果曲线
2.5 耦合系统高效去除Cr(Ⅵ)及总铬的机理
为了分析光催化耦合系统高效去除Cr(Ⅵ)和总铬的机理,首先对初始小球藻和反应后小球藻的表面形貌进行了表征,如图9所示。
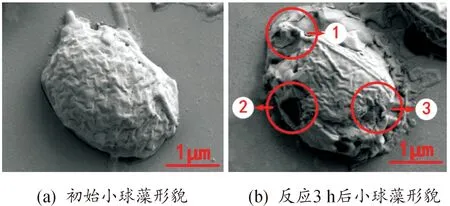
图9 小球藻的表面形貌图
图9(a)显示初始小球藻形态呈椭球型,表面饱满且无破损;图8(b)显示,与Cr(Ⅵ)反应后的小球藻呈现扁平状,图中①、②、③处有明显的破损和凹陷。这是由于小球藻细胞壁中的金属离子K(Ⅰ)、Na(Ⅰ)、Ca(Ⅱ)、Mg(Ⅱ))与带负电的基团之间拥有较强的静电吸引和配位键,而较低配位键的重金属离子Cr(Ⅵ)与Cr(Ⅲ)会代替小球藻细胞壁中的金属离子,导致小球藻表面反应后结构松弛,表面变得扁平[19]。
为了进一步探究小球藻反应前后表面离子的变化信息,对初始小球藻和反应3 h后的小球藻进行了EDS表征,表征结果如图10所示,Si为基底元素,Au为表征所需元素。
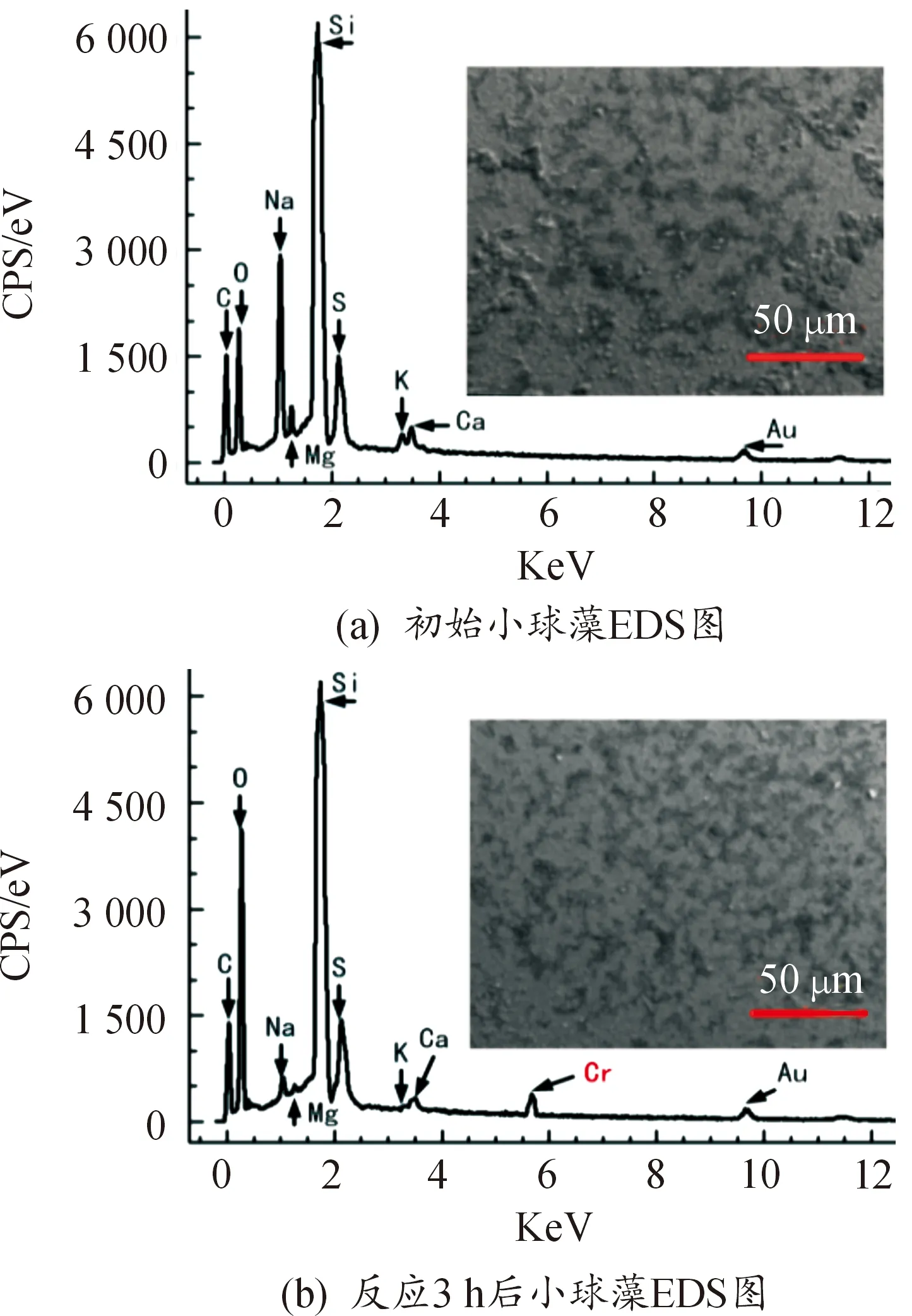
图10 小球藻EDS表征结果图
图10(a)显示,初始小球藻细胞表面除了本身必须的C、O元素外,还富含金属元素K、Na、Ca、Mg。在反应之后,金属元素K、Na、Ca、Mg都有所下降,图10(b)显示,当小球藻暴露于Cr(Ⅵ)溶液中时,细胞表面的EDS能谱图中出现了Cr峰,证明了反应过程中小球藻通过离子交换成功对Cr进行吸附。表1为初始和反应后小球藻表面具体元素占比。
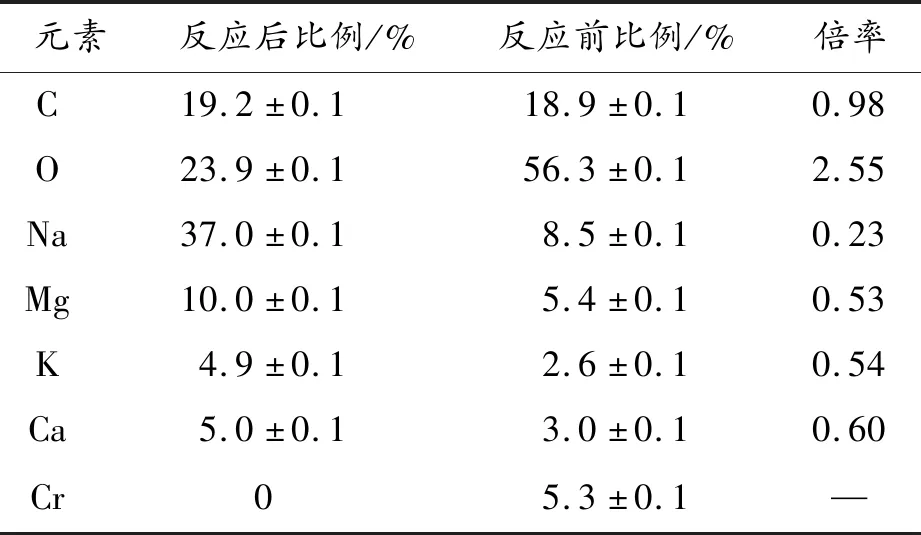
表1 反应前后小球藻表面元素占比
表1显示,反应后小球藻表面除了K、Na、Ca、Mg金属元素下降外,C元素略微下降,O元素上升。原因在于小球藻被Cr(Ⅵ)破坏后,部分有机物浸出,因此C元素有所下降;有机物在反应过程中,一方面会消耗光催化所产生的空穴和·OH,另一方面会与Cr(Ⅵ)发生氧化还原反应,使Cr(Ⅵ)被还原成Cr(Ⅲ),因此O元素会升高[20]。光催化与微藻耦合去除液相Cr(Ⅵ)及总铬的机理见图11。
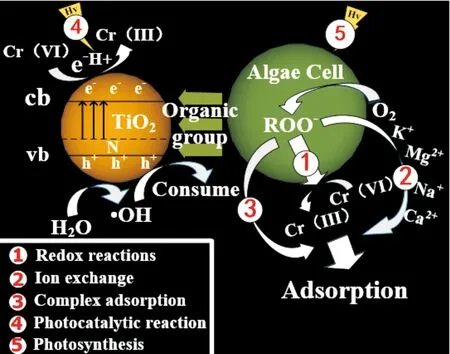
图11 光催化耦合微藻系统原理分析示意图
在光催化与微藻耦合除去Cr(Ⅵ)及总铬的体系中,固定化N-TiO2光催化剂能快速将Cr(Ⅵ)还原为Cr(Ⅲ),从而降低高毒性的Cr(Ⅵ)对小球藻活性的影响,并减少Cr(Ⅵ)与Cr(Ⅲ)在小球藻表面的竞争吸附,提高小球藻去除总铬的能力。小球藻细胞在反应过程中会释放溶解的有机物(羧基,酚羟基,仲醇基等),能有效消耗TiO2的激发空穴和·OH,抑制电子空穴复合,增强光催化剂的活性。有机物能与Cr(Ⅵ)进行氧化还原反应,还能络合吸附Cr(Ⅵ)及Cr(Ⅲ)形成络合物,藻中的金属离子能与Cr(Ⅲ)进行离子交换,进一步提高光催化耦合微藻还原Cr(Ⅵ)的性能并去除产物Cr(Ⅲ),使液相中总铬降低。最终实现光催化与微藻紧密耦合,快速去除Cr(Ⅵ)。
3 结论
1)耦合系统中光催化与微藻相互耦合、相互促进,实现了液相总铬的快速去除。
2)当初始Cr(Ⅵ)浓度为5 μmol/L、pH值为2、光催化剂质量为70 mg、微藻生物量浓度为60 mg时,光催化与微藻耦合系统在3 h内实现了对Cr(Ⅵ)完全还原,单位时间内去除速率(Rcs)达到0.334 μmol/(L·h-1),同时单位时间内总铬去除速率(Rgs)达到0.148 μmol/(L·h-1)。
本研究成果扩展了光催化与微藻耦合技术在重金属废水治理方面的应用领域。
