BiOCl/Bi2WO6复合材料的制备及其光催化性能研究
2022-01-05陈飘张晓燕熊刘燕杨水金
陈飘,张晓燕,熊刘燕,杨水金
(湖北师范大学化学化工学院,污染物分析与资源化技术湖北省重点实验室, 湖北 黄石 435002)
0 引言
随着相关应用研究的不断推进,半导体光催化技术在废水治理中可以发挥出重要作用,它可以充分利用太阳能资源中既廉价又高效的可见光资源[1].Bi基光催化剂是近年来发现的一种较为有效的光催化材料,解决了研究中的很多问题[2-5].但由于铋基催化剂的光生电子空穴对易复合,从而导致光催化效率降低,目前对铋基催化剂的改性方法有很多.例如,杨等[6]人,通过一步溶剂热法实现了Fe3+对Bi2MoO6的掺杂改性.结果表明,掺杂量为32.5%的Fe3+/Bi2MoO6复合物的可见光光催化效果最优;此外,他们还通过调节五水硝酸铋的含量,采用溶剂热法制备Bi/Bi2O2CO3复合物,实现半金属Bi的沉积[7].在可见光下对罗丹明B (C28H31ClN2O3)进行降解.与纯的Bi2O2CO3相比,沉积金属Bi后光催化降解RhB的效率高达99%,降解速率常数高达0.120 7 min-1,并且对BPA(双酚A,(CH3)2C(C6H4OH)2)也有一定的降解效果.而增强的光催化活性可能归因于Bi的SPR(表面等离子体共振)效应,使得Bi2O2CO3被可见光激发,并且促进了光生载流子的分离;张等[8]人通过溶剂热法制备了C/Bi2MoO6光催化复合材料,并在可见光下进行RhB以及BPA的降解实验,发现C负载量为5%时,C/Bi2MoO6复合材料的光催化降解RhB具有最高的光催化活性,60 min内降解率达到93%,速率常数是纯Bi2MoO6的4.6倍;胡豪等[9]人,通过水热法制备不同BiOCl负载量的BiOCl/ Bi2MoO6,形成复合异质结,在可见光下照射污染物RhB,研究光催化降解的反应机理,并探究不同BiOCl负载量的催化剂对光催化降解的影响,其中最优负载BiOCl/Bi2MoO6催化剂在可见光照射80 min时,对罗丹明B的降解率达到88.1%.
钨酸铋是铋基材料中深受广大研究者喜爱的半导体材料之一.它是Aurivillius化合物中的一种,带隙值为2.72 eV,有较高的光降解活性.但是因为它的光生电子与空穴之间结合的几率很高,所以光催化活性又受到了一定的限制10].据文献报道,BiOCl是四方结构的结晶,有着独特的层状结构,并且可以形成氧空位,带隙也较大,有一定的光降解活性,同时毒性和成本都比较低,在环境修复上有重要意义[11-13].但是BiOCl带隙较宽,只在紫外光下被激发,不能在可见光的范围内拥有较好的活性[14-15].因此,我们将BiOCl和Bi2WO6这两种结构不同的物质结合,构成异质结构,可以降低Bi2WO6的电子和空穴的结合效率,提高降解活性,同时解决了BiOCl只能在紫外光下被激发的问题,且环保、节能和高效,未来在污水处理方向有着很好的应用前景.
1 实验部分
1.1 实验试剂五水硝酸铋(Bi(NO3)3·5H2O),二水钨酸钠(Na2WO4·2H2O),氯化钠(NaCl),无水乙醇(C2H5OH),罗丹明B(C28H37ClN2O3,RhB),环丙沙星(C17H18FN3O3,CIP),去离子水,以上所使用的试剂均为分析纯,不经过进一步的纯化.
1.2 材料的制备BiOCl的制备:称取0.485 1 g的Bi(NO3)3·5H2O,向其中加入80 mL H2O,充分搅拌后,再加入0.058 4 g NaCl,持续搅拌30 min后,转入100 mL 反应釜,在120 ℃下反应24 h,待冷却到室温后,产物经离心并用去离子水和无水乙醇各洗涤3次后在80 ℃下烘干,得到纯的BiOCl,将其标记为BOC.
Bi2WO6的制备:称取0.970 1 g的Bi(NO3)3·5H2O,向其中加入80 mL H2O,再加入0.329 9 g Na2WO4·2H2O,持续搅拌30 min后,转入100 mL反应釜,在120 ℃下反应24 h,待冷却到室温后,产物经离心并用去离子水和无水乙醇各洗涤3次后在80 ℃下烘干,得到纯的Bi2WO6,将其标记为BWO.
BiOCl/Bi2WO6复合物的制备:称取1.452 2 g Bi(NO3)3·5H2O,向其中加入80 mL H2O,充分搅拌后,再分别向其中加入0.329 9 g的Na2WO4·2H2O和0.040 6 g NaCl,持续搅拌1 h后转入100 mL反应釜,在120 ℃下反应24 h,待冷却到室温后,产物经离心并用去离子水和无水乙醇各洗涤3次后在80 ℃下烘干,得到BiOCl/Bi2WO6复合物,将其标记为0.7Cl-/BWO.
1.3 光催化性能测试使用300 W氙灯(CEL-HXF300)模拟可见光光源.在同一条件下,将20 mg催化剂以及罗丹明B溶液(50 mL 10 mg/L)和环丙沙星溶液(50 mL 10 mg/L),分别加入反应器中,先在不开灯的情况下,暗处理30 min,使得污染物分子与催化剂之间达到吸附与脱附的平衡.30 min后取样并打开灯,对于罗丹明B,在每隔10 min后取1次样;而CIP溶液在每隔20 min取1次样,两者均取出约2 mL的上清液.在高速离心(10 000 r/min 2 min)后,测试两者的紫外-可见吸收光谱.
2 结果与讨论
2.1 XRD分析图1是实验所制备的3种样品的粉末衍射图.可以发现,纯BWO的衍射峰在2θ=27.17°、34.62°、46.97°和58.54°分别对应于(041)、(260)、(202)、(262)晶面的衍射峰.根据标准可以很好地指示到BWO的四方相卡(JCPDS#26-1044).对于纯的BOC,其衍射峰在2θ=11.98°、24.10°、25.86°、32.49°、33.44°、36.54°、43.56°、49.69°和58.56°分别对应于四方相BiOCl(JCPDS#06-0249)的(001)、(002)、(101)、(110)、(102)、(003)、(103)、(113)、(212)晶面.XRD分析表明制备好的BOC/BWO异质结中只有BOC和BWO两相,并且没有观察到其他新相,表明异质结仅由BOC和BWO两相组成,无其他杂质相的加入.

图1 样品的XRD图谱
2.2 SEM图为进一步分析样品的形貌特征,我们做了扫描电镜测试,从图2(a)中我们可以看到纯BOC为不规则的片状结构,直径在300 nm到1 200 nm之间,片状很薄,易于附着在其他物质上;从图2(b)中可以看出纯BWO为扁平的鸟巢状结构,直径约3 μm,每一个小结构中又有较多空隙,因此其他物质易于附着.然而在图(c)所示的复合物0.7Cl-/BWO中,两者通过组装形成了松散的微球.

图2 样品BOC(a)、BWO(b)和0.7Cl-/BWO(c)的SEM图
2.3 结构分析红外测试通常被用于对材料的结构进行表征,如图3所示,并结合文献可知[16],对于纯BOC:524 cm-1处为BOC中Bi—O键的伸缩振动峰;对于纯BWO:589 cm-1处对应Bi—O键的伸缩振动峰;730 cm-1处对应W-O键的伸缩振动峰;1 382 cm-1处对应W—O—W键的伸缩振动峰.我们还可以看到复合物0.7Cl-/BWO在524 cm-1、589 cm-1、730 cm-1、1 382 cm-1等处的振动峰,证明BOC和BWO均同时存在.此外,3种材料在波数为3 500 cm-1左右出现的峰,都可能归结于吸附于催化剂表面的水分子中O—H键的伸缩振动峰.
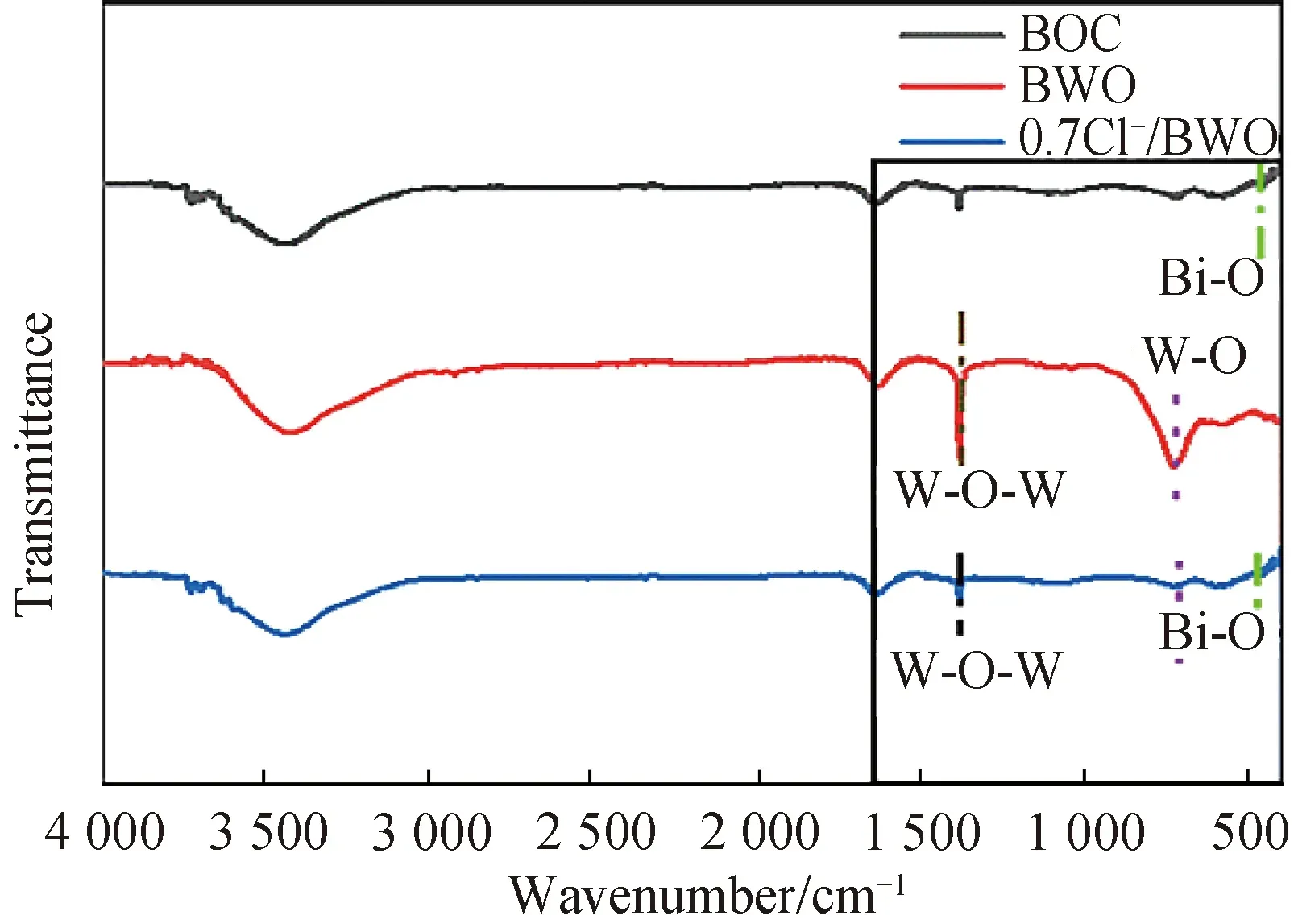
图3 样品的FT-IR图
3 光催化性能测试
3.1 光催化降解RhB和CIP图4(a)是CIP的降解曲线图,光照120 min后,纯BWO对CIP的降解率达64.00%;纯物质BOC在光照120 min后对CIP的降解率仅仅达到30.01%.而复合物在光照120 min后,对CIP的降解率高达93.91%,可以明显看出复合材料对CIP的降解率大大提高,说明在BiOCl复合到Bi2WO6后,相比于纯物质,复合物的活性增强明显.图4(c)是RhB的降解活性曲线图.纯的BWO、BOC和复合物0.7Cl-/BWO在光照下降解RhB与降解CIP效果相似,但其在相同条件下降解所用时间更短,在光照70 min时,降解率分别达到33.49%、16.70%、99.19%.而且,从图4(b)和图4(d)两图中可以看出,催化剂对于CIP和RhB的降解均符合一级动力学模型.由此可见复合之后,催化剂的活性提高明显.

图4 CIP降解曲线(a)和对应的动力学曲线(b);RhB降解曲线(c)和对应的动力学曲线(d)
3.2 光催化剂的稳定性光催化剂的稳定性是污水净化实际应用中的衡量标准之一.如图5所示,经过5次循环实验之后,催化剂的活性保持较好,没有因多次实验而明显降低活性,可以证明此光催化剂的稳定性良好,回收与利用十分方便.
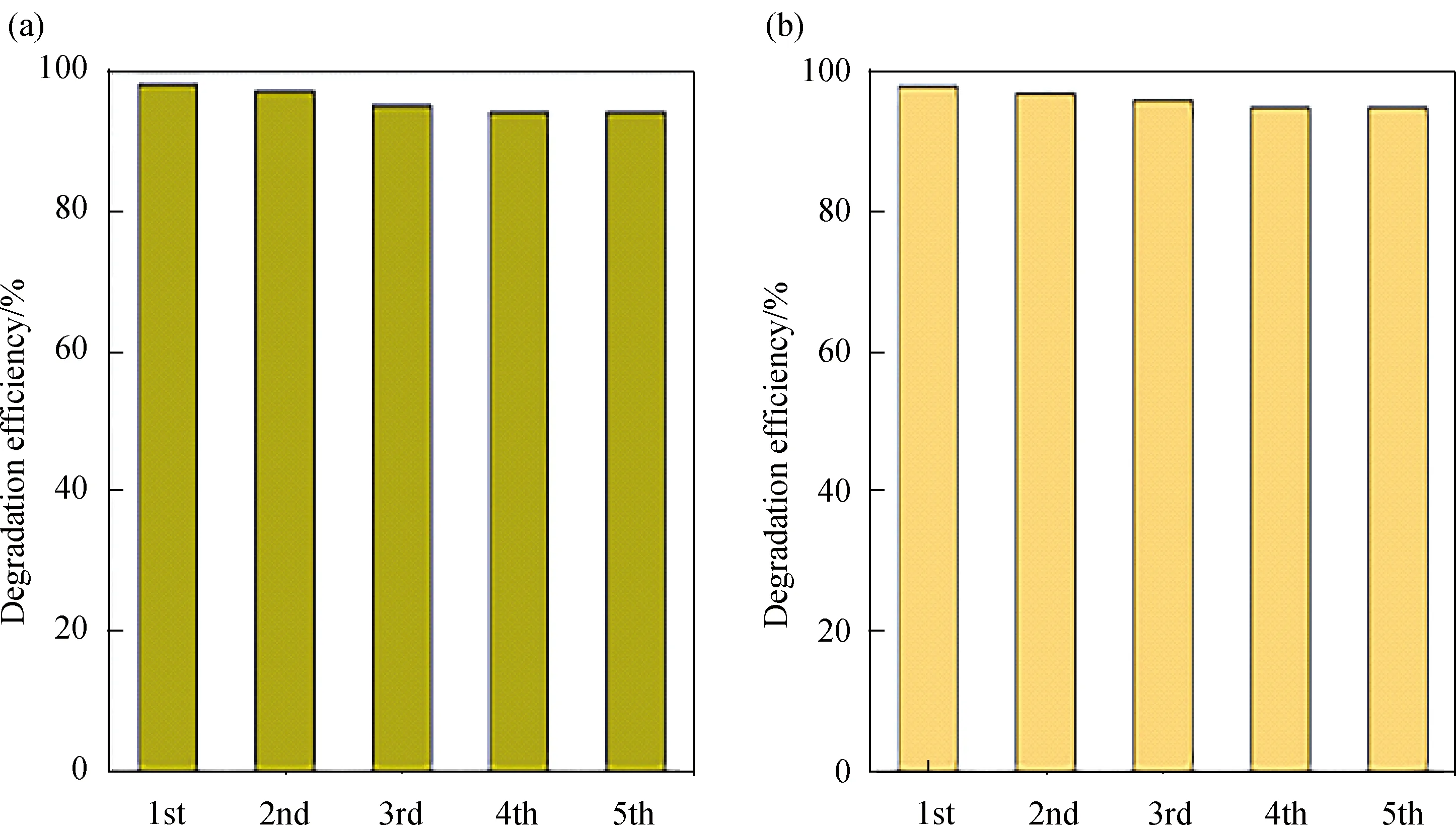
图5 光催化剂降解RhB的循环实验图(a)和CIP的循环实验图(b)
3.3 反应活性物种测试实验加入10 mmol/L对苯醌(BQ)用来捕获催化剂中的活性物质·O2-;10 mmol/L乙二胺四乙酸二钠(EDTA-2Na)用于捕获催化剂中的活性物质h+和10 mmol/L异丙醇(IPA)用来捕获·OH.如图6所示,加入EDTA-2Na后,光催化降解效率明显降低,说明h+在光催化降解中占主要作用.加入BQ后,光催化降解效率发生了微小变化,可以说明·O2-在光催化降解中起到了辅助作用;IPA的加入对光催化的降解效率的影响极小.

图6 不同捕获剂对RhB降解的光催化活性影响
3.4 光催化降解机理分析通过对材料的荧光光谱测试得知,复合物的荧光强度明显比两种纯物质的要低,表明光生电子能有效分离.基于以上的实验结果和过去关于BiOCl以及Bi2WO6能带结构的报道[17],我们将该反应可能的反应机理用图7进行描述.首先在可见光照射下,Bi2WO6的电子被激发,由于Bi2WO6的导带比BiOCl的导带高,因此Bi2WO6的导带中的电子迁移至BiOCl的导带上,又与氧气结合,形成活性物质超氧自由基(·O2-).Bi2WO6价带空穴则直接与污染发生氧化还原反应而达到降解目的.

图7 光催化降解机理图
4 结论
本研究通过水热法合成了BiOCl/Bi2WO6的复合物.在一定时间内,对罗丹明B和环丙沙星的降解率由纯物质的33.49%和64.00%提高到了99.19%和93.91%,证明了复合物相比于纯物质的光催化降解活性有了很大的提高.通过自由基捕获实验和光催化剂稳定性的探究实验,我们尝试着探究了本次实验可能的实验机理,h+在本次实验中发挥主要作用,·O2-起辅助作用,参与了有机污染物的降解,且证明了光催化剂的稳定性较高,具有很好的应用前景.
