海藻希瓦氏菌及其特异性脂多糖对结直肠腺瘤的影响及机制
2022-01-04周俊潇李俊彦刘凯杰梁颜笑王红
周俊潇 李俊彦 刘凯杰 梁颜笑 王红,
1华南理工大学医学院(广州 510006);华南理工大学医学院附属第二医院2消化内科,3病理科(广州 510120)
当肠上皮细胞的DNA修复和增殖机制改变时,异常增殖的细胞由隐窝基底向管腔延伸,形成散落的腺瘤[1]。从结直肠腺瘤(colorectal adenoma,CRA)到结直肠腺癌(colorectal cancer,CRC)通常需要很多年,包括异常的细胞增殖、侵袭和转移[2]。近年来,人们越来越关注炎症-腺瘤-腺癌序列中不同阶段的肠道菌群变化,但关于CRA癌前病变的生物标记物却知之甚少。本课题组前期发现在CRA人群的肠道细菌中,海藻希瓦氏菌(Shewanella algae,S.algae)的丰度明显上调[3]。并将S.algae对APCmin/+小鼠进行灌胃,发现S.algae可以通过改变APCmin/+小鼠肠道炎性微环境促进CRA的发展。目前已经从肠黏膜、伤口、粪便、尿液、结膜、胆汁、腹水、胸膜液和血液中分离出 S.algae[4]。据报道,韩国首尔的一家医院暴发了海藻希瓦氏菌属的感染,导致了31例腹部、肝胆感染和菌血症病例,说明该类细菌可能成为医院内潜在的严重人类病原体,并可能被纳入医院感染监测系统[5]。后续实验在APCmin/+小鼠腺瘤组织中发现了大量的巨噬细胞和脂多糖(lipopolysaccharide,LPS)水平的升高。LPS又叫内毒素,是革兰氏阴性细菌外膜的主要组成部分。不同细菌的LPS活性并不相同,大肠杆菌(Escherichia coli,E.coli)LPS被认为是Toll样受体4(toll-like receptor 4,TLR4)的天然激动剂,而Bartonella quintana LPS却是TLR4的天然抑制剂[6]。目前E.coli LPS的作用机制已被广泛研究,然而本课题组发现的S.algae特异性LPS的作用机制尚不明确。已知E.coli LPS在体内并不直接攻击细胞或器官,而是通过激活免疫器官,尤其是刺激巨噬细胞。巨噬细胞高度表达CD11b,可以根据环境刺激,极化为M1和M2不同的表型,分别高表达CD86、CD80和CD163、CD206,可用于评估巨噬细胞的含量[7-8]。
本研究采用T-sol法提取S.algae特异性LPS,将S.algae及其LPS对C57BL/6J雌性小鼠以灌胃的形式,观察S.algae特异性LPS对早期CRA的影响。
1 材料与方法
1.1 菌株、细胞及动物 S.algae,ATCC 51192,购自北京北纳研究院。THP-1、Caco-2和HT29细胞均购自ATCC细胞库。SPF级8~12周龄雌性C57BL/6J小鼠24只,购买于广东省动物中心。饲养于SPF级环境,12 h:12 h昼夜间断照明。每3 d更换动物垫料,所有的饮用水、水瓶、鼠笼都经高温高压灭菌消毒。
1.2 主要试剂 氧化偶氮甲烷(Azoxymethane,AOM),佛波醇12-肉豆蔻酸酯13-乙酸酯(Phorbol-12-myristate-13-acetate,PMA)和E.coli O55:B5 LPS均购自Sigma公司,右旋糖酐硫酸酯钠(Dextran sodium sulfate,DSS)购自 Mpbio公司,TLR4和p-IKKβ抗体购自Abcam公司,p-IkBα、NF-κB p65和p-NF-κB p65抗体购自Cell signaling公司。
1.3 主要方法
1.3.1 LPS提取 采用T-sol法[9]提取并纯化S.algae特异性LPS,冻干机冻干称重,4℃密封保存。
1.3.2 小鼠造模与干预 小鼠适应性喂养至体质量为20~25 g。随机分为Control组和3组实验组:AOM/DSS组、AOM/DSS+LPS组、AOM/DSS+S.algae组,每组6只。实验组给予腹腔注射AOM 10 mg/kg,对照组注射等量生理盐水。休息一周后,实验组小鼠根据体质量重新分组,饮用2.5%的DSS 5 d[10],每3天称一次体质量。后改用无菌水两周,在实验终点第26天处死小鼠。给予DSS当日开始LPS和S.algae灌胃干预,每两天灌胃一次,对照组予等量PBS溶液灌胃。LPS和S.algae灌胃浓度为0.1 mg/kg,S.algae灌胃浓度为1×106CFU/mL。
1.3.3 标本留取与HE染色 麻醉小鼠后暴露胸腔,注射器抽出心脏血液。暴露小鼠腹部,分离肛门处到回盲部的肠管,测量其长度,纵向剪开后收集粪便,冰PBS冲洗肠道后,于光学显微镜下,记录结直肠息肉数量、位置和大小,剪下息肉组织在10%福尔马林溶液中固定24 h,行HE染色,观察小鼠结直肠有无腺瘤形成。
1.3.4 实时荧光定量PCR(Real-time quantitative PCR,qRT-PCR) 用Trizol提取腺瘤组织中的总RNA,使用PrimeScriptTMRT reagent Kit说明书进行qRT-PCR,各引物序列均由上海生工公司设计。
1.3.5 免疫组化及评分标准 将小鼠肿瘤组织制成蜡块标本,行免疫组化(Immunohistochemistry,IHC)检测,每组至少3只。每张切片随机选取3个高倍镜视野,进行打分。阳性细胞评分标准:≤25%(1分),26% ~50%(2分),51% ~75%(3分),≥75%(4分)。着色强度评分标准:无色(0分),淡黄色(1分),棕黄色(2分),棕褐色(3分),最后将两者分数相加[11]。
1.3.6 Western blot法 用常规方法对蛋白提取液进行电泳及转膜[12]。结束后用Image J检测及定量条带强度。实验所用抗体:TLR4、p-IKKβ、p-IKBα、NF-κB、p-NF-κB。
1.3.7 细胞培养 100 ng/mL的PMA刺激THP-1细胞24 h,PBS洗涤两次,加入RPMI-1640培养基24 h,稳定细胞状态,即为M0巨噬细胞,再加入0.5 μg/mL的S.algae特异性LPS进行孵育48 h,将M0巨噬细胞极化为M1型巨噬细胞。共培养实验中,将THP-1细胞在Transwell小室的上层诱导并极化为M0巨噬细胞,在小室下层铺满Caco-2或HT29细胞,待贴壁后与M0巨噬细胞共培养,加入0.5 μg/mL E.coli LPS、S.algae LPS和等量PBS,共培养48 h。
1.3.8 流式检测巨噬细胞表型和细胞周期 用THP-1和S.algae LPS诱导出M0和M1巨噬细胞后,用CD11b、CD86和CD163抗体避光孵育30 min后,流式机上机检测。使用Cell Cycle Staining Kit测定细胞周期,流式细胞仪检测。
1.3.9 细胞增殖实验 细胞计数试剂盒-8(cell counting kit-8,CCK-8)检测细胞增殖能力。各组重复3次,分别添加10%CCK-8。2.5 h后,用酶标仪450 nm吸光度值测定光密度。
1.3.10 划痕实验 Transwell小室下层铺满单层的Caco-2和HT29后,用枪头笔直画一条直线,用PBS缓冲液洗涤3次。加入无血清培养基和LPS溶液,48 h后记录细胞迁移图像。
1.4 统计学方法 采用SPSS 22.0软件进行数据统计分析。计量资料若符合正态分布,则采用均数±标准差表示。采用独立样本t检验进行两两比较,采用单因素方差分析进行多组间比较,P<0.05认为有统计学意义。双变量之间的相关性采用Spearman相关性分析。
2 结果
2.1 体质量及息肉情况 与对照组相比,实验组小鼠在饮用DSS溶液后体质量均下降,AOM/DSS组和AOM/DSS+S.algae组小鼠在第14天体质量出现最低值,体质量分别降低约6.61%和9.08%。AOM/DSS+LPS组小鼠体质量出现更明显且更持续地降低,在第17天体质量出现最低值,体质量约降低16.98%(图1A)。与AOM/DSS组相比,LPS和S.algae干预的小鼠结直肠长度缩短(P<0.01;P>0.05)(图1B-C),息肉数量明显增加(P<0.000 1;P<0.05)(图1D-E,表1),且 >0.5 mm的息肉比例增加(图1F,表1)。

图1 小鼠体质量、结直肠长度及息肉情况Fig.1 Body weight,colorectal length,polyps of mice
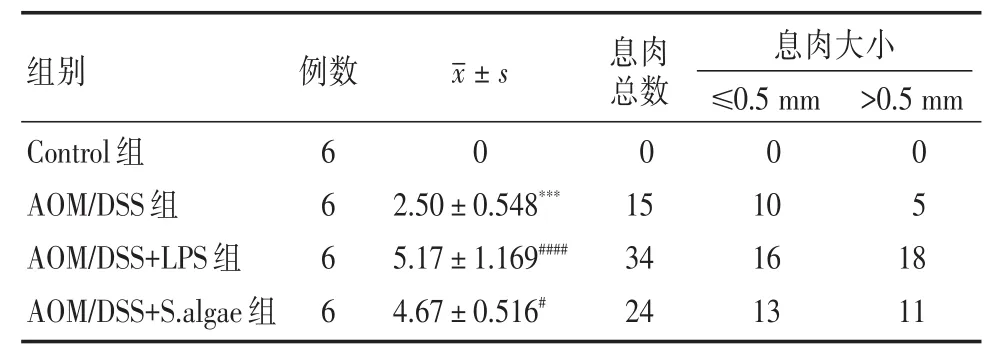
表1 各组小鼠结直肠息肉的计数情况Tab.1 Count of colorectal polyps in each group of mice
2.2 HE染色 对照组小鼠肠上皮粘膜完整,腺体排列整齐,细胞核位于基底部,隐窝完整。其余各组小鼠肠上皮腺体结构紊乱,隐窝增大,胞核拉长,出现轻至重度不典型增生。固有层见大量中性粒细胞浸润。其中,AOM/DSS组小鼠结直肠上皮呈现轻度不典型增生,S.algae及其特异性LPS干预后结直肠上皮腺体结构更为紊乱,细胞异型性更为明显,呈现重度不典型增生(图2)。

图2 各组小鼠结直肠息肉的HE染色图(放大倍数为100×,200×)Fig.2 The HE staining of colorectal polyps in mice of each group(100×,200× magnification)
2.3 巨噬细胞水平改变 qRT PCR结果显示(图3),与AOM/DSS组相比,LPS和S.algae干预后CD11b和CD86 mRNA表达均升高(P<0.000 1;P<0.000 1;P<0.000 1;P<0.01)。CD163在各组小鼠中均有少量表达,未见明显改变。IHC结果显示,与AOM/DSS组相比,LPS和S.algae干预后CD11b和CD86表达均升高(P<0.000 1,图3)。说明S.algae及其LPS灌胃可以增加M1巨噬细胞,但M2巨噬细胞改变不明显。

图3 各组小鼠CD11b、CD86、CD163的mRNA及蛋白质水平Fig.3 The mRNA and protein levels of CD11b,CD86,and CD163 in mice of each group
2.4 增殖和周期情况 IHC结果显示(图4),与AOM/DSS组相比,LPS和S.algae干预后,Ki-67、PCNA、Cyclin D1蛋白的表达量均明显升高(P<0.000 1)。说明S.algae及其LPS均可以促进小鼠腺瘤细胞的增殖和周期蛋白表达。

图4 各组小鼠Ki-67、PCNA和Cyclin D1的蛋白质水平Fig.4 The mRNA and protein levels of Ki-67,PCNA and Cyclin D1 in mice of each group
2.5 相关性分析 将IHC评分结果与各组小鼠息肉数量做Spearman相关性分析(表2)。结果显示,CD11b、CD86、Ki-67、PCNA、Cyclin D1和小鼠结直肠息肉数量呈正相关(P=0.008;P=0.018;P=0.028;P=0.003;P=0.024),CD163与小鼠结直肠息肉数量未见明显相关性(P=0.198)。

表2 免疫组化指标与息肉数量的相关性分析Tab.2 Spearman correlation analysis of immunohistochemical indexes and the number of polyps
2.6 炎症微环境的改变 ELISA结果显示,与AOM/DSS组相比,LPS和S.algae干预后,观察到血清IL-1β、IL-6、TNF-α水平均升高(P<0.05),LPS也升高(P<0.001,图5A-D)。
qRT PCR结果显示,与AOM/DSS组相比,LPS干预后IL-1β、TNF-α、iNOS mRNA水平升高(P<0.0001),IL-6、IL-23 mRNA水平均升高(P<0.001;P<0.01)(图5E-I)。S.algae干预后IL-1β、TNF-α mRNA水平升高(P<0.0001)、IL-6、IL-23 mRNA水平升高(P<0.05;P<0.01),iNOS mRNA水平未见明显改变(图5E-I)。

图5 小鼠腺瘤组织中炎症因子和LPS的表达情况Fig.5 Expression of inflammatory factors and LPS in adenoma tissues of mice in each group
2.7 TLR4/NF-κB通路蛋白的表达情况 Western Blot结果显示,与AOM/DSS组相比,LPS干预后小鼠TLR4、p-IKKβ、p-IkBα和p-NF-κB蛋白的表达量明显增加(P<0.01;P<0.05;P<0.01;P<0.05),NF-κB的蛋白表达量未见明显改变(图6)。S.algae干预后小鼠TLR4、p-IKKβ、p-IkBα和p-NF-κB蛋白的表达量明显增加(P<0.05),NF-κB的蛋白表达量未见明显改变(图6)。
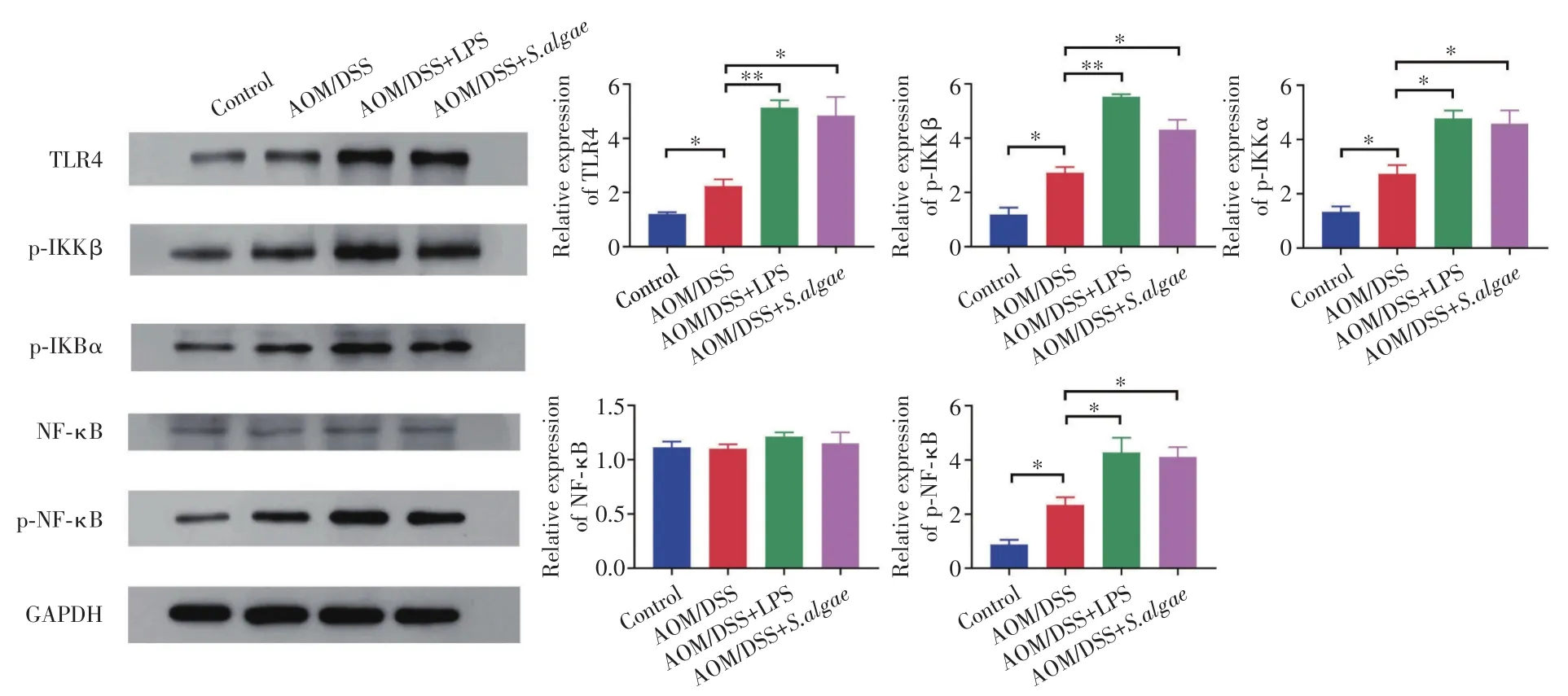
图6 小鼠腺瘤组织中TLR4/NF-κB通路蛋白表达情况Fig.6 Expression of TLR4/NF-κB pathway proteins in adenomas tissue of mice
2.8 THP-1诱导为M1巨噬细胞 分别用不同浓度的S.algae LPS刺激M0巨噬细胞48 h,然后采用qRT-PCR检测不同浓度刺激下,IL-6和iNOS的mRNA水平,以评估S.algae LPS诱导巨噬细胞炎症的最适浓度。见图7,当S.algae LPS浓度为0.5μg/mL时,促炎因子IL-6和iNOS mRNA的表达量最高,差异有统计学意义(P<0.001;P<0.01)。采用0.5 μg/mL S.algae LPS诱导极化后,M1巨噬细胞比例由7.00%到41.40%,差异有统计学意义,M2巨噬细胞比例由2.30%到2.39%,差异无统计学意义。说明该方案诱导后,M1型巨噬细胞的比例明显增加,M2巨噬细胞比例未见明显改变(图8)。

图7 S.algae LPS的最适浓度Fig.7 Optimal concentration of S.algae LPS

图8 细胞流式分析结果Fig.8 Results of cell flow analysis
2.9 S.algae LPS对M0巨噬细胞增殖的影响 用0.5 μg/mL的 S.algae LPS和 E.coli LPS刺激 M0巨噬细胞,用等量PBS缓冲液做阴性对照,48 h后CCK-8法显示S.algae LPS可以明显促进M0巨噬细胞的增殖(图9A)。
2.10 S.algae LPS和M0巨噬细胞对结直肠肿瘤细胞增殖和周期的影响 Caco-2或HT-29与M0巨噬细胞共培养后,其增殖能力增加(图9B-C)。与PBS组相比,用S.algae LPS和E.coli LPS刺激可以更明显地促进结肠肿瘤细胞的增殖和迁移(图9B-C,表3),且G1期细胞百分比降低,S期升高,G2期较稳定,未出现明显变化(图9D-E、表3)。提示S.algae LPS可能促进细胞从G1期进入S期,从而促进细胞增殖。
表3 划痕实验显示各组细胞在不同干预下48 h后的迁移率Tab.3 The migration rate of cells under different interventions after 48h in each group was shown by scratch experiment ±s

表3 划痕实验显示各组细胞在不同干预下48 h后的迁移率Tab.3 The migration rate of cells under different interventions after 48h in each group was shown by scratch experiment ±s
注:*表示与Caco-2组相比的P值;#表示与HT29组相比的P值;***P<0.001;****P<0.0001;###P<0.05;####P<0.0001
PBS(%)E.coli LPS(%)S.algae LPS(%)Caco-2 17.853±1.397 30.478±1.033 30.819±1.565 Caco-2+M0 29.078±0.657***49.396±1.997***64.201±0.892****HT29 5.437±1.726 13.543±0.400 20.325±2.005 HT29+M0 20.692±0.532###32.414±1.723####42.109±1.317####

图9 S.algae特异性LPS和M0巨噬细胞对Caco-2和HT29细胞的增殖和周期影响Fig.9 The effects of S.algae specific LPS and M0 macrophages on proliferation and cycle of Caco-2 and HT29 cells
3 讨论
有学者在小鼠结肠腔内通过灌肠给予E.coli LPS,导致局部细胞炎症因子发生改变,这表明结肠内的E.coli LPS水平升高会引起肠道炎症[13]。近年来,学者们在CRA和CRC患者的血液和肿瘤组织中都观察到了LPS的升高[14]。高血清LPS水平的患者更有可能发展为CRA,且与结肠息肉的数量以及肠内炎性细胞因子的水平都呈现正相关[15]。
本研究中通过S.algae LPS灌胃后,小鼠结直肠的息肉数量和>0.5 mm的息肉比例明显增加,并且加重腺瘤组织的不典型增生。通过qRT PCR和IHC,还检测到S.algae LPS可以提高腺瘤中M1巨噬细胞的水平,且与小鼠息肉数量成正相关,但未改变M2巨噬细胞水平。这些结果说明本实验中小鼠腺瘤组织中主要以M1巨噬细胞为主,这与CHANMEE、CHENG和GUTTING等[16-18]研究一致。S.algae LPS干预还可以改变小鼠的肿瘤炎性微环境,促使肿瘤细胞的增殖和周期蛋白的表达。通过Spearman相关性分析证实细胞的增殖和周期蛋白的表达与息肉数量呈正相关。在体外,选取高分化的结直肠肿瘤细胞Caco-2和中分化的HT29细胞进行验证,发现S.algae LPS可以促进更多细胞从G1期进入S期,加快细胞周期,促进结直肠肿瘤细胞的增殖和迁移能力,使腺瘤向腺癌发生转变。
本实验中S.algae LPS对TLR4/NF-κB通路同样具有激活作用。肠道中富含LPS的细菌过多可能会提供有利于慢性炎症并增加促炎性细胞因子和活性氧产生的环境,这些细胞因子可以激活NF-κB途径,并促进细胞增殖和DNA损伤,导致癌变[19]。LPS通过LPS结合蛋白(lipopolysaccharide binding protein,LBP)运输到巨噬细胞膜上,与mCD14结合[19]。LPS被解离成单体后,活性激活,暴露出内部结构,可以使TLR4-MD-2复合物识别并结合。随后该复合物发生的二聚化引起构象改变,将信号传递给下游的MyD88,进而IKK-β和IkB-α发生磷酸化,促使NF-κB磷酸化后易位到细胞核中[19]。
LPS性质极其稳定,与细菌灌胃相比,采用LPS灌胃既可以减少人体消化液对细菌的损伤,又可以避免细菌对肠道菌群的直接干扰作用。以往学者们多将E.coli LPS以腹腔注射的形式,用于内毒素血症的研究[20],而在本实验中,通过比较S.algae及其LPS的灌胃处理,首次证明了S.algae LPS灌胃干预CRA的可行性,并且较S.algae灌胃有更大的优势。SONG等通过纳米颗粒,特异性地阻断了肿瘤组织内的LPS,改善了肿瘤的免疫抑制微环境,甚至减轻了CRC的肝转移[21]。但并非所有的革兰氏阴性细菌均为人体有害菌,未来我们或许可以运用纳米颗粒技术,靶向清除S.algae特异性LPS,进一步研究其对CRA产生的影响,或许可为CRA防治提供新思路。
