壳聚糖基复合膜的合成及对蛋白质吸附能力的对比研究
2021-12-31刘佳鑫汤琦龙赵珺刘梦林李瑞雪
刘佳鑫,汤琦龙,赵珺*,刘梦林,李瑞雪
长春大学食品科学与工程学院(长春 130022)
民以食为天,近年来食品工业迅速发展,随之而来的食品加工废水排放量也日益加大,例如生产加工豆制品时会排放大量高浓度有机废水,马铃薯加工淀粉过程中同样也会产生大量有机废水,这类废水中含有大量蛋白质,长期排放会造成水体污染和富营养化等,而且食品废水中的蛋白质还能为许多藻类和浮游类生物提供生长能源,引起藻类大量繁殖,水体溶氧量下降,水质恶化,导致鱼类和其他水中生物大量死亡[1-3]。目前,去除食品加工废水中蛋白质的常用方法有蒙脱土吸附法、等电点沉淀法、自然沉淀法、泡沫分离法、超滤法等[4-5],但这些方法存在操作复杂、成本高、处理效率低、耗时长等问题。由于壳聚糖具有吸附作用且不会造成二次污染,近年来,常被用于处理含阴离子[6]、蛋白质、染料和重金属离子[7-10]等生活和工业废水。
壳聚糖是一种天然的生物高分子聚合物,由甲壳素脱乙酰基而产生,在自然界大量存在,具有天然、无毒、易溶于水、对人体健康和自然环境无损害等特性[11-13]。在水处理中对蛋白质等有机物有很强的絮凝作用,可用来回收食品加工废水中的蛋白质,但壳聚糖的抗水性差,用它制成的膜在酸性溶剂中很容易被溶解[14];可溶性淀粉空间构象卷曲成螺旋形,具有近似纤维的性能,用它制成的薄膜,具有良好的透明度、柔韧性、抗张强度和水不溶性;竣甲基纤维素是纤维素通过羧甲基化改性后的产物,具有良好的成膜性、生物降解性和低毒性等特点,且亲水性强,内部网络结构稳定,能很好地增强复合膜性能[15-16]。
壳聚糖、淀粉和羧甲基纤维素安全、无毒,在水处理过程中对环境无污染,因此分别将可溶性淀粉和羧甲基纤维素交联至壳聚糖分子链上,得到壳聚糖/淀粉复合膜和壳聚糖/羧甲基纤维素复合膜,用以处理废水中的蛋白质,以降低废水中蛋白质的含量,使水资源得到净化,综合开发利用,实现环境经济双赢[17]。
1 材料和方法
1.1 主要材料与试剂
可溶性淀粉,天津市风船化学试剂科技有限公司;羧甲基纤维素钠,国药集团化学试剂有限公司;壳聚糖(脱乙酰度80.0%~95.0%),国药集团化学试剂有限公司;戊二醛,天津市光复精细化工研究所;丙三醇、柠檬酸,北京化工厂;牛血清白蛋白,美伦生物;蒸馏水、氢氧化钠、丙三醇、柠檬酸,均为分析纯。
1.2 主要设备与仪器
HH-ZK1恒温水浴锅(巩义市予华仪器有限责任公司);AM-3250A磁力搅拌恒温器(上海硕光电子科技有限公司);JJ-1BA搅拌器(常州润华电器有限公司);GFL-230鼓风干燥箱(天津市莱玻特瑞仪器设备有限公司);AUW120电子天平(日本岛津仪器有限责任公司);JW-1048低速离心机(安徽嘉文仪器装备有限公司);NTS-4000B恒温震荡水槽(日本东京理化械株式会社);Nicolet iS5傅里叶红外光谱仪(日本岛津仪器有限责任公司);PHS-3C pH计(上海仪电科学仪器股份有限公司);JSM-6510LA扫描电镜(日本电子株式会社)。
1.3 试验方法
1.3.1 壳聚糖基复合膜的制备
称取2份0.6 g壳聚糖分别溶解于20 mL 2%乙酸溶液中,再分别称取不同质量的淀粉和羧甲基纤维素钠分别溶于20 mL蒸馏水中,待完全溶解后,分别将两种溶液倒入烧杯中混匀,再向烧杯中缓慢滴加0.1 g甘油,放入水浴磁力搅拌锅中,在一定温度下搅拌10 min,再缓慢滴加2 mL 0.25%的戊二醛溶液,恒温搅拌1 h,待反应结束后离心,取25 g上清液,采用流延法铺平,放入50 ℃烘箱中烘至恒重,然后将所得的膜用30 mL一定浓度的氢氧化钠溶液浸泡1 h,浸泡完用蒸馏水冲洗干净,放入50 ℃烘箱恒温烘干[18-19],即得壳聚糖/淀粉复合膜和壳聚糖/羧甲基纤维素复合膜。
1.3.2 FT-IR表征
分别将壳聚糖膜、壳聚糖/淀粉复合膜和壳聚糖/羧甲基纤维素复合膜分别剪成细小的片状,加入溴化钾、研磨、制片,放于红外扫描槽内进行扫描[20]。
1.3.3 SEM表征
分别将壳聚糖膜、壳聚糖/淀粉复合膜和壳聚糖/羧甲基纤维素复合膜进行喷金处理,在1 000倍放大倍数下观察其形貌[21]。
1.3.4 拉伸强度的测定
选择平整、无破损、整洁的壳聚糖膜、壳聚糖/淀粉复合膜样品和壳聚糖/羧甲基纤维素复合膜,裁成长30 mm、宽10 mm的长条状,用质构仪夹持探头平整垂直地固定夹紧膜样品。参数设置:返回距离60 mm,速度300 mm/min,触发力5 N,有效拉伸距离80 mm。当膜试样条中间断裂时,记录最大拉力。每个膜样品做平行测定3次,最终取其平均值[22]。拉伸强度按式(1)计算。

式中:Ts为拉伸强度,MPa;F为断裂时最大拉力,N;S为试样的截面积(宽度×厚度),m2。
1.3.5 溶胀度的测定
取干燥后的膜样品,剪成30 mm×10 mm的长条状,称定膜的质量M,然后在去离子水中浸泡24 h,使其充分溶胀,然后用滤纸快速地吸除膜样品表面的水分,称定膜的质量M0,平行测量3次,取其算术平均值[23]。溶胀度(Sd)按式(2)计算。

1.3.6 吸附对比试验
1.3.6.1 蛋白质标准曲线的制作
采用考马斯亮蓝法测定废水中蛋白质的质量浓度,首先绘制标准曲线如图1所示。
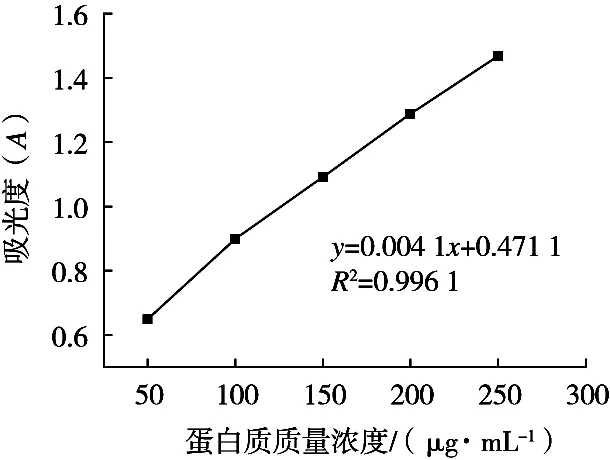
图1 蛋白质标准曲线
1.3.6.2 吸附量和吸附率的测定
将进行吸附操作的蛋白溶液在100 r/min转速下25 ℃恒温振荡2 h,离心并取上清液测定吸光度,通过蛋白质质量浓度标准曲线方程计算上清液的质量浓度Ct值,并按式(3)和(4)计算蛋白质的吸附率和吸附量。
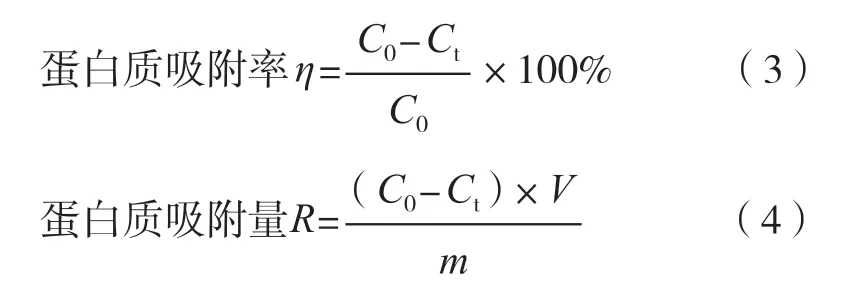
式中:C0为蛋白初始质量浓度,μg·mL-1;Ct为恒温振荡2 h后蛋白质量浓度,μg·mL-1;V为蛋白质溶液的体积,mL;m为吸附时所用复合膜的质量,g。
对比研究最佳制备条件下壳聚糖/淀粉复合膜和壳聚糖/羧甲基纤维素复合膜对蛋白质吸附效率。
2 结果与分析
2.1 FT-IR结果与分析
采用FT-IR对壳聚糖膜、壳聚糖/淀粉复合膜和壳聚糖/羧甲基纤维素复合膜进行结构表征,其结果如图2所示。

图2 壳聚糖膜、壳聚糖/淀粉复合膜和壳聚糖/羧甲基纤维素复合膜FT-IR图
由图2可知,a图中3 448 cm-1是壳聚糖膜的—OH的伸缩振动吸收峰,2 918 cm-1和2 862 cm-1处是壳聚糖膜的—CH3和—CH的伸缩振动峰,1 634 cm-1是CO—NH—振动峰;3 423 cm-1是壳聚糖/淀粉复合膜的—OH的伸缩振动吸收峰,2 918 cm-1和2 830 cm-1处是壳聚糖/淀粉复合膜的—CH3和—CH的伸缩振动峰。此外,壳聚糖/淀粉复合膜在1 626 cm-1处CO—NH—振动峰比壳聚糖膜在该波数附近的振动峰更强,这是由于复合膜中淀粉和壳聚糖均在该波数附近存在此振动峰,壳聚糖与淀粉之间强烈的相互作用使溶液中的分子发生重排,并使各组分之间有更好的相容性,因此可推断合成了壳聚糖/淀粉复合膜。b图中,壳聚糖膜和壳聚糖/羧甲基纤维素复合膜的红外吸收光谱图大体相似,3 448 cm-1是壳聚糖膜的—OH的伸缩振动吸收峰,2 918 cm-1和2 862 cm-1处是壳聚糖膜的—CH3和—CH的伸缩振动峰,1 634 cm-1是CO—NH—振动峰;壳聚糖/羧甲基纤维素复合膜对应的特征吸收峰向低波数发生了不同程度的偏移,3 432 cm-1是壳聚糖/羧甲基纤维素复合膜的—OH的伸缩振动吸收峰,2 902 cm-1和2 854 cm-1处是壳聚糖/纤维素复合膜的—CH3和—CH的伸缩振动峰,1 626 cm-1是CO—NH—振动峰,这是因为壳聚糖和羧甲基纤维素分子间生成氢键,产生了强烈的相互作用,因此可推断合成了壳聚糖/羧甲基纤维素复合膜。
2.2 SEM结果与分析
采用SEM对壳聚糖膜、壳聚糖/淀粉复合膜和壳聚糖/羧甲基纤维素复合膜进行样品形貌的分析,其结果如图3所示。
由图3可知,a为壳聚糖膜,表面光滑较少褶皱;b为壳聚糖/淀粉复合膜,其表面较壳聚糖膜粗糙,并附有多颗粒状淀粉,说明淀粉颗粒复合到壳聚糖膜表面合成了壳聚糖/淀粉复合膜;c为壳聚糖/羧甲基纤维素复合膜,表面粗糙细密,比表面积大,说明羧甲基纤维素附着在壳聚糖膜表面,并有利于吸附。

图3 壳聚糖膜、壳聚糖/淀粉复合膜和壳聚糖/羧甲基纤维素复合膜SEM图
2.3 拉伸强度结果与分析
如表1和图4所示,壳聚糖膜的拉伸强度为2 179.49 MPa、壳聚糖/淀粉复合膜为1 824.43 MPa、壳聚糖/羧甲基纤维素复合膜为3 490.14 MPa。这是因为加入淀粉后,其羟基与壳聚糖的基团相互作用,从而减少了壳聚糖分子间的氢键,使得壳聚糖分子结构排列杂乱无序,降低了壳聚糖/淀粉复合膜的拉伸强度,但无序的结构使得复合膜具有更多孔隙,增加了壳聚糖/淀粉复合膜的吸附能力;而壳聚糖/羧甲基纤维素复合膜的拉伸强度大于壳聚糖膜这是因为羧甲基纤维素同壳聚糖一样具有成膜性并且自身具有稳定的网状结构,因此同壳聚糖复合后会增加膜的拉伸强度,这将增加在废水处理过程时膜的耐受程度。
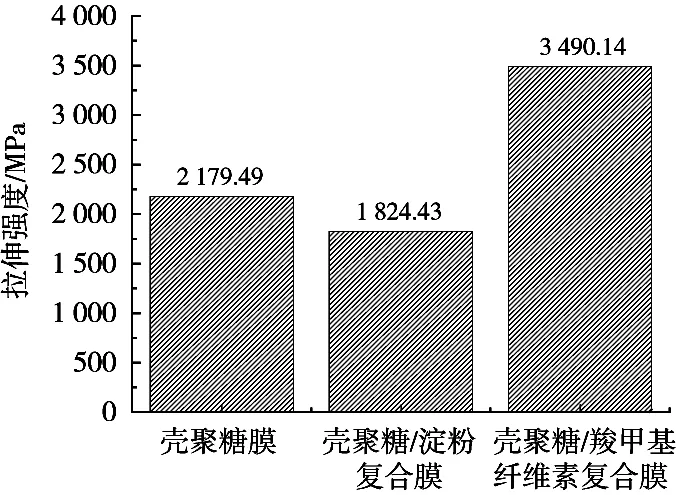
图4 壳聚糖膜、壳聚糖/淀粉复合膜和壳聚糖/羧甲基纤维素复合膜拉伸强度对比图

表1 壳聚糖膜、壳聚糖/淀粉复合膜和壳聚糖/羧甲基纤维素复合膜的拉伸强度基本数据
2.4 溶胀度
由表2可以看出壳聚糖/淀粉复合膜和壳聚糖/羧甲基纤维素复合膜的溶胀度低于壳聚糖膜的溶胀度,这是由于交联剂戊二醛、淀粉和纤维素的引入,使壳聚糖/淀粉复合膜和壳聚糖/羧甲基纤维素复合膜交联度增大,溶胀平衡作用提高,增强了复合膜的稳定性,方便了复合膜在吸附后的回收再利用。
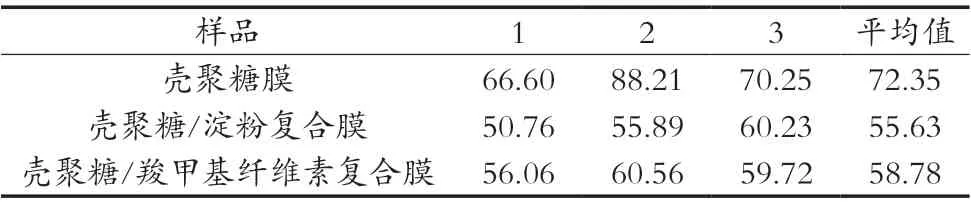
表2 壳聚糖膜、壳聚糖/淀粉复合膜的溶胀度
2.5 壳聚糖/淀粉复合膜和壳聚糖/羧甲基纤维素复合膜对蛋白质的吸附能力
根据试验可知:当壳聚糖与淀粉质量比为3∶5、制备温度为40 ℃、浸泡膜的NaOH浓度为4%、蛋白样液稀释倍数为1.0倍、废水pH为9时,所得到复合膜对蛋白质吸附率和吸附量达到最大;当壳聚糖与羧甲基纤维素质量比为3∶4、温度为50 ℃、NaOH为浓度4%、稀释倍数为2倍、pH为4时,所得到复合膜对蛋白的吸附率与吸附量最大。如图5所示,在最佳条件下壳聚糖/淀粉复合膜对蛋白质吸附率和吸附量分别为46.04%和9.56 mg/g,壳聚糖/羧甲基纤维素复合膜对蛋白质吸附率和吸附量分别为26%和2.81 mg/g,这是由于壳聚糖和淀粉对废水中蛋白质起协同作用,增强了吸附效率,但羧甲基纤维素呈负电性,壳聚糖在弱酸性条件下成正电性,对于大多数呈现负电性的蛋白质废水吸附效率减弱,因此壳聚糖/淀粉复合膜对蛋白质吸效率要高于壳聚糖/羧甲基纤维素复合膜。

图5 壳聚糖膜、壳聚糖/淀粉复合膜和壳聚糖/羧甲基纤维素复合膜吸附能力对比图
3 结论与讨论
通过FT-IR和SEM表征得出壳聚糖同淀粉和羧甲基纤维素分别合成了壳聚糖/淀粉复合膜和壳聚糖/羧甲基纤维素复合膜。对膜样品进行拉伸性能、溶胀度测试,其结果较单一壳聚糖膜具有更高稳定性,利于吸附后回收。在最佳条件下壳聚糖/淀粉复合膜和壳聚糖/羧甲基纤维素复合膜对蛋白质进行吸附效率对比,得出壳聚糖/淀粉复合膜对蛋白质的吸附效率高于壳聚糖/羧甲基纤维素复合膜。由于壳聚糖、淀粉和羧甲基纤维素安全无毒,用来处理废水不会对环境造成二次污染,因此对含蛋白食品工业废水的处理具有极其重要的现实意义。
