司来吉兰治疗帕金森病有效性及安全性的系统评价再评价
2021-12-30李佳芮李燕飞刘泽辉易湛苗
李佳芮 李燕飞 刘泽辉 易湛苗





中圖分类号 R971+.5 文献标志码 A 文章编号 1001-0408(2021)24-3031-08
DOI 10.6039/j.issn.1001-0408.2021.24.15
摘 要 目的:对司来吉兰治疗帕金森病(PD)有效性和安全性的系统评价/Meta分析进行再评价。方法:计算机检索PubMed、Embase、Cochrane图书馆、中国知网、万方数据等数据库以及国内外卫生技术评估机构官方网站,在手工检索、回顾参考文献的基础上,收集司来吉兰单药或联合其他抗PD药物(试验组)对比安慰剂或空白对照或其他抗PD药物(对照组)的系统评价/Meta分析,检索时限均为建库起至2020年11月。筛选文献并提取资料后,采用PRISMA声明评价纳入文献的报告质量,采用AMSTAR 2量表评价纳入文献的方法学质量,采用GRADE方法评价纳入文献结局指标的证据质量并进行汇总分析。结果:共纳入12篇系统评价/Meta分析,其中4篇为系统评价、8篇为Meta分析,共包括31个结局指标。PRISMA评分为16.5~27.0分,其中2篇文献(16.67%)为15.0~21.0分、10篇(83.33%)为22.0~27.0分。AMSTAR 2量表评价结果显示,2篇文献的方法学质量等级为高质量,3篇为低质量,7篇为极低质量。GRADE证据质量评价结果显示,高质量指标1个,中质量指标3个,低质量指标5个,极低质量指标21个,不可评价结局指标1个;导致降级的因素主要为偏倚风险(87.10%)、发表偏倚(77.42%)、不精确性(51.61%)和不一致性(41.94%)。在疗效方面,与对照组比较,无论是单用或联合其他抗PD药物,司来吉兰均可改善患者的统一帕金森病评分量表总评分,精神、行为和情绪评分,日常生活能力评分,运动评分和韦氏综合评定量表评分(P<0.05)。在安全性方面,两组患者的不良事件发生率、病死率比较,差异均无统计学意义(P>0.05),但使用司来吉兰患者的因不良事件退出率更高(P<0.05)。结论:司来吉兰治疗PD的疗效和安全性均较好,但目前相关系统评价/Meta分析的方法学质量和证据质量均偏低,需进一步规范研究方法。
关键词 司来吉兰;帕金森病;系统评价再评价;有效性;安全性
Efficacy and Safety of Selegiline for Parkinson’s Disease: A Reevaluation of Systematic Reviews
LI Jiarui1,2,LI Yanfei1,3,LIU Zehui1,4,YI Zhanmiao1,5(1. Dept. of Pharmacy, Peking University Third Hospital, Beijing 100191, China; 2. Dept. of Pharmacy, Beijing Northern Hospital of Weaponry Industry/Northern Section of Peking University Third Hospital, Beijing 100089, China; 3. Dept. of Pharmacy, the First Hospital of Changsha, Changsha 410005, China; 4. Dept. of Pharmacy, China Aerospace Center Hospital, Beijing 100049, China; 5. Center for Drug Evaluation, Peking University Health Science Center, Beijing 100191, China)
ABSTRACT OBJECTIVE: To conduct reevaluation of systematic review/Meta-analysis on the efficacy and safety of selegiline in the treatment of Parkinson’s disease (PD). METHODS: Retrieved from PubMed, Embase, Cochrane Library, CNKI, Wanfang database as well as official websites of domestic and foreign health technology assessment institutions, based on manual retrieval and review of references, systematic review/Meta-analysis on selegiline alone or combined with other anti-PD drugs (trial group) versus placebo or blank control or other anti-PD drugs (control group) were collected. The time limit was from database inception to November 2020. After literature screening and data extraction, PRISMA statement was adopted to evaluate the quality of the included reports. AMSTAR 2 scale was used to evaluate the methodological quality, and GRADE method was adopted to evaluate the evidence quality, the outcome indicators of the included studies were summarised and analyzed. RESULTS: A total of 12 systematic reviews/Meta-analysis were included, involving 4 systematic reviews and 8 Meta-analysis; there were 31 outcome indexes in total. PRISMA scores of them ranged from 16.5 to 27.0, including 15.0 to 21.0 for 2 literatures (16.67%) and 22.0 to 27.0 for 10 literatures (83.33%). Results of AMSTAR 2 scale showed that the methodological qualities of 2 literatures were classed as high quality, 3 as low quality and 7 as very low quality. Results of GRADE evidence quality evaluation showed that 1 evidence quality was high-level, 3 were medium-level, 5 were low-level, 21 were very low-level, and 1 was no evaluable. The main factors leading to the degradation were bias risk (87.10%), publication bias (77.42%), inaccuracy (51.61%) and inconsistency (41.94%). In terms of therapeutic efficacy, compared with control group, selegiline could improve the total score of UPDRS, UPDRS Ⅰ score, UPDRS Ⅱ score, UPDRS Ⅲ score and Webster score in patients with Parkinson’s disease, either monotherapy or in combination with other anti-PD drugs (P<0.05). In terms of safety, there was no significant difference in the incidence of adverse events or mortality between 2 groups (P>0.05), but the rate of withdrawal due to adverse events was higher (P<0.05). CONCLUSIONS: Selegiline is effective and safe in the treatment of Parkinson’s disease, but current methodological quality and evidence quality of included systematic reviews/Meta-analysis are low, which requires further standardization of research methods.
KEYWORDS Selegiline; Parkinson’s disease; Reevaluation of systematic review; Efficacy; Safety
基金项目:国家自然科学基金资助项目(No.72104003);国家重点研发计划课题(No.2020YFC2008305)
主管药师,硕士。研究方向:药理学。电话:010-68966677- 8227。E-mail:lijiaruihappy@126.com
通信作者:副主任药师,副教授,博士。研究方向:临床药学。电话:010-82265740。E-mail:yzm@bjmu.edu.cn
帕金森病(Parkinson’s disease,PD)是最常见的神经退行性疾病之一,以纹状体多巴胺减少和黑质多巴胺能神经元变性为特征,好发于40~70岁人群,以60岁左右为发病高峰,其传统药物治疗方案是基于多巴胺的替代治疗[1]。左旋多巴是治疗PD最有效的药物,但长期使用会导致运动并发症,包括症状波动和异动症[2]。随着疾病的进展和左旋多巴使用时间的延长,上述不良反应的发生率也随之增加,严重影响了患者的生活质量[3]。新的抗PD药物不断被研发与应用,如多巴胺受体激动剂(dopamine agonists,DAs)、单胺氧化酶B型抑制剂(monoamine oxidase type B inhibitor,MAO-BI)和儿茶酚-O-甲基转移酶抑制剂(catechol-O-methyltransferase inhibitor,COMTI)[4]。虽然,最新的《中国帕金森病治疗指南(第4版)》规定了PD治疗药物的选择流程及治疗方案,但并未明确各类药物的证据级别及推荐强度[5]。
司来吉兰为MAO-BI,可选择性地抑制中枢神经系统中的单胺氧化酶B型(monoamine oxidase type B,MAO-B),减少脑内多巴胺的降解代谢,增加多巴胺的蓄积;同时,其可减少突触前膜对多巴胺的再摄取,促进多巴胺的释放,从而延长PD患者的生存期,改善长期使用左旋多巴所致的症状波动现象[6]。目前,国内外虽然已有针对司来吉兰治疗PD的系统评价/Meta分析的文献发表[7-8],但这些研究的结局指标存在差异,其方法的质量和证据的可靠性亦不明确。
系统评价再评价是对同一健康或同一疾病问题相关系统评价进行再评价的一种方法,可以提供更为整合的可靠证据[9]。证据推荐分级的评估、制订与评价(The Grading of Recommendations Assessment,Development and Evaluation,GRADE)工作组推荐系统评价研究者应用GRADE方法从结局指标层面进行证据质量评价[10]。若纳入的系统评价本身已进行了证据质量评价,则应该对评价结果谨慎评估以确保原评价结果的正确性;若未进行质量评价,则应依据GRADE方法进行评价[11]。基于此,本研究对司来吉兰治疗PD的系统评价/Meta分析的报告、方法学和证据质量进行再评价,以期通过证据的整合来提示后续临床研究的改进方向,为司来吉兰的指南更新和临床应用提供循证证据。
1 资料与方法
1.1 纳入与排除标准
1.1.1 研究类型 本研究纳入的文献为基于随机对照试验(randomized controlled trial,RCT)或临床对照试验的系统评价/Meta分析;语种限定为中文和英文。
1.1.2 研究对象 研究对象为符合《英国脑库帕金森病诊断标准》[12]、《原发性帕金森病的诊断标准(2005年)》[13]相关诊断标准的PD患者。患者的性别、年龄、发病时间、种族等均不限。
1.1.3 干预措施 试验组患者给予司来吉兰单药或联合其他抗PD药物治疗,对照组患者给予安慰剂或空白对照或其他抗PD药物治疗。
1.1.4 结局指标 本研究的疗效指标包括统一帕金森病评分量表(unified Parkinson’s disease rating scale,UPDRS)总评分,精神、行为和情绪评分(UPDRS Ⅰ),日常生活能力评分(UPDRS Ⅱ),运动评分(UPDRS Ⅲ),韦氏综合评定量表(Webster)评分;安全性指标包括不良事件发生率、因不良事件退出率、病死率。
1.1.5 排除标准 本研究的排除标准为:①重复发表的系统评价;②单个病例报告、作用机制探讨文献;③未对纳入研究进行定量分析的文献;④数据不完全或无法获取原文的文献;⑤给编辑的信或评论;⑥网状Meta分析。
1.2 文獻检索策略
计算机检索PubMed、Embase、Cochrane 图书馆、中国知网、万方数据等数据库以及国内外卫生技术评估机构官方网站,同时手工检索、回顾参考文献,并追溯纳入文献的参考文献作为检索补充。中文检索词包括“司来吉兰”“帕金森病”,英文检索词包括“selegiline”“Parkinson”。检索时限均为各数据库建库起至2020年11月。检索方式以主题词与自由词相结合为主,根据各数据库的特征选择相匹配的检索策略(以Embase为例,具体检索策略见表1)。利用NoteExpress 3.2软件管理文献资料。
1.3 文献筛选与资料提取
由2位经过系统评价/Meta分析训练的研究者独立按照文献检索策略初步获取文献并交叉核对,从题目、摘要、干预措施和结局指标判断是否纳入;若遇分歧,则与第3位研究者协商决定。对于缺失的资料,尽量与作者联系予以补充。提取资料包括第一作者、发表(或更新)年份、第一作者国籍、纳入原始文献数量、患者例数、干预措施、质量评价工具、结局指标等。
1.4 文献质量评价
1.4.1 报告质量评价 采用PRISMA声明评价纳入文献的报告质量,该声明共有 27 个条目,具体条目参考文献[14]。评分标准为:单条目完整报告计1分,部分报告计0.5分,未报告计0分。<15.0分为报告有相对严重的信息缺失,为低质量;15.0~21.0分为报告有一定缺失,为中等质量;22.0~27.0分为报告相对完整,为高质量[14]。
1.4.2 方法学质量评价 采用AMSTAR 2量表评价纳入文献的方法学质量,共包括16个条目,其中条目1表示研究问题和纳入标准是否包括PICO(P为研究对象,I为干预措施,C为对照措施,O为结局);条目2表示是否报告系统评价研究方法在实施前就已确定,是否有报告与计划书不一致的情况;条目3表示作者是否解释了选择系统评价纳入研究设计类型的原因;条目4表示作者是否使用了全面的文献检索策略;条目5表示是否由两人独立完成文献筛选;条目6表示是否由两人独立完成数据提取;条目7表示是否提供了排除文献的清单及排除理由;条目8表示作者是否足够详细地描述了纳入研究的基本特征;条目9表示作者是否使用合理工具评估了纳入研究的偏倚风险;条目10表示作者是否报告了该系统评价纳入研究的资金来源;条目11表示如进行了Meta分析,作者是否使用了适当的统计学方法进行结果合并分析;条目12表示如果进行了Meta分析,作者是否考虑了纳入研究的偏倚风险对Meta分析或其他证据整合的潜在影响;条目13表示在解释/讨论系统评价结果时,作者是否考虑了纳入研究的偏倚风险;条目14表示作者是否对系统评价结果的异质性给予了满意的解释/讨论;条目15表示如果进行定量合成,作者是否充分调查了发表偏倚,并讨论了其对研究结果的可能影响;条目16表示作者是否报告了任何潜在的利益冲突,包括开展系统评价所接受的任何资助。其中,条目2、4、7、9、11、13、15为关键条目,≤1个非关键条目不满足为高质量;>1个非关键条目不满足为中质量;1个关键条目不满足,伴或不伴非关键条目不满足为低质量;>1个关键条目不满足,伴或不伴非关键条目不满足为极低质量[15]。
1.4.3 结局指标的证据质量评价 采用GRADE工具评价结局指标的证据质量,包括5个降级因素(偏倚风险、不一致性、不间接性、不精确性、发表偏倚)和3个升级因素(大效应量、有剂量-效应关系、相关混杂),分为高、中、低和极低4个等级[10]。RCT被预设为高级证据,根据降级因素进行降级处理,其中未降级为高级、降1级为中级、降2级为低级、降3级为极低级。
1.5 统计学方法
采用描述性分析方法进行文献结局指标的汇总分析。
2 结果
2.1 纳入文献筛选流程及结果
初检共获得相关文献3 534篇,经阅读题目、摘要及全文后,最终纳入12篇文献[7-8,16-25]。文献筛选流程见图1。
2.2 纳入文献的基本信息
12篇文献中,有英文9篇[7-8,16-22]、中文3篇[23-25],包括系统评价4篇[8,17,21,23]、Meta分析8篇[7,16,18-20,22,24-25];原始研究类型均为RCT,纳入的数量为2~25篇;样本量为589~4 581例;发表时间为1998-2020年;3篇文献采用Jadad量表[18-19,22],7篇文献采用Cochrane手册推荐的偏倚风险评估工具[7-8,17,21,23-25],2篇文献未报告评价方法[16,20]。纳入系统评价/Meta分析的基本信息见表2。
2.3 纳入文献的报告质量评价
纳入文献的PRISMA评分为16.5~27.0分(表2)。其中,2篇(16.67%)为15.0~21.0分[16,20],为中等质量,提示报告有一定缺失;10篇(83.33%)为22.0~27.0分[7-8,17-19,21-25],为高质量,提示报告相对完整,纳入研究中无相对严重的信息缺失。存在报告信息缺失的条目主要有:条目5(83.33%)、条目8(16.67%)、条目10(16.67%)、条目16(16.67%)、条目17(16.67%)、条目22(16.67%)、条目23(33.33%)和条目27(41.67%)。结果见表3。
2.4 纳入文献的方法学质量评价
AMSTAR 2量表评价结果显示,7篇文献的方法学质量等级为极低质量[7,16,20-21,23-25],3篇文献为低质量[18-19,22],2篇文献为高质量[8,17]。有10篇文献实施前制定的报告与计划书内容不一致[7,16,18-25];1篇文献提供的检索策略不全面[16];6篇文献列出但未充分证明排除理由[7,16,20,23-25];1篇文献未使用合理的评估工具研究文献间的偏倚风险[20];2篇文献在解释/讨论结果时,未考虑纳入研究的偏倚风险[20,23],2篇文献在定量合成时未充分调查发表偏倚[20-21];所有文献均未报告纳入研究的资金来源[7-8,16-25]。结果见表4。
2.5 纳入文献的证据质量分级
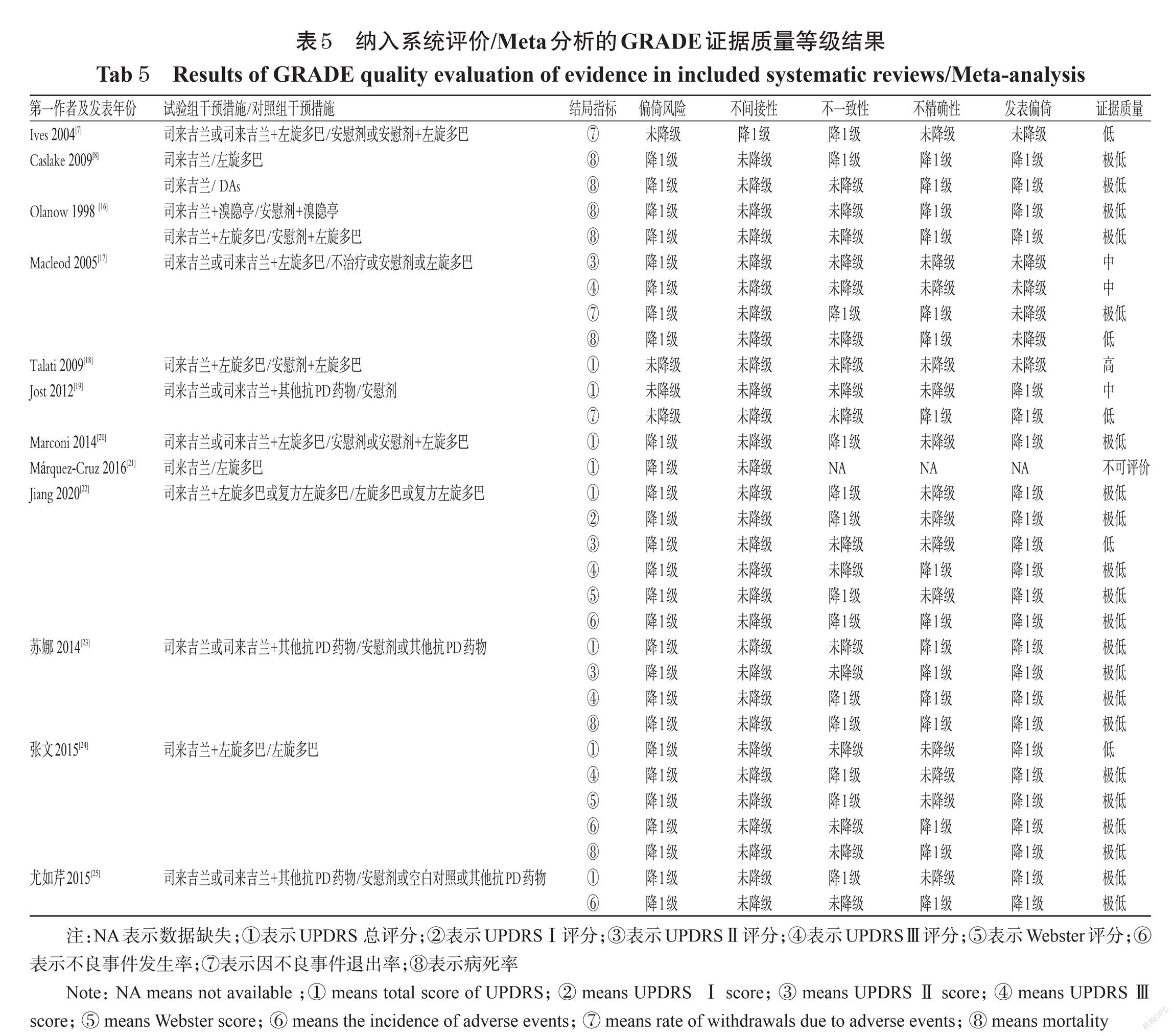
12篇文献均采用Meta分析合并[7-8,16-25],共有31个结局指标,其中高质量指标1个(3.23%)[18],中质量指标3个(9.68%)[17,19],低質量指标5个(16.13%)[7,17,19,22,24],极低质量指标21个(67.73%)[8,16-17,20,22-25],不可评价结局指标1个(3.23%)[21]。所有纳入文献的证据质量均未有升级因素;造成证据质量降级的主要因素有偏倚风险(87.10%)、发表偏倚(77.42%)、不精确性(51.61%)、不一致性(41.94%)。结果见表5。
2.6 纳入文献的结局指标评价
2.6.1 UPDRS总评分 共有8项研究报道了UPDRS总评分[18-25]。其中,3项研究结果显示,与对照组比较,单用司来吉兰可显著改善患者的UPDRS总评分(P<0.05)[19,23,25];3项研究结果显示,与对照组比较,司来吉兰+左旋多巴可显著改善患者的UPDRS总评分(P<0.05)[18,22,24];1项研究结果显示,与对照组比较,司来吉兰单用或联用左旋多巴均可显著改善患者的UPDRS总评分(P<0.05)[20]。1项研究结果显示,司来吉兰+其他抗PD药物组患者的UPDRS总评分与对照组比较差异无统计学意义(P=0.24)[23]。1项研究结果显示,司来吉兰组患者的UPDRS总评分与对照组比较差异无统计学意义(P>0.05)[21]。
2.6.2 UPDRSⅠ评分 1项研究报道了UPDRSⅠ评分[22]。结果显示,与对照组比较,司来吉兰+左旋多巴(或复方左旋多巴)均可显著改善患者的UPDRSⅠ评分(P=0.002)[22]。
2.6.3 UPDRSⅡ评分 共有3项研究报道了UPDRSⅡ评分[17,22-23]。其中,1项研究结果显示,与对照组比较,单用司来吉兰或联用其他抗PD药物均能显著改善患者的UPDRSⅡ评分(P<0.05)[23]。1项研究结果显示,与对照组比较,司来吉兰+左旋多巴(或复方左旋多巴)均可显著改善患者的UPDRSⅡ评分(P<0.000 01)[22]。1项研究结果显示,与对照组比较,司来吉兰治疗1年可显著改善患者的UPDRSⅡ评分(P=0.006)[17]。
2.6.4 UPDRS Ⅲ评分 共有4项研究报道了UPDRS Ⅲ评分[17,22-24]。其中,1项研究结果显示,与对照组比较,司来吉兰治疗1年患者的UPDRS Ⅲ评分显著降低(P<0.05)[17]。1项研究结果显示,与对照组比较,司来吉兰+其他抗PD药物可显著改善患者的UPDRS Ⅲ评分(P=0.000 1)[23]。2项研究结果显示,与对照组比较,司来吉兰+左旋多巴(或复方左旋多巴)均可显著改善患者的UPDRS Ⅲ评分(P<0.000 1)[22,24]。
2.6.5 Webster评分 共有2项研究报道了Webster评分[22,24]。结果显示,与对照组比较,司来吉兰+左旋多巴(或复方左旋多巴)均可明显改善患者的Webster评分(P<0.000 1)[22,24]。
2.6.6 不良事件发生率 共有3项研究报道了不良事件发生率[22,24-25]。其中,1项研究结果显示,司来吉兰与患者的不良事件发生率无关(P=0.10)][25]。2项研究结果显示,司来吉兰+左旋多巴(或复方左旋多巴)组患者的不良事件发生率与对照组比较差异均无统计学意义(P>0.05)[22,24]。
2.6.7 因不良事件退出率 共有3项研究报道了因不良事件退出率[7,17,19]。结果显示,与对照组比较,使用司来吉兰患者的因不良事件退出率更高(P<0.05)[7,17,19]。
2.6.8 病死率 共有5项研究报道了病死率[8,16-17,23-24]。其中,4项研究结果显示,司来吉兰与患者病死率的提高无关(P>0.05)[8,16-17,23]。1项研究结果显示,司来吉兰+左旋多巴组患者的病死率与对照组比较差异无统计学意义(P=0.22)[24]。
3 讨论
目前,虽然已有关于司来吉兰治疗PD有效性和安全性的系统评价/Meta分析[7-8,16-25],但这些研究的临床证据级别无法确定,因此本研究从方法学、报告质量等方面进一步规范了系统评价/Meta分析研究的流程,以重新集中评定循证医学的证据质量,旨在为临床决策提供更为可靠的证据,为提高证据转化效率奠定基础。
本研究结果显示,司来吉兰在改善PD患者UPDRS总评分、UPDRSⅠ评分、UPDRSⅡ评分、UPDRSⅢ评分及Webster评分等方面均具有显著效果,也未提高不良事件发生率及病死率。这提示司来吉兰具有较好的疗效和安全性。报告质量的评价结果显示,研究报告主要存在以下问题:缺少系统评价/Meta分析方案制定和注册意识,10项研究未提供方案及注册信息[7,16,18-25];4项研究对于纳入研究的筛选流程描述不够全面[16,20,23-24];3项研究对于纳入研究的偏倚风险评价不够全面或缺乏[7,20,23];5项研究缺乏资金支持利益冲突的相关描述[16,22-25]。方法学质量的评价结果显示,7项研究为极低质量[7,16,20-21,23-25],3项研究為低质量[18-19,22],2项研究为高质量[8,17];所有研究的整体方案设计、方法实施、结局指标合并均较为规范,但均未报告纳入研究的资金来源[7-8,16-25];10项研究实施前制定的报告与计划书内容不一致[7,16,18-25];4项研究未报告潜在利益冲突[16,23-25]。这提示纳入的系统评价/Meta分析整体质量偏低。证据质量等级的评价结果显示,高质量指标1个、中质量指标3个、低质量指标5个、极低质量指标21个、不可评价结局指标1个;未有升级因素,造成证据质量降级的主要因素为偏倚风险、发表偏倚、不精确性、不一致性。这提示纳入系统评价/Meta分析的结局指标总体证据质量偏低,部分研究存在选择偏倚和发表偏倚,部分结局指标的异质性较大,结果可靠性一般。
本研究的局限性为:(1)仅纳入了中英文文献,其他语种的数据缺失可能会对结果造成一定影响;(2)检索时间截至2020年11月,后续证据的更新可能会对结果产生影响;(3)评价分析过程存在的主观性可能会造成偏倚。
综上所述,司来吉兰治疗PD的疗效和安全性均较好,但目前相关系统评价/Meta分析的方法学质量和证据质量均偏低,需进一步规范研究方法。基于此,笔者建议研究人员后续应在系统评价/Meta分析计划书制定、报告文献排除原因、原始RCT偏倚风险控制等方面进行改善,可根据GRADE方法对结局指标进行证据质量分级,尽量排除质量等级低的原始研究;同时注重研究方案的注册,严格按照AMSTAR 2量表及PRISMA声明的要求撰写文章,以期为司来吉兰在PD治疗中的应用提供高质量证据。
参考文献
[ 1 ] GOETZ C G,PAL G. Initial management of Parkinson’s disease[J]. BMJ,2014,349:g6258.
[ 2 ] RASCOL O,LOZANO A,STERN M,et al. Milestones in Parkinson’s disease therapeutics[J]. Mov Disord,2011,26(6):1072-1082.
[ 3 ] CERAVOLO R,ROSSI C,DEL PRETE E,et al. A review of adverse events linked to dopamine agonists in the treatment of Parkinson’s disease[J]. Expert Opin Drug Saf,2016,15(2):181-198.
[ 4 ] CONNOLLY B S,LANG A E. Pharmacological treatment of Parkinson disease:a review[J]. JAMA,2014,311(16):1670-1683.
[ 5 ] 中華医学会神经病学分会帕金森病及运动障碍学组,中国医师协会神经内科医师分会帕金森病及运动障碍学组.中国帕金森病治疗指南:第4版[J].中华神经科杂志,2020,53(12):973-986.
[ 6 ] GROUP P S. Effects of tocopherol and deprenyl on the progression of disability in early Parkinson’s disease[J]. N Engl J Med,1993,328(3):176-183.
[ 7 ] IVES N J,STOWE R L,MARRO J,et al. Monoamine oxidase type B inhibitors in early Parkinson’s disease: meta-analysis of 17 randomised trials involving 3 525 patients[J]. BMJ,2004,329(7466):593.
[ 8 ] CASLAKE R,MACLEOD A,IVES N,et al. Monoamine oxidase B inhibitors versus other dopaminergic agents in early Parkinson’s disease[J]. Cochrane Database Syst Rev,2009(4):CD006661.
[ 9 ] 刘雅莉,袁金秋,杨克虎,等.系统评价再评价的制作方法简介及相关资料分析[J].中国循证儿科杂志,2011,6(1):58-64.
[10] ATKINS D,BEST D,BRISS P A,et al. Grading quality of evidence and strength of recommendations[J]. BMJ,2004,328(7454):1490.
[11] The Cochrane Collaboration. Chapter 22:overviews of reviews in:Higgins JPT,Green S,editors cochrane handbook for systematic reviews of interventions version 5.0.2[EB/OL].[2021-04-10]. https://training.cochrane.org/handbook.
[12] HUGHES A J,DANIEL S E,KILFORD L,et al. Accu- racy of clinical diagnosis of idiopathic Parkinson’s disease:a clinico-pathological study of 100 cases[J]. J Neurol Neurosurg Psychiatry,1992,55(3):181-184.
[13] 蒋雨平,王坚,丁正同,等.原发性帕金森病的诊断标准:2005年[J].中国临床神经科学,2006,14(1):40.
[14] MOHER D,LIBERATI A,TETZLAFF J,et al. Preferred reporting items for systematic reviews and meta-analyses:the PRISMA statement[J]. PLoS Med,2009,6(7):e1000097.
[15] SHEA B J,REEVES B C,WELLS G,et al. AMSTAR 2:a critical appraisal tool for systematic reviews that include randomised or non-randomised studies of healthcare interventions,or both[J]. BMJ,2017,358:j4008.
[16] OLANOW C W,MYLLYLÄ V V,SOTANIEMI K A,et al. Effect of selegiline on mortality in patients with Parkinson’s disease:a meta-analysis[J]. Neurology,1998,51(3):825-830.
[17] MACLEOD A D,COUNSELL C E,IVES N,et al. Mono- amine oxidase B inhibitors for early Parkinson’s disease[J]. Cochrane Database Syst Rev,2005(3):CD004898.
[18] TALATI R,REINHART K,BAKER W,et al. Pharma- cologic treatment of advanced Parkinson’s disease:a meta-analysis of COMT inhibitors and MAO-B inhibitors[J]. Parkinsonism Relat Disord,2009,15(7):500-505.
[19] JOST W H,FRIEDE M,SCHNITKER J. Indirect meta- analysis of randomised placebo-controlled clinical trials on rasagiline and selegiline in the symptomatic treatment of Parkinson’s disease[J]. Basal Ganglia,2012,2(4):S17-S26.
[20] MARCONI S,ZWINGERS T. Comparative efficacy of selegiline versus rasagiline in the treatment of early Parkinson’s disease[J]. Eur Rev Med Pharmacol Sci,2014,18(13):1879-1882.
[21] MÁRQUEZ-CRUZ M,DÍAZ-MARTÍNEZ J P,SOTO- MOLINA H,et al. A systematic review and mixed treatment comparison of monotherapy in early Parkinson’s di- sease:implications for Latin America[J]. Expert Rev Pharmacoecon Outcomes Res,2016,16(1):97-102.
[22] JIANG D Q,LI M X,JIANG L L,et al. Comparison of selegiline and levodopa combination therapy versus levodopa monotherapy in the treatment of Parkinson’s disease:a meta-analysis[J]. Aging Clin Exp Res,2020,32(5):769-779.
[23] 蘇娜,吴斌,徐珽.司来吉兰治疗帕金森病的有效性与安全性的系统评价[J].中国医院药学杂志,2014,34(14):1206-1212.
[24] 张文,路宁维,谢华,等.司来吉兰联合左旋多巴治疗帕金森病的Meta分析[J].中国现代应用药学,2015,32(12):1498-1502.
[25] 尤如芹.司来吉兰治疗帕金森病的Meta分析[D].长春:吉林大学,2015.
(收稿日期:2021-06-22 修回日期:2021-11-07)
