浅析金属镍离子的测定
2021-12-26尹金标
尹金标
(山东畜牧兽医职业学院,山东 潍坊 261000)
随着现代科技的不断发展,金属镍被广泛运用到电镀行业上,电镀过程中会产生大量的废水,废水中的镍离子有很强的毒性。分析废水中镍离子的含量,采取有针对性的措施,消除镍污染带来的危害,保护我们赖以生存的环境是我们每一位分析工作者应尽的义务和担负的责任。在分析过程中,各个环节要考虑周全、终点颜色变化要严格把握,仪器分析要精益求精,努力提高分析结果的准确度。
1 实验部分
1.1 仪器50mL
酸式滴定管、托盘天平、电子天平、200mL烧杯、100mL烧杯、250mL容量瓶1个、1000mL容量瓶1个、50mL容量瓶15个、25mL移液管、250mL锥形瓶、量筒(100mL、10mL)、胶头滴管、洗瓶、紫外可见分光光度计(UV-1800PC-DS2)、配对1cm石英比色皿2个、5mL、10mL吸量管。
1.2 试剂
①氧化锌;②Na2H2Y.2H2O;③10%氨水:量取400mL氨水,稀释至1000mL。④NH3H2O-NH4Cl(pH=10)称取NH4Cl54g,加20mL蒸馏水溶解,加0.9g/mL的浓氨水350mL,再用蒸馏水稀释至1L。⑤(1+4)盐酸:量取504mL盐酸,稀释至1000mL。⑥紫脲酸铵(0.1g~0.2g)。称取1g紫脲酸铵,200g干燥的NaCl混合(不要求精准)。⑦镍标准储备液:1000mg/L准确称取金属镍0.1000g溶于10mL(1:1)硝酸中,加热蒸发至干,冷却再加入(1:99)的硝酸中溶解,转入100mL容量瓶定容至刻度。镍标准溶液:10.0mg/L,取10mL镍于1000mL容量瓶中加去离子水定容至刻度。⑧铬黒T指示剂:将1g铬黒T指示剂与100g分析纯NaCl混合、磨细、装瓶备用。⑨5g/L丁二酮肟:称取0.5g丁二酮肟溶解50mL氨水中,用水稀释至100mL。⑩过硫酸铵。硫酸镍。
2 化学分析法测镍离子
2.1 0.05mol/LEDTA的配制
配制0.05mol/LEDTA溶液250mL所需Na2H2Y.2H2O约为4.65g。称取分析纯Na2H2Y.2H2O4.66g置于烧杯中,加100mL的温水,溶解,转入250mL的容量瓶,定容至刻度。
2.2 EDTA的标定
准确称取已灼烧至恒重的工作试剂氧化锌1.3249g(不除皮法)于100mL小烧杯中,用少量去离子水润洗,加入20mL20%盐酸溶解后定量转入250mL的容量瓶,用去离子水定容至刻度,摇匀。用25.00mL移液管移取25.00mL上述溶液于250mL的锥形瓶中(不能从容量瓶中直接移取溶液),加75mL去离子水,用氨水溶液(10%)调至溶液pH至7~8,加入10mL NH3H2ONH4Cl缓冲溶液(pH≈10)及3~5滴铬黑T(5g/L),用待标定的EDTA溶液滴定至溶液由紫红色变为纯蓝色。
平行测定 3 次,同时做空白实验。
EDTA标准滴定溶液浓度C(EDTA)的计算,单位mol/L。
V实际消耗EDTA的体积=V滴定消耗EDTA的体积+V体积校正值+V溶液温度校正值。
标定EDTA物质的量浓度:

氧化锌的摩尔质量:M(ZnO)=81.39g/mol。
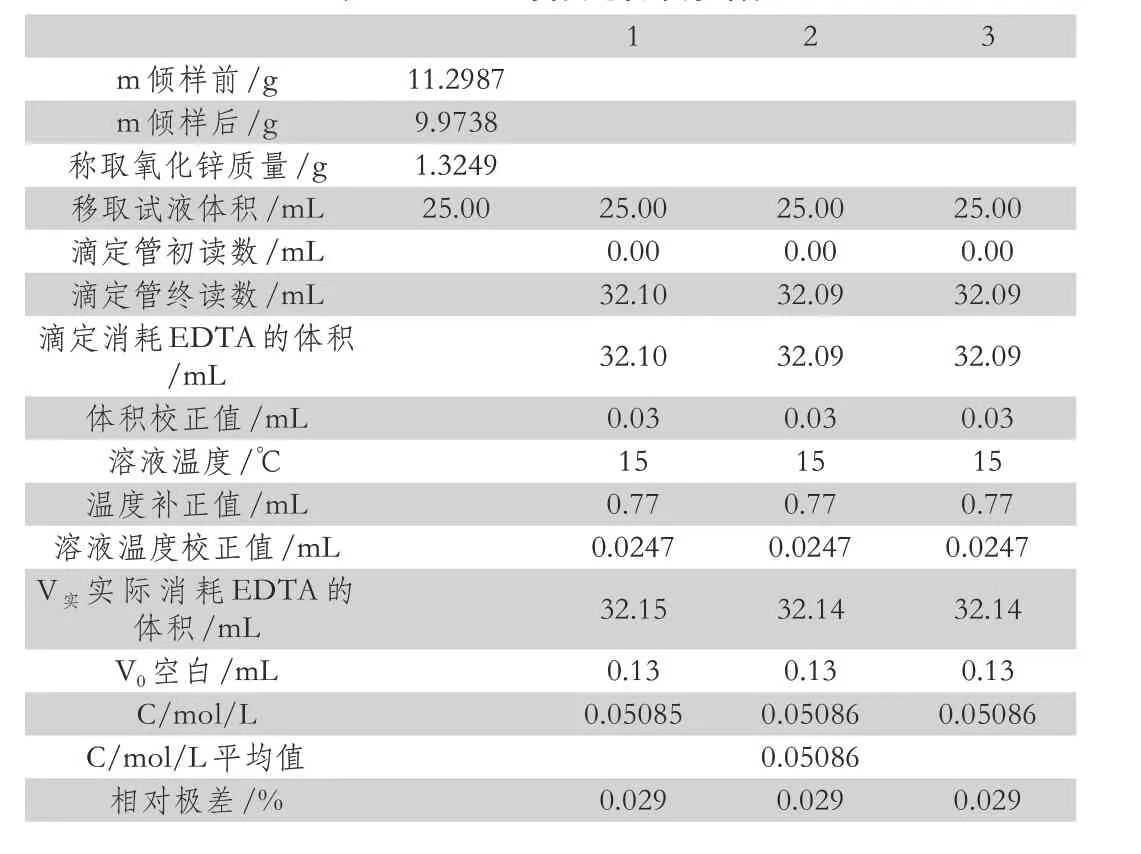
表1 EDTA的标定物质参数
3 镍含量的测定方法分析
3.1 化学分析法硫酸镍试样中镍含量的测定
称取镍液体样品0.2361g;0.2360g;0.2362g分别加水70mL,加入10mLNH3H2O-NH4Cl缓冲溶液(pH≈10)及0.1~0.2g紫脲酸铵指示剂,摇匀,用EDTA标准溶液[C(EDTA)=0.05086mol/L]滴定至溶液呈蓝紫色。平行测定3次。
3.2 镍质量分数ωNiSO4/%的计算
镍的摩尔质量:M(NI)=58.69g/mol。
计算式:

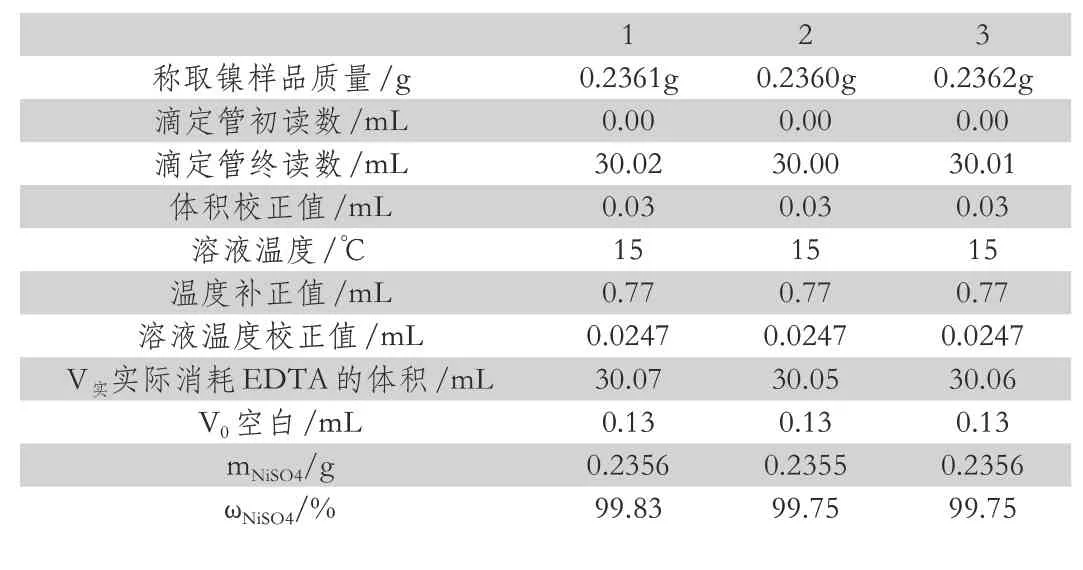
表2 镍质量分数计算
4 分光度光度法测镍离子
(1)吸收池配套性检查:石英吸收池在220nm处装蒸馏水,以一个吸收池作参比,调节透射比为100%,测定其余吸收池的投射比,其偏差应小于0.5%,可配套使用。
(2)在氨溶液中,碘存在,过硫酸铵作用下镍离子与丁二酮肟反应生成酒红色配合物。在分光光度计上测量该溶液对400nm~500nm不同波长单色光的吸收程度(吸光度),以波长为横坐标,吸光度为纵坐标,绘制成曲线为吸收曲线,找到最大吸收波长为435nm。
(3)配制标准溶液及待测溶液用分光光度计测定镍离子的含量:取50mL容量瓶7个,用10mL的吸量管分别移取1mL、2mL、4mL、6mL、8mL、10mL的10μg/mL镍 标 准 溶 液 装 入6个容量瓶,7号容量瓶加入镍试液10mL。然后在1~7号容量瓶中分别加入0.5mL1mol/LNaOH溶液;1.5mL3%过硫酸铵(NH4)2S2O8;15mL0.1%的丁二酮肟溶液,分别加去离子水至50mL,充分摇匀,静置13~15分钟,充分显色。在435nm波长下,用1cm石英比色皿,用空白液作为参比溶液,分别测定2~7号标准溶液及待测溶液的吸光度。在操作台上显示工作曲线。确定未知液的稀释倍数,根据待测液测得的吸光度,确定未知样品的浓度。根据位置溶液的稀释倍数,求出未知物的含量。
试样溶液中镍的含量(μg/mL)=标准曲线上差得的浓度(μg/mL)×试液稀释倍数。
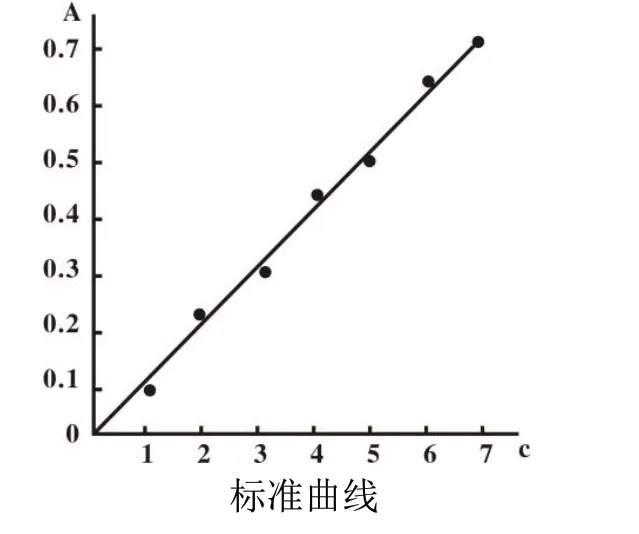
图1 试样溶液中镍的含量
5 实验结论
5.1 注意事项
不能从容量瓶直接移取溶液,应该选择干净烧杯,用去离子水洗涤烧杯内壁多次,用容量瓶中配制的液体洗涤烧杯多次,将容量瓶中溶液倒入烧杯中,再从烧杯中移液溶液,这样可以预防容量瓶中的溶液被移液管污染。
在络合滴定中,所用蒸馏水应符合国家标准(符合GB6682-2008中分析实验用水规格)要求。若蒸馏水中含有钙镁离子等,在滴定过程中会消耗一定量的EDTA,影响分析结果的测定。因此,在络合滴定中,所用蒸馏水一定要进行质量检查。为了保证测定结果的准确性,最常用二次蒸馏水或去离子水来配制标准溶液。
在测定过程中,有可能影响分析结果的玻璃仪器,一定要用去离子水多次洗涤。如移液管、锥形瓶、容量瓶、烧杯、滴管等。尽可能的减少分析误差。为了减少称量误差,使用电子天平(用不除皮法)称量试样。称量范围应控制在2.5%范围内。为了减少仪器误差,应校正仪器。在计算过程中,要带入体积校正值、溶液温度补正值。为了减少系统误差,在测定过程中一定要做空白实验,扣去空白值。
5.2 讨论
(1)在镍离子的测定过程中,滴定终点颜色变化是由黄色变为蓝紫色。但多数分析工作者在测定过程中对于终点颜色的把握往往不准,滴定过程中终点颜色将黄色变为了紫红色,这样会造成较大误差。逼近终点时控制好最后一滴流出的体积是做好本实验的关键。滴定管尖嘴流出体积0.1mL约1/4滴;0.2mL约1/2滴;0.4mL约1滴。控制好最后一滴流出体积使终点颜色由黄色变为蓝紫色。
(2)分光光度计测镍离子,入射光的波长对测量结果的准确度和灵敏度会有较大影响.选择入射光的波长时,应绘制镍离子与丁二酮肟反应生成的有色溶液光的吸收曲线,选择该溶液的最大吸收波长λmax的光作为入射光。如果遇到其它离子的干扰,可选择灵敏度低但能避免干扰的波长进行测定。如测定镍离子时,用丁二酮肟作显色剂,镍离子与丁二酮肟反应生成的有色溶液的最大吸收波长为435nm。若待测液中混有三价铁离子,需要加柠檬酸,形成柠檬酸铁配合物,而柠檬酸在435nm处也有一定的吸收,对镍离子的测定有一定的干扰,此时可选用420nm~430nm的波长。
(3)重视比色皿的配对。 在吸光光度分析的过程中,同一台仪器要使用符合配对的比色皿,否则会对测定结果的准确度有着较大的影响。
(4)用比色皿装液过程中,比色皿的透光面容易被去离子水或试液覆盖,处理不好会影响测定结果的准确度。装入样品池前认真观察,用擦镜纸蘸取少许去离子水润洗透光面,再吸干。
5.3 建议
化学分析法测镍离子的过程中,从称量、溶液配制、滴定及到计算要严格要求,反复练习,要找到由黄色变为篮紫色的关键操作点,通过颜色对比及终点液滴流出速度的控制来提高分析结果的准确度。用分光光度计测定镍离子的含量,灵敏度较高,准确度较高,仪器操作简便,相对误差一般在2~5%。只要反复练习,认真操作就能够完成实验的要求。
