血管内介入治疗肝移植术后门静脉狭窄或闭塞:5例报告
2021-12-25刘文浩朱文科黄湘荣方泰石王立非
刘文浩,朱文科,黄湘荣,冯 凯,方泰石,王立非*
(1.深圳市第三人民医院放射介入科,2.肝脏外科,广东 深圳 518114)
肝移植术后门静脉(portal vein, PV)并发症相对少见,主要包括PV狭窄和闭塞,一旦发生常引起移植肝功能严重受损,甚至危及患者生命,使得及时发现并处理PV并发症成为保证肝移植成功的重要环节。本研究观察血管内介入治疗肝移植术后PV狭窄或闭塞的效果。
1 资料与方法
1.1 一般资料 回顾性分析2017年10月—2020年12月5例于深圳市第三人民医院接受肝移植后发生PV并发症患者,均为男性,年龄39~55岁,均接受同种异体原位肝移植术。5例患者基本资料见表1。

表1 5例肝移植术后发生PV并发症患者资料
1.2 仪器与方法 采用GE Innova3100-IQ DSA作为引导设备。嘱患者仰卧,于透视下定位穿刺平面;局部麻醉后采用22G Chiba穿刺针于腋中线经皮经肝穿刺PV右支,穿刺成功后引入0.018inch导丝至PV主干,交换0.035inch导丝(Cook),沿导丝置入6~8F血管鞘(Cook)。经血管鞘引入导管,在透视下尝试通过PV狭窄或闭塞段进入肠系膜上静脉或脾静脉进行造影,显示PV狭窄部位、程度及其长度。置换超硬导丝(Terumo),引入球囊扩张导管(Cook)扩张PV狭窄或闭塞段;根据血管管径适当选择球囊及支架(Cordis),球囊扩张时间一般为40~60 s。术后回退导管鞘,以弹簧圈封闭穿刺道。
2 结果
病例1:PV造影显示PV主干远端局部狭窄,狭窄程度约60%,其近段扩张;以8 mm×60 mm球囊扩张60 s后,植入1枚10 mm×60 mm裸支架;复查造影示狭窄消失,血流通畅。
病例2:造影示PV主干狭窄,狭窄程度约90%(图1);以10 mm×60 mm球囊扩张60 s,植入1枚12 mm×60 mm裸支架后狭窄消失,血流通畅。
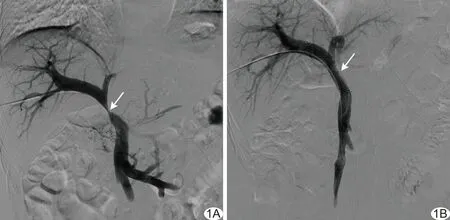
图1 病例2,男,39岁,肝移植术后3个月 A.直接法PV造影示PV主干狭窄,狭窄程度约90%(箭); B.以10 mm×60 mm球囊扩张后,植入1枚12 mm×60 mm裸支架,复查造影示狭窄消失(箭),PV血流通畅,远段血流明显改善
病例3:造影示PV主干-胃冠状静脉吻合口狭窄,狭窄程度约90%;以10 mm×80 mm球囊扩张40 s后,植入10 mm×80 mm、10 mm×60 mm裸支架各1枚及8 mm×50 mm覆膜支架1枚,复查造影示PV恢复通畅。术中患者血压下降,行肝动脉造影未见异常;床边超声提示穿刺部位肝包膜处出血,以弹簧圈封堵穿刺道后仍见出血;行开腹探查术,证实穿刺致肋间动脉出血,以5-0 Prolene线缝合受损动脉壁后出血停止。
病例4:造影示PV主干远端球状充盈缺损、闭塞(图2);导丝通过闭塞段后,引入6 mm×60 mm球囊扩张40 s,经导管缓慢推注尿激酶30万U(溶于150 ml生理盐水)行局部溶栓,复查造影示充盈缺损范围缩小,留置溶栓导管;予尿激酶持续溶栓(50万U/天),3天后复查造影示PV通畅、血栓进一步减少、管壁光滑而撤管。

图2 病例4,男,50岁,肝移植术后1天 A.造影示PV主干未显影,远端球状充盈缺损(箭); B.导管通过闭塞段后,肠系膜上静脉造影示PV主干扩张,左、右支分支部见球样充盈缺损(箭),PV显影浅淡; C.球囊扩张后予尿激酶行局部溶栓,复查造影示充盈缺损范围较前缩小(箭); D.留置溶栓导管,尿激酶持续溶栓3天后造影示PV通畅,血栓进一步缩小(箭)
病例5:造影示PV主干纡曲、远端闭塞;以10 mm×80 mm球囊扩张40 s后,植入12 mm×80 mm支架1枚,复查造影血流通畅,支架局部扭曲;结合CT考虑为肝肿胀压迫所致,未予特殊处理。
5例均有效开通PV。病例1术后随访至今41个月,PV通畅无狭窄,肝功能正常。病例2术后随访至今31个月,PV通畅,少许附壁血栓,无明显狭窄,肝功能正常。病例3术后并发胆总管狭窄,行胆道支架植入术,后因重症肺炎、急性呼吸窘迫综合征、脓毒性休克死亡。病例4术后随访至今12个月,PV通畅无狭窄,肝功能正常。病例5术后随访至今约4个月,PV通畅无狭窄,肝功能正常。
3 讨论
3.1 PV并发症病因 PV并发症是肝移植术后较少见的血管并发症,发生率约1.0%~12.5%[1-3],狭窄程度较轻时可无明显症状,严重时可致肝功能异常甚至肝衰竭,导致患者死亡。肝移植术后PV狭窄多发生于吻合口处,多与吻合技术有关,如吻合口成角、扭曲、张力过大等[3],亦可能与供、受体静脉直径不匹配,移植术前受体存在严重PV高压或接受TIPS、脾切除术等治疗,或移植后排斥反应等有关[4-6]。肝移植术后PV闭塞的主要危险因素包括:①术前PV病变(血栓、纤维化、海绵样变性);②体循环静脉盗血,如自发门-体静脉分流;③术中损伤PV内膜或PV扭曲;④急性排斥反应。此外,肝移植术后数周内PV周围淋巴水肿,压迫PV致管腔变窄亦可能是急性PV闭塞的因素之一。
本组5例患者中,2例曾于肝移植术前接受TIPS;2例PV主干附壁血栓,其中1例PV主干壁钙化;1例PV海绵样变,近端瘤样扩张,主干血栓,移植术中发现PV主干机化血栓,予血栓剥离后吻合PV。病例3术中剥离PV机化血栓后吻合受体PV,可能是导致PV狭窄的主要原因。病例5 接受肝移植后PV闭塞,复查CT发现肝尾状叶压迫PV致PV扭曲,可能因其曾接受右半肝切除手术,腹腔粘连致空间较小,叠加移植肝肿胀压迫PV致其闭塞。
3.2 诊断和治疗PV并发症 超声是肝移植术后观察PV的便捷、有效的检查方式,敏感度高;CTA则能较超声更客观地反映PV形态及血流。本组病例5肝移植后第1天超声发现PV无血流,之后数日超声检查示PV血流通畅,但吻合口显示不清,PV左支反向血流。术后第5天行CTA检查,发现PV主干闭塞,PV左、右支于动脉期明显强化,提示存在肝动脉-PV瘘。本例提示,超声发现血流异常时应提高警惕,密切监测肝功能,必要时及时行CTA检查。
治疗肝移植术后PV并发症的主要方法包括血管内介入及抗凝治疗等。抗凝治疗适用于急性血栓所致PV轻-中度狭窄,需密切观察PV血流,避免延误治疗时机。血管内介入治疗包括经导管局部溶栓、球囊扩张及支架植入术。球囊扩张及支架植入是治疗肝移植术后PV并发症的主要方法[7-9]。球囊及支架的直径应与邻近正常段PV相仿,最大直径不超过正常段PV直径的15%,其长度应大于狭窄段长度。YABUTA等[6]报道,约81.4%的PV狭窄患者可于1~2次球囊扩张成形术后恢复正常。儿童处于生长期,对肝移植后PV狭窄患儿多采用单纯球囊扩张术[10]。
本组1例(病例4)术后1天发现PV闭塞,造影显示PV远端球状充盈缺损,行球囊扩张及尿激酶局部溶栓后血栓缩小,乃留置溶栓导管持续进行溶栓;3天后再次复查造影显示血栓进一步减少,PV通畅且管壁光滑。本例提示,部分肝移植后PV急性血栓形成的原因可能是PV周围淋巴水肿压迫致管腔狭窄、血流减慢,经抗凝、溶栓再通后,随着移植肝淋巴系统的重新建立,淋巴水肿减轻或消失,PV血流可获改善,无需支架植入亦可保持通畅。对此类患者可尝试以球囊扩张+置管溶栓术开通PV,可避免因支架植入后长期接受抗凝治疗,但存在短期内再发狭窄或闭塞风险,需监测肝功能指标并以超声严密监测PV血流。刘煜等[11]报道,仅行球囊扩张术治疗肝移植术后PV狭窄,术后再狭窄发生率为50%~60%,故主张植入支架;KIM等[12]指出,植入支架较单纯球囊扩张术成功率更高,且术后再狭窄率较低。孙军辉等[13]认为植入支架后易致PVT,且支架选择不当会对再次肝移植手术造成困难。本组对3例PV狭窄均行球囊扩张+支架植入术,均成功开通PV。针对此类PV并发症患者采用哪种治疗方法可使患者受益更多尚需进一步观察。
PV球囊扩张及支架植入术主要并发症为腹腔出血、气胸、胆道损伤及球囊扩张所致吻合口破裂出血。本组1例术中发现血压降低,经开腹探查证实为穿刺致肋间动脉损伤出血。肋间动脉出血时PV压力较低,如术中患者出现大量失血迹象,应及时行肝动脉造影;如肝动脉无异常,则应考虑穿刺引起肋间动脉出血的可能。
综上,血管内介入治疗肝移植术后PV狭窄或闭塞效果良好。但本研究为回顾性观察,且样本量小,仍需多中心、大样本量研究进一步观察。