负载型过渡金属催化剂催化还原水中硝酸盐氮的研究进展
2021-12-23孟柏宇
孟柏宇
(哈尔滨工业大学(深圳)土木与环境工程学院,广东 深圳518055)
前 言
近百年来,工农业高速发展,化肥和含氮杀虫剂在农业生产中的广泛使用和工业生产中高浓度含氮废水的肆意排放造成了地球水环境愈发严重的污染问题[1]。在自然界中,氮的自然循环已经遭到了人为破坏,在地表水和地下水中硝酸盐的污染已成为全球性的环境问题[2]。在20 世纪60 年代,美国与欧洲就有相关报道,造成天然水体硝酸盐污染的主因是氮肥的大量广泛使用[3]。调查表明:在美国有接近1/4 事例因饮用水中硝酸盐氮超标对人体造成健康危机;在英国供给180 万人的125 处饮用水源中硝酸盐含量也均超标;而我国部分大中城市的饮用水源中硝酸盐污染问题也时有发生。硝酸盐氮化学性质稳定,通过自然水体中反硝化微生物和水体自净难以去除[4]。
1 负载型过渡金属催化剂还原硝酸盐氮的原理
催化还原硝酸盐氮是一个多相催化还原过程,如图1 所示,成功的负载型催化剂可以催化化学反应的发生,使反应进行完全,并且在反应结束后,通过简单分离即可进行回收,使催化剂可以循环使用[10]。
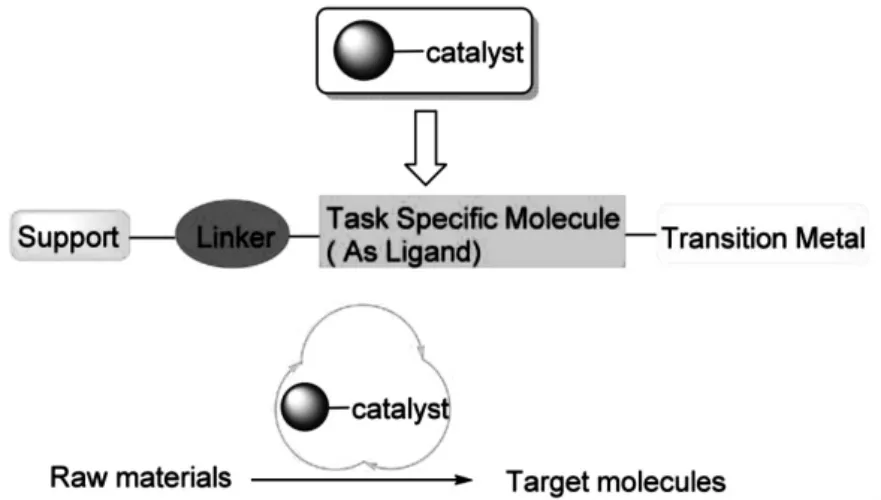
图1 负载催化剂的设计策略和催化作用Fig. 1 Design and application of the supported catalyst
催化还原硝酸盐氮的研究最早可以追溯到20世纪80 年代末,德国学者Vorlop 等人[9]首次提出了利用负载型的二元金属催化剂将硝酸盐氮催化还原为氮气的脱氮技术。在负载型过渡金属催化剂的作用下硝酸盐氮还原为氮气的过程可表示如下:

在目前研究中,吸引研究者目光较多的是在负载型过渡金属催化剂作用下,以H2作还原气将硝酸盐氮催化还原为氮气。拥有高活性和高选择性是这种方法的最大优点,只要在理论上选择合适的负载型过渡金属催化剂和相应的控制反应条件,可将硝酸盐全部催化还原为氮气。Tang T,Xing Q,Zhang S 等以铜作为催化材料,将其与铁粉复合,制得双金属催化剂[11]。该研究是将催化还原法与物理离子交换树脂工艺联用,选择离子交换树脂D407 作为载体,在最优pH 值为3 条件下,铜铁负载型过渡金属催化剂有效降低了树脂表面的硝酸根、亚硝酸根浓度,达到了延长离子交换树脂使用时间和使用寿命的目的。Pizarro A H,Torija I,Moreno R 等将钯与氧化铟复合,催化氢气作为还原剂的反硝化反应[12]。该研究是在室温下催化氢气还原硝酸根、亚硝酸根的反应,且还原效果很好。钯基氧化铟催化剂被负载于氧化铝上,这可以提高催化剂的整体稳定性。该催化过程也需要在酸性条件下进行,通过将二氧化碳与氢气一起通入水中的方法,达到降低溶液pH 值的效果。将H2用作还原剂不会产生二次污染,因此该处理工艺受到了研究者们的密切关注。
2 反应动力学及反应机理
对于负载型过渡金属催化剂多相催化反应,反应物质会在负载型过渡金属催化剂表面发生一系列的反应,这些过程包括扩散、吸附、物质传输和化学反应、脱附等,过程中的每个步骤都有概率成为催化反应速度控制步骤。因此,我们需要花费时间和精力对负载型过渡金属催化剂催化还原硝酸盐氮反应动力学和机理做进一步研究,以此来提高负载型过渡金属催化剂催化还原硝酸盐氮的选择性。
目前,研究者关于负载型过渡金属催化剂催化还原硝酸盐氮的动力学研究主要将目光汇集在使用粉末状Pd-Cu 双金属负载于氧化铝上。Vorlop 等人使用粉末状Pd-Cu 双金属催化剂提出硝酸盐氮催化还原的过程方程,整个催化过程符合兰格缪尔-修斯伍德(L-H)理论[9]。Pintar 等人按照该机理推导出负载型过渡金属催化剂催化还原水中硝酸盐氮的动力学方程(3),后续实验进行了验证[13]。
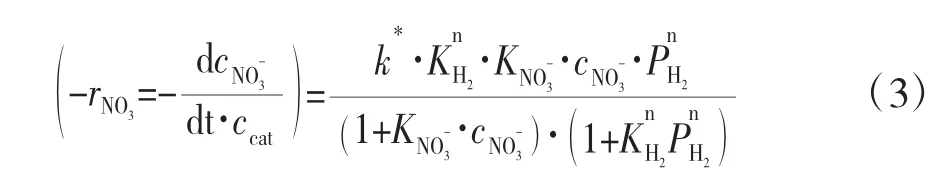
Prusse 等[14]提出了PbMe(其中Me 代表金属助剂)负载型过渡金属催化剂催化还原硝酸盐氮过程的反应机理假说。如图2 所示,该假说认为:负载型过渡金属催化剂表面负载着由PbMe 双金属混合簇团和纯Pb 单金属簇团构成的微小晶粒,还原剂被吸附在Pb 单金属催化剂上成为吸附态还原剂,并向Pb单金属催化剂上的氮元素中间价态物质传递H,硝酸盐氮的还原活性由PbMe 双金属催化剂决定,硝酸盐氮吸附在PbMe 催化剂表面被催化还原成亚硝态氮,亚硝态氮在Pb 催化作用下还原成NO,两个NO 分子进一步结合形成N2;若NO 与吸附态H 相遇时,则会生成N。

图2 负载型过渡金属催化剂催化还原硝酸盐氮过程的反应机理Fig.2 Reaction mechanism of the catalytic reduction of nitrate nitrogen by loaded transition metal catalysts
Prüsse 等[15]使用Pd-Cu、Pd-Sn、Pd-In 三种不同的双金属负载于Al2O3上,以氢气和甲酸分别作为还原剂催化还原硝酸盐氮,研究了该反应机理。作者研究认为负载型过渡金属催化剂表面具有催化活性的金属存在两种形式:一种是纯Pd 单金属微晶;另一种是双金属混合微晶,它们在惰性载体表面均匀分布。该研究表明Pd-Sn/Al2O3和Pd-In/Al2O3与Pd-Cu/Al2O3相比,催化剂催化还原硝酸盐氮的选择性增加。单金属微晶Pd 不能对N产生吸附,N只能在双金属混合微晶表面发生吸附,N被催化还原为N,而生成的N无法在双金属混合微晶催化剂表面还原为低价态的含氮化合物,需要先进行脱附后再被单金属Pd 微晶吸附进一步被还原。
3 负载型过渡金属催化剂催化还原硝酸盐氮的影响因素
负载型过渡金属催化剂催化还原硝酸盐氮的影响因素很多,包括主催化剂与助催化剂、负载材料、催化剂载量和硝酸盐氮浓度以及反应体系pH 值等。
3.1 主催化剂与助催化剂对催化反应的影响
主催化剂与助催化剂的选择是负载型过渡金属催化剂研制的最为紧要的步骤,既要保证负载型过渡金属催化剂有较高的活性催化还原硝酸盐氮,又要尽量避免等副产物的生成。
Yun 等[16]考察研究了以Al2O3为载体上几种主金属催化剂对的催化加氢性能,其催化还原活性次序为Pd(5%)>Rh(5%)>Ir(2%)>Ru(2%);催化还原选择性次序为Pd(5%)>Ru(2%)>Ir(2%)>Rh(5%)。由此可见,Pd 对的催化加氢有较高的活性和选择性。Fuentes 等[17]的研究表明,主金属催化剂Pd 的活性中心可以对产生强有力的吸附,而Pd 的活性中心附近的吸附态氢原子可以将还原生成NO 和N2O,最终生成N2。
助催化剂是负载型过渡金属催化剂的辅助添加成分,它通过使主金属催化剂的形态和结构发生改变,来间接影响负载型过渡金属催化剂的活性和选择性。常见的助催化剂有Ag、Fe、Hg、Ni、Cu、Zn、Sn、In 等。Huang 等[18]将Pd 作为主催化剂,Fe 作为助催化剂,金属Pd 与助金属Fe 之间有很强的作用力,且有生成PdFe 合金的可能性。在弱酸性条件下PdFe对硝酸盐氮、亚硝酸盐氮催化还原效果良好。表1 记录了负载型过渡金属催化剂的不同金属组合在催化还原硝酸盐氮过程中的活性和选择性。
表1 负载型过渡金属催化剂的不同金属组合在还原N过程中的活性和选择性Table 1 Activity and selectivity of different metal combinations of loaded transition metal catalysts in the reduction of N
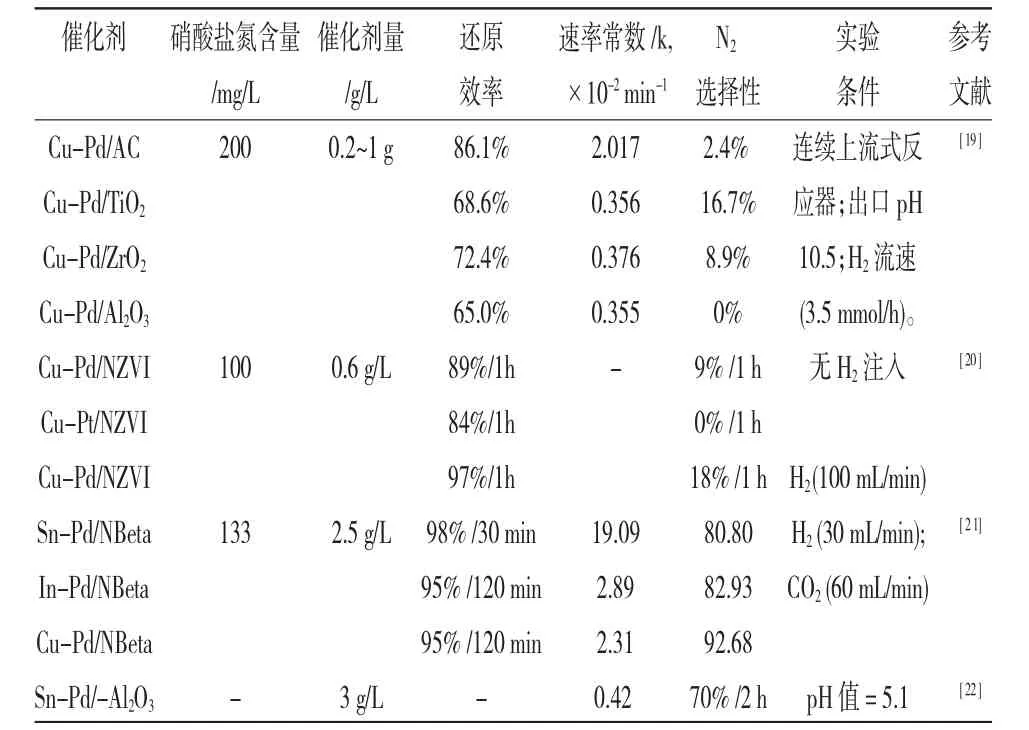
表1 负载型过渡金属催化剂的不同金属组合在还原N过程中的活性和选择性Table 1 Activity and selectivity of different metal combinations of loaded transition metal catalysts in the reduction of N
催化剂N2参考文献Cu-Pd/AC Cu-Pd/TiO2 Cu-Pd/ZrO2 Cu-Pd/Al2O3 Cu-Pd/NZVI Cu-Pt/NZVI Cu-Pd/NZVI Sn-Pd/NBeta In-Pd/NBeta Cu-Pd/NBeta Sn-Pd/-Al2O3硝酸盐氮含量/mg/L 200催化剂量/g/L 0.2~1 g [19]100 0.6 g/L速率常数/k,×10-2 min-1 2.017 0.356 0.376 0.355-实验条件连续上流式反应器;出口pH 10.5;H2 流速(3.5 mmol/h)。无H2 注入[20]133 2.5 g/L H2(100 mL/min)H2(30 mL/min);CO2(60 mL/min)[21]-3 g/L还原效率86.1%68.6%72.4%65.0%89%/1h 84%/1h 97%/1h 98%/30 min 95%/120 min 95%/120 min-19.09 2.89 2.31 0.42选择性2.4%16.7%8.9%0%9%/1 h 0%/1 h 18%/1 h 80.80 82.93 92.68 70%/2 h pH 值=5.1[22]
3.2 负载材料的影响
在前人的工作中[19~22],我们可以知道两种不同的负载型过渡金属催化剂使用了相同的主催化剂和助催化剂,但由于是使用了不同的负载材料达到了不同的实验目标。这种现象表明负载材料可以对负载型过渡金属催化剂催化还原N的活性和选择性产生显著影响。Sakamoto 等[19]的研究结果表明,Cu-Pd/AC(活性炭)催化剂与其他载体(TiO2、ZrO2、Al2O3)相比具有较高的N去除率(86.1%),但是Cu-Pd/TiO2表现出更好的N2选择性(16.7%),但N去除率仅为68.6%。此外,当Cu 和Pd 用作主催化剂时,NZVI 载体对N的还原显示出非常快的还原效率(>97%in 30min),但对N的还原成N2没有显示出最高的选择性(仅18%,表1)[20]。另一方面,Hamid 等[22]提出带有Cu 和Pd 的NBeta- 沸石负载双金属催化剂在120min 内去除了95%的N,对N2的选择性为92.68%(表1)。
负载材料的性质(表面积、孔隙率等)也会影响负载型过渡金属催化剂催化还原N的性能。Hao和Zhang[22]表明了负载材料表面积和孔隙率对催化性能的重要性。在研究中,以γ-Al2O3-Diato 为载体的催化剂因为存在高孔隙率和大表面积,而表现出最佳的催化活性和N2选择性[22]。此外,Chaplin 等人[23]发现在负载材料的表面存在较多的低配位点,这会使N-N 成键的可能性降低,从而降低对N2的选择性。
Miyazaki 等人[24]研究了有无负载材料过渡金属催化剂对催化还原硝酸盐氮的影响。研究发现,较大金属粒径(2.5~5 nm)的负载型和非负载型催化剂在将N还原为N时显示出相似的反应速率常数,但是金属颗粒越大,负载材料的增益越小。而较小颗粒(1.4~2.5 nm)催化剂的反应速率常数是不同的。与较大金属颗粒相比,较小金属颗粒的反应动力学受负载材料的影响更显著。因此,负载材料和金属颗粒都会对催化剂的活性和选择性产生影响。Fuentes 等[17]制备了钯铜双金属催化剂,铜可提高催化过程中电子转移效率。该催化剂被负载于活性碳上,在没有化学还原剂存在的情况下,依旧可以催化硝酸盐氮的还原。
3.3 催化剂载量和硝酸盐氮浓度的影响
催化剂载量和硝酸盐氮浓度会显著影响硝酸盐氮的催化还原,且催化剂载量越高,同浓度N去除率越高。例如,当Cu-Pd/TiO2催化剂的金属载量从3 %(wt)升到20%(wt)时,Zhang 等[25]观察到N去除效率由82%增加到100%。Gao 等[26]发现负载型过渡金属催化剂金属颗粒分散程度对N的还原作用尤为显著。虽然在低催化剂负载下观察到速率增加,但随着催化剂浓度的进一步增加[27],这种增加之后会出现一个平台期,并且在整个反应过程中N的初始特定去除率是恒定的,Mortazavi等[28]推测可能是由于N的固定浓度所导致的。
催化剂负载也对选择性有影响。从大量研究中可以明显看出[29,30],对N的选择性通常随着催化剂载量而增加。例如,随着Cu-Pd/NZVI 催化剂的浓度从0.125 g 增加到0.500 g,更多的N转化为N[31]。在4 g/L 时,沸石作为负载材料的催化剂N的选择性达到最大值,然后在更高的催化剂剂量下保持不变[29]。此外,对于Cu-Pd/Al2O3催化剂N的选择性随着其载量从0.5 增到2g 时趋于降低[31]。
3.4 反应体系pH 值的影响
负载型过渡金属催化剂的反应体系pH 值也对硝酸盐氮的活性和选择性有明显影响。当Cu-Pd/NZVI催化剂悬浮液中的pH 值从4 增加到10 时,其还原N的动力学速率常数将会从从0.0007 减少到0.0003 M-1min-1[34],原因可能是由于催化剂的表面形成了钝化氧化铁层。但它能在酸性条件下溶解,使NZVI活性位点再次暴露而使N去除率增加[34,35]。酸性条件还增加了H2的生成,进一步促进N的还原[15]。负载型过渡金属催化剂的反应体系对pH 值的依赖性随着pH 值先降后升。
最佳pH 值由催化剂类型决定。Pd-In/Al2O3的最佳pH 值为6,而Pd-Sn/Al2O3的最佳pH 值为4[15]。不同最佳pH 值的助催化剂金属最大去除率是由催化剂表面所带电荷决定的。这决定了在不同的最佳pH 值下,在催化剂表面可吸附的N最大量。随着
但是一些催化剂不受反应体系pH 变化的影响,包括Fe0、Cu-Fe 和Mn-Fe,或NaY-zeolite 负载的催化剂。在pH 值(3.0~9.0)的范围内,随着悬浮液pH 值的增加,负载型过渡金属催化剂的活性和选择性保持稳定。在pH 值为3.0 时,所有三种负载型过渡金属催化剂的N去除率均高于97%,在pH 值为9.0 时没有显著变化,仍然保持较高去除率(>94%)。N的形成也没有明显变化,表明pH 值对三种催化剂的选择性没有明显影响[30]。
