新型冠状病毒疫苗接种后免疫球蛋白抗体检测结果分析
2021-12-17王宁吕金娥张丽晶李娅萍陶然
王宁 吕金娥 张丽晶 李娅萍 陶然
新型冠状病毒肺炎(新冠肺炎)是由新发病原体新型冠状病毒(2019 novel coronavirus,2019-nCoV)引起的以肺炎为主要表现的感染性疾病,由世界卫生组织(World Health Organization,WHO)命名为“coronavirus disease 2019(COVID-19)”[1]。2019-nCoV主要通过呼吸道飞沫传播以及特定条件下的气溶胶传播,消化道等传播途径尚待明确[2]。作为一种新出现的疾病,新冠肺炎因其传染性较强而被广泛关注,且针对该疾病目前尚无特效药物[3]。自2019年12月以来,新冠肺炎在全球范围内蔓延,目前我国已将其纳入《中华人民共和国传染病防治法》规定的乙类传染病,并采取甲类传染病的预防、控制措施。2019-nCoV疫苗接种能预防新冠肺炎,形成群体免疫[4]。2020年4月,中国医学科学院研究团队发表了关于一种在研2019-nCoV疫苗“PiCoVacc”在动物实验中具有免疫原性及保护作用的研究结果[5]。巴西圣保罗州政府于当地时间2021年1月12日公布了北京科兴中维生物技术有限公司2019-nCoV灭活疫苗的Ⅲ期临床试验结果,该疫苗对新冠肺炎重症和住院的保护效力为100.0%,对需要医疗救治的轻症保护效力为78.0%,总体保护效力为50.4%。2019-nCoV核酸检测使用荧光探针反转录-聚合酶链反应(reverse transcription polymerase chain reaction,RT-PCR)检测2019-nCoV的ORFIab、E、N 3个靶标,具有快速、简便、成本低、特异性高等特点。机体被病毒感染后,可通过体液免疫应答反应产生病毒抗原特异性抗体,2019-nCoV免疫球蛋白(immunoglobulin,IgM和IgG)抗体检测有助于新冠肺炎的辅助诊断、近期或既往感染的鉴别以及疗效判断[6]。医院是疫情防控的重点部门,对医务人员以及相关后勤保障人员进行全面的2019-nCoV核酸检测和抗体检测非常必要[7]。本研究对接种2针2019-nCoV疫苗1个月后的150名医务人员进行IgM、IgG抗体检测,比较阳性率,现报告如下。
1 资料与方法
1.1 研究对象与一般资料 将2021年1月12日—3月20日接种2019-nCoV疫苗(2针)的本院150名医务人员作为研究对象,其中男性组21名,女性组129名;年龄22~55岁,平均(36.36±8.39)岁。将疫苗接种者根据年龄分为两组,即<35岁组(82名)和≥35岁组(68名)。本研究符合医学伦理学标准,并经本院伦理批准(审批号:2021-800),对研究对象进行的检测均获得过知情同意。
1.2 检测方法 采集所有疫苗接种者空腹静脉血3~5 mL,以3 500 r/min(离心半径为13.5 cm)离心10 min,分离血清后尽快检验。IgM、IgG抗体检测采用磁微粒化学发光法,使用安图AutoLumo A2000 Plus全自动化学发光测定仪,检测试剂由郑州安图生物工程股份有限公司提供。
1.3 结果判定 采用试剂盒检测206份血液样本,通过绘制受试者工作特征曲线(receiver operator characteristic curve,ROC)进行统计分析,取其约登指数最高点(敏感度89%,特异度100%)确定阳性临界值系数为0.2,即阳性判断值(cut-off值)=阳性对照孔平均发光值×0.2。S/CO=待测样本发光值/Cut off值,其中S为样本在试剂溶液中的发光值,CO为阳性临界值。S/CO≥1.00时,结果判定为阳性;S/CO<1.00时,结果判定为阴性。S/CO在0.80~1.20时,结果判定为可疑样本。
1.4 统计学方法 采用SPSS 15.0和R 3.6.2统计软件处理数据,正态分布的计量资料以均数±标准差(±s)表示,组间比较采用t检验;计数资料以构成比或率(%)表示,组间比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 IgM、IgG抗体检测结果 150名接种者中,IgM抗体阳性34例,弱阳性6例,阳性率为26.67%;IgG抗体阳性131例,弱阳性6例,阳性率为91.33%。见表1。IgM与IgG抗体同时阴性13例,阴性率为8.67%;IgM和IgG抗体同时阳性或弱阳性40例,阳性率为26.67%;IgG和IgM抗体至少1项阳性或弱阳性137例,阳性率为91.33%。见表2。抗体检测结果马赛克图见图1。

表1 150名2019-nCoV疫苗接种者的基本情况以及IgM、IgG检测结果
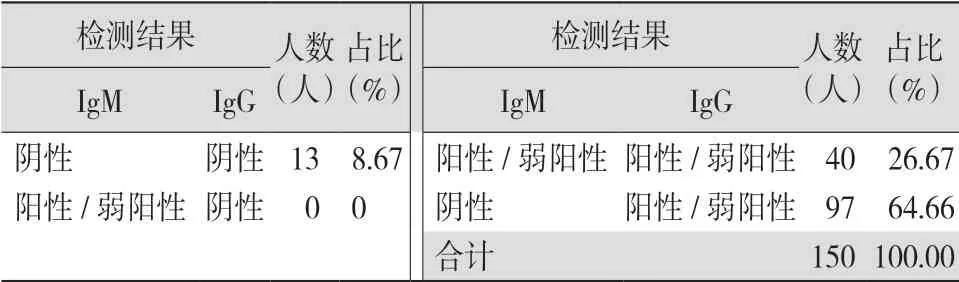
表2 150名2019-nCoV疫苗接种者IgM、IgG抗体检测

图1 新型冠状病毒疫苗接种者的免疫球蛋白(IgG、IgM)抗体检测结果马赛克比例图
2.2 不同性别接种者IgM、IgG抗体阳性率比较男性组(21名)和女性组(129名)年龄比较差异无统计学意义(P>0.05);IgG和IgM抗体检测阳性率比较差异亦均无统计学意义(均P>0.05)。见表3。
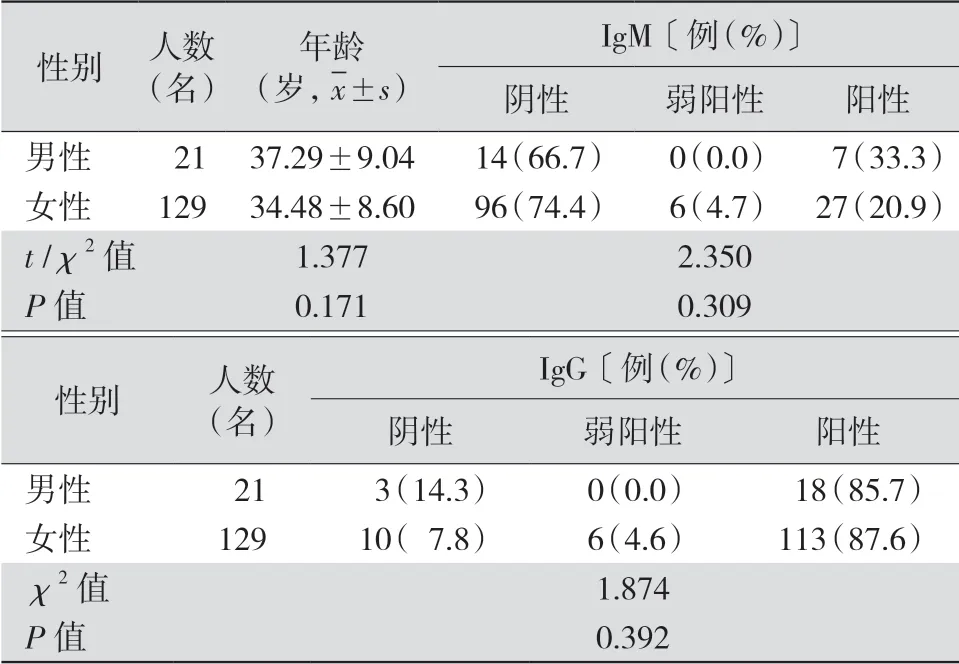
表3 男性组与女性组血清IgM、IgG抗体检测结果比较
2.3 不同年龄接种者IgM、IgG抗体阳性率比较<35岁组(82名)和≥35岁组(68名)人群的性别构成比较差异无统计学意义(P>0.05);IgG和IgM抗体检测阳性率比较差异均无统计学意义(均P>0.05)。见表4。
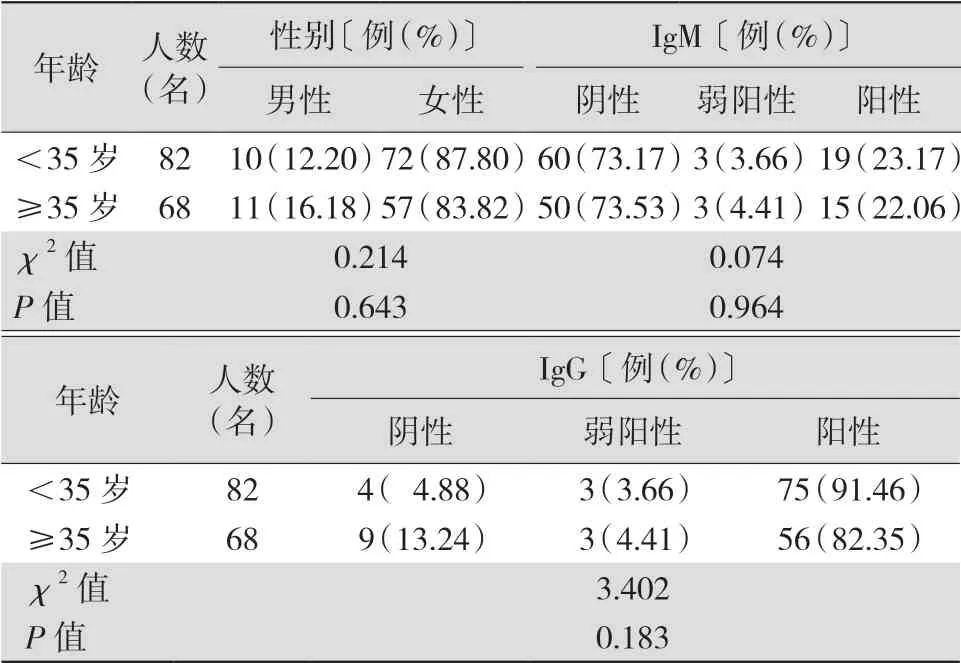
表4 不同年龄组间IgM、IgG抗体检测结果比较
2.4 IgM、IgG抗体同时阳性情况分析 IgG与IgM抗体检测同时阴性的接种者为13例,同时阳性的接种者为40例,两组人群性别构成比较差异无统计学意义(P>0.05),年龄比较差异亦无统计学意义(P>0.05)。见表5。IgG和IgM抗体同时阳性者40例,单独IgG抗体检测阳性者97例,两组人群性别构成比较差异无统计学意义(P>0.05),年龄比较差异亦无统计学意义(P>0.05)。见表6。

表5 IgM、IgG同时阳性组与IgM、IgG同时阴性组资料比较
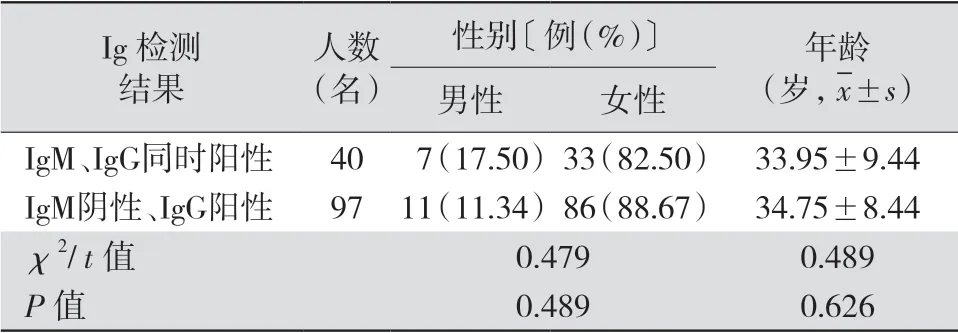
表6 IgM、IgG同时阳性组与IgM阴性、IgG阳性组资料比较
3 讨论
2019年12月,新冠肺炎疫情暴发,目前已蔓延全球多个国家和地区。作为公共卫生事业基础的疫苗接种至关重要,有助于形成真正有效的群体免疫力[8]。群体免疫是指当人群中对某种传染病具备免疫力的人数达到一定比例时,整个人群能形成一道免疫屏障,即使一个或多个传染源进入社区人群,也不会发生大规模的疾病暴发流行[9]。根据新冠肺炎的基本传播指数R0值测算,人群中需要47%~85%的人感染或接种有效疫苗,才能达到群体免疫的保护效果[10]。2019-nCoV疫苗开发种类主要包括灭活疫苗、减毒活疫苗、病毒样颗粒疫苗、亚单位疫苗、非复制病毒载体疫苗、复制病毒载体疫苗、DNA疫苗和RNA疫苗[11]。中国目前获得国家药品监督管理局批准注册申请的有国药集团中国生物北京生物制品研究所新冠病毒灭活疫苗、北京科兴中维生物技术有限公司新冠病毒灭活疫苗、国药集团中国生物武汉生物制品研究所新冠病毒灭活疫苗和康希诺生物股份有限公司腺病毒载体新冠病毒疫苗。根据国家卫生健康委官网,截至2021年5月13日,31个省(市、自治区)及新疆生产建设兵团累计报告接种2019-nCoV疫苗36 691.0万剂次。
本院医务人员注射的2019-nCoV疫苗均为国药集团中国生物北京生物制品研究所2019-nCoV灭活疫苗或北京科兴中维生物技术有限公司生产的2019-nCoV灭活疫苗。灭活疫苗是将体外培养的病毒灭活和纯化获得,为致病性丧失或减弱的完整病毒,但保持病毒的全部或部分免疫原性,接种后病毒抗原可以刺激机体产生免疫应答,达到保护作用。新冠疫苗接种后2019-nCoV主要依靠病毒的表面膜刺突蛋白受体结合域(S1-receptor binding domain,S1-RBD)与人体细胞血管紧张素转换酶2(angiotensinconverting enzyme 2,ACE2)受体结合而侵染细胞,人体免疫系统被病毒或疫苗刺激后产生的特定抗体(主要为抗-RBD)能与病毒的S1-RBD结合,从而阻断病毒侵染人体细胞的途径,这类特定抗体就是中和抗体。中国医学科学院在研2019-nCoV灭活疫苗“PiCoVacc”的Ⅲ期临床试验于2020年7月16日启动,分析数据显示PiCoVacc接种后安全性良好,接种者均产生高滴度抗体,中和抗体阳性率为99.52%,保护效率达79.34%。
机体被2019-nCoV感染后,可通过体液免疫应答反应产生病毒抗原特异性抗体,IgM抗体是人体感染2019-nCoV后最早产生的抗体,其水平随病情进展而升高。患者经有效治疗后,IgM抗体逐渐消失,而IgG抗体逐渐增多[6]。因此,IgM、IgG抗体检测有助于新冠肺炎的辅助诊断、对近期或既往感染的鉴别以及疗效判断[6]。本研究对本院医务人员接种2019-nCoV疫苗(2针剂)1个月后进行IgM、IgG抗体检测,结果显示IgM、IgG抗体同时阴性13例,阴性率为8.67%;IgM、IgG抗体同时阳性或弱阳性40例,IgM抗体阳性率为26.67%,IgG抗体阳性131例,弱阳性6例,阳性率为91.33%。上海市卫生健康委发布的2019-nCoV疫苗接种报告显示:接种灭活疫苗第1剂后7 d普遍开始产生抗体,14~28 d抗体阳性率约60%~90%接种第2剂28 d后抗体阳性率均达到90%以上[12],与本研究结果一致。
疫苗并不能让所有接种人群产生免疫,其原因复杂,与遗传和免疫因素、疫苗本身质量及疫苗的运输、储存、接种操作等均有关[13]。云南省曲靖市自2019年12月以来为新冠肺炎疫情低风险地区,共确诊13例新冠肺炎患者,均为省外输入型病例,未出现过新冠肺炎本土病例。本院为普通综合医院,非新冠肺炎定点收治医院,未诊断、收治过新冠肺炎患者,排除150名医务人员既往感染过新冠肺炎,可以明确IgM、IgG抗体阳性为2019-nCoV疫苗接种后产生的抗体。而能否用IgM、IgG抗体检测替代疫苗中和抗体检测有待疫苗研发团队进一步验证。
2019-nCoV抗体检测自2020年3月《新型冠状病毒肺炎诊疗方案(试行第七版)》[14]中加入,可辅助核酸诊断,用于核酸检测阴性的疑似病例的补充检测或在疑似病例诊断中与核酸检测协同使用。病毒抗体检测方便、快速、价廉、易推广,目前有数十种试剂盒获国家药监局审批市售。《新冠病毒疫苗接种技术指南(第一版)》[15]中说明,在疫苗接种前无需开展2019-nCoV核酸及抗体检测;接种后也不建议常规检测抗体作为免疫成功与否的判断依据。2019-nCoV中和抗体检测目前仅在疫苗研发机构中进行,未能在医疗机构推广普及,且目前并无取得医疗器械注册证的中和抗体检测试剂,若能用IgM、IgG抗体检测作为2019-nCoV疫苗接种成功的实验室检测依据,将大大提高群众对疫苗接种的积极性,也将消除部分人群认为疫苗无效而抗拒接种的心理,为我国快速、有效推进疫苗接种工作起到积极的作用,同时尽快形成群体免疫,在国内甚至世界范围内筑起新冠肺炎免疫屏障。
利益冲突所有作者均声明不存在利益冲突
