316L不锈钢、ND钢和Q245R 钢的耐酸露点腐蚀性能
2021-12-17何萌康昊源陈昇曹逻炜薛俊鹏谢国山
何萌,康昊源,陈昇,曹逻炜,薛俊鹏,谢国山
(1.中国特种设备检测研究院,北京 100029;2.安工腐蚀检测实验室科技(无锡)有限公司,无锡 214028)
酸露点腐蚀是化工行业生产过程中长期存在的问题,常发生在燃煤、天然气、重油和减压渣油等燃料加热炉和锅炉、燃烧塑胶类物质的垃圾焚化炉等装置中[1-2]。这些燃料中常含有硫和氯等元素,燃烧过程中会生成SO2和HCl气体,其中部分SO2在一定条件下会继续转化为SO3[3]。SO3和HCl气体容易与烟气中的水蒸气结合,导致烟气露点温度大幅度提升。当硫酸和盐酸蒸汽与低于露点温度的设备表面接触时,高浓度的酸性液滴会发生凝结,造成设备严重的酸露点腐蚀和氯离子应力腐蚀开裂,如锅炉排烟系统的烟道、省煤器、余热锅炉和空气预热器等低温设备常发生此类腐蚀[4]。
面对日益突出的酸露点腐蚀问题,常用的防护方法有:控制燃料中硫和氯的含量,控制过量空气系数,适当提高设备壁温[5],选择耐蚀涂层、耐酸露点腐蚀用钢等。近年来,ND 钢(09Cr CuSb)广泛应用于控制设备的酸露点腐蚀[6-7],其中的Cr、Cu和Sb元素能在酸露点腐蚀过程中形成致密的钝化膜,从而降低基体的腐蚀速率[8-9]。316L 不锈钢由于含有质量分数为2%~3%的Mo,具有良好的耐硫酸腐蚀和耐Cl-腐蚀性能。Q245R 钢是压力容器常用钢,耐蚀性不突出,但由于其价格低于不锈钢的,在许多行业仍被作为首选材料[10]。
目前,ND 钢和316L不锈钢耐酸露点腐蚀性能的强弱仍不明确。大多数研究认为ND 钢比316L不锈钢具有更好的耐蚀性,如顾国亮等[11]研究了ND 钢、316L不锈钢和20 号碳钢在硫酸介质中的腐蚀情况,得出ND 钢耐硫酸腐蚀性能最优。但一些研究结论却相反,张知翔等[12]利用新型试验装置研究了ND 钢、Corten钢和316L 不锈钢的腐蚀特性,结果表明316L 不锈钢比ND 钢更耐硫酸露点腐蚀。另外,现有的酸露点腐蚀研究大多数采用单一的硫酸溶液或盐酸溶液[13-14],没有考虑到多组分烟气的协同作用,因此无法反映实际工作中金属发生酸露点腐蚀的情况。
本工作在模拟工业多组分酸露点腐蚀环境中,利用失重法、极化曲线和循环极化测试,对比研究了Q245R 钢、ND 钢和316L 不锈钢的腐蚀行为,分析了三种材料在不同温度、氯离子质量浓度和硫酸质量分数下的腐蚀行为及机理,以期为酸露点腐蚀环境中设备的选材提供数据和理论支撑。
1 试验
1.1 试样
试验材料为ND 钢、316L 不锈钢和Q245R 钢,其化学成分如表1所示。
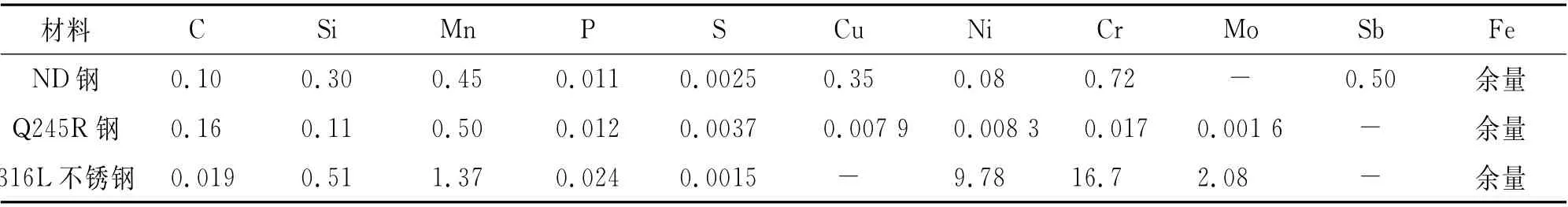
表1 ND钢、316L不锈钢和Q245R 钢的化学成分(质量分数)Tab.1 The chemical composition of ND steel,316L stainless steel and Q245R steel(mass fraction)%
1.2 试验方法
采用浸泡试验和电化学测试研究316L 不锈钢、ND钢和Q245R钢三种材料在酸露点腐蚀模拟溶液中的腐蚀特性。其中,浸泡试验参照GB 10124-1988《金属材料实验室均匀腐蚀全浸试验方法》,电化学测试方法参照ASTM G3-2014《腐蚀检验中使用的电化学测量用常规的实践规程》和ASTM G5-2014《进行电动位阳极极化测量的标准参考试验方法》。
1.2.1 浸泡试验
化工设备中酸露点腐蚀发生在几十摄氏度到一百几十摄氏度之间。当烟气中的水蒸气质量分数达到10%时,冷凝液滴中的硫酸含量最高可达93%(质量分数)[9],且燃料中氯含量不同也会导致冷凝液滴中盐酸含量的变化。为模拟化工设备的实际腐蚀情况,配置硫酸溶液以及硫酸和Cl-混合溶液作为酸露点腐蚀介质,试验条件设置见表2。
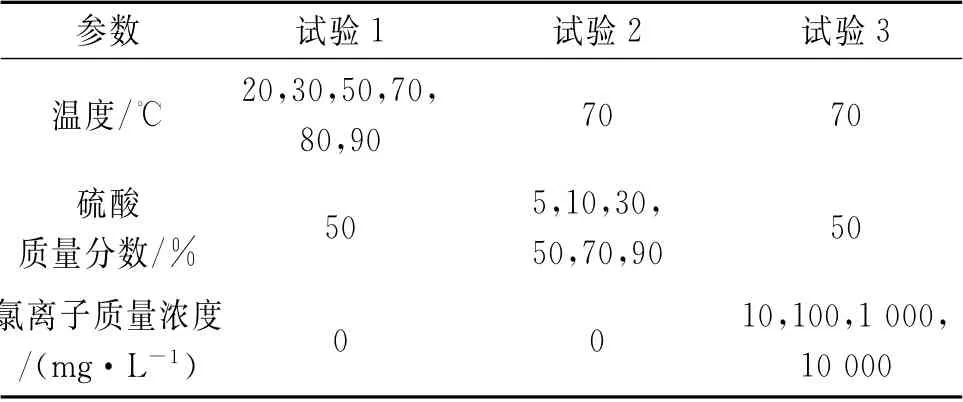
表2 浸泡试验的条件设置Tab.2 Condition setting of immersion test
采用失重法[15]计算ND 钢、316L 不锈钢和Q245R 钢三种材料在酸露点腐蚀模拟溶液中的腐蚀速率,见式(1)[15-16],研究硫酸含量、Cl-含量和温度对腐蚀速率的影响,试验周期为6 h。每种材料重复三次试验,由于重复试验结果差距都较小,仅对其中两次试验的试样进行称量,计算其腐蚀速率并做误差分析,最大相对误差为2.6%。
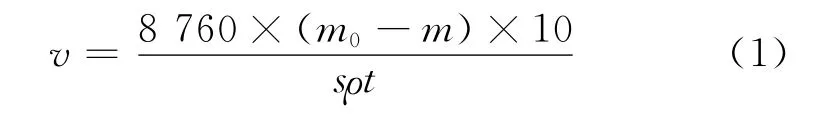
式中:v为试片的平均腐蚀速率,mm/a;m0为试验前试片的质量,g;m为试验后试片的质量,g;s为试片的工作面积,cm2;ρ为试片的密度,g/cm3;t为试片的浸泡时间,h。
1.2.2 电化学测试
电化学测试采用三电极体系,待测试样为工作电极,暴露面积1 cm2,铂片为辅助电极,银/氯化银电极为参比电极,测试仪器为电化学工作站Gamry Interface 1000。配置硫酸和Cl-混合溶液作为酸露点腐蚀模拟溶液,试验条件设置见表3。
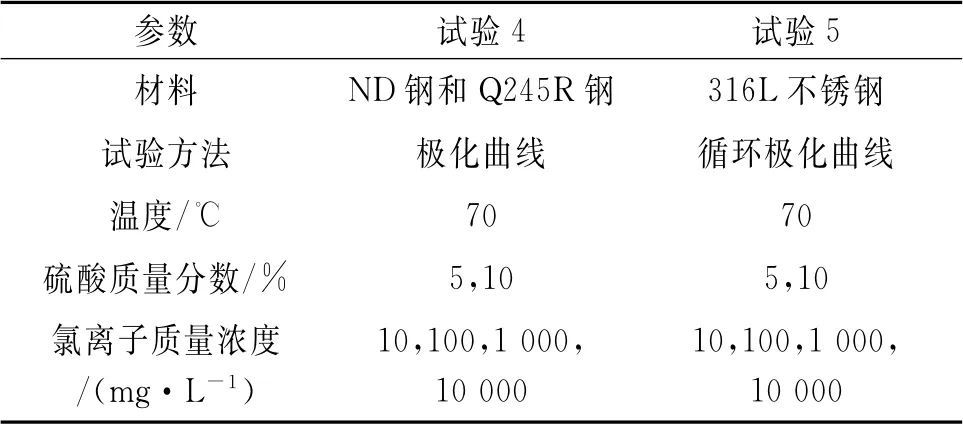
表3 电化学测试的条件设置Tab.3 Condition setting of electrochemical test
采用极化曲线考察5%和10% H2SO4溶液中,Cl-质量浓度对Q245R 钢和ND 钢腐蚀行为的影响;采用循环极化曲线考察5%和10% H2SO4溶液中,Cl-质量浓度对316L不锈钢腐蚀行为的影响。
2 结果与讨论
2.1 浸泡试验
2.1.1 温度对腐蚀速率的影响
由图1可知,Q245R 钢的腐蚀速率随溶液温度的升高呈先增大后减小的趋势,温度为50 ℃和70 ℃时,其腐蚀速率达到最大值,Q245钢完全溶解于溶液中;当温度为80 ℃和90 ℃时,Q245R 钢的腐蚀速率明显受到抑制,可能是因为温度过高导致硫酸溶液浓缩且没有及时补充溶剂,Q245R 钢表面生成致密的氧化膜,阻碍了基体腐蚀。ND 钢的腐蚀速率随温度的升高变化并不明显,其腐蚀速率均低于Q245R 钢和316L 不锈钢的。这是因为在高含硫酸溶液中,ND 钢中的Cr、Cu和Sb元素在试样表面形成致密的钝化膜,从而抑制基体腐蚀。316L不锈钢的腐蚀速率随温度的升高而增大,在低温段(20~30 ℃),其腐蚀速率增加较慢,当温度超过50 ℃时,其腐蚀速率迅速增大,在90 ℃时达到最大值,试样完全溶解于溶液中。原因是温度的升高,加快了溶液中氢离子的扩散,从而加速腐蚀。
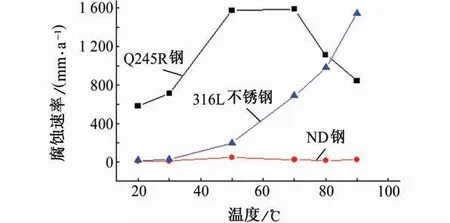
图1 三种材料在不同温度50%硫酸溶液中浸泡6 h的腐蚀速率Fig.1 The corrosion rate of the three materials immersed in 50%sulfuric acid solution for 6 h at different temperatures
由图2 可知,试验后Q245R 钢全部溶解,ND钢表面发生轻微的均匀腐蚀,已无金属光泽,但边缘仍平整光滑,且试样尺寸没有明显变化。与ND 钢相比,316L不锈钢表面均匀腐蚀痕迹更明显,表面粗糙不平,边缘出现大量缺陷,尺寸略有减小。三种材料的腐蚀情况与图1的腐蚀速率相吻合。

图2 在70 ℃、50%硫酸溶液中浸泡6 h前后三种材料的宏观腐蚀形貌Fig.2 Macroscopic corrosion morphology of the three materials before(a-c)and after(d-e)immersing in 50%sulfuric acid solution at 70 ℃for 6 h
2.1.2 硫酸含量对腐蚀速率的影响
由图3可知,Q245R 钢和316L 不锈钢的腐蚀速率均随硫酸含量的升高呈先增大后减小的趋势。当硫酸质量分数为30%和50%时,两种材料的腐蚀速率均较高,此时Q245R 钢完全溶解于硫酸溶液中。当硫酸质量分数为5%和30%时,ND 钢的腐蚀速率较高。对比分析可知,在5%和10%硫酸溶液中,316L不锈钢的腐蚀速率最低;当硫酸质量分数超过10%后,三种材料的腐蚀速率按从大到小的顺序依次为:Q245R 钢、316L 不锈钢、ND 钢;当硫酸质量分数达到70%后,三种材料的腐蚀速率均处于较低水平,这是由于硫酸质量分数较高时表现出的强氧化性导致材料表面生成致密的钝化膜,降低了基体的腐蚀速率[10]。
由图4可知,在70℃、30%硫酸溶液中,Q245R钢全部溶解,ND 钢发生均匀腐蚀,表面腐蚀产物为黑色,无金属光泽,但其边缘仍平整光滑,尺寸略有减小;与ND 钢相比,316L 不锈钢表面的均匀腐蚀痕迹更加明显,表面粗糙不平,边缘出现大量的缺陷,尺寸略有减小。三种材料的腐蚀情况与图3中的腐蚀速率相吻合。
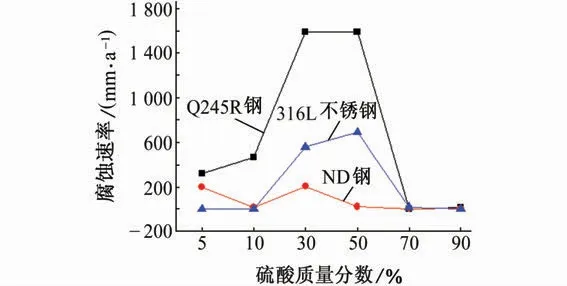
图3 在70 ℃不同浓度硫酸溶液中浸泡6 h三种材料的腐蚀速率Fig.3 The corrosion rate of the three materials immersed in sulfuric acid solution with different concentrations at 70 ℃for 6 h

图4 在70 ℃、30%的硫酸溶液中浸泡6 h前后三种材料的宏观腐蚀形貌Fig.4 Macroscopic corrosion morphology of the three materials before(a-c)and after(d-e)immersing in 30%sulfuric acid solution at 70 ℃for 6 h
2.1.3 Cl-质量浓度对腐蚀速率的影响
由图5可知,在不同Cl-质量浓度下Q245R钢的腐蚀速率均最高,且完全溶解于溶液中,故无腐蚀形貌;ND 钢的腐蚀速率较低,未表现出与Cl-质量浓度呈正相关或者负相关的规律;316L 不锈钢的腐蚀速率随Cl-质量浓度的升高呈明显的下降趋势,当Cl-质量浓度为10 000 mg/L 时,其腐蚀速率最低(18.3 mm/a)。在Cl-和SO42-共存的溶液中,金属表面的Cl-和SO42-为竞争吸附的关系[17-18],同时,Cl-和溶解氧也为竞争关系[19],316L 不锈钢的腐蚀行为可能是三种因素共同作用的结果。随着溶液中Cl-含量的升高,溶解氧含量减少,抑制了腐蚀的阴极去极化过程,减缓腐蚀的发生。另外,SO42-更易吸附在金属表面,排挤吸附在金属表面的Cl-,有效抑制Cl-的点蚀作用[20]。进一步考察了不同温度下该腐蚀环境中316L 不锈钢表面是否也存在Cl-和SO42-的竞争吸附关系,由图6可知,316L不锈钢的腐蚀速率随Cl-质量浓度的升高呈明显的下降趋势,说明不同温度下316L 不锈钢表面Cl-和SO42-也存在竞争吸附关系。
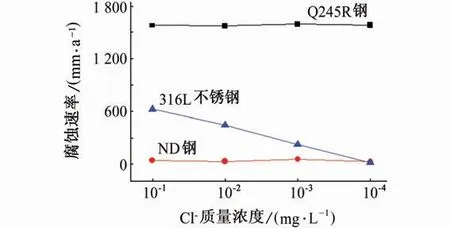
图5 在70 ℃、50%硫酸溶液(含不同量Cl-)中浸泡6 h三种材料的腐蚀速率随Cl-质量浓度的变化Fig.5 The corrosion rate of the three materials immersed in 70 ℃,50%sulfuric acid solution(containing different concentrations of Cl-)for 6 h
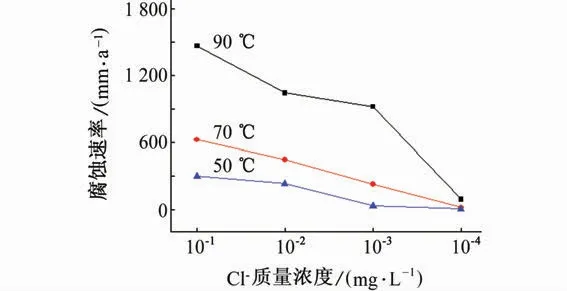
图6 316L不锈钢在不同温度50%硫酸溶液(含不同量Cl-)中浸泡6 h的腐蚀速率Fig.6 Corrosion rates of 316L stainless steel immersed in 50%sulfuric acid solution(containing different concentrations of Cl-)for 6 h at different temperatures
由图7 可知,在Cl-质量浓度为10 mg/L 的7 0℃、50%硫酸溶液中浸泡6 h后,Q245R钢已全部溶解,ND 钢虽失去金属光泽,但无明显腐蚀痕迹,其边缘仍平整光滑,尺寸几乎没有变化;316L 不锈钢表面出现大量的点蚀痕迹,其表面粗糙不平,尺寸略有减小。三种材料的腐蚀情况与图5中的腐蚀速率相吻合。

图7 在Cl-质量浓度为10 mg/L的70 ℃、50%硫酸溶液中浸泡6 h前后三种材料的宏观腐蚀形貌Fig.7 Macroscopic corrosion morphology of the three materials before(a-c)and after(d-e)immersing in 70 ℃,50%sulfuric acid solution with Cl- mass concentration of 10 mg/L for 6 h
2.2 电化学测试
2.2.1 Q245R 钢和ND 钢的极化曲线
由图8可知,Q245R 钢和ND 钢均存在极化曲线活化区,未发现活化-钝化转变的现象,阴极过程为H+去极化反应,阳极过程为Fe的溶解反应。
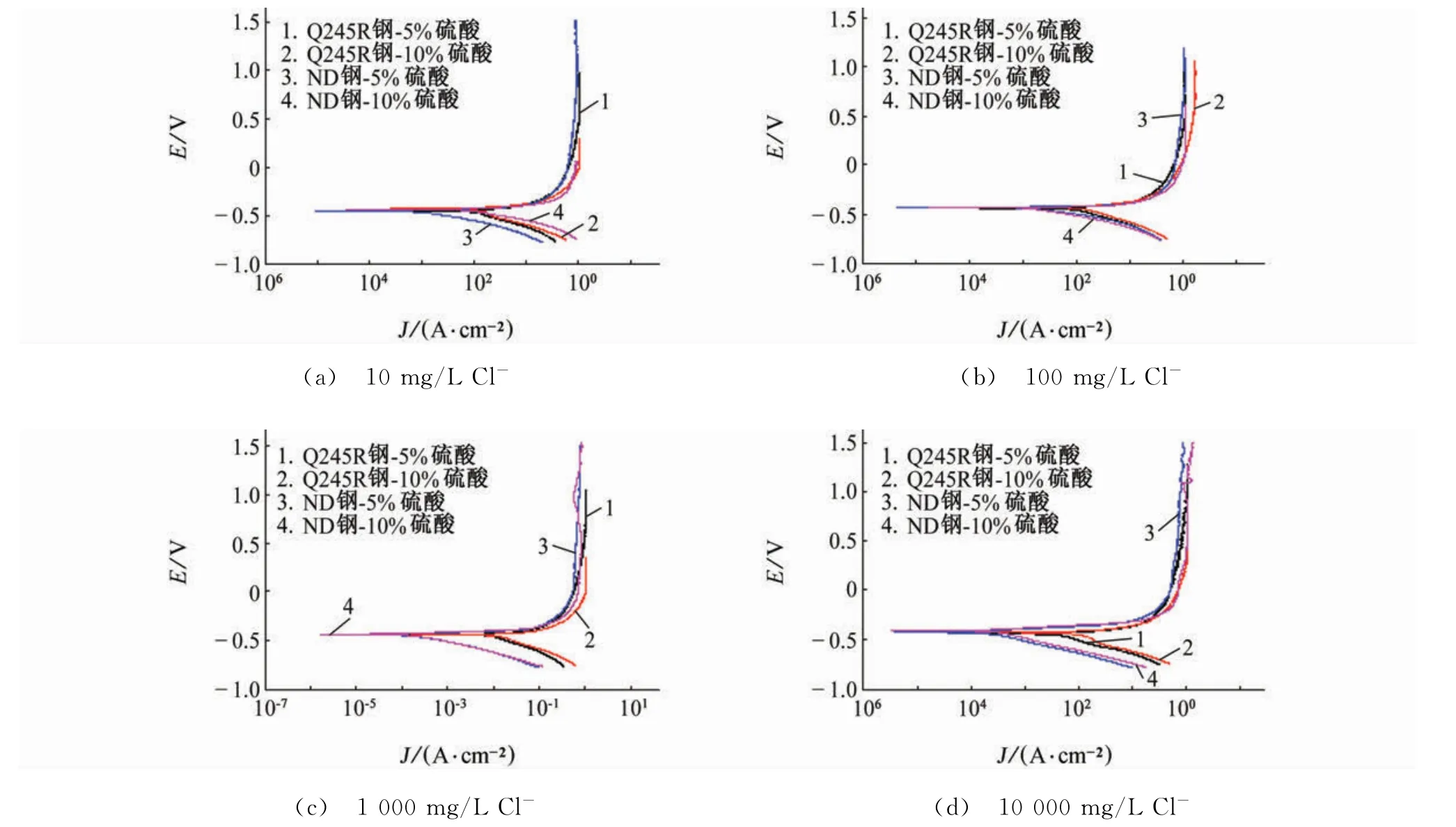
图8 在含不同量Cl-的5%和10%硫酸溶液中Q245R 钢和ND 钢的极化曲线Fig.8 Polarization curves of Q245R steel and ND steel in 5%and 10%sulfuric acid solutions with different concentrations of Cl-
由图9可知,在5%和10%硫酸溶液中,随Cl-质量浓度的升高,Q245R 钢和ND 钢的自腐蚀电流密度(Jcorr)均呈先增大后减小的趋势,说明其腐蚀速率也先增大后减小;当Cl-质量浓度逐渐升高至1 000 mg/L以上时,ND 钢自腐蚀电流密度的变化显著减小,表明腐蚀速率随Cl-质量浓度升高基本维持不变。在相同Cl-质量浓度的硫酸溶液中,ND钢的自腐蚀电流密度均小于Q245R 钢的,即ND 钢的腐蚀速率小于Q245R 钢的,且Q245R 钢和ND钢在10%硫酸溶液中的自腐蚀电流密度均大于在5%硫酸溶液中的。
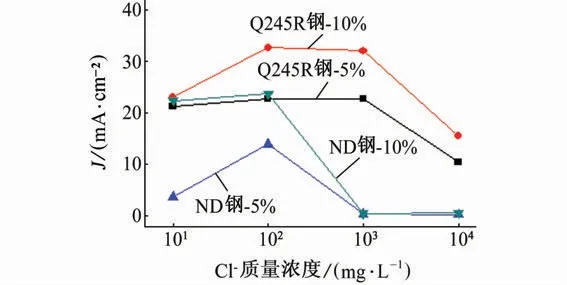
图9 在含不同量Cl-的5%和10%硫酸溶液中Q245R 钢和ND 钢的自腐蚀电流密度Fig.9 Free-corrosion current density of Q245R steel and ND steel in 5%and 10%sulfuric acid solutions with different concentrations of Cl-
此外,较低Cl-质量浓度下ND 钢的腐蚀速率接近Q245R 钢的,与上文中浸泡试验结果存在差异。这是因为浸泡试验中硫酸质量分数高达50%,具有强氧化性,能够使ND 钢表面迅速生成致密的钝化膜从而保护基体。而电化学试验中硫酸质量分数较低(5%和10%),ND 钢表面钝化膜不稳定[21],容易受Cl-作用而发生点蚀[22]。当Cl-质量浓度为10~100 mg/L 时,ND 钢表面点蚀作用逐渐增强,且在10%硫酸溶液中的腐蚀速率高于在5%硫酸溶液中的,说明Cl-降低了ND 钢表面氧化膜的稳定性。当Cl-质量浓度更高时,ND 钢的腐蚀速率反而降低,可能发生了与316L 不锈钢类似的表面离子竞争吸附,具体原因有待进一步研究。
2.2.2 316L不锈钢的循环极化曲线
由图10 可知,当Cl-质量浓度为10,100,1 000 mg/L时,316L不锈钢阳极极化均表现为明显的活化-钝化转变特征,电位回扫形成闭合曲线,交点发生在原阳极活化区而并未在钝化区,不存在保护电位。当Cl-质量浓度达到10 000 mg/L 时,316L不锈钢阳极极化表现为活化-钝化转变特征,且电位回扫时与原阳极极化曲线钝化区相交形成闭合曲线,存在保护电位。
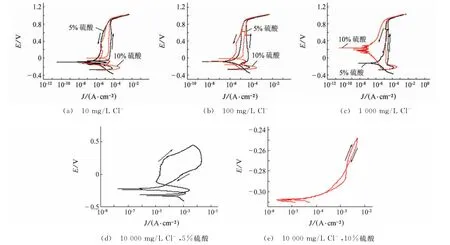
图10 在含不同量Cl-的5%和10%硫酸溶液中316L不锈钢的循环极化曲线Fig.10 The cyclic polarization curves of 316L stainless steel in 5%and 10%sulfuric acid solutions with different concentrations of Cl-
如表4 所示,当Cl-质量浓度分别为10,100,1 000 mg/L时,316L不锈钢致钝电位(相对于饱和甘汞电极SCE,下同)及点蚀电位(相对于饱和甘汞电极SCE,下同)相差不大,钝化电位比较接近,即钝化膜修复能力相近,且受Cl-质量浓度的影响较小;316L不锈钢的维钝电流密度随Cl-质量浓度的升高而降低,即其钝化膜保护性能提高,这是Cl-、SO42-和溶解氧共同作用的结果。
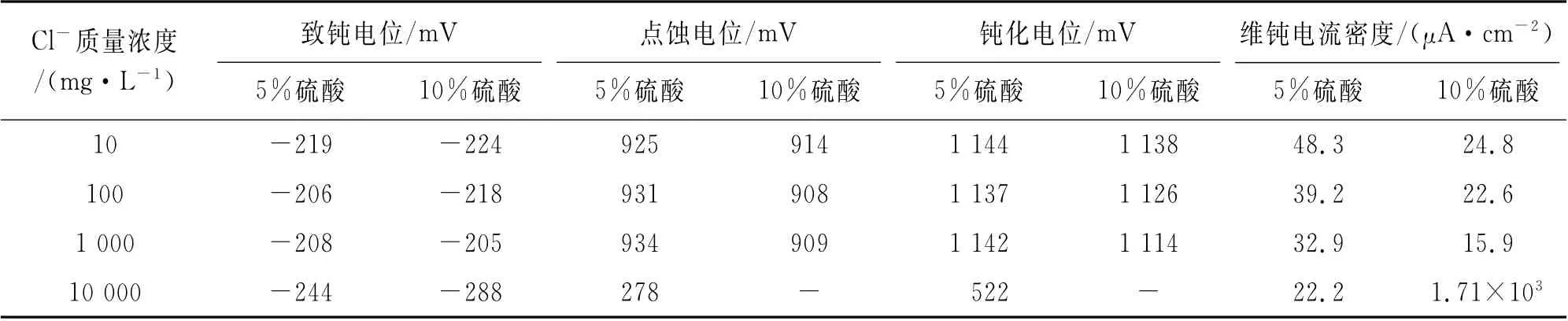
表4 316L不锈钢循环极化曲线拟合数据Tab.4 Cyclic polarization curve fitting data of of 316L stainless steel
当Cl-质量浓度为10 000 mg/L时,5%硫酸溶液中316L不锈钢的钝化电位为522 m V,显著小于其他溶液中的,维钝电流密度为22.2μA/cm2,钝化膜保护性能较好;在10%硫酸溶液中316L 不锈钢的维钝电流密度较大(1.71×103μA/cm2),认为该条件下钝化膜失去了保护作用,其耐蚀性较差。究其原因,一方面由于Cl-质量浓度的升高导致其在金属表面的吸附占主要地位,点蚀开始形核,导致钝化膜变得不稳定,SO42-逐渐失去保护作用;另一方面是硫酸含量相对较高,加剧了钝化膜破坏部位的腐蚀,使316L不锈钢的腐蚀痕迹变得更加明显[23]。
3 结论
(1)浸泡试验中,ND 钢和Q245R 钢在50%硫酸溶液中的腐蚀速率随温度的升高先增大后减小,316L不锈钢的腐蚀速率随温度的升高而增大。其中,ND 钢的耐硫酸露点腐蚀性能更好。
(2)浸泡试验中,当硫酸质量分数低于10%时,三种材料腐蚀速率从大到小依次为:Q245R 钢、ND钢、316L 不锈钢;当硫酸质量分数为10%~70%时,腐蚀速率从大到小依次为Q245R 钢、316L 不锈钢ND 钢。当硫酸质量分数达到70%以上时,三种材料的腐蚀速率均处于较低水平,硫酸露点腐蚀受到抑制。
(3)电化学测试中,在含不同Cl-质量浓度的5%硫酸溶液中,三种材料的腐蚀速率从大到小依次为:Q245R 钢、316L 不锈钢、ND 钢。其中,316L 不锈钢的腐蚀速率随Cl-质量浓度的升高而明显下降。
(4)电化学测试中,在5%和10%硫酸溶液中,随Cl-质量浓度的升高,Q245R 钢和ND 钢的腐蚀速率先增大后减小;硫酸含量相同的溶液中Q245R钢的腐蚀速率明显高于ND 钢的,且硫酸含量越高,材料的腐蚀速率也越高。316L 不锈钢的循环极化曲线存在活化-钝化转变特征,且腐蚀速率受到Cl-、SO42-和溶解氧共同作用的影响。
