夏枯草乙酸乙酯部位对离体大鼠胸主动脉环舒张作用的研究
2021-12-13郑洋滨刘宁艾力奇龚玮洪燕
郑洋滨,刘宁,艾力奇,龚玮,洪燕
1.江西省药品检验检测研究院,国家药品监督管理局中成药质量评价重点实验室,江西省药品与医疗器械质量工程技术研究中心,江西 南昌 330029;2.南昌大学第一附属医院,江西 南昌 330006
高血压是威胁人类生命健康的一种常见病,多发病。高血压一般表现为头痛、眩晕、气急、疲劳、心悸、耳鸣等;常常伴随心、脑、血管等多种并发症。夏枯草为唇形科夏枯草属植物夏枯草的干燥果穗,始载汉代《神农本草经》,历代本草著作多有记载,其味辛、苦、性寒,归肝胆经,具有清肝明目、消肿散结等功效[1]。现代药理学研究表明,夏枯草的主要活性化学成分是三萜类、甾体类、黄酮类、香豆素类等,主要具有抗肿瘤、抗炎、抗菌、抗病毒、降血压、降血糖、调节免疫、保肝等药理作用[1]。本实验通过观察夏枯草乙酸乙酯提取物对离体大鼠主动脉环的影响,观察夏枯草乙酸乙酯提取物的降压作用,并对其作用机制作了进一步探讨。
1 材料与方法
1.1 实验动物
雄性 SD 大鼠30 只,体质量范围180~220 g,购自长沙市天勤生物技术有限公司,动物合格证号:NO.430726211100071368,实验动物生产许可证号:SCXK(湘)2019-0014。饲养于江西省药品检验检测研究院屏障级环境中,实验动物使用许可证号:SYXK(赣)2019-0001。
1.2 实验样品及试剂
夏枯草药材购自黄庆仁栈华氏大药房,经国家药品监督管理局中成药质量评价重点实验室鉴定为真品。苯肾上腺素(PE),乙酰胆碱(Ach),hemoglobin(NO 清除剂),亚甲蓝(MB),吲哚美辛(Indo),左旋硝基精氨酸甲酯盐酸盐(L-NAME),左旋甲基精氨酸(L-NMMA),甲基异硫脲硫酸盐(SMT),四乙胺(TEA),4-氨基吡啶(4-AP),格列苯脲(GLB)。Krebs-Henseleit(K-H)溶液(mmol/L):NaCl 118.3,KCl 4.7,KH2PO41.2,MgSO41.2,NaHCO325.0,CaCl21.25,葡萄糖11.0(pH 7.4)。无钙K-H 溶液用0.05 mmol/L 的乙二醇双(2-氨基乙基醚)四乙酸(EGTA)代替CaCl2加入K-H 溶液。
1.3 实验仪器
离体组织器官恒温灌流系统(成都泰盟软件有限公司),旋转蒸发仪,电子天平,动物天平,液体真空浓缩煎药机(北京东华原医疗设备有限责任公司)
1.4 实验方法
1.4.1 样品提取 将2 kg 的夏枯草全草粉碎,75%乙醇进行加热回流提取,重复两次,每次约2 h。合并提取液,回收溶剂得乙醇提取部分,然后将乙醇提取部分依次用三氯甲烷、乙酸乙酯、正丁醇进行萃取,得夏枯草三氯甲烷提取液、夏枯草乙酸乙酯提取液、夏枯草正丁醇提取液[2],旋转蒸发得浸膏进行实验。前期实验结果得知,夏枯草三氯甲烷提取物无舒张血管作用,夏枯草乙酸乙酯提取物的舒张血管作用强于正丁醇提取物,故本次实验选择夏枯草乙酸乙酯提取物进行后续实验。
1.4.2 离体胸主动脉环实验 将SD 大鼠用3%戊巴比妥钠麻醉,打开胸腔,取出胸主动脉,置于预冷的含95% O2和5% CO2混合气体预饱和的K-H 液,剔除血管周围结缔组织,剪成3~4 mm 长的血管环。将血管悬挂于37 ℃预热的15 mL K-H 液的浴槽内,一端固定于挂钩,一端通过张力换能器连接在生物信号采集系统。持续通入 95% O2和5% CO2的混合气体,调节基础张力至2.0 g,稳定60 min,期间每15 min 换1 次K-H 液。而后用60 mmol/L 氯化钾刺激血管环达峰值,用K-H 液冲洗3~4 次,重复操作3 次,诱发血管环最大收缩幅度。待血管环重新稳定,用1 μmol/L 的PE 收缩血管环达峰值,加入10 μmol/L 的Ach 检验血管内皮完整性,PE 预收缩的血管环舒张70%以上,可认为血管内皮是完整的;PE 预收缩的血管环舒张10%以下或者不舒张,则可认为血管内皮已去除。
以0.3 μmol/L 的PE 诱发的最大收缩幅度为100%,以加入药物后的血管张力幅度与PE 诱发的最大收缩幅度之间的比率反映血管张力的变化。舒张率=(血管环预收缩最大张力―不同药物浓度血管环的张力)/(血管环预收缩最大张力―基础平衡张力)×100%。
1.4.3 实验分组(1)对PE 预收缩内皮完整与去内皮血管环张力的影响。当血管环达到稳定状态后,用0.3 μmol/L 的PE 预收缩血管环达峰值,而后给予低、中、高剂量的夏枯草乙酸乙酯提取物(终浓度0.33、1.67、3.33 mg/mL),上一个浓度稳定后加下一个浓度,观察对内皮完整血管环的张力变化,阴性对照组以同体积K-H 溶液替代。部分血管依据机械法,将血管用与血管内径相适的棉签从管腔轻擦血管内膜,制备成去内皮细胞的血管环,后采用前述方法进行实验,观察对去内皮血管环的张力变化,重复8 次。
(2)对血管活性物质相关试剂预处理血管环张力的影响。内皮完整的血管环在K-H 溶液中稳定后,分别用一氧化氮(NO)清除剂Hemoglobin(终浓度10 μmol/L)、鸟苷酸环化酶抑制剂MB(终浓度10 μmol/L)和环氧合酶抑制剂Indo(终浓度10 μmol/L)与血管环预孵育15 min,等重新到达稳定后,用0.3 μmol/L 的PE 预收缩血管环,使其收缩达顶峰,给予0.33、1.67、3.33 mg/mL 终浓度的夏枯草提取物,观察血管环张力的变化,重复8 次。
(3)对不同的NOS 抑制剂预处理血管环的影响。内皮完整的血管环在K-H 溶液中稳定后,分别采用内皮型一氧化氮合酶(eNOS)抑制剂左旋硝基精氨酸甲酯盐(L-NAME,终浓度100 μmol/L),诱导型一氧化氮合酶(iNOS)抑制剂甲基异硫脲硫酸盐(SMT,终浓度100 μmol/L),总一氧化氮合酶(NOS)抑制剂左旋甲基精氨酸(L-NMMA,终浓度100 μmol/L)分别与主动脉环预孵育15 min,等重新到达稳定后用0.3 μmol/L的PE预收缩血管环,使其达顶峰,给予0.33、1.67、3.33 mg/mL 终浓度的夏枯草提取物,观察血管环张力的变化,重复8 次。
(4)对钾离子通道阻断剂预处理的血管环张力的影响 内皮完整的血管环在K-H 液中稳定后,在孵育体系中分别加入KATP 阻断剂格列苯脲(GLB,终浓度1 μmol/L),电压依赖性延迟整流钾通道阻断剂4-氨基吡啶(4-AP,终浓度0.1 μmol/L)以及钙离子激活钾通道阻断剂四乙胺(TEA,终浓度10 μmol/L)分别与主动脉环预孵育15 min,等重新到达稳定后用0.3 μmol/L 的PE 预收缩血管环,使其达顶峰,给予0.33、1.67、3.33 mg/mL 终浓度的夏枯草提取物,观察血管环张力的变化,重复8 次。
(5)对细胞内钙释放和外钙内流所引起的血管环收缩反应的影响 采用Ca2+剥夺和复加法,将去内皮血管环置于正常K-H 溶液中,稳定60 min。换无钙K-H 溶液冲洗4~5 次,浸泡平衡20 min,加入1 μmol/L 的PE 或60 mmol/L KCl,待收缩的高度到达峰值并稳定后,记录在无钙的K-H 溶液中促使细胞内钙释放所引起的收缩反应。随后,恢复原K-H 溶液中的Ca2+量(即加入100 μL 250 mmol/L的CaCl2于10 mL 浴槽中),待收缩达坪值后,记录细胞外Ca2+进入细胞内所致的收缩反应。用无钙K-H 溶液冲洗数次,待回归基线后,加入高剂量的夏枯草乙酸乙酯提取物(3.33 mg/mL)孵育,10 min后重复上述步骤,比较给药孵育前后肌张力的变化,重复8 次。
1.5 统计学方法
2 结果
2.1 对PE 预收缩内皮完整与去内皮血管环张力的影响
夏枯草乙酸乙酯提取物在1.67、3.33 mg/mL 终浓度下对内皮完整的血管环均具有浓度依赖性舒张作用,最大的舒张率达67.72%,与阴性对照比较,差异有统计学意义(P<0.05)。夏枯草乙酸乙酯提取物对去内皮血管环的血管舒张作用明显低于对内皮完整的血管环,差异有统计学意义(P<0.05)。同时,去除血管环的内皮并不能完全阻断夏枯草乙酸乙酯提取物的舒血管作用,见表1。
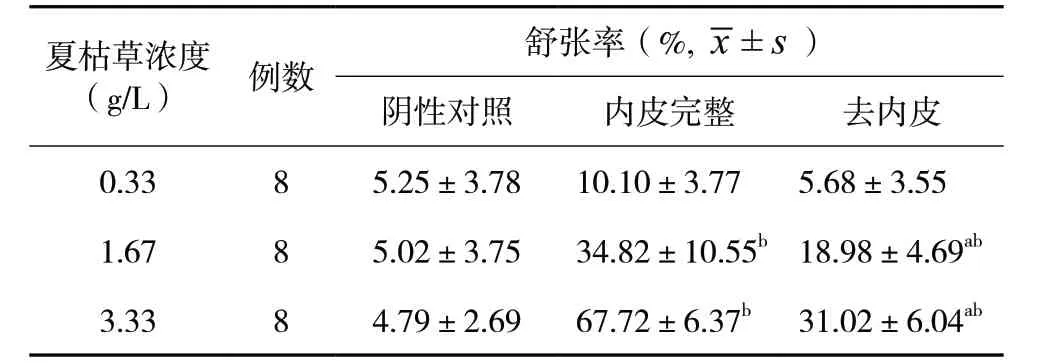
表1 夏枯草提取物对PE预收缩血管环张力的影响
2.2 对血管活性物质相关试剂预处理血管环张力的影响
在MB 和Hemogloin 预孵育下,夏枯草乙酸乙酯提取物对预收缩血管环的舒张作用明显低于未孵育情况下的舒张作用,差异有统计学意义(P<0.05)。而在Indo 预孵育下,夏枯草乙酸乙酯提取物对预收缩血管环的舒张作用未见明显改变,差异无统计学意义(P>0.05),见表2。

表2 夏枯草提取物对血管活性物质相关试剂预处理血管环张力的影响
2.3 对NOS 抑制剂预处理血管环张力的影响
在不同的NOS 抑制剂预孵育下,夏枯草乙酸乙酯提取物对预收缩血管环的舒张作用明显低于未孵育情况下的舒张作用(P<0.05),见表3。

表3 夏枯草提取物对NOS抑制剂预处理血管环张力的影响
2.4 对钾离子通道阻断剂预处理的血管环张力的影响
在不同的钾离子通道阻断剂预孵育下,夏枯草乙酸乙酯提取物对预收缩血管环的舒张作用与未孵育情况下的舒张作用比较,差异无统计学意义(P>0.05),见表4。

表4 夏枯草提取物对钾离子通道阻断剂预处理血管环张力的影响
2.5 对细胞内钙释放以及细胞外钙内流所引起的主动脉环收缩的影响
在无钙K-H 液中,夏枯草乙酸乙酯提取物与血管环孵育后,PE 或KCl 的预收缩幅度与孵育前比较,差异无统计学意义(P>0.05);在孵育体系中恢复原有Ca2+浓度后,高剂量的夏枯草乙酸乙酯提取物可显著抑制PE 与KCl 引起的血管收缩,与孵育前的张力比较,差异有统计学意义(P<0.05)。见表5。
表5 高剂量夏枯草提取物对钙释放及钙内流所致主动脉环收缩的影响(g,)

表5 高剂量夏枯草提取物对钙释放及钙内流所致主动脉环收缩的影响(g,)
注:PE为苯肾上腺素,Kcl为氯化钾。
3 讨论
高血压作为临床常见的心血管疾病,常伴有动脉压增高等临床症状,多发于中老年群体当中。夏枯草汤是临床常用中药方剂,其中夏枯草可有效扩张血管,具有良好的降压效果[3]。夏枯草做为方中君药,可清肝泻火,与何首乌、丹参、牡丹皮、芍药、泽泻、陈皮等诸药共奏清热泻火、通经活络、镇肝熄风等作用,还能调节患者免疫系统,利于控制血压水平。现代药理学研究证实,夏枯草醇性成分对高血压大鼠有较为明显的降压作用[4],这与本课题前期实验结果一致。另有文献报道,夏枯草提取物的降压作用与升高NO 含量有关[5-7],与本次实验结论一致。
本次实验结果表明,夏枯草提取物的血管舒张作用具有部分内皮依赖性,在中、高剂量下,夏枯草提取物能舒张内皮完整的血管环,去除血管环的内皮细胞并不能完全阻断夏枯草提取物的舒血管作用。故推测夏枯草提取物的舒张血管作用可能与内皮细胞以及血管平滑肌均有关系。
众所周知,NO 和前列环素是血管内皮细胞释放的最重要的血管活性物质。NO 在血管内皮细胞内是由L-精氨酸经过NOS 生成,然后扩散到血管平滑肌细胞并激活可溶性鸟苷酸环化酶(GC),使环磷酸鸟苷(cGMP)含量升高,后者通过血管平滑肌细胞内cGMP 依赖行蛋白激酶使钙内流减少,增加钙ATP 酶对钙的摄取或直接作用从而引起血管舒张。前列环素是由血管内皮细胞内的花生四烯酸生成,主要是通过环腺苷酸(cAMP)来完成。为了进一步阐明夏枯草提取物的作用机制,本次实验首先采用鸟苷酸环化酶抑制剂MB、NO 清除剂Hemoglobin 和环氧合酶抑制剂Indo 分别与血管环孵育,随后加入3 个剂量的夏枯草提取物。结果表明,Hemoglobin 与MB 可以阻断夏枯草提取物的血管舒张作用,表明夏枯草提取物的血管扩张作用与NO释放有关,与前列环素的释放无关。
为了进一步验证实验结果,分别采用总NOS 抑制物L-NMMA、eNOS 抑制物L-NAME 和iNOS 抑制物SMT 分别与血管环预孵育,观察夏枯草提取物对孵育后的预收缩血管环的反应。结果发现,夏枯草提取物的血管舒张作用同样可以被NOS 抑制剂所阻断。结果提示,夏枯草叶提取物的血管舒张作用与激活内皮细胞内的NOS,促进NO 释放密切相关。
本实验中,采用电压依赖性延迟整流钾通道阻断剂4-AP,钙离子激活钾通道阻断剂TEA 和KATP 阻断剂GLB[8-9]与主动脉环预孵育,结果发现三种钾通道阻断剂对夏枯草提取物的血管舒张作用均无阻断作用。表明夏枯草提取物的血管舒张作用与K+通道无关。
Ca2+是血管平滑肌收缩的关键因子,血管平滑肌的收缩依赖于细胞外Ca2+内流和细胞内Ca2+释放导致细胞内钙浓度增加[10]。PE 是选择性α1受体激动剂,属受体偶联的钙通道激活剂,一方面开放受体操纵性钙离子通道,另一方面,可通过信使三磷酸肌醇(IP3)释放平滑肌细胞肌浆网内的钙离子。而KCl 引起平滑肌细胞去极化,激活电压依赖性的钙离子通道,二者均可增加细胞质钙离子浓度[11]。本实验采用Ca2+剥夺和复加法,观察夏枯草乙酸乙酯提取物对细胞内钙释放和外钙内流所引起的血管环收缩反应的作用[12]。实验结果发现,不论是PE预收缩的血管环还是KCl 预收缩的血管环,夏枯草乙酸乙酯提取物可以阻断受体偶联的钙通道和电压依赖性钙通道,阻止细胞外钙离子内流。
综上所述,夏枯草乙酸乙酯提取物对大鼠胸主动脉环的舒张作用与促进NO 释放和阻止细胞外钙离子内流有关,与前列环素途径和K+通道无关。
