阿替普酶静脉溶栓后口舌部血管性水肿的相关因素分析
2021-12-02李雨晴张佩兰
李雨晴 张佩兰
天津市环湖医院,天津 300350
阿替普酶(rt-PA)静脉溶栓治疗是目前急性缺血性脑卒中发病超早期有效的内科治疗方法[1],可以显著降低急性脑梗死的致残率,改善患者预后,很大程度减轻其家庭及社会压力[2]。随着rt-PA静脉溶栓治疗的不断推广和深入,其相关并发症或不良反应也越来越受到关注,其中较常见的是rt-PA静脉溶栓后颅内出血转化[1],研究认为这与rt-PA 可增加血管内皮细胞位点上基质金属蛋白酶9、基质金属蛋白酶3水平,从而增加急性缺血性脑卒中出血转化风险有关[1]。另外,rt-PA 治疗的不良反应还包括蛛网膜下腔出血、脊髓血肿、颈部血肿、牙龈出血、过敏反应和血管性水肿等[1],而近年来rt-PA 静脉溶栓治疗后出现口舌部血管性水肿(orolingual angioedema,OA)也逐渐引起临床医师的重视。
rt-PA相关性口舌部血管性水肿是指在溶栓治疗中出现的暂时性的口唇、舌、咽部血管性水肿,可导致气道梗阻、呼吸困难,甚至窒息,是一种临床罕见却会危及生命的并发症[3]。临床研究报道rt-PA 相关性OA 的发病率为0.89%~7.90%[4-5],且认为使用血管紧张素转化酶抑制剂的患者在接受rt-PA 治疗时会增加口舌部血管性水肿的发生率[4]。然而rt-PA溶栓治疗后出现口舌部血管性水肿的发病机制及相关因素目前仍不明确,因此,了解rt-PA相关性口舌部血管性水肿发生的相关因素,提高急性缺血性脑卒中静脉溶栓治疗发生rt-PA相关性口舌部血管性水肿的预测能力,对临床工作具有很重要的指导意义。
1 对象与方法
1.1 研究对象回顾性分析天津市环湖医院2019-06—2020-08 接受rt-PA 静脉溶栓治疗的急性缺血性脑卒中患者1 218例,所有患者发病时间均在4.5 h 内。收集患者的基本信息,见表1。

表1 rt-PA静脉溶栓治疗患者人口统计学信息及临床资料Table 1 Demographic information and clinical data of patients receiving Intravenous thrombolytic therapy with rt-PA
1.2 入选及排除标准依据2018版美国心脏协会/卒中协会(AHA/ASA)急性缺血性脑卒中的早期诊治指南[6]与2018 版中国急性缺血性脑卒中诊治指南制定入选标准及排除标准。
1.2.1 发病后3 h内应用rt-PA静脉溶栓的入选及排除标准:入选标准:①年满18 周岁;②3 h及以内发病;③明确诊断为急性脑梗死;④获得知情同意书。排除标准:①有脑出血史;②3 个月内有头外伤或脑梗死史;③1 周内有体内较深部位且不可压迫的血管穿刺;④脑血管畸形、脑肿瘤、脑动脉瘤、脑手术史;⑤蛛网膜下腔出血;⑥有活动性出血,或相关实验室检查提示具有出血高危风险。
1.2.2 发病后3~4.5 h内应用rt-PA静脉溶栓的入选及相对排除标准:入选标准:①有明确的神经功能缺损,临床诊断为急性缺血性脑卒中;②在开始治疗前症状发生在3~4.5 h。排除标准:①年龄>85岁;②重度脑梗死,NIHSS评分>25分;③目前使用抗凝药物。
1.3 rt-PA 溶栓治疗方法常规监测患者的各项生命体征,溶栓前维持良好的血氧饱和度及通气状态,将高血糖患者的血糖控制在7.8~10.3 mmol/L,高血压患者的血压控制在140~150/80~90 mmHg(1 mmHg=0.133 kPa)。按照0.9 mg/kg 的剂量给予阿替普酶治疗,其中总剂量的10%在1 min 内静脉注入,余90%剂量+0.9%氯化钠溶液稀释,在1 h 内静滴完成,最大剂量不超过90 mg。
溶栓后24 h 复查头MRI/CT、头MRA/CTA检查,如无脑出血,则给予阿司匹林100 mg,qd及氯吡格雷75 mg,qd抗血小板聚集治疗。
1.4 统计学分析应用SPSS 21.0 统计软件进行数据处理,符合正态分布的连续变量以均数±标准差(±s)表示,分类变量以频数(百分率)[n(%)]表示,rt-PA相关性OA的相对危险系数采用95%置信区间。以P<0.05 为差异有统计学意义。
2 结果
2.1 rt-PA 相关性OA 患者的临床特点及治疗1 218 例患者中OA 发病率1.07%,其中5例(38.5%)有荨麻疹史,3例(23.1%)有药物过敏史,2例(15.4%)有食物过敏。13例患者中9例为静脉溶栓过程中发生OA,4 例静脉溶栓之后发生OA,其中10例表现为口唇水肿,8例表现广泛舌部肿胀,3例表现半侧舌部肿胀,2例合并呼吸窘迫,2 例在静脉输注rt-PA 后同时出现OA和荨麻疹,给予地塞米松和苯海拉明抗过敏治疗,数小时内完全缓解。
2.2 rt-PA 相关性OA 与降压药物使用的相关性1 218 例入组患者中578 例(47.5%)有高血压史,其中434 例(35.6%)患者曾口服降压药物,未服用药物或未规律服用药物144例(11.8%)。不同降压药物的用药情况:ACEI类药物43 例(9.9%),ARBs 类药物199 例(45.9%),β受体阻滞剂247例(56.9%),CCB类药物253 例(58.3%),利尿药157 例(36.2%),其他类降压药物48例(11.1%)。见表2。
ACEI 类药物的相对危险系数最高(3.1,95% CI 3.0~96.9),表明既往口服ACEI 类药物可以增加rt-PA相关性OA发生的风险。不同降压药与发生rt-PA相关性OA的危险系数见表2。
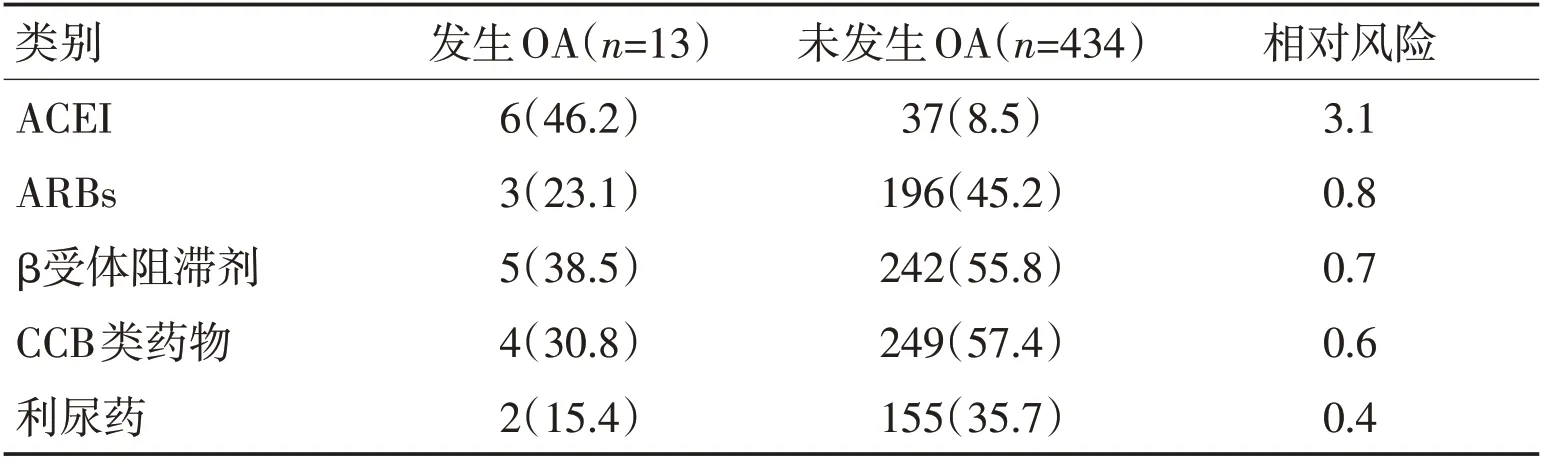
表2 不同降压药物与rt-PA相关性OA的危险系数 [n(%)]Table 2 Risk coefficients of OA associated with different anti-hypertensive drugs and rt-PA [n(%)]
3 讨论
随着rt-PA 静脉溶栓的深入开展,与其相关的不良反应的报道越来越多,除大家经常关注的出血性转化、蛛网膜下腔出血、脊髓血肿、颈部血肿、牙龈出血、过敏反应等常见并发症或不良反应外[1],rt-PA 静脉溶栓后出现口舌部水肿[7-8]的报道越来越多,也有关于rt-PA静脉溶栓后发生急性弥漫性和瞬态甲状腺肿胀[9]的个案报道,说明rt-PA相关性OA也是临床不可忽视的并发症,具有潜在的风险,严重者可危及生命[4]。
本研究发现rt-PA相关性OA的发病率为1.07%,低于其他研究中白种人群中的发病率(1.2%~5.1%)[10-12]。有研究表明rt-PA 相关性OA与不同的基因和种族倾向有关,这可能与基因多态性导致酯酶C1 的缺乏,致缓激肽的产生过剩,增加rt-PA 相关性OA 的易感性有关,基因辅因子同样可以增加rt-PA相关性OA的易感性[13]。既往研究报道,rt-PA相关性OA的发病率为0.89%~7.90%[4-5],这一结果与本研究相似,但对患者评估的差异可能造成发病率的差异,应进一步增加样本量进行深入研究。
本研究发现ACEI类药物的相对危险系数最高(3.1,95% CI 3.0~96.9),表明既往口服ACEI 类药物可以增加rt-PA 相关性OA 发生的风险。目前国内外对于rt-PA相关性OA的可能影响因素及发病机制仍不明确,多数研究认为与口服ACEI类降压药物有关,HURFORD等[14]通过分析以往使用ACEI类药物治疗与口舌部血管水肿之间的关系发现,rt-PA 治疗启动后5~189 min(中位65 min),出现口腔舌部血管水肿率7.9%(95% CI 5.5%~10.6%),rt-PA 相关性OA 发生率为7.9%,多因素分析发现以往ACEI类药物治疗是血管水肿的重要独立预测因素,与本研究结果一致。
其他研究也证实ACEI类降压药物的应用是rt-PA 相关性OA 的主要诱导因素[15],血管紧张素转换酶抑制剂诱导血管性水肿可能发生在几天或几年后,ACEI 药物诱导的血管性水肿主要影响面部,特别是舌头,但也影响腹部[16]。ACEI类降压药物是临床常用的降压药物之一,临床研究发现卒中前口服ACEI 类药物发生OA 的概率是其他降压药物的3.56倍[17-18]。在正常生理状态下主要由氨肽酶P、激酶Ⅰ和激肽酶Ⅱ参与体内缓激肽的代谢,而缓激肽的分解主要由激肽酶Ⅱ催化,即血管紧张素转化酶(ACE),当激肽酶Ⅱ缺乏时,缓激肽会被激酶Ⅰ转化为精氨酸-BK,不易被代谢清除而在体内蓄积[19],因此ACEI 类药物可以抑制激肽酶Ⅱ,导致体内缓激肽的大量累积,从而激发血管性水肿[17-18,20]。此外,静脉应用rt-PA 之后可以激活激肽酶通路,使体内缓激肽生成增加[21],因此,ACEI类药物可能通过抑制缓激肽的分解而增加OA 发生的风险[17-18]。与以往研究结果一致,本研究也观察到其较高的相对危险系数。研究认为rt-PA 相关性OA是药物相关性血管性水肿,而药物相关性血管性水肿分为过敏反应和非过敏反应两种,过敏性水肿是指那些药物摄入后1 h 内发生的不良反应,通常表现形式为荨麻疹、鼻炎、结膜炎、支气管痉挛、过敏反应或过敏性休克,由免疫球蛋白介导的肥大细胞脱颗粒,最常见的表现为荨麻疹[23]。相反,非过敏反应是由于大量炎症细胞因子的产生和大量累积引起的[24-25],研究报道在患者血清中检出具有rt-PA 活性的免疫球蛋白E,说明虽然rt-PA 是一种内源性的蛋白质,也具有一定的抗原性[26-27]。本研究中2 例患者在静脉输注rt-PA 后同时出现OA和荨麻疹,表明rt-PA相关性OA可能是一种急性过敏反应。
也有学者认为口服β受体阻滞剂也可以增加rt-PA相关性OA的发生率[28]。但本研究未能发现既往服用β受体阻滞剂与rt-PA相关性OA 发生风险之间的关系。HILL 等[29]认为岛叶和前额部位的缺血与颅内其他部位的缺血相比,发生rt-PA相关性OA的风险更高,考虑出现单侧唇舌部肿胀是由于病灶侧岛叶皮质功能受损,导致对侧自主神经功能紊乱及血管舒缩功能障碍而发生OA,这反映出OA 的发生可能与脑梗死发生的部位也有一定关系,但本研究未能深入研究rt-PA相关性OA和脑梗死部位之间的关系。
目前对于rt-PA 相关性OA 的治疗,可给予抗组胺类药物或糖皮质激素,一旦症状进展加重,出现喉痉挛、过敏性休克等危及生命的情况时,建议停止rt-PA的输注并严密观察病情变化[30],经验性的治疗过敏性水肿常用的药物包括抗组胺药、糖皮质激素、肾上腺素,虽然这些药物并不能改变缓激肽的浓度,但在其他一些报道中使用此类药物却成功治愈了rt-PA相关性OA[31-32]。进展性气道梗阻有潜在的致命风险,而抗过敏药物的治疗风险却相对较低,因此,一旦出现明显的血管性过敏性水肿的临床症状,应积极给予药物干预,必要时应考虑气管插管[33-34]。
本研究发现溶栓前口服ACEI 类降压药物,既往过敏史可增加rt-PA 相关性OA 发生的风险。在应用rt-PA 治疗急性缺血性脑卒中患者时应注意对于此类患者进行严密监护,以防出现rt-PA 相关性OA,威胁患者生命安全。本研究未能深入研究rt-PA相关性OA和过敏反应的关系,在以后的研究中将进一步深入研究两者之间的关系。
本研究也有一定的局限性,入选对象中11.8%既往用药史不详,这可能增高了ACEI类药物与OA 的相关性,另外口服ACEI 类药物会影响OA发生的风险,而亚洲人群中ACEI类药物的利用率低[22]。本研究结果并不能完全衡量整个人群中ACEI 类药物对OA 发生的风险,需要扩大样本量并进行多中心研究深入评估。
