复方丹参胶囊对替格瑞洛在大鼠体内药动学的影响及其机制
2021-11-30周帅韩战营迟骁玮
周帅,韩战营,迟骁玮
(1.郑州大学第一附属医院心内科,河南 450052;2.国家卫生健康委员会医药卫生科技发展研究中心,北京 100044)
急性冠状动脉综合征(acute coronary syndrome,ACS)主要是由动脉粥样硬化斑块破裂导致组织因子和胶原蛋白的暴露引发血小板活化与聚集而引起,最终形成血栓[1-2]。作为冠心病中发病率、死亡率最高的类型,主要包括不稳定性心绞痛、非ST段抬高型心肌梗死和ST段抬高型心肌梗死[3]。血小板在ACS血栓形成的过程中发挥着重要的作用,故抗血小板药是目前抗血栓形成的主要治疗策略[4-5]。
替格瑞洛是环戊基三唑嘧啶类新型口服抗血小板药物,可逆性地与P2Y12受体结合,于2012年通过原国家食品药品监督管理局(NMPA)审批正式进入中国市场[6]。PLATO研究表明,替格瑞洛可显著降低心血管死亡、心肌梗死及脑卒中发生率及死亡率,不良反应较小[7]。与传统P2Y12受体拮抗剂比较,替格瑞洛具有起效迅速,停药后恢复较快,不受年龄、性别、饮食影响等优势[8]。研究表明,替格瑞洛口服后吸收迅速,主要分布于血液,可与血浆蛋白广泛结合(>99%)[9-10];该药大部分经CYP3A5代谢生成活性代谢产物AR-C124910XX,部分经CYP3A4代谢生成AR-C133913XX,此外,替格瑞洛主要由P糖蛋白(P-gp)等转运体进行外排[11]。食物及药物等同服均可影响其体内的代谢清除,HOLMBERG等[12]研究发现连续服用西柚汁可抑制CYP3A进而使替格瑞洛的血药峰浓度(Cmax)及血药浓度-时间曲线下面积(AUC)增加65%和121%,使消除半衰期延长1.1倍。而与利福平同服后,健康志愿者体内替格瑞洛的Cmax、AUC和t1/2分别降低73%,86%和67%[13]。
复方丹参胶囊主要由丹参、三七及冰片组成,其中酚酸类具有提高机体纤溶及抗凝活性、抗血栓、抗血小板聚集、抗氧化、保护心脏微血管内皮细胞、改善微循环障碍等作用[14];皂苷类可显著改善血管内皮细胞功能、抑制血管平滑肌细胞增殖、抗血栓形成、扩张血管及保护心肌[15]。有研究发现丹参提取物可显著增强抗血小板聚集活性[16]。复方丹参胶囊也可显著提高氯吡格雷的抗血栓、抗血小板聚集、抗氧化等作用[17],故常与替格瑞洛合用于心血管疾病治疗中。研究发现,丹参提取物可调控CYP3A活性[18],但复方丹参胶囊对替格瑞洛药动学的影响未见报道,因此,笔者研究了复方丹参胶囊对替格瑞洛在大鼠体内药动学的影响,并探讨其作用机制。
1 材料与方法
1.1仪器 液质联用系统(AB ScieX Qtrap 4000三重四级杆质谱仪;安捷伦1100高效液相色谱系统;Analyst TF 1.5 Software数据采集分析软件);冷冻高速离心机(美国Thermo Fish公司);超纯水系统(美国Millipore公司);超微量电子天平(梅特勒-托利多仪器有限公司,感量:0.1 mg);微量移液器(德国Eppendorf公司)。
1.2药品与试剂 复方丹参胶囊(规格:每粒30 mg,批号:D17A005,云南白药集团股份有限公司);替格瑞洛片(规格:每片90 mg,批号:TDKT,阿斯利康制药有限公司);替格瑞洛对照品(批号:L1613016,含量:99.5%,上海阿拉丁公司,货号:T125095);咪达唑仑对照品(中国食品药品检定研究院,含量:99.8%,货号:130557,批号:130557-201604);CYP3A2抗体(美国Abcam公司,批号:ab195627);RNAiso Plus(Takara公司,批号:9108);FastQuant cDNA第一链合成试剂盒(天根生化科技,批号:KR106-03);SuperReal PreMix荧光定量PCR试剂盒(天根生化科技,批号:FP205);甲醇、乙腈(色谱纯,美国Fisher公司);醋酸铵(分析纯,美国Fisher公司);甲酸(分析纯,上海阿拉丁有限公司),所有其他溶剂和化学试剂均为分析纯或以上。
1.3实验动物 Sprague-Dawley大鼠,SPF级,雄性,体质量200~240 g,购自北京维通利华技术有限公司,实验动物生产许可证号:SCXK(京)2017-0028,饲养于河南省实验动物中心。大鼠的饲养、使用、操作等均符合中国《实验动物管理条例》。大鼠于室温18~24 ℃,相对湿度(65±5)%,明暗交替12 h的条件下环境适应性饲养7 d后用于实验。本研究中动物实验方案获得郑州大学实验动物管理与使用委员会批准。
1.4方法
1.4.1药动学实验 采用平行对照实验,16只雄性大鼠适应性饲养后随机分为两组,对照组与复方丹参胶囊组,分别连续7 d每天灌胃给予等量0.9%氯化钠溶液、复方丹参胶囊(将18 mg复方丹参胶囊溶于0.9%氯化钠溶液1 mL中,制备成复方丹参胶囊灌胃用制剂18 mg·mL-1,按大鼠体质量每200克给予1 mL复方丹参胶囊灌胃用制剂,即给药剂量为90 mg·kg-1)。第8天给药前12 h禁食不禁水,第8天分别给予两组大鼠0.9%氯化钠溶液、复方丹参胶囊30 min后,灌胃给予两组大鼠替格瑞洛(将4 mg替格瑞洛溶于0.9%氯化钠溶液1 mL中制成替格瑞洛溶液灌胃用制剂4 mg·mL-1,按大鼠体质量每200克给予1 mL替格瑞洛灌胃用制剂。即给药剂量为20 mg·kg-1,i.g.),并在给药前、给药后0.08,0.25,0.5,1,1.5,2,3,4,6,8,10,24及36 h于大鼠眼内眦采血0.25 mL,置于肝素钠抗凝的离心管中,3000 r·min-1离心10 min(r=10 cm),取血浆置于-80 ℃保存待测。
1.4.2肝微粒体的制备 大鼠药动学实验完成后,采用乌拉坦(50%,W/V)腹腔注射麻醉,取出肝脏,用预冷的冲洗液冲洗肝脏2或3次至土黄色并用滤纸吸干,剪取同部位肝脏组织在冰浴条件下切碎,按1:4加入的Tris-HCl(0.05 mol·L-1)制备肝匀浆液。采用差速离心法制备大鼠肝微粒体,9000×g4 ℃离心20 min,小心取上清液后100 000×g4 ℃离心60 min,弃上清液,沉淀用Tris-HCl(0.15 mol·L-1)洗涤,100 000×g4 ℃离心60 min,所得肝微粒体均匀混悬于蔗糖(250 mmol·mL-1)中,置于-80 ℃保存备用。采用考马斯亮蓝法测定肝微粒体总蛋白浓度。
1.4.3复方丹参胶囊对大鼠肝脏CYP3A mRNA表达的影响 药动学实验结束后采取腹主动脉采血并处死各组大鼠,分别取出两组大鼠的肝脏置于干冰中。用RNA提取试剂盒提取肝组织中总RNA,将RNA用FastQuant cDNA第一链合成试剂盒反转录成cDNA模板,取稀释后的cDNA 4 μL,分别加入CYP3A1及CYP3A2的引物和荧光标记探针,利用SuperReal PreMix荧光定量PCR试剂盒,在iQ5荧光定量PCR仪(Bio-Rad Laboratories)上进行扩增反应(反应参数见表1),检测mRNA表达水平。基因表达数据用内参β-actin进行校正,相对表达差异采用荧光定量PCR实验中常用的ΔΔCt的方法。

表1 CYP3A1和CYP3A2基因引物序列
1.4.4复方丹参胶囊对大鼠肝脏CYP3A2蛋白表达的影响 提取肝组织中总蛋白,采用SDS-PAGE凝胶电泳,将蛋白转移至聚偏氟乙烯(PVDF)膜,采用5%BSA封闭2 h后孵育一抗,加入一抗(1:600)、β-actin(1:3000),4 ℃孵育过夜。在室温条件下采用摇床将二抗孵育2 h。采用Tris-HCl与吐温等渗缓冲盐溶液(TBST)将PVDF膜洗涤3次,每次15 min,加入化学发光显色试剂(ECL)显色剂。应用凝胶成像系统检测,分析目的条带/对应内参的相对表达量。
1.4.5复方丹参胶囊对大鼠肝脏CYP3A酶活性的影响 采用CYP3A特异性探针底物咪达唑仑(midazolam,MDZ)来检测酶活性。肝微粒体孵育反应体系为100 μL,在大鼠肝微粒体(0.3 mg·mL-1)中分别加入MDZ(20,50,100 μmol·L-1),磷酸盐(PBS)缓冲液(0.1 mol·L-1,pH值7.4),于37 ℃预孵育5 min,加入NADPH(1 mmol·L-1)启动反应,孵育20 min后将样品迅速置于冰浴中,并立即加入冰乙腈终止反应,涡旋振荡2 min,15 000×g离心10 min,取上清液20 μL进样。代谢消除率=(加入探针底物的量-测得探针底物的量)/加入探针底物的量。
1.4.6测定方法 按照文献中大鼠血浆中替格瑞洛的测定方法[19-20],对所采用的方法分别进行了专属性、线性、精密度与回收率、基质效应及稳定性等验证,结果均符合《中华人民共和国药典》2020年版生物样品定量分析要求。具体条件如下。
(1)色谱条件。色谱柱为Phenomenex C18(2.1 mm×50 mm,2.1 μm);进样量:5 μL;流动相:甲醇-0.1%甲酸(80:20);流速:0.4 mL·min-1;柱温:40 ℃;内标:硝苯地平。替格瑞洛在大鼠血浆中的线性范围为5~2000 ng·mL-1。
(2)质谱条件。采用负离子电喷雾离子源多反应模式进行监测,替格瑞洛和内标(硝苯地平)的离子对分别为m/z521.4→361.1,内标528.3→368.1。替格瑞洛的去簇电压(DP) 和碰撞能(CE) 值分别为-99.26 V和-32.56 V;内标的去簇电压(DP) 和碰撞能(CE) 值分别为-55.35 V和-42.85 V;扫描时间100 ms,碰撞气压95.05 kPa,气帘气325.90 kPa,离子源喷射电压5500 V,离子源温度600 ℃,源内气体1(GS1)425.30 kPa,源内气体2(GS2) 385.05 kPa。
(3)血浆样品处理。采用蛋白沉淀法处理血浆样品。取血浆样品100 μL,加入含内标的沉淀剂(甲醇:乙腈=1:1)400 μL,涡旋1 min,14000 r·min-1离心10 min(r=10 cm),取上清液5 μL进样分析。
1.4.7方法学验证
(1)专属性。分别取空白血浆、空白血浆及替格瑞洛、大鼠给药后血浆样品,按“2.5”项下方法处理。结果显示,血浆内源性物质基本对替格瑞洛和内标的测定无干扰。替格瑞洛与内标的峰形良好,分离良好,保留时间分别为2.42,3.49 min,表明方法学专属性好,可满足生物样品的测定要求。
(2)线性范围。采用加权(W=1/x2)最小二乘法,以待测物与内标的峰面积比值(Y)分别对替格瑞洛的浓度(X)进行线性回归,替格瑞洛的回归方程为:Y=7.63×10-4X-4.28×10-4(r=0.998 8)。线性范围为5~2000 ng·mL-1,最低定量下限为5 ng·mL-1,说明方法灵敏度较高。
(3)精密度与回收率。分别精密量取对照品溶液与空白血浆涡旋混匀,制成低、中、高3种质量浓度(10,100,1000 ng·mL-1),按“2.5”项下方法处理,连续3 d进行测定,替格瑞洛日内精密度RSD分别为7.2%,5.9%,3.4%,日间精密度RSD分别为9.6%,7.1%,3.5%,回收率分别为(90.3±2.4)%,(91.7±3.6)%,(94.6±4.5)%。内标的回收率为(92.8±1.9)%。
(4)稳定性。制备中浓度(100 ng·mL-1)的替格瑞洛标准血浆样品,按“2.5”项下方法处理,分别置于室温下4 h、4 ℃自动进样器中10 h、-20 ℃反复冻融3次及-20 ℃放置30 d,考察不同存放条件下样品的稳定性。4种条件下RSD均<8.7%。表明处理后的样品在上述4种条件下稳定性符合生物样本的分析要求。
(5)基质效应。分别取空白血浆,按“1.4.5”项下方法处理,分别加入低、中、高浓度的标准品溶液,涡旋后进行测定(A),同时测定相同浓度的对照品溶液(B),以两者峰面积比值(A/B)求得基质效应。替格瑞洛的基质效应分别为85.2%,89.3%和92.1%。内标溶液经同法处理,计算得基质效应为91.7%。表明本方法基质效应符合生物样本的分析要求。
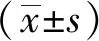
2 结果
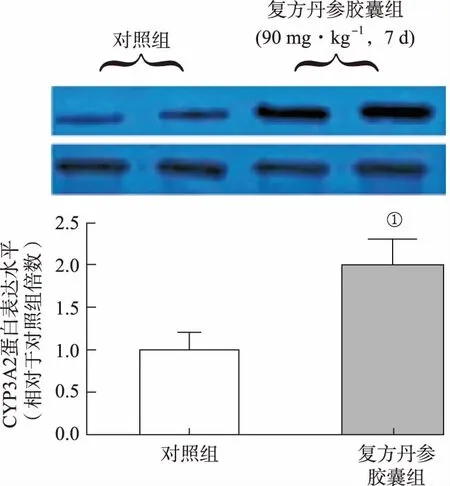
2.1复方丹参胶囊对替格瑞洛大鼠体内药动学的影响 两组大鼠血浆中替格瑞洛的时间-药物浓度曲线见图1,相应的药动学参数见表2。由结果可知,与对照组比较,复方丹参胶囊组大鼠血浆中替格瑞洛Cmax、AUC0-t及AUC0-∞显著降低32.03%,30.65%及30.89%(P<0.01),而CL/F、Vz/F显著升高至1.43及1.37倍(P<0.01)。
2.2复方丹参胶囊对大鼠肝脏CYP3A1及CYP3A2 mRNA表达的影响 与对照组比较,复方丹参胶囊组的CYP 3A1及 CYP 3A2 mRNA表达水平均增加至对照组(1.23±0.57)及(3.33±1.19)倍(P<0.05)。结果表明,复方丹参胶囊可能诱导CYP3A2 mRNA表达,但对CYP3A1 mRNA表达无显著性影响(P>0.05)。见图2。
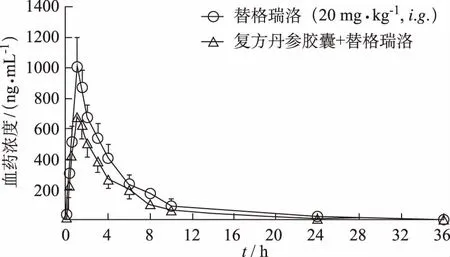
图1 替格瑞洛在大鼠体内的血药浓度-时间曲线
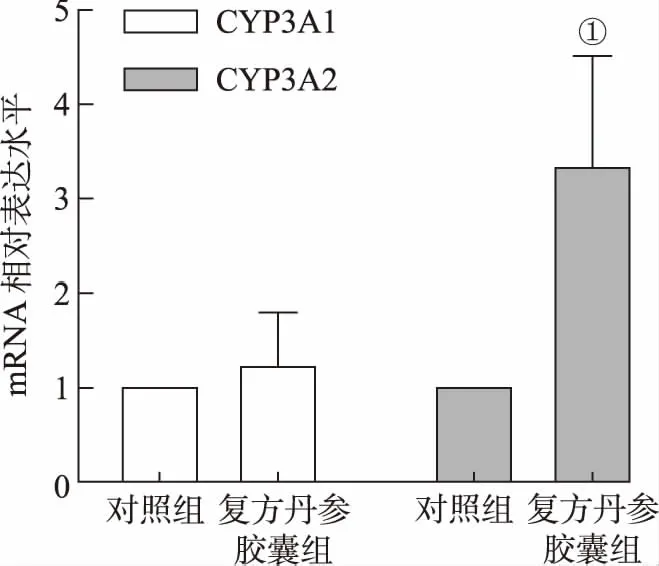
2.3复方丹参胶囊对大鼠肝脏CYP3A2蛋白表达的影响 与对照组比较,复方丹参胶囊组肝脏CYP3A2蛋白表达显著升高,差异有统计学意义(P<0.05)。见图3。
2.4复方丹参胶囊对大鼠CYP3A酶活性的影响 对照组及复方丹参胶囊组大鼠肝微粒体CYP3A底物MDZ的代谢消除率如表3所示。由此可知,复方丹参胶囊可诱导大鼠CYP3A酶活性。
3 讨论
研究表明,复方丹参胶囊可提高抗血小板聚集,抗血栓形成、抗氧化等药理活性,具有显著降低心血管不良事件,且常与抗血小板药物合用[8]。本实验所选用复方丹参胶囊及替格瑞洛的剂量为80及20 mg·kg-1,均为所对应的临床等效剂量,且选用平行对照多剂量给药,更符合临床用药规律。药动学结果显示,单次灌胃给予大鼠替格瑞洛(20 mg·kg-1)后替格瑞洛在大鼠体内约1.13 h达到峰浓度,吸收速度较快;消除半衰期也较短,表观分布容积较大。此结果与文献[10]中研究结果相似。
连续7 d灌胃给予复方丹参胶囊后,大鼠体内替格瑞洛的Cmax、AUC0-t及AUC0-∞显著降低(P<0.05),
且使替格瑞洛的CL/F、Vz/F显著升高(P<0.05)。暴露量的降低可能由吸收减少、代谢增多、分布增多所致。因替格瑞洛在人体内主要经CYP3A5代谢生成活性代谢产物AR-C124910XX,并经CYP3A4催化生成AR-C133913XX,而在大鼠体内CYP3A1/CYP3A2为人体内CYP3A4/CYP3A5的同工酶。因此,笔者测定了连续7 d灌胃给予复方丹参胶囊后两组大鼠CYP3A1及CYP3A2 mRNA表达的影响,结果发现CYP3A2 mRNA表达显著升高。进一步检测CYP3A2蛋白表达,结果发现大鼠肝脏中CYP3A2表达显著升高,提示大鼠体内替格瑞洛暴露量的降低可能是因为复方丹参胶囊诱导肝脏CYP3A2表达,从而使其代谢增多。这与ZHOU等[17]的研究结果相似,他们发现复方丹参胶囊可诱导CYP3A,导致氯吡格雷体内暴露量减少。本研究结果表明,连续7 d灌胃给予复方丹参胶囊后可使大鼠体内替格瑞洛的暴露量降低,清除率加快,但半衰期无显著性变化。由药动学结果可知,复方丹参胶囊可致大鼠体内替格瑞洛清除率增加,表观分布容积也增加,而半衰期无显著性变化,其原因可能与复方丹参胶囊可调控大鼠体内的转运体活性有关。
研究结果表明,连续7 d灌胃给予复方丹参胶囊(90 mg·kg-1)后大鼠肝脏的CYP3A2 mRNA及蛋白表达水平均显著升高。笔者进一步探索了复方丹参胶囊对CYP3A酶活性的影响。为进一步观察CYP3A活性表达水平,分别将对照组及复方丹参胶囊组(90 mg·kg-1)大鼠处死制备肝微粒体,采用肝微粒体孵育体系测定CYP3A活性,所选用复方丹参胶囊的剂量与临床使用剂量等效。结果显示,复方丹参胶囊组CYP3A探针底物MDZ的代谢消除率显著增加,说明复方丹参胶囊可显著升高CYP3A 酶活性,也进一步验证了复方丹参胶囊可诱导CYP3A2酶表达活性,这与部分文献报道一致[21-22]。但是,WANG等[18]研究发现丹参提取物对CYP3A表达无影响,且WANG等[23]发现隐丹参酮可抑制CYP3A活性,其原因可能与所采用的浓度不同有关。复方丹参胶囊主要由丹参、三七、冰片经提取精制而成,其中丹参的主要活性成分为丹参酮ⅡA、隐丹参酮、二氢丹参酮Ⅰ等;三七的主要活性成分为人参皂苷Rg1、人参皂苷Rb1等皂苷类化合物[14,24]。马静等[25]研究报道隐丹参酮、丹参酮ⅡA可诱导人肝HepG2细胞CYP3A4酶活性及蛋白的表达。陈艳进等[26]发现三七总皂苷等可显著诱导CYP3A mRNA表达。因此,复方丹参胶囊诱导大鼠体内CYP3A酶可能主要与隐丹参酮、丹参酮ⅡA、三七皂苷可诱导大鼠CYP3A活性与表达有关。

表2 替格瑞洛在大鼠体内的主要药动学参数
①与对照组比较,P<0.05。
①与对照组比较,P<0.05。

表3 两组大鼠肝微粒体MDZ的消除率
综上所述,本研究证实了连续灌胃给予大鼠复方丹参胶囊可显著降低其体内替格瑞洛的暴露量,其作用机制可能与诱导CYP3A2活性及蛋白表达有关。故在临床合用时应关注此问题,及时监测替格瑞洛的血药浓度以达到最佳治疗效果。此外,笔者将进一步选用健康志愿进行临床试验来验证复方丹参胶囊与替格瑞洛药动学/药效学的相互作用,以期为替格瑞洛的临床合理应用奠定理论和实验基础。
