超高效液相色谱-串联质谱法测定纸制食品接触材料中丙烯酰胺的迁移量
2021-11-28李伟涛葛文秀刘丽娜李金凤
钱 凯,李伟涛,葛文秀,刘丽娜,陈 明,李金凤
(1.常州工业及消费品检验有限公司,江苏 常州 213000;2.南京海关危险货物与包装检测中心,江苏 常州 213000)
丙烯酰胺(AM)是聚合生成聚丙烯酰胺(PAM)的起始化合物。聚丙烯酰胺作为造纸行业最早使用的添加剂,被广泛用作助留剂、助滤剂等,并能提高纸张强度[1-3]。在自然条件下,聚丙烯酰胺会缓慢降解成丙烯酰胺[3-5],而残留的丙烯酰胺单体会随着聚丙烯酰胺终产物引入纸制品中,在与食品接触过程中不断被迁移出来。丙烯酰胺属于水溶性有机化合物,渗透性较强,可通过消化道、呼吸道、粘膜、皮肤等多种途径被人体吸收[1,6],存在慢性中毒的安全隐患。研究显示,丙烯酰胺具有神经、生殖、遗传等毒性,已被国际癌症研究机构列为2类致癌物[2,4,7-8]。因此,我国在GB 9685-2016《食品安全国家标准 食品接触材料及制品用添加剂使用标准》[9]中明确规定了丙烯酰胺的特定迁移限量为不得检出(检出限为0.01 mg/kg)。
目前,公众对丙烯酰胺的关注主要来自食品、环境、纺织品和化妆品等领域[7,10-15],而关于纸制食品接触材料的安全性问题却鲜有报道。随着人们对塑料污染的认识及环保意识的提高,纸类食品接触材料由于易降解、可回收等特点逐渐受到市场青睐,成为人们日常生活用品的“新宠儿”。我国对食品接触材料及制品中丙烯酰胺迁移量的测定方法主要为高效液相色谱法,其原理是采用离子排斥色谱柱和紫外检测器进行分离和检测[16]。由于不同食品模拟物存在不同程度的基质效应,尤其是酒精类食品模拟物含有机成分,会对离子排斥色谱柱的分离性能造成影响,导致方法检出限无法满足要求,定性定量结果不准确等问题。除液相色谱法外,国内外对于丙烯酰胺的测定主要采用气相色谱法、气相色谱-串联质谱法和液相色谱-串联质谱法等[8,17-18]。其中,气相色谱法、气相色谱-串联质谱法普遍需进行衍生化和固相萃取等处理,操作步骤较繁琐;液相色谱-串联质谱法具有操作简便、选择性好、灵敏度高、结果准确可靠等优点,广泛应用于食品、环境等领域[1,11-12,19-21],但鲜见关于纸制食品接触材料的报道。
本研究采用超高效液相色谱-串联质谱建立了纸制食品接触材料中丙烯酰胺迁移量的测定方法。并进行了方法优化,有效解决了基质效应问题,对评估纸及纸制食品接触材料中丙烯酰胺迁移的合规性和风险性具有重要意义。
1 实验部分
1.1 试剂与材料
冰乙酸(分析纯,国药集团化学试剂有限公司);无水乙醇(分析纯,江苏彤晟化学试剂有限公司);光谱纯甲醇、色谱纯甲酸(上海安谱实验科技股份有限公司);橄榄油(化学纯,上海泰坦科技股份有限公司);丙烯酰胺标准品(1 000µg/mL,北京坛墨质检科技有限公司);实验用水为GB/T 6682规定的一级水。
一次性针式注射器(5 mL)、亲水PTFE针式滤器(0.22µm)购于上海安谱实验科技股份有限公司。
随机采集具有代表性的不同类型纸制食品接触材料样品,共20批次。其中淋膜纸杯5批、淋膜纸碗5批、纸基复合包装袋5批、纸吸管5批。每个样品平行采集2份。
1.2 仪器与设备
Agilent 1290高效液相色谱仪及Agilent 6460 QQQ三重四极杆质谱仪(美国安捷伦公司);XS205DU万分之一分析天平(瑞士Mettler Toledo公司);Milli-Q Advantage纯水仪(美国Millipore公司)。
1.3 实验方法
1.3.1 迁移实验按GB 31604.1-2015[22]和GB 5009.156-2016[23]的要求,分别采用4%(体积分数,下同)乙酸溶液模拟酸性食品,采用水、10%乙醇溶液、20%乙醇溶液、50%乙醇溶液模拟水和酒精类食品(以下称水溶性食品模拟物),用精制橄榄油模拟油脂类食品(以下称油性食品模拟物),对纸制食品接触材料及制品进行迁移实验。所得模拟物充分混匀,用于以下分析测试。
1.3.2 标准工作溶液配制丙烯酰胺标准中间液(5 mg/L):准确移取50µL丙烯酰胺标准品(1 000µg/mL)于10 mL容量瓶中,分别用相应水溶性食品模拟物定容至刻度。
水溶性食品模拟物标准工作溶液:分别准确移取丙烯酰胺标准中间液(5 mg/L)0、10、20、60、100、160、200µL于10 mL容量瓶中,分别用相应水溶性食品模拟物定容,得到丙烯酰胺质量浓度分别为0、5、10、30、50、80、100µg/L的标准系列工作溶液。
油性食品模拟物标准工作溶液:分别称取5 g橄榄油(精确至0.01 g)于6个带盖玻璃离心管中,离心管中分别加入丙烯酰胺标准中间液(5 mg/L)0、10、20、50、100、200µL并混匀,加入5 mL水涡旋振荡1 min,4 000 r/min离心5 min后,取下层水溶液经微孔滤膜过滤至2 mL进样小瓶,得到丙烯酰胺含量分别为0、10、20、50、100、200µg/kg的标准系列工作溶液。
1.3.3 样品前处理水溶性食品模拟物试液的制备:取1~2 mL水溶性食品模拟物试液,经微孔滤膜过滤至2 mL进样小瓶,待测。
油性食品模拟物试液的制备:准确称取5 g(精确至0.01 g)油性食品模拟物试液至带盖玻璃离心管中,加入5 mL水涡旋振荡1 min进行液液萃取,4 000 r/min离心5 min后,取下层水溶液经微孔滤膜过滤至2 mL进样小瓶,待测。
1.3.4 液相色谱条件色谱柱为Agilent Poroshell 120 SB-Aq(4.6 mm×100 mm,2.7µm);流动相:0.1%甲酸水溶液-甲醇(9∶1,体积比);洗脱方式:等度洗脱;流速:0.6 mL/min;柱温:30℃;进样量:1µL。
1.3.5 质谱条件离子源:电喷雾离子源(ESI);干燥气温度:350℃;干燥气流量:10 L/min;雾化气压力:310 264 Pa(45 psi);鞘气温度:350℃;鞘气流量:10 L/min;毛细管电压:2 500 V;电喷嘴电压:1 000 V;碰撞气为氮气;检测方式:多反应监测(MRM),正离子模式。
2 结果与讨论
2.1 仪器条件的优化
2.1.1 色谱柱的选择丙烯酰胺是一种亲水的强极性化合物,在普通C18液相色谱柱上难以实现较好的保留,易出现峰形差和拖尾等现象。因此实验考察了Phenomenex Kinetex C18(2.1 mm×150 mm,2.6µm)和Agilent Poroshell 120 SB-Aq(4.6 mm × 100 mm,2.7µm)2种液相色谱柱的分离效果。结果表明,采用Agilent Poroshell 120 SB-Aq(4.6 mm×100 mm,2.7µm)柱的分析保留时间以及峰高、峰宽等参数均较优,且峰形和拖尾现象也有明显改善。因此,实验选择Agilent Poroshell 120 SB-Aq(4.6 mm ×100 mm,2.7µm)作为液相色谱柱。
2.1.2 流动相的优化分别比较了甲醇和乙腈作为流动相有机相的分离效果,发现采用甲醇和水作为流动相时,丙烯酰胺的响应高于乙腈和水。此外,还考察了水和甲醇(9∶1)、甲酸水溶液和甲醇(9∶1)作为流动相时对响应强度、保留时间、回收率和精密度的影响。结果显示,采用水和甲醇作为流动相时,4%乙酸基质中丙烯酰胺仪器响应的精密度(n=6)较差。当在水相中加入0.1%甲酸后,精密度得到明显改善,因此实验选择0.1%甲酸水溶液-甲醇(9∶1)为流动相。
2.1.3 质谱条件的优化丙烯酰胺具有氨基与不饱和双键,采用ESI正离子扫描模式的响应优于负离子模式。经过方法参数优化,丙烯酰胺的母离子m/z为72.1,碎裂电压为40 V,特征子离子的m/z分别为55和44,碰撞能量分别为10 eV和12 eV。优化条件下,10µg/L丙烯酰胺标准溶液在代表性食品模拟物(4%乙酸)中的MRM色谱图(m/z72.1/55)如图1所示。

图1 4%乙酸中丙烯酰胺的MRM色谱图Fig.1 MRM chromatogram of acrylamide in 4% acetic acid
2.2 基质效应
基质效应是被测样品中除目标分析物以外的组分对目标物定性、定量分析产生的干扰和影响[24]。为评估本方法的可靠性和准确性,采用基质校准曲线与溶剂校准曲线的线性方程斜率比(Slope ratio,SR)评价基质效应[25]。当SR=1,表明无基质效应;当SR>1或SR<1时,说明存在基质干扰和影响。
分别用4%乙酸(AcOH)、10%乙醇(EtOH)、20%乙醇、50%乙醇和橄榄油5种食品模拟物对丙烯酰胺阴性样品进行迁移试验,获得的迁移试验溶液按照“1.3.2”方法制备基质校准曲线,得到拟合线性方程的斜率K1。同法制备溶剂校准曲线,得到拟合线性方程的斜率K2,则SR=K1/K2。结果显示,水溶性食品模拟物的SR均接近1(0.983~1.01),表明基质影响较小;油性食品模拟物的SR为0.839,表明存在基质抑制效应。为降低基质效应影响,本研究采用在空白橄榄油中加入不同体积的丙烯酰胺标准溶液,得到一系列质量浓度的油性食品模拟物标准工作溶液。按照油性食品模拟物试液的制备方法对上述标准工作溶液进行液液萃取,得到的水溶液经上机测试,获得拟合线性方程的斜率K2’,则油性食品模拟物的SR=0.974,说明本方法的基质效应影响较小,测定结果准确可靠。
2.3 方法学验证
2.3.1 线性关系、检出限与定量下限在4%乙酸、10%乙醇、20%乙醇、50%乙醇和橄榄油中分别添加不同体积的丙烯酰胺标准中间溶液,按照“1.3.2”制备标准工作溶液上机测试,分别以基线噪音的3倍(3S/N)和10倍(10S/N)仪器响应所对应的丙烯酰胺质量浓度作为仪器检出限和定量下限,从而计算方法检出限(LOD)和定量下限(LOQ)。以食品模拟物中丙烯酰胺的质量浓度或含量(x,µg/L或µg/kg)为横坐标,以对应的峰面积(y)为纵坐标,绘制标准工作曲线。迁移量计算参考GB 5009.156-2016的相关规定,结果如表1所示。数据显示,不同食品模拟物中丙烯酰胺的含量与响应值均呈良好线性关系,相关系数(r2)均大于0.999。油性食品模拟物中丙烯酰胺的检出限和定量下限分别为5.0µg/kg和10.0µg/kg,水溶性食品模拟物的检出限和定量下限分别为1.0µg/L和5.0µg/L,说明该方法灵敏度较高。

表1 本方法的线性方程、线性范围、相关系数、检出限与定量下限Table 1 Linear equations,linear ranges,correlation coefficients,LOD and LOQ of the method
2.3.2 回收率与相对标准偏差为进一步验证方法的准确性,分别在不同空白食品模拟物中添加10、50、100µg/kg 3个水平的丙烯酰胺标准物质,每个浓度分别制备6个平行样,计算其平均回收率和精密度,精密度以相对标准偏差(RSD)表示(见表2)。由表2可见,在3个加标水平下,丙烯酰胺在不同食品模拟物中的平均回收率为90.0%~113%,RSD为0.40%~4.6%,说明本方法的准确度和精密度较好。
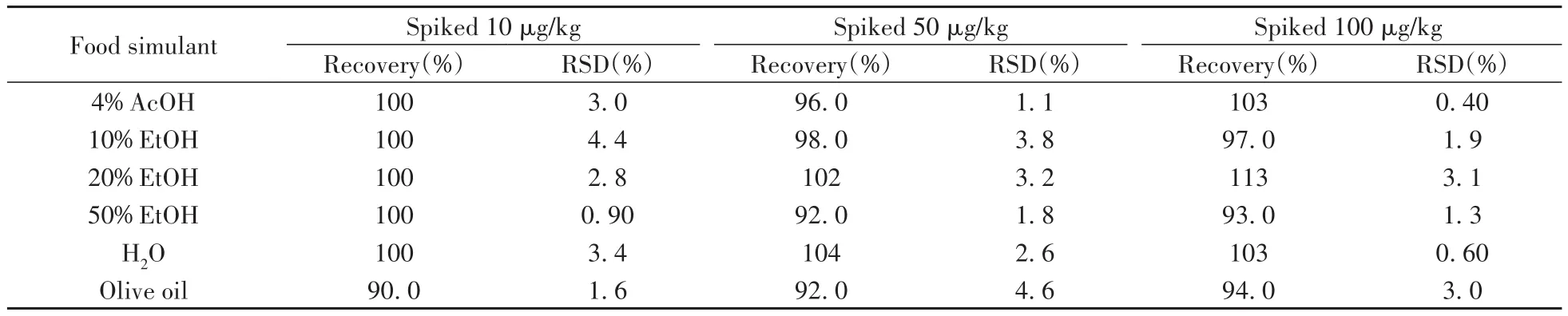
表2 不同食品模拟物中丙烯酰胺的回收率及相对标准偏差(n=6)Table 2 Recoveries and RSDs of acrylamide in different food simulants(n=6)
2.4 实际样品测定
随机采集20批纸制食品接触材料样品,根据实际使用情况选择合适的食品模拟物进行迁移试验(依据GB 31604.1-2015[22]和GB 5009.156-2016[23]),所得溶液采用本方法进行分析。结果显示,有2批纸吸管检出丙烯酰胺,其迁移量分别为13.2、80.7µg/kg,其余18批样品均未检出。按纸制食品接触材料的材质类型进行统计可知,单一材质的纸吸管的阳性检出率高于塑料淋膜类纸制品和纸基复合包装材料(见表3)。

表3 不同材质中丙烯酰胺迁移量的检出率分析Table 3 Analysis of the detection rates of acrylamide migration in different paper-based materials
3 结 论
本研究采用超高效液相色谱-串联质谱建立了纸制食品接触材料中丙烯酰胺迁移量的测定方法。实验结果表明,该方法操作简便、结果准确、灵敏度高、重复性好,在不同食品模拟物中具有良好的准确度和精密度。水溶性食品模拟物中丙烯酰胺的检出限为1.0µg/L,定量下限为5.0µg/L;油性食品模拟物(橄榄油)的检出限为5.0µg/kg,定量下限为10.0µg/kg,完全满足我国法规限量要求。实际样品测试发现,纸吸管作为单一材质的纸制食品接触材料存在丙烯酰胺迁移风险和食品安全隐患。本研究所建立的测定方法适用于纸制食品接触材料中丙烯酰胺迁移量的定性和定量分析,能为检测机构和相关监管部门评估纸制食品接触材料中丙烯酰胺迁移的合规性和风险性提供技术支持,为广大消费者的健康保驾护航。
