基于SPME/GC×GC-QTOF MS法测定回收PET中的挥发性有机物
2021-11-28叶智康林勤保吴学峰郝天英钟怀宁
叶智康,曾 莹,林勤保*,吴学峰,郝天英,董 犇,李 丹,钟怀宁*
(1.暨南大学 包装工程研究所,广东普通高校产品包装与物流重点实验室,广东 珠海 519070;2.广州海关技术中心,国家食品接触材料检测重点实验室(广东), 广东 广州 510623)
聚对苯二甲酸乙二醇酯(Polyethylene terephthalate,PET)是应用较多的热塑性聚合物,具有优良的物理性能、化学稳定性、加工性能和安全性,被广泛用于碳酸饮料、矿泉水、茶饮料、果汁等饮品的包装[1-3]。聚酯不能自发在自然界中降解,而人为降解不经济环保,为了不造成环境污染和资源浪费,最好的处理办法是回收利用[4-5]。
目前回收的PET往往被用于降级再生利用,更多用于非食品接触的工业制品上,如从食品接触材料转化为纺织纤维,这种相对低端的回收利用使食品级的PET材料与有更多杂质的非食品级PET混合,造成资源浪费[6-7],而理想的回收是同级之间的回收,即“瓶到瓶”之间的回收利用[8]。实际上,PET是一种具有低扩散率和低吸附特性的惰性材料,在前期消费中对外源化合物的吸收较低,因此是一种适合回收的材料[2,8-9]。许多国家和组织如美国和欧盟已经允许回收PET(rPET)用于食品接触材料。回收PET材料需要通过相关法规的风险评估方可在食品接触材料中使用[10]。回收的PET中存在着有意或者非有意添加的风险物质,一旦这些物质从回收PET瓶中迁移至食品,将造成安全隐患[11]。残留在回收PET中的挥发性化合物除了存在安全风险,还可能会影响再生PET瓶中食品的感官特性[12]。回收PET中的污染物主要来源于聚酯的降解产物、人为误用(消费后的PET瓶可能被用于储存其他化学品)、环境污染以及初期使用时的污染(如瓶上标签的油墨污染)[4,13]。据调查,回收PET中的挥发性有机物有脂肪族类、芳香族醛、醚类、酯类、脂肪酸类、芳香族化合物、烷烃类、烯烃类、酮类和醇类[9]。目前我国对食品接触用PET瓶的回收状况了解不足,缺乏足够的回收PET污染物数据进行安全性评估[10]。
对回收PET中的挥发性有机物进行调查首先需建立合适的检测方法。回收PET和其他塑料中挥发性有机物的前处理方法包括索氏提取[14]、浸泡提取[15]、静态顶空提取[16-17]、吹扫捕集[13]和顶空-固相微萃取[18]等。对于大规模的样品检测,方法应具备高效、灵敏的特点。固相微萃取(SPME)具有绿色无污染、高效快速、操作简单方便、易于自动化等优点[19],相比于静态顶空,拥有更高的灵敏度,能够富集更低浓度的挥发性有机物[20]。仪器方面,常用气相色谱[21]和气相色谱-质谱联用法[22]对挥发性有机物进行检测,但对于复杂样品的检测,化学性质相近的物质可能会出现共流出现象,从而导致物质定性不准确。全二维气相色谱-串联四极杆飞行时间高分辨质谱具有高灵敏度、高峰容量以及高分辨率的特点,可以很好地解决物质共流出的问题[23],在非靶向物质的筛查方面有很好的效果[24]。目前已有学者将GC×GC-QTOF-MS用于高分子聚合物聚己二酸-对苯二甲酸丁二酯(PBAT)生物降解膜的检测[25],而用于回收PET中挥发性有机物测定的研究还较少。
本研究建立了顶空-固相微萃取结合全二维气相色谱-串联四极杆飞行时间高分辨质谱测定回收PET中挥发性有机物的方法,对SPME萃取头纤维、萃取温度、顶空平衡时间、调制周期和升温速率进行了优化。对9个回收PET样品中的挥发性有机物进行测定,采用NIST谱库匹配结合色谱保留指数定性,并对高频检出物质进行半定量分析。
1 实验部分
1.1 仪器与试剂
全二维气相色谱-串联四极杆飞行时间高分辨质谱仪(GC×GC-QTOF MS)由7890 GC/5975C气相色谱-串联四极杆飞行时间质谱仪(美国Agilent公司)和固态热调制器(中国雪景科技公司)组成;顶空-固相微萃取自动进样器(美国Agilent公司),ME204电子天平(瑞士Mettler Toledo仪器公司),固相微萃取针纤维为聚二甲基硅氧烷(PDMS)、二乙烯基苯/聚二甲基硅氧烷(DVB/PDMS)和二乙烯基苯/碳分子筛/聚二甲基硅氧烷(DVB/C-WR/PDMS)(美国Agilent公司)。
正十三烷(CAS No.629-50-5,纯度99.6%,德国Dr.Ehrenstorfer公司),(+)-柠檬烯(CAS No.5989-27-5,纯度98.55%,德国Dr.Ehrenstorfer公司),正构烷烃(C7~C40,1 000 mg/L,中国安谱公司)。
1.2 样品前处理
样品制备:将回收PET样品(S0)经液氮粉碎成粉末后进行优化实验,称取1 g(精确至0.001 g)置于20 mL顶空瓶中上机测试。测定回收PET样品(S1~S9)时,将其裁剪成约8 mm×8 mm的碎片,称取1 g(精确至0.001 g)置于20 mL顶空瓶中,称重后立即密封,以减少挥发性物质的损失。
样品处理:样品由HS-SPME自动进样器进样,顶空瓶在110℃下平衡30 min,固相微萃取针(DVB/C-WR/PDMS)在振摇模式下吸附10 min,并在250℃前进样口中解吸2 min,解吸后的挥发性物质进入全二维色谱-飞行时间质谱仪进行分析。第一次使用固相微萃取针前将萃取针置于260℃下老化40 min,测试中吸附样品前老化10 min,进样结束后老化2 min,以消除萃取针中的吸附物质残留。
1.3 GC×GC-QTOF MS条件
色谱条件:一维色谱由2根HP-5MS 15 m×0.25 mm×0.25µm柱相连(两柱间配备反吹系统);二维色谱柱为DB-17MS(1 m × 0.25 mm × 0.25 µm);载气:氦气(流速:1.2 mL/min);调制柱:SV调制柱(C6~C40);调制器调制周期:4 s;柱箱升温程序:初始温度40℃保持5 min,以8℃/min升至260℃,保持8 min;不分流模式进样。
质谱条件:MSD传输线温度:320℃;采集模式:全扫描;扫描质量范围:35~500 amu;EI电离能量:70 eV;溶剂延迟:0 min。
1.4 前处理及仪器参数优化
本实验对样品前处理中的固相微萃取纤维类型、萃取温度、顶空平衡时间以及仪器条件中柱箱的二维调制器周期和升温速率进行了优化,以得到最佳的检测参数。
对比了3种不同类型的固相微萃取纤维头(100µm PDMS、65µm DVB/PDMS和80µm DVB/C-WR/PDMS)的萃取效果,并对萃取温度(50、70、90、110、130、150℃)和顶空平衡时间(15、30、60 min)进行了考察。
仪器参数优化方面,对比了3种调制周期(2、4、6 s)的出峰效果以及3、5、8、10℃/min 4个升温速率下色谱峰的分离效果。
1.5 物质定性与定量
采用NIST 17谱库匹配结合色谱保留指数(RI)定性,将正构烷烃混合标准品(C7~C40)在相同的仪器条件下上机检测,根据保留时间计算物质的保留指数并与NIST 17谱库中的参考值对比,使用全二维色谱数据处理工作站Canvas软件(W1.8.0.29165)进行数据处理。谱库匹配度高于800(满分为1 000)的物质被列为定性物质,采用(+)-柠檬烯和正十三烷对检测物质进行半定量。
2 结果与讨论
2.1 方法优化
利用GC×GC-QTOF MS对萃取纤维头类型、萃取温度、平衡时间、调制周期和柱箱升温速率进行优化,以色谱峰总面积和色谱峰数量作为优化依据。
2.1.1 SPME纤维头的选择由图1A可知,采用80µm DVB/C-WR/PDMS纤维头时色谱峰总面积最大,色谱峰的数量最多,65µm DVB/PDMS次之,100µm PDMS最少。这是因为,固相微萃取针的萃取效率取决于纤维上的涂层,PDMS纤维涂层的主要成分为聚二甲基硅氧烷,对于极性较低的物质,如烷烃、烯烃类有较好的吸附性;DVB/PDMS涂层在PDMS的基础上添加二乙烯基苯,除烷烃和烯烃外,还检出了醛和醇类物质;DVB/C-WR/PDMS混合萃取头的吸附范围最广,检出物质最多,物质类型涵盖烷烃、烯烃、苯类、醛酮类以及酯类等。对于未知样品的分析,萃取纤维所吸附的物质范围应尽可能广,因此采用DVB/C-WR/PDMS作为最佳萃取纤维头。

图1 不同顶空条件下的色谱峰总面积和挥发性有机物数量(样品S0)Fig.1 Total areas of chromatographic peaks and VOC numbers of rPET sample(S0)in different headspace conditions
2.1.2 萃取温度的优化考察了萃取温度(50、70、90、110、130、150℃)对萃取效果的影响。由图1B可知,色谱峰的总响应与色谱峰数量均呈现先增加后下降的趋势,并均在萃取温度为110℃时达到最大值。当温度较低时,样品内沸点较高的物质未能挥发至空气中,导致色谱峰较少。随着萃取温度的上升,更多物质汽化至样品上空被纤维涂层吸附,且在110℃时萃取效率达到最佳。由于纤维涂层的吸附和解吸同时进行,当温度过高时,物质反而被解吸,导致吸附效率下降,色谱峰的响应和数量也随之下降。因此,选择110℃为萃取温度。
2.1.3 平衡时间的优化平衡时间是顶空的重要参数,影响各组分在气相中的分压。对比了15、30、60 min的顶空平衡时间对萃取效果的影响。由图1C可看出,色谱峰总响应面积与色谱峰数量随着平衡时间的上升呈先上升后下降的趋势,并在30 min时达到最大。平衡时间为15 min时,由于样品中的挥发性物质未达到气液平衡,色谱峰总面积与峰数量仍有继续上升的趋势。当平衡时间达到60 min时,色谱峰总响应与物质数量下降,可能是由于平衡时间过长,使气相中的水蒸气含量增加,导致目标物浓度和数量下降[26]。因此,选择30 min作为方法的顶空平衡时间。
2.1.4 调制周期的优化全二维气相色谱中,二维调制器的调制周期对色谱峰的峰形和分离效果影响较大。调制周期是指从一维色谱柱流出的物质被调制器捕集到释放的时间,调制周期需要设定为合理值。调制周期过大,可能会影响物质在一维柱上的分离效果,使已在一维柱上分离的物质重新聚集在二维柱上分离,导致一维的分离效果减弱。调制周期过小,容易造成“峰迂回”现象,使物质无法在一个完整的调制周期内从二维柱中流出,并影响下一个周期内物质的出峰。
由图2可知,回收PET样品均可在不同周期内出峰,且色谱峰分离良好,无“峰迂回”现象。从峰形上看,调制周期为2 s的色谱峰在二维上出现轻微拖尾,调制周期为4 s和6 s的色谱峰峰形较好。由于过大的周期会牺牲一维的分离效果,因此选择4 s为最佳调制周期。
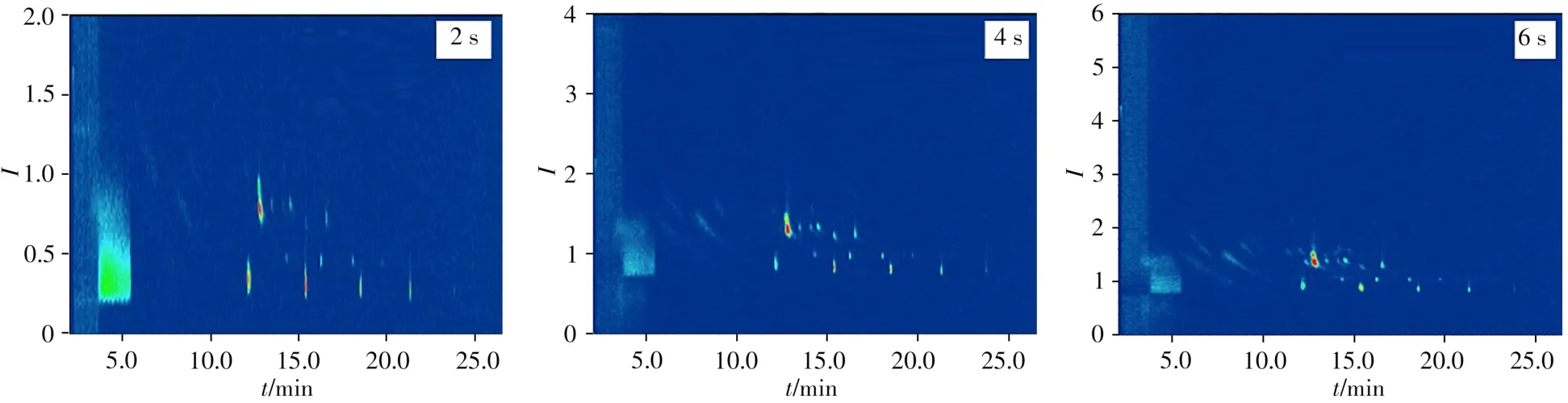
图2 不同调制周期下典型回收PET样品的二维总离子流色谱图(样品S0)Fig.2 Two-dimensional total ion chromatograms(TICs)with different modulation periods for typical rPET sample(S0)
2.1.5 升温速率的优化柱箱升温速率也会对物质出峰造成影响。升温速率降低,物质在一维上的流出温度降低,经过二维柱的温度也会降低,导致物质更容易在色谱柱中被保留,易造成色谱峰在二维上拖尾。而升温速率过高,沸点和性质相近的物质在一维上可能出现难以分离的现象,造成共流出。另外,升温速率提高时,物质在一维柱的流出温度升高,二维柱的温度随之提高,也可能导致物质在二维上的分离效果不佳。
由图3可以看出,4种升温速率下色谱峰均能很好地分离。从峰形上看,升温速率为3℃/min的色谱峰在二维上出现拖尾,导致峰形不聚焦,可能会造成定量不准确。随着升温速率的提高,色谱峰的峰形越来越聚焦,但在二维上的分离效果变差。综合考虑色谱峰峰形和分离效果,选择8℃/min的升温速率用于样品分析。

图3 不同升温速率下的典型回收PET样品的二维总离子流色谱图(样品S0)Fig.3 TICs with different heating rates for typical rPET sample(S0)
2.2 样品检测
2.2.1 物质定性经过实验优化,确定rPET挥发性物质测定的最佳方法参数为:SPME纤维头类型为80µm DVB/C-WR/PDMS,顶空萃取温度110℃,平衡时间30 min,调制周期4 s,柱箱升温速率8℃/min。利用GC×GC-QTOF MS对9个rPET样品(S1~S9)进行检测,通过NIST谱库匹配结合色谱保留指数定性。
9个回收PET样品中共检出209种挥发性有机物,其中苯系物40种、烷烃类29种、醇类28种、醛酮类28种、酯类27种、烯烃类25种、萘类11种、羧酸类3种、酚类2种以及其他类16种,与已有文献所检测到的挥发物种类基本相同[9]。
苯系物是检出数量最多的物质,大多数苯系物的苯环上存在短链烷烃的支链,如邻二甲苯、均三甲苯、1-乙基-2-甲基-苯等。苯系物产生的原因可能是回收PET在不同环境的作用下发生降解[27]。
烷烃类物质有较多检出,大多数烷烃的出峰时间在19 min后,碳数范围为C14~C21。烯烃类是回收PET中的典型物质,其中萜烯有较多检出,如柠檬烯、γ-松油烯、β-红没药烯等。此类萜烯可能源自早期PET瓶中灌装的饮料,在茶类饮料和柑橘类饮料中萜烯类是重要的风味化合物[28-30],饮料中的萜烯经长时间与PET瓶接触造成在回收PET中的残留。
醛酮类物质中,2-癸酮在样品中有较多检出,苯甲醛、苯乙酮为聚酯热降解中释放的物质[27],另外还在3个样品中检测到壬醛和辛醛。
醇类物质也有较多检出,检出频次相对较高的为2-十二醇、十二醇、2-甲基-1-十一醇。
酯类物质中,各样品的共同检出物质较少,检出频率最高的为邻苯二甲酸二甲酯,此物质是塑料加工过程中常用的塑化剂。萘类物质在样品中也有检出,此类物质的存在可能源自环境的污染[14]。其他类物质为少量醚类、硅氧烷,以及带有S、N、Br等元素的化合物。
2.2.2 高频检出物质分析图4为样品2的二维总离子流色谱图。9个rPET样品中,检出频次大于5的物质有(+)-柠檬烯、十四烷、γ-松油烯、2-十二醇、萘、1-甲基萘、5-甲基-1-十一烯、2,4-二叔丁基苯酚、2-癸酮和1-亚乙基-1H-茚。(+)-柠檬烯是常见的rPET中的污染物,由原生PET瓶与饮料接触而来[31]。2,4-二叔丁基苯酚可能源自原生PET中的抗氧剂168,在使用和回收过程中,抗氧剂降解为2,4-二叔丁基苯酚并残留在rPET样品中。
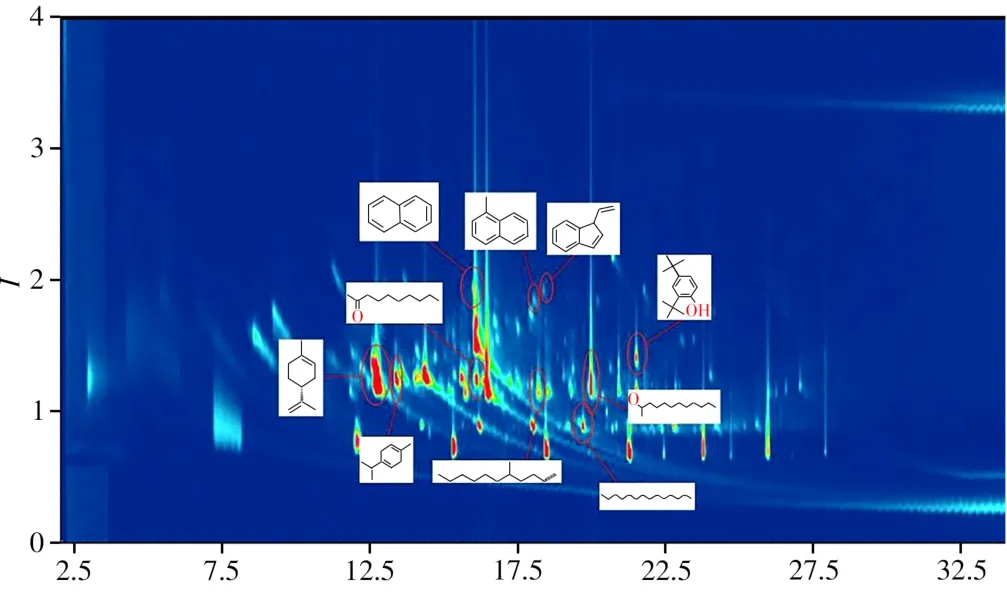
图4 样品2的二维总离子流色谱图及高频检出物质Fig.4 TIC for sample 2 with high frequency detection of compounds
对以上物质进行半定量,定量结果如表1所示。结果显示,10种高频物质的含量均低于3 mg/kg,十四烷和(+)-柠檬烯的含量最高。十四烷的最高含量为2.13 mg/kg,平均含量为0.85 mg/kg;(+)-柠檬烯的含量在0.10~1.42 mg/kg之间,平均含量为0.52 mg/kg。需要说明的是,回收PET材料中可能存在误用情况[32],即消费者可能忽略PET产品的原始用途而用于其他方面(如用矿泉水瓶储存农药),从而导致某个污染物的浓度水平极高,在本研究的样品中未发现误用情况。

表1 高频挥发性有机物的定量结果Table 1 Quantitative results of high frequency volatile organic compounds
3 结 论
本文构建了GC×GC-QTOF MS检测回收PET中挥发性有机物的方法,并对相关前处理参数和仪器参数进行了优化。顶空-固相微萃取的最佳条件为:80µm DVB/C-WR/PDMS萃取纤维头,萃取温度110℃,平衡时间30 min,二维调制器调制周期4 s,仪器升温速率8℃/min。实际样品检测中,共检出209种挥发性有机物,检出物包括苯系物、烷烃类、醇类、醛酮类、酯类、烯烃类、萘类、羧酸类和酚类等,检出(+)-柠檬烯、十四烷、γ-松油烯等高频物质。回收PET中含量最高的挥发性成分为十四烷,其次为(+)-柠檬烯,回收PET中的污染物来源主要为聚酯降解产物、前期使用残留以及环境污染。
