不同剂量右美托咪定滴鼻在婴儿MRI检查中的应用
2021-11-26杨海扣孙剑周静张浩张玉凤
杨海扣,孙剑,周静,张浩,张玉凤
(扬州大学附属淮安医院,淮安市妇幼保健院麻醉科,江苏 淮安 223002)
MRI检查有独特优势,且无放射性辐射,但检查室噪声高达70~80 db,婴儿必须达到足够镇静深度才能完成检查,否则可能产生假象或伪影,影响检查的有效性和准确性。右美托咪定无色无味,几乎无鼻黏膜刺激性,鼻腔给药生物利用度高,患儿及家长易于接受,尤其适用于婴幼儿无创性检查,目前已广泛用于儿童门诊镇静。本研究旨在探讨不同剂量右美托咪定滴鼻在婴儿MRI检查的应用效果,现报道如下。
1 资料与方法
1.1 临床资料 选取2020年1—7月于本院接受MRI检查患儿61例,年龄1~12个月,体质量4.3~9.5 kg,ASAⅠ~Ⅱ级,随机分为D1组(Dex 2µg/kg,n=30)和D2组(Dex 3µg/kg,n=31),所有患儿法定代理人均签署知情同意书,研究经本院医学伦理委员会审核批准。纳入标准:患儿近期无呼吸道感染,无过敏史,无心肺肝肾疾病,无智力及精神发育异常,48 h内未接受过麻醉及镇静药物。
1.2 方法 患儿禁清饮2 h,禁乳4 h,清理鼻腔,患儿在家长协助下采取仰头平卧位,使用1 mL 不带针注射器分别注入双侧鼻腔等量右美托咪定原液(Dex,江苏恒瑞医药股份有限公司,国药准字H20090248,批号190221BP),给药后维持患儿滴鼻时体位3 min,并轻捏双侧鼻翼促进药物吸收。D1组Dex用量为2µg/kg,D2组为3µg/kg。滴药后30 min内进行Ramsay评分,1分:焦虑躁动或烦躁不安;2分,平静配合,有定向力;3分,只对指令有反应;4分,嗜睡但对轻叩眉间或强声刺激反应敏捷;5 分,嗜睡且对轻叩眉间或强声刺激反应迟钝;6分,对刺激无反应,呈深睡状态。Ramsay评分达5分后进行MRI检查,30 min仍未达5分者或检查过程患儿体动需追加七氟醚吸入麻醉完成检查为Dex 镇静失败。患儿入睡后使用便携式监护仪(血氧仪JERRY-Ⅱ,山西洁瑞医疗器械股份有限公司)观察SpO2、心率及呼吸,异常情况酌情处理,其中有3 例患儿检查过程中出现体动,家长拒绝吸入七氟醚,改日检查,退出研究。
1.3 观察指标 ①镇静起效时间,从滴药完毕至镇静满意所需时间;②苏醒时间,从检查完毕至患儿清醒时间;③镇静失败率,患儿用药后30 min镇静深度不能达到检查要求,或在检查中途醒来导致检查失败者;④不良反应,包括低氧血症、心动过缓(HR<80次/min)、恶心呕吐、呼吸抑制等。
1.4 统计学方法 采用SPSS 19.0 统计学软件进行数据分析,计量资料以“±s”表示,采用t检验,计数资料以[n(%)]表示,采用χ2检验,以P<0.05为差异具有统计学意义。
2 结果
2.1 两组患儿临床资料比较 两组患儿性别、年龄、体质量、检查时间比较差异无统计学意义,具有可比性,见表1。
表1 两组患儿临床资料比较(±s)Table 1 Comparison of clinical date between two groups(±s)

表1 两组患儿临床资料比较(±s)Table 1 Comparison of clinical date between two groups(±s)
检查时间(min)17.70±1.53 18.60±2.20组别D1(n=30)D2(n=31)性别(男/女)21/9 20/11年龄(月)3.53±1.98 3.75±2.21体质量(kg)6.93±1.59 6.51±1.97
2.2 两组患儿镇静效果比较 两组患儿起效时间、苏醒时间及镇静成功率比较差异有统计学意义(P<0.05),见表2。
表2 两组患儿镇静效果比较(±s)Table 2 Comparison of sedative effects between two groups(±s)
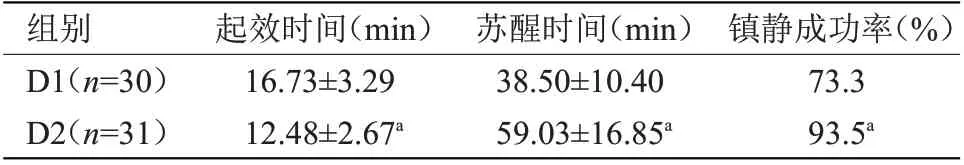
表2 两组患儿镇静效果比较(±s)Table 2 Comparison of sedative effects between two groups(±s)
注:与D1组比较,aP<0.05
组别D1(n=30)D2(n=31)镇静成功率(%)73.3 93.5a起效时间(min)16.73±3.29 12.48±2.67a苏醒时间(min)38.50±10.40 59.03±16.85a
2.3 两组患儿不良反应发生情况比较 两组患儿均未出现严重低氧血症(SpO2<90%)、呼吸抑制、恶心呕吐等不良反应。两组心动过缓分别为1例、3例,给予刺激足底或耳垂后升至正常,未予以药物干预。
3 讨论
MRI 检查耗时长,噪音嘈杂且音量大,要求检查者完全静止不动。婴儿由于其心理及生理发育不成熟常无法完成此项检查。传统麻醉门诊镇静药物包括咪达唑仑、水合氯醛、氯胺酮、芬太尼等勋在诸多缺点,难以推广使用。Dex已经广泛应用于儿童门诊心脏彩超、听力筛查、CT、MRI 及听力诱发电位等检查,是一种高选择性α2受体激动剂,用于儿童镇静的独特优势在于不影响呼吸,可以发挥类似生理睡眠时的非快速动眼睡眠状态[1]。Dex 无色无味,对鼻黏膜几乎无刺激,有报道认为滴鼻给药生物利用度达65%,血药浓度35~45 min 即达峰值[2],本研究中患儿给药后30 min 左右达满意镇静效果,与上述研究相符。有研究[3]认为,Dex体内清除率在儿童期随年龄和体质量增长,新生儿期为42.4%,1岁时则达84.5%。因此,年龄是影响临床药效的因素之一。另外,经鼻给药可以绕过肝脏首过消除效应,还可以通过三叉神经和嗅神经绕过血脑屏障直接作用于中枢神经系统[4]。
在一项对比研究中[5],Dex 静脉注射的镇静起效时间为15 min,95%CI为15~20 min;雾化装置给药的起效时间为47.5 min,95%CI为25~135 min;滴鼻给药的起效时间为60 min,95%CI为30~75 min。3 种给药方式的镇静持续时间无显著差异。使用PK 模式进行药代动力学研究,雾化装置和滴鼻给药的Dex 生物利用度无显著差异,EC50 为903 pg/mL。本院门诊使用滴鼻方式给药镇静效果满意,未使用特殊装置,可减轻治疗费用,提高患者满意度。
本研究结果显示,随着药物剂量增加镇静起效时间缩短,苏醒时间有所延长。侯慧艳等[6]对脑瘫患儿使用右美托咪定2µg/kg 滴鼻镇静起效时间为(23.45±4.25)min,苏醒时间为(65.48±5.69)min,起效及苏醒时间较本研究同等剂量延长,可能与脑瘫患儿大脑兴奋性不同于正常儿童有关。随着剂量递增,苏醒时间显著延长,符合右美托咪定药物代谢规律。纪宏新等[7]对CT检查患儿采用改良序贯法测得镇静的ED50 为2.09 µg/kg,95%CI 为1.69~2.45 µg/kg;ED95 为2.94µg/kg,95%CI为2.54~5.05µg/kg,可以为临床用量提供参考。Miller 等[8]研究表明,患儿经鼻给药离院时间为44~91 min,给药剂量高未必延长患儿离院时间。
本研究结果显示,D1 组(Dex 2µg/kg)滴鼻成功率显著低于D2组(P<0.05)。有研究[9]认为,此剂量对1~4岁儿童镇静满意率仅为60%,低于本研究成功率,可能与本研究患儿年龄小有关。临床观察到随着年龄增加,滴药时患儿易发生抵抗,导致药物从口鼻流出。对于镇静失败者,追加七氟醚吸入可控性好,效果确切,对苏醒时间影响小。但是冯雷[10]使用Dex 1.5µg/kg 滴鼻用于CT 和MRI 检查,镇静效果满意,血流动力学稳定,起效和苏醒迅速,且不良反应少。在一项对9 985 名患儿回顾性研究中[11],体质量5~10 kg 患儿Dex滴鼻剂量为1.5~2.5µg/kg,体质量>10 kg用量为2.5~3 µg/kg,结果显示首次镇静成功率为82.49%。Tug 等[12]研究表明在MRI 检查时,4µg/kg 较3µg/kg 镇静效果更好,更易与亲人分离,成功率更高,两组起效时间,镇静持续时间比较差异无统计学意义,心血管及低氧血症的发生率比较差异无统计学意义。出现这些差异可能与操作、检查类型、患儿基础情况、药品厂家批号等因素有关。
在一项对2~5岁135名儿童研究中[13],对比不同剂量右美托咪定联合氯胺酮后进行静脉穿刺,单用右美托咪定的成功率为47%,单用氯胺酮的成功率为68%,两者联合使用的成功率为80%,但是单用氯胺酮组的精神异常,呼吸异常等并发症明显增高。对于无禁忌证患儿,尤其是伴随疼痛刺激的操作,氯胺酮可作为补救措施之一。
Dex 常见不良反应包括心动过缓、低血压、口干、恶心等。本研究观察到用药后患儿心率均有不同程度下降,除药物作用外,也与镇静状态有关。多数儿童刺激耳垂或足底心率可达正常水平,无需使用药物干预。患儿清醒后先饮水,未观察到低氧血症等其他不良反应。Dex 的不良反应主要表现在对心血管系统的影响,但是仍有导致低氧血症和高碳酸血症的报导[12,14]。Miller等[15]对147例唐氏综合征患儿使用Dex 2.5µg/kg滴鼻,未见显著心血管系统不良反应。尽管如此,仍应关注Dex可能存在的不良反应。
本研究的不足之处在于:①无空白对照组;②多数家长诉患儿离院后仍处于入睡状态,无法继续进行Ramasy评分;③缺乏Dex血药浓度监测指导临床;④需要纳入更多样本和影响因素。因此,应增加研究样本数量,完善研究结果。
