联合使用氨甲环酸在减少肱骨骨折内固定围术期失血中的作用
2021-11-23王陶然高嘉锴孙守斌郝志龙李泽伟潘静心牛志霞
王陶然,高嘉锴,毕 龙,孙守斌,郝志龙,李泽伟,潘静心,牛志霞
空军军医大学第一附属医院骨科,西安 710032
创伤骨科中肱骨骨折属于常见的类型,其按部位分为肱骨近端骨折、肱骨干骨折及肱骨远端骨折,占全身骨折的9%~12%[1-4],手术若处理不当可能遗留功能障碍。其中肱骨近端骨折、肱骨干骨折及合并劈裂骨块较长的肱骨远端骨折等较复杂骨折手术由于无法使用止血带止血处理,围术期出血有时无法控制,需输血治疗,甚至出现血肿、感染、伤口不愈合等并发症[5]。
近年来,抗纤溶药物在预防严重创伤患者出血性死亡方面引起了广泛的关注,氨甲环酸(tranexamic acid,TXA)已被列入世界卫生组织的基本药物清单[6],临床上常用于减少髋、膝关节置换术围术期失血和输血量。对于上肢骨折患者,尤其无法使用止血带的肱骨骨折患者,同样原理使用TXA对其围术期出血影响的研究较少[7-8]。本研究回顾性分析2016年5月—2019年9月空军军医大学第一附属医院骨科治疗的肱骨骨折患者70例,旨在评价TXA应用于上肢骨折的效果。
临床资料
1 一般资料
纳入标准:(1)年龄18~70岁;(2)肱骨骨折,包括肱骨近端骨折(Neer分型为3部分或4部分骨折)、肱骨干骨折(AO分型为B型或C型)及肱骨远端骨折(AO分型为C型);(3)均予以开放复位手术治疗。排除标准:(1)转移性或原发性肿瘤所致病理性骨折;(2)肝肾功能不全;(3)既往或治疗时发现患有血栓性疾病,包括肺栓塞、深静脉血栓形成等;(4)合并血液系统疾病,包括弥漫性血管内凝血等;(5)患有意识障碍或精神疾病;(6)合并严重消化道、呼吸道、心脑血管疾病;(7)合并骨肿瘤、骨髓炎、骨结核;(8)合并下肢多发创伤。
本组肱骨骨折患者70例,男性50例,女性20例;年龄23~58岁,平均38.3岁。根据术中使用TXA与否分为TXA组及对照组。两组患者一般资料比较差异无统计学意义,见表1。本研究获笔者医院医学伦理委员会批准,患者及家属均签署知情同意书。
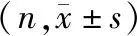
表1 两组患者一般资料比较
2 方法
2.1手术方法及围术期处理 由同一手术团队完成两组患者手术,适当消肿后于伤后2~7d手术。术前30~60min使用一代或二代抗生素预防感染,术后持续使用抗生素1~2d。根据具体情况选择全身麻醉或神经阻滞麻醉进行手术。以相应方式麻醉后,采用标准手术入路,予以开放复位钢板内固定,然后置引流管1根,关闭创口。
TXA组患者术前15min静脉滴注1g TXA,并将1g TXA溶解于100mL生理盐水中,2块纱布浸润后于透视期间及闭合切口前填塞止血,术毕伤口引流管逆向打入剩余TXA溶液并夹闭3h后打开;对照组则予以术前静脉滴注平衡盐、生理盐水浸润纱布填塞止血,术毕伤口引流管夹闭于3h后打开。
2.2术后处理及观察指标 术后第2天开始常规予以肩、肘关节功能锻炼,下地活动预防卧床并发症。同时术后第1天记录术中失血量、总失血量、术中纱布使用量(普通条形纱布,术中常规使用擦拭、填塞术野)、手术时间、术后引流管引流量、术中术后输血及并发症发生率。
其中术中失血量=吸引器瓶中的液体总量-术中冲洗液体量+纱布称重净增加重量(术中浸满1块纱布按25mL计算)。根据Gross方程式计算总失血量[9],总失血量=术前血容量(PBV)×(术前Hct-术后Hct),本病例使用的红细胞压积(Hct)数据来源于术前3d内及术后第1天血常规。通过Nadler方程计算PBV[10],PBV=K1×h3+K2×w+K3[h:身高(m),w:体重(kg)]。男性患者K1=0.3669,K2=0.03219,K3=0.6041;女性患者K1=0.3561,K2=0.03308,K3=0.1833。对于血红蛋白(Hgb)<80g/L,给予输血治疗,目标纠正至Hgb>95g/L,对于Hgb在80~100 g/L者根据实际情况决定是否输血,记录输血量及输血率。
术后切口并发症:住院期间伤口换药时严格记录切口并发症情况,包括红肿、渗出增多、感染、脂肪液化、切口愈合不良等;全身并发症:包括肺栓塞、深静脉血栓、心脑血管意外等;术后关节僵硬及骨折不愈合等。
3 统计学分析
结 果
通过病例查找、电话及门诊复诊等方式进行随访,时间10~18个月,平均13.0个月。TXA组术中失血量、纱布使用量、术后引流量均显著少于对照组(P<0.05)。两组患者手术时间、总失血量比较差异无统计学意义(P>0.05)。见表2。两组患者术后伤口均未出现感染、血管神经医源性损伤、心脑血管及局部伤口延迟愈合等并发症;术后两组患者均获得骨折愈合,两组比较差异无统计学意义(P>0.05)。
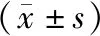
表2 两组患者术中及术后指标比较
讨 论
创伤骨科中的血液管理策略已经取得初步效果,尤其下肢关节手术的围术期失血量控制已成为研究重点[5,7-8,11]。同时在肱骨骨折手术中,特别是较为复杂的肱骨骨折手术由于无法应用止血带,临床中主要使用电凝止血、缝线结扎、纱布填塞按压等方式,效果有限,有导致围术期出血量增多、术者操作难度增加、医疗风险增加的可能。对于减少上肢骨折围术期失血量的研究,尤其肱骨骨折手术应用TXA在文献中的报道及探讨少见。TXA是一种合成赖氨酸衍生物,通过竞争性地与纤溶酶原赖氨酸结合位点结合发挥作用,从而阻断与纤维蛋白的相互作用以减少失血[12],临床中已常规使用于髋、膝关节置换术中[5,13]。本文在肱骨骨折手术中,采用了静脉给药全身应用结合TXA溶液纱布填塞、血浆引流管逆向注射局部应用,并探讨其安全性及有效性。
在骨科的脊柱手术和关节置换术中,TXA已被广泛应用于减少术中和术后的出血和肿胀,降低输血率,同时并未增加血栓形成率[6]。近年来临床上对于TXA的应用已从传统的静脉给药途径延伸至局部用药[14],还有肌肉注射、口服及局部应用等[15]。本研究中联合1g TXA溶液静脉使用,1g TXA溶解于100mL生理盐水浸湿纱布后局部使用。其静脉应用在60min后达到血药浓度峰值,可以维持2h左右的半衰期,基本符合肱骨骨折手术时间需求,且在24h后90%可清除。Sabatini 等[5]在全膝关节置换术中推荐术前15min开始静脉使用TXA,并认可其安全性。Ishida等[10]研究认为剂量<2g较为安全。Gillette 等[13]认为全身及局部使用TXA均不会增加深静脉血栓、肺栓塞风险,且认为局部使用TXA可以保留局部药物浓度,使TXA具有足够的时间来发挥抗纤溶作用。本研究将全身使用与局部应用相结合,同样未发生肺栓塞、心脑血管意外、切口延迟愈合等相关并发症,术前、术后D-二聚体两组比较差异无统计学意义。由于本文的研究对象为肱骨骨折患者,术前及术后均鼓励患者下地活动,故相对于髋、膝关节置换的患者,卧床相关并发症的预防更加容易。以上也说明TXA应用在肱骨骨折内固定手术中安全可靠。
另外,本研究发现静脉滴注联合局部使用TXA,可以减少肱骨骨折内固定手术的术中失血量。同样,Zhang等[15]在31例肘关节僵硬松解术中,分别使用TXA纱布填塞、血浆引流管逆向注射等局部方式使用TXA,相较对照组获得良好松解效果的同时,也减少术中出血及血浆引流管引流量,未出现并发症。李坤和刘云鹏[11]在股骨近端防旋髓内钉(PFNA)手术中从股骨髓腔内注入TXA,同样减少围术期失血量及输血量,未显著增加并发症发生率。但近年来的研究多局限于全身或局部应用TXA,或联合其他抗凝药物及措施进行探讨[5,7-8,11,15],而本研究则将全身和局部应用TXA相结合,通过对照发现TXA组的术中出血量、术后引流量及纱布使用量均少于对照组,且差异有统计学意义。笔者认为静脉滴注给药可以发挥全身抗纤溶作用;而局部使用TXA纱布填塞加压及术毕伤口引流管逆向打入TXA溶液,可以在局部较长时间保留其浓度,且术中可以看到,TXA组的骨折断端间及软组织间渗血量都有所减少。需指出的是,TXA组比对照组的总失血量少,但差异无统计学意义(P>0.05),也说明使用TXA无法显著减少总失血量。笔者考虑除了术中出血量,不同患者身体素质、营养状况及围术期补液量的不同等因素均可影响从而导致总失血量差值的中和。另外,本文将纱布使用量也纳入研究中,这是由于在日常手术时,纱布并不是完全浸湿方才丢弃。出血量的增多必然会导致纱布使用量的增加,从而增加术者以及助手的操作频次,影响手术顺畅度。
另有文献显示TXA除了可以减少失血,还可以减少感染、局部血肿形成,改善伤口愈合和加速皮肤屏障的恢复[6,16]。本研究中两组患者均获得骨折愈合。但如果局部血肿形成,通过成骨因子刺激血管内皮间充质通路或直接来源于血液的间充质干细胞[17],可能导致骨化性肌炎,造成关节功能不佳,影响功能康复,所以局部应用TXA依然有减少局部血肿形成的作用[10],从而减少风险。结合本组病例,全身与局部相结合应用TXA于上肢创伤患者,可以在安全的基础上获得良好的疗效。
综上所述,许多较为复杂的肱骨骨折疾患由于无法使用止血带导致失血量增多,临床应予以足够重视。静脉滴注途径的全身抗纤维蛋白溶解凝血作用,以及局部应用途径的充足时间发挥抗纤溶作用,两者相结合可减少肱骨骨折开放复位内固定手术术中失血量、纱布使用量、术后引流管引流量,减少围术期失血,效果显著且安全。
