超细MoSi2的分散性研究
2021-11-21刘靠斌张建军陈卫华韦学龙杨先军
刘靠斌,张建军,陈卫华,韦学龙,杨先军
(南昌航空大学 材料科学与工程学院,南昌 330063)
引 言
MoSi2具有较高的熔点(2030 ℃),高强度和良好的导热性等优点,是下一代高温材料的候选材料[1-6]。MoSi2基复合材料作为高温结构材料,在航空航天领域主要用作涡轮飞行器发动机的高温部件,如叶片、燃烧器、喷嘴、密封环等,在汽车领域主要用作涡轮增压器转子、气体阀门、火花塞和先进涡轮发动机高温部件等[7]。MoSi2有三大缺点:高温强度不足,室温韧性差,在400~800 ℃会发生Pest现象。为了解决这三大缺陷,首先要解决MoSi2的团聚问题。众所周知,当MoSi2晶粒尺寸减小到亚微米或纳米时,MoSi2陶瓷的硬度、抗弯强度和断裂韧性会显著提高。然而,当MoSi2粉体尺寸减小时易于发生团聚,在烧结过程中,导致材料局部过热,晶粒异常长大,降低MoSi2材料的致密度,从而降低其机械性能。因此,超细MoSi2粉的均匀性分散对提高烧结能力和力学性能起着至关重要的作用。
由于高的表面自由能,纳米颗粒容易形成团聚体[8-9],为了避免颗粒聚集,通常使用物理方法(如高能球磨、磁力搅拌、超声波)和化学方法(添加分散剂)来分散纳米颗粒。近年来,由于优异的化学性质,如稳定性和良好的润湿性,表面活性剂已成为分散纳米颗粒的有效分散剂,如阴离子、阳离子、聚合物和无机分散剂。纳米颗粒通过静电排斥或静电阻碍在液相介质中的分散已被广泛研究,悬浮液的稳定可以通过添加分散剂控制颗粒表面的静电荷,类似地,静态稳定可以通过添加分散剂来实现。因此,在纳米材料制备过程中,保证纳米材料均匀分布、防止团聚是获得高性能纳米复合材料的前提,如何改善纳米粉体在液相介质中的分散和稳定性是十分重要的课题[10]。
以MoSi2粉体为分散对象,采用搅拌振荡分散技术对MoSi2粉体进行分散,本文通过对改变表面活性剂浓度、固液比以及搅拌时间,对在水介质中的分散性进行研究,优化实验参数,制备一种稳定且均匀分散的悬浮液,研究其分散机理,克服比表面积大所导致的易团聚。
1 实 验
1.1 原材料
原材料MoSi2粉(原始尺寸为1 μm)来源于上海乃欧纳米科技有限公司。表面活性剂为十二烷基硫酸钠(SDS),十二烷基苯磺酸钠(SDBS),聚乙烯吡咯烷酮(PVP),十二烷基三甲基溴化铵(CTAB)。
1.2 MoSi2的分散
首先,球磨MoSi2原料粉,以硬质合金罐为球磨罐,使用硬质合金球,球料比7∶1,使用QM-QX全方位行星式高能球磨机,球磨转速为150 r/min,球磨时间12 h,球磨介质为无水乙醇。然后烘干、过筛,获得均匀细小的MoSi2超细粉末。第二步,制备MoSi2/分散剂的均匀分散的悬浮液。在本文中研究了以下几种实验参数,包括SDS含量(0.4、0.8、1.6和3.2 g/L),固液比(MoSi2粉体与蒸馏水的重量比,1∶40、1∶60、1∶80、1∶100)。分散时间(1、2、4、6和8 h)处理后,分别静置24、48、72 h。根据沉降层来判断悬浮液的分散程度。
1.3 表征
相对沉降高度(RSH)可以通过以下公式进行表征MoSi2/表面活性剂的悬浮液的稳定性。RSH =H1/H,H1和H分别表示MoSi2/表面活性剂的沉降层以及悬浮液高度。使用美国Colloidal Dynamics公司生产的ZetaProbe测量MoSi2/SDS表面活性剂的Zeta电位值。采用美国FEI公司研发的型号为Nova Nano SEM 450的场发射扫面电子显微镜观察MoSi2颗粒的微观结构,使用德国BRUKER/AXS公司生产的D8 ADVANCE 型号的X射线衍射仪进行物相分析。
2 结果与讨论
2.1 表面活性剂对MoSi2分散的影响
图1为表面活性剂对MoSi2悬浮液相对沉降高度(RSH)的影响,固定参数:转速为800 r/min,搅拌时间为1 h,分散剂浓度为0.4 g/L,固液比(MoSi2粉末与蒸馏水的质量比)为1∶100。采用机械搅拌和超声方法,分别用SDS、SDBS和PVP作为分散剂研究MoSi2的分散性。实验结果如图1所示,从图中可以发现,3种分散剂都能对MoSi2起到一定的分散效果,而SDS的分散效果更好一些。其原因可能是因为阴离子表面活性剂SDS、SDBS和PVP吸附在溶液中细小MoSi2颗粒表面形成带负电的颗粒,由于静电作用,而颗粒之间相互排斥,从而使其悬浮液分散均匀。而从图1发现,CTAB增加了MoSi2的团聚,悬浮液与上层清液严重分层,MoSi2纳米颗粒全部都沉降下来。其原因可能是CTAB是阳离子表面活性剂,很容易与弱碱性的水结合导致吸附于MoSi2颗粒表面的浓度较低,因此,MoSi2悬浮液很快沉降下去。所以加入SDS、SDBS和PVP三种阴离子表面活性剂会沉降的比较慢一点,根据以上分析,表面活性剂选SDS较佳。
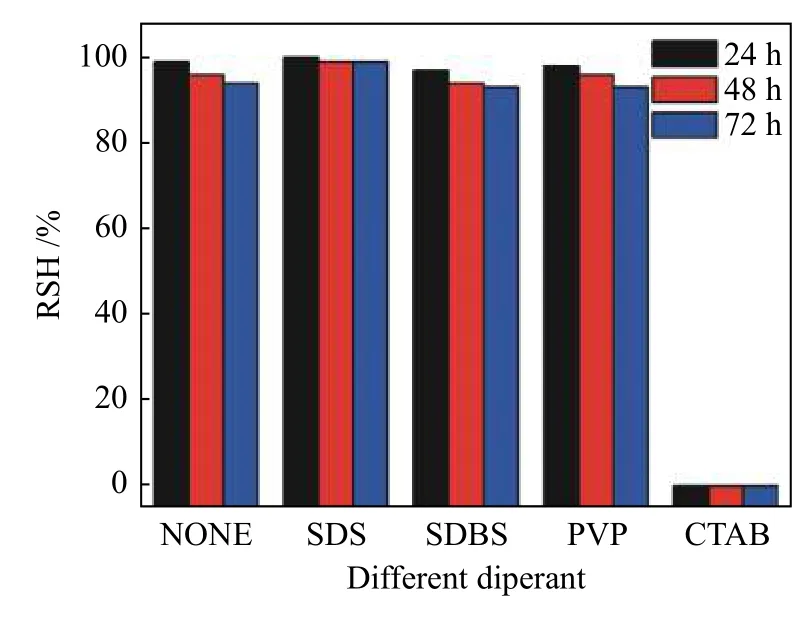
图1 表面活性剂种类对MoSi2均匀分散的影响
2.2 表面活性剂浓度对MoSi2分散的影响
图2为表面活性剂(SDS)浓度对MoSi2悬浮液相对沉降高度(RSH)的影响。固定参数:转速为800 r/min,拌时间为1 h,液比为1∶100。从图2可以看出,SDS的较佳含量为1.6 g/L。随着SDS含量从0.4 g/L增加到3.2 g/L,MoSi2的分散效果先增加后减小。当SDS含量为1.6 g/L时,沉降时间为24、48、72 h的相对沉降高度分别为100%、100%、99%。随着SDS浓度的增加,SDS在MoSi2颗粒表面的吸附容量增大。当SDS在MoSi2颗粒表面的平衡吸附量达到最大值时,分散剂SDS几乎占据了所有吸附点。因此,多余的分散剂SDS会通过溶液中碳氢链的疏水作用将SDS分子结合在MoSi2颗粒表面,导致颗粒团聚[11]。因此,最佳SDS含量为1.6 g/L。
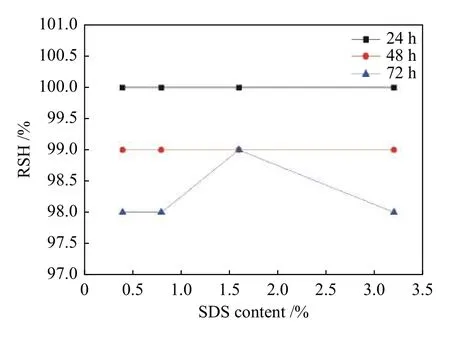
图2 表面活性剂(SDS)浓度对MoSi2均匀分散的影响
2.3 固液比对MoSi2分散的影响
图3为固液比对MoSi2悬浮液相对沉降高度(RSH)的影响。固定参数:转速为800 r/min;搅拌时间为1 h,分散剂浓度为1.6 g/L。结果表明,在较低的固液比(1∶40、1∶60)和较高的固液比(1∶100)下,MoSi2颗粒均未得到有效分散。可能的原因是在分散过程中,超声搅拌依靠超声振动来实现MoSi2颗粒的分散。当固液比较小时,MoSi2颗粒在液体中的浓度较高,不能承受相同的振动,导致分散效果降低。然而,当固液相浓度较高时,由于悬浮液中含有大量的液体,MoSi2颗粒不能得到足够的振动,这也会导致降低粉末的分散效果。很明显,固液比可以确定为1∶80。
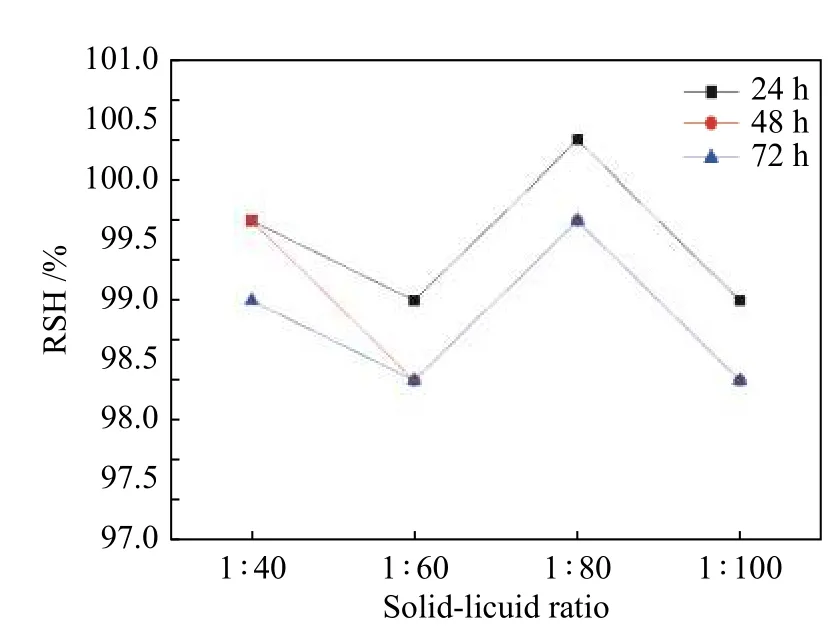
图3 固液比对MoSi2均匀分散的影响
2.4 分散时间对MoSi2分散的影响
图4为分散时间对MoSi2悬浮液相对沉降高度(RSH)的影响。所有结果均在转速为800 r/min,固液比1∶80,SDS含量1.66 g/L下测定。结果表明,从图4可以看出,当分散时间达到6 h时,MoSi2悬浮液的RSH显著增加。进一步增加分散剂时间只会使RSH略有降低。当MoSi2/SDS悬浮液分散6 h时,几乎所有曲线都表现出良好的分散性能。SDS在分散过程中主要起润湿和渗透作用,SDS的渗透速率与膨胀颗粒的大小有关[12-14]。随着分散时间的增加,润湿和渗透作用增强,聚集的MoSi2颗粒不断释放,形成新的表面。分散6 h后,SDS分子完全在MoSi2颗粒上形成,MoSi2颗粒分散良好。
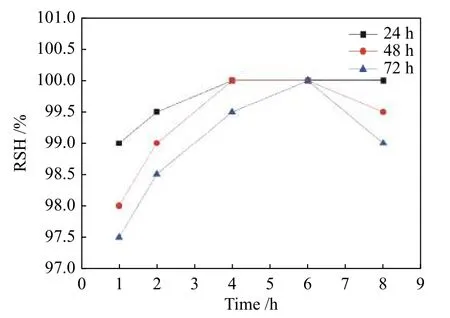
图4 分散时间对MoSi2均匀分散的影响
2.5 pH对MoSi2分散的影响
图5通过Zeta电位测量可以评价悬浮液的分散性和稳定性。表面电势绝对值越大,纳米颗粒间电荷排斥力越大,粒子越倾向于分散,体系越稳定,分子或分散粒子越小;表面电势绝对值越小,纳米粒子越倾向于凝结或凝聚[15]。所有粒子的表面电势绝对值大于30 mV,该分散体系被认为较稳定。在2~11的pH范围内对MoSi2粉末和MoSi2/SDS进行Zeta电位测量。调解pH使用4 mol/L的NaOH溶液和2 mol/L的HCl溶液。如图5所示,MoSi2颗粒Zeta电位的变化是随着pH值的增大,负值绝对值先增大后减小。说明分散稳定性先增加后减小。pH大于7时,加入SDS的悬浮液为碱性溶液时,MoSi2纳米点材料的表面电势分布在−30~−40 mV之间,绝对值均大于30 mV,说明该体系稳定,分散性较好。保持Zeta电位的绝对值达到最大值,这样,纳米颗粒之间可产生最大的电荷斥力。然而,未加分散剂的MoSi2悬浮液,pH大于6.5左右时,绝对值均小于30 mV。说明MoSi2纳米点材料分散性较差。因此,高Zeta电位是MoSi2/SDS具有良好稳定性和分散性的条件。
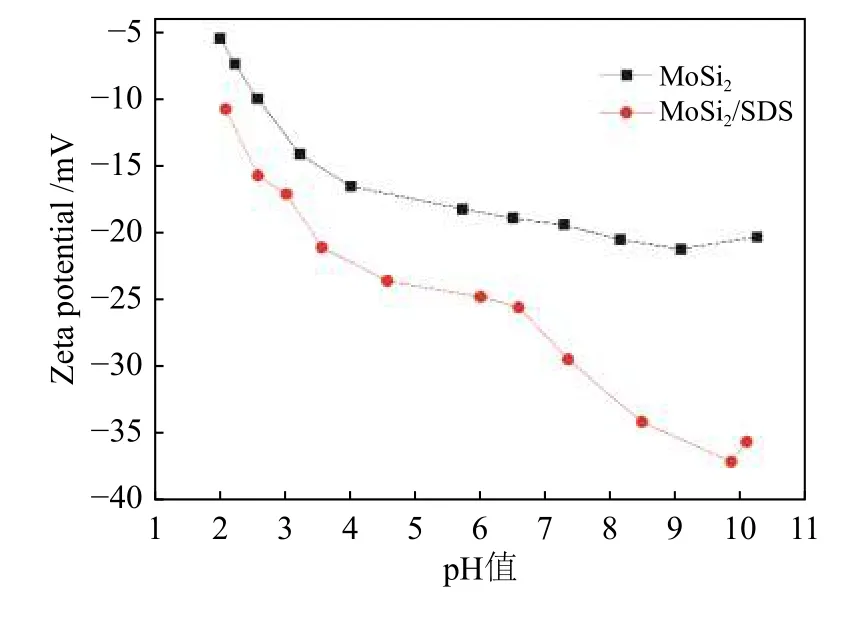
图5 pH对MoSi2和MoSi2/SDS的Zeta电位的影响
2.6 MoSi2分散的微观形貌
图6为分散前后超细MoSi2颗粒的SEM图像。图6a为搅拌6 h后MoSi2分散的SEM图,未加入分散剂的MoSi2颗粒大小不均匀,出现明显团聚。图6b为搅拌时间6 h的MoSi2/SDS分散的SEM图。搅拌6 h后,MoSi2颗粒大小均匀细小,减少了MoSi2颗粒的团聚。MoSi2粉粒径在0.2~0.6 μm之间。从图中可以看出,加入SDS分散剂,采用机械搅拌方法,减少了团聚,使其均匀分散。因此,加入SDS分散剂的MoSi2颗粒具有良好的分散效果。图7为MoSi2和MoSi2/SDS粉体的XRD对比图。从图7可以看出,MoSi2颗粒的衍射峰表明了MoSi2的特征,加入SDS之后,MoSi2/SDS的粉末具有更宽化的衍射峰,表明MoSi2/SDS的粉末晶粒尺寸较小。图8为MoSi2分散机理的示意图。当MoSi2颗粒溶解在水中时,SDS的疏水性烷基链基团将被吸附在MoSi2颗粒的表面上,而亲水基团将浸入水中。然后,疏水性烷基链分子通过排斥力彼此相互作用,以实现MoSi2颗粒在水性介质中的分散。另外,一些SDS分子可能吸附在团聚的MoSi2颗粒的间隙位置上,这会增加MoSi2颗粒之间的静电排斥力。因此,当疏水性烷基链中的静电排斥力与SDS电离产生的静电排斥力共同作用时,适当条件的MoSi2颗粒有偏离聚集的趋势。

图6 搅拌6 h的MoSi2和MoSi2/SDS分散的SEM图

图7 MoSi2和MoSi2/SDS的XRD图谱
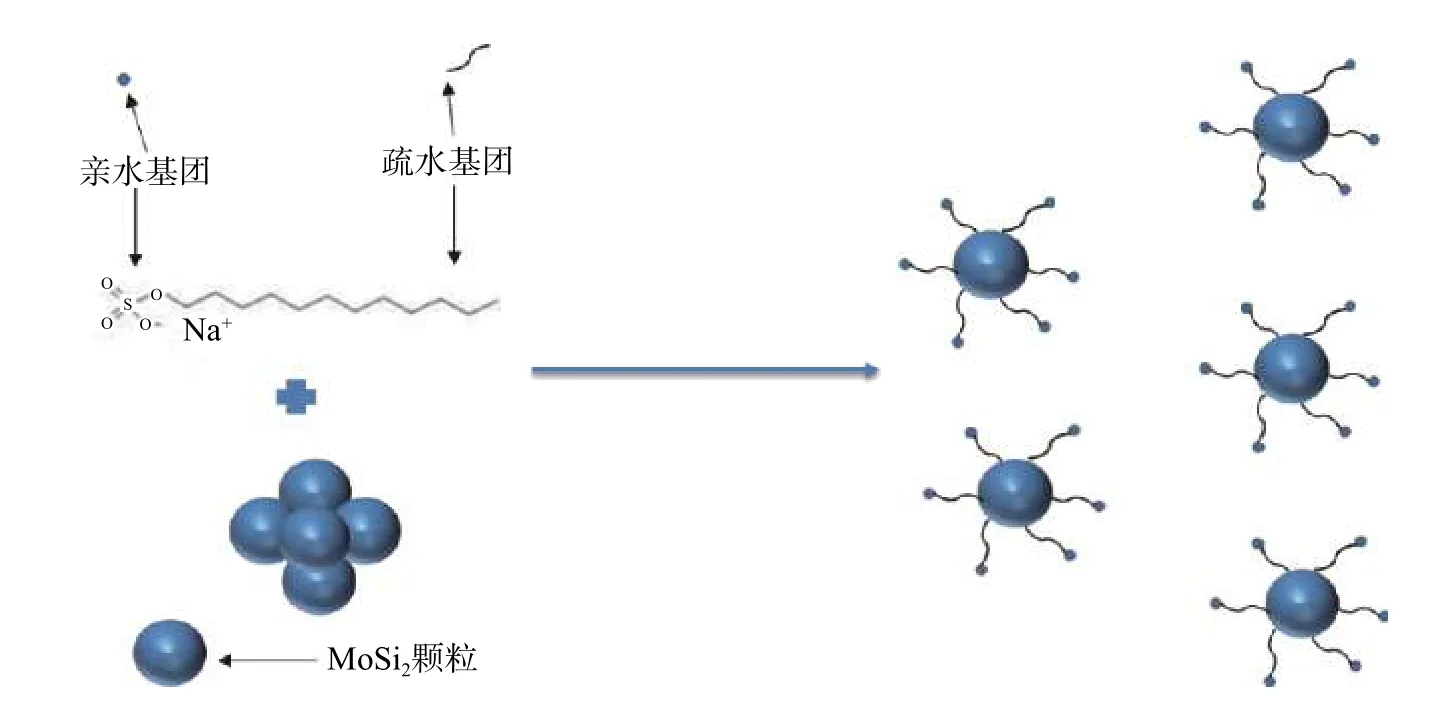
图8 SDS吸附在MoSi2颗粒表面的分散机理示意图
3 结 论
本研究以SDS为分散剂,采用机械搅拌和沉降方法,研究了SDS对MoSi2颗粒分散性的影响,使超细MoSi2颗粒得到良好的分散。分散MoSi2颗粒粒径均匀,粒径在0.2~0.6 μm之间,SDS的分散性能取决于悬浮液的含量、分散时间以及固液比。随着分散时间从1 h增加,但当分散时间进一步增加到2、4、6、8 h时,MoSi2分散更加均匀。随着SDS浓度从0.4 g/L增加到3.2 g/L,分散效果先改善后降低。固液比为1:80时,分散效果最好。结果表明:分散后,SDS分子在MoSi2颗粒内部和部分表面被吸附,降低了MoSi2颗粒的表面能,改善了MoSi2颗粒的分散性。此外,静电斥力和静电阻碍共同作用,实现了MoSi2颗粒的分散和稳定。在本研究中,分散MoSi2粉的较佳分散时间6 h,固液比1:80,SDS浓度1.6 g/L。
