ChCl-Urea低共熔溶剂中电沉积锌的工艺研究
2021-11-17孙海静杨帅王贺徐飞杜俊荣王媛媛毕铭雪从铭玥孙杰
孙海静,杨帅,王贺,徐飞,杜俊荣,王媛媛,毕铭雪,从铭玥,孙杰
(沈阳理工大学环境与化学工程学院,辽宁沈阳110159)
锌作为金属防护和电池制造等领域的重要有色金属材料,被广泛应用于能源、车辆和船舶等行业[1-4]。目前,锌的电沉积主要是在氰化物镀液、锌酸盐镀液等水溶液体系中进行。然而,这些电解液普遍存在毒性较高、腐蚀性较强和析氢严重等弊端[5],因此,寻找新型电沉积锌的电解液是十分必要的。
低共熔溶剂(Deep Eutectic Solvents,DESs)是以一定化学计量比的氢键受体(如季铵盐)和氢键给体(如酰胺、多元醇)组合而成的低共熔混合物[6],其作为一种新型的价格低廉、合成简单的绿色溶剂,具有电化学窗口宽、液态温度范围大、无析氢反应、无毒性和溶解性能好等优良性质[7-9],是作为电沉积锌的优良电解液。
在低共熔溶剂中电沉积锌方面,已有较多报道。如Abbott等[10]在摩尔比为1∶2的ChCl-Urea DES(含0.5 mol/L ZnCl2)中成功沉积了金属锌,并以Al2O3为例证明了ChCl-Urea DES中可沉积复合材料。王巍[11]等采用ChCl-Urea DES(摩尔比为1∶2)于镁合金表面成功获得了锌镀层,并分析了电流密度对锌镀层的厚度和耐蚀性的影响。Pereira[12]和Song[13]等分别研究了在摩尔比为1∶2的氯化胆碱-乙二醇低共熔溶剂中锌的电沉积机理和添加剂对锌镀层耐蚀性的影响。
目前,低共熔溶剂中锌的电沉积研究主要集中在电沉积机理、添加剂的添加等方面,但对于低共熔溶剂中锌电沉积工艺的优化研究却相对较少。因此,本文以摩尔比为1∶2的ChCl-Urea DES作为电解液进行锌的电沉积工艺的研究,系统研究了沉积温度、沉积电位和锌盐配比对锌镀层耐蚀性能的影响,采用正交实验得到了耐蚀性较高的电沉积锌工艺。最后,采用动电位极化曲线对比研究了ChCl-Urea DES和传统水溶液中锌镀层的耐蚀性能,并利用扫描电子显微镜(SEM)和X-射线衍射技术(XRD)对ChCl-Urea DES中锌镀层的微观形貌和物相组成进行了表征。
1 实验
1.1 主要试剂及溶液制备
氯化胆碱(ChCl)、尿素(Urea)、氧化锌(ZnO)、氯化锌(ZnCl2)、氯化钠(NaCl)。药品均为分析纯。将ChCl和Urea放入电热干燥箱,在80℃下干燥24小时。然后,按照摩尔比为1∶2准确称取ChCl和Urea,置入烧杯中并混合均匀,用数显磁力搅拌器加热至80℃并搅拌至澄清黏稠,再加入锌盐继续搅拌至锌盐完全溶解。
1.2 电沉积
锌镀层采用CS350型电化学工作站进行制备。实验采用三电极体系:以纯铜片为工作电极,以216型银电极为参比电极,213型铂电极为辅助电极。电沉积前对铜片进行前处理。首先依次使用400#、600#、1200#和2000#金相砂纸将试样打磨抛光;然后在60℃的碳酸钠(50 g/L)、氢氧化钠(50 g/L)和磷酸钠(10 g/L)的混合溶液中浸泡20 min,以除去表面油污;使用去离子水清洗后,再放入稀盐酸和稀硫酸的混合液中活化10 s;最后,超声波清洗10 min后得到待用的试样。电沉积完毕后,将得到的沉积片用丙酮清洗后,再用去离子水彻底清洗,室温干燥后备用。电沉积时间均为30 min。
1.3 镀层质量标准评价
锌镀层的宏观表面质量用肉眼进行观察和评价,其质量评价标准如表1所示。

表1 锌镀层质量评价标准Tab.1 Quality evaluation standard of zinc coatings
1.4 耐蚀性测试
采用CS350型电化学工作站进行极化曲线测试。测试采用三电极体系:工作电极为镀锌试片,参比电极和辅助电极分别为217型饱和甘汞电极和213型铂电极。待开路电位稳定后,进行动电位极化曲线的测试。起始电位为相对开路电位-300 mV到300 mV,扫描速度为0.5 mV/s,并采用自动补偿方法来补偿体系电阻的欧姆降。测试介质为3.5%NaCl溶液,试片测试面积为1 cm2,所有实验均在室温下(25±1℃)进行。
1.5 表征分析
采用VEGA3XUM型扫描电子显微镜(SEM,捷克TESCAN公司)研究了锌镀层的表面形貌;采用D/max-2200PC型X-射线衍射仪(XRD,Cu Kα靶,γ=0.15406 nm,日本日立公司)分析了锌镀层的物相组成。其中,XRD测试电压为40 kV,测试电流为100 mA,扫描范围为10°~90°,扫描速度8°/min。
2 结果与讨论
2.1 单因素实验
2.1.1 沉积温度的影响
在配方1(含0.50 mol/L ZnCl2)、沉积电压1.5 V和沉积时间30 min的条件下,不同沉积温度(40℃、50℃、60℃、70℃和80℃)对锌镀层单位面积增重及耐蚀性(以腐蚀电流密度icorr表征)的影响如表1所示。

表1 温度对锌镀层单位面积增重和耐蚀性的影响Tab.1 Effect of temperature on the weight gain per unit area and corrosion resistance of zinc coatings
从表1中可以看出,随着沉积温度的增加,锌镀层的宏观形貌由均匀致密、乳白色变为表面较粗糙、暗灰色,且其单位面积增重呈现出先增加后降低的趋势,镀层增厚明显,并于60℃时达到极大值,镀层最厚。从腐蚀电流密度来看,随着沉积温度的增加,腐蚀电流密度呈现先减少后增加的趋势,60℃时锌镀层的腐蚀电流最小。因此以腐蚀电流表征,同时以镀层表面质量和单位面积增重辅助考量可知,沉积温度选取50℃~80℃为宜。
2.1.2 沉积电位的影响
在配方1(含0.50 mol/LZnCl2)、沉积温度60℃和沉积时间30 min的条件下,不同沉积电压(0.5 V、1.0 V、1.5 V、2.0 V和2.5 V)对锌镀层单位面积增重及耐蚀性的影响如表2所示。
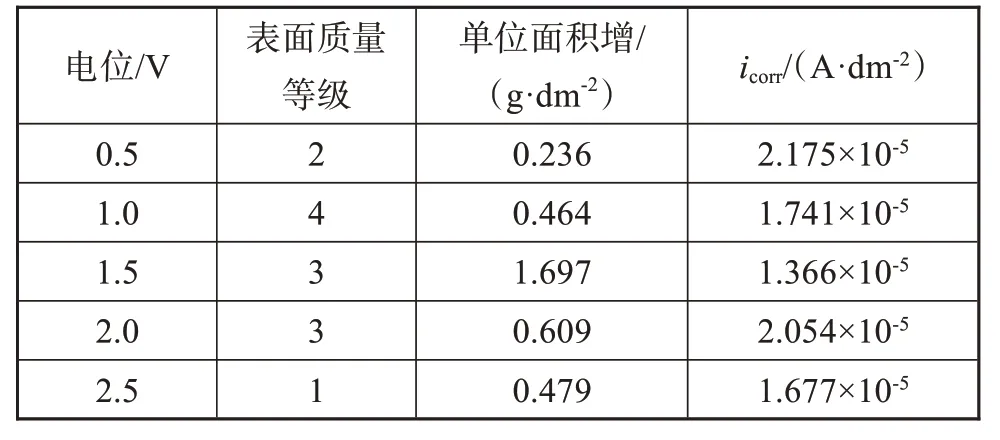
表2 沉积电位对锌镀层单位面积增重和耐蚀性的影响Tab.2 Effect of deposition potential on the weight gain per unit area and corrosion resistance of zinc coatings
从表2中可以看出,随着沉积电位的增加,锌镀层的宏观形貌由均匀致密、乳白色变为表面较粗糙、暗灰色,且单位面积增重呈现出先增加后降低的趋势,镀层增厚较为明显,而腐蚀电流呈现出先降低后增加的趋势。因此以腐蚀电流表征,同时以镀层表面质量和单位面积增重辅助考量可知,沉积电位选择1.0 V~2.5 V为宜。
2.1.3 锌盐配比的影响
在沉积电压1.5 V、沉积温度60℃和沉积时间30 min的条件下,不同锌盐配比(配方1、2、3和4)对锌镀层单位面积增重及耐蚀性的影响如表3所示。其中,配方1、2、3和4分别代表不同摩尔比的ZnCl2与ZnO,具体为:配方1含0.50 mol/L ZnCl2、配方2中ZnCl2和ZnO的摩尔比为2∶1(锌盐总浓度为0.50 mol/L)、配方3中ZnCl2和ZnO的摩尔比为1∶2(锌盐总浓度为0.50 mol/L)和配方4中仅含0.50 mol/L ZnO。

表3 锌盐配比对锌镀层单位面积增重和耐蚀性的影响Tab.3 Effect of zinc salt ratio on the weight gain per unit area and corrosion resistance of zinc coatings
由表3可以看出,随着溶剂中ZnO含量的不断增加(从配方1到配方4),锌镀层的宏观形貌均呈现出均匀致密的特点,且单位面积增重整体呈现减小的趋势,镀层逐渐变薄。从腐蚀电流来看,配方1得到的锌镀层腐蚀电流密度最小,而配方2、3和4的腐蚀电流相近。
2.2 正交实验
根据上述单因素实验结果,遂选择进行三因素四水平L16(43)正交实验。正交实验因素水平设计如表4所示,其中,A(℃)代表沉积温度,B代表锌盐配比,C(V)代表沉积电压。表5为正交实验结果。表中,Kij表示的是任一列水平号为i时,对应j列的实验结果之和。在此正交实验中,为锌镀层腐蚀电流密度之和或镀层表面质量等级分数之和;R表示的是极差,为任一列上最大的Kij与最小的Kij之差。极差R的大小反映了各因素对指标的影响程度,R值越大则表示该因素对指标的影响越大。由表5中计算结果可知:对于两个评价指标而言,均有RC>RB>RA,这说明沉积电压对锌镀层耐蚀性能和镀层表面质量的影响最为显著,锌盐配比次之,沉积温度的影响最小。在正交实验中,对于耐蚀性能而言,Ki最小值所对应的水平即为优方案中该影响因素对应的最优水平,由表5可知:A因素列:K3<K1<K4<K2;B因数列:K2<K4<K1<K3;C因数列:K1<K2<K4<K3。因此,A3B2C1为最优方案。而对于镀层表面质量而言,Ki最大值为最优水平,即A3B2C1或A1B2C1。综合考虑镀层耐蚀性和镀层表面质量可得,最优方案为A3B2C1,即沉积温度70℃、配方2(2ZnCl2∶1ZnO(摩尔比))和沉积电压1.0 V。

表4 正交实验因素水平表Tab.4 Orthogonal experimental design

表5 正交实验结果Tab.5 The result of orthogonal experiment
3 耐蚀性能
对锌镀层在3.5%NaCl溶液中进行动电位极化曲线测试,并与传统水溶液中的锌镀层作对比,结果如图1所示,其中,ChCl-Urea DES中的锌镀层是在正交实验的最优方案下得到的,而传统水溶液中的锌镀层是在氧化锌10 g/L、氢氧化钠130 g/L、电流密度3 A/dm2、温度40℃的条件下得到的。沉积时间均为30 min。结果显示,ChCl-Urea DES和水溶液中的锌镀层阳极均呈现出活性溶解的特征,且阴、阳极塔菲尔斜率十分相近,两者的动电位极化曲线几乎重合。进一步比较可以发现,在相同极化电位下,水溶液中锌镀层的电流密度略低于ChCl-Urea DES中的锌镀层,这表明两种体系中锌镀层的耐蚀性能是相近的。对极化曲线进行塔菲尔拟合得到的腐蚀电位Ecorr和腐蚀电流密度icorr,结果列于表6。由表中数据可以发现,两个体系中锌镀层的自腐蚀电位十分接近,水溶液中锌镀层的自腐蚀电流密度略低于ChCl-Urea DES中锌镀层的自腐蚀电流密度,但十分接近,这表明ChCl-Urea DES中可获得与传统水溶液中耐蚀性相当的锌镀层。

图1 低共熔溶剂和水溶液中锌镀层在3.5%NaCl溶液中的动电位极化曲线Fig.1 Potentiodynamic polarization curves of zinc coatings in deep eutectic solvents and aqueous solutions in 3.5%NaCl solution
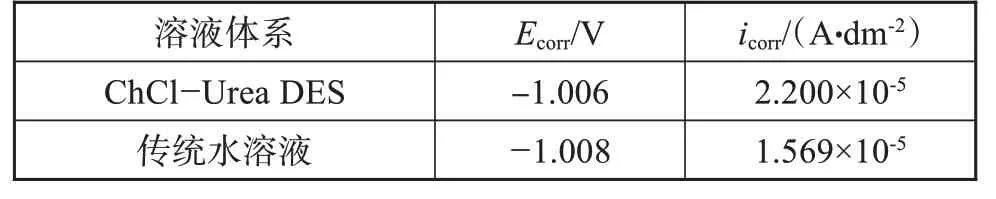
表6 ChCl-Urea DES和水溶液中锌镀层极化曲线的拟合结果Tab.6 Parameters extracted from potentiodynamic polarization curves of of zinc coatings in ChCl-Urea deep eutectic solvents and aqueous solutions
4 形貌及物相组成
图2为ChCl-Urea DES和传统水溶液中锌镀层的宏观相貌。由图2可发现,两个体系中的锌镀层均呈现出均匀、致密的特点,但镀层的颜色有所差别,ChCl-Urea DES中锌镀层呈现乳白色,而传统水溶液中锌镀层呈灰黑色。为进一步研究两个体系中锌镀层的微观形貌和物相组成,对得到的锌镀层进行了SEM和XRD测试,结果分别如图3、4所示。由图3可以观察到,两种体系中锌镀层的微观形貌相差较大,水溶液中的锌镀层主要是由羽毛状的微粒构成,而ChCl-Urea DES中锌镀层是由排列紧密的多边形立体结构的灰白色颗粒物质构成的,这种规则的多边形颗粒更易形成宏观和微观上的平坦、致密的镀层。从图4中可以发现,相较于图4(a)(ChCl-Urea DES锌镀层),水溶液中锌镀层的XRD图谱上还出现了金属铜的能谱,这是由于锌沉积层过薄,在测试时被击穿所致。这也能从侧面表明,同一沉积时间下(电沉积30 min),ChCl-Urea DES可获得比传统水溶液中更厚的锌镀层。此外,实验中还记录了同一沉积时间下两个体系中电沉积锌的单位面积增重,由此发现,ChCl-Urea DES中锌的单位面积增重(0.822 g/dm2)比水溶液(0.682 g/dm2)稍多,这也证明了ChCl-Urea DES体系中可获得更厚、沉积速度更快的锌镀层。

图2 锌镀层的宏观形貌Fig.2 Morphology of zinc coatings in ChCl-Urea deep eutectic solvents and aqueous solutions

图3 锌镀层的微观形貌Fig.3 Micro-morphology of zinc coatings in ChCl-Urea deep eutectic solvents and aqueous solutions
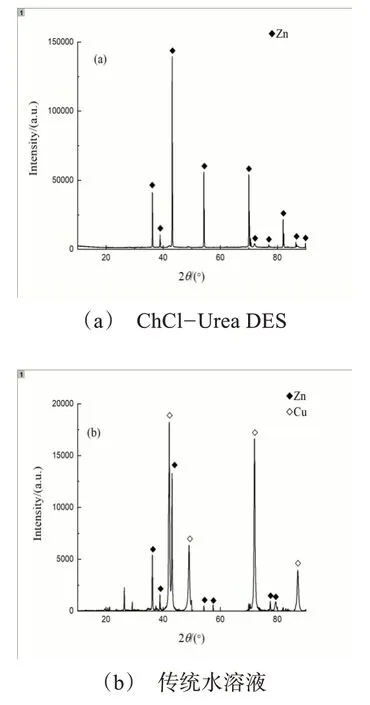
图4 锌镀层的XRD图谱Fig.4 XRD spectrum of zinc coatings in ChCl-Urea deep eutectic solvents and aqueous solutions
5 结论
(1)在ChCl-Urea低共熔体系中,以腐蚀电流密度为表征,同时以镀层单位面积增重辅助考量可知,在1.0 V、70℃的条件下,选用配方2可获得耐蚀性最佳的锌镀层。
(2)在ChCl-Urea低共熔体系中可得到均匀平整、颗粒致密的锌镀层,且其耐蚀性与传统水溶液相当。
(3)SEM表明,锌镀层是由排列紧密的六方形立体结构的灰白色颗粒物质构成。XRD表明,锌镀层主要由六方结构的多晶锌组成。
