3.0T闭合式大孔径MR引导下肝癌微波消融15例
2021-11-15焦德超王朝艳李兆南张全会韩新巍
焦德超,王朝艳,李兆南,田 川,张全会,韩新巍
消融治疗已成为≤3 cm肝癌的首选根治性微创手段,远期疗效与外科治疗相当[1]。目前临床上主要消融导向手段为超声(US)或CT。但两种影像均有劣势,US对肝硬化背景下小病灶显示欠佳,尤其是靠近膈肌、肠管和肝门病变;CT导向存在电离辐射损伤且对消融范围判断欠佳[2]。而磁共振(MR)具有无电离辐射损伤、软组织分辨率高、快速多平面成像等优点[3]。本团队2019年10月开展3.0T闭合式大孔径(孔径70 cm)MR引导下肝癌MWA术,疗效确切,现报道如下。
1 材料与方法
1.1 材料
1.1.1 临床资料:2019年10月至2020年2月,15例原发性肝癌患者(13例初诊,2例切除后复发)共24个病灶采用3.0T闭合式大孔径MR引导下微波消融术。其中S4段7个,S6和S8段各5个,S3段4个,S7段2个,S5段1个。入选标准:①符合中国临床肿瘤学会《原发性肝癌诊疗指南-2018》标准[4];②拒绝或存在切除手术禁忌证者;③肿瘤最大径≤5 cm且病灶数≤3个;④无门脉侵犯;⑤Child-Pugh分级A或B;⑥患者ECOG评分≤2分。排除标准:①肝良性病变;②不可控腹水;③严重凝血功能障碍,PLT≤30×109/L或PT≥25 s;④合并门静脉癌栓;⑤肿瘤最大径>5 cm或病灶数>3个;⑥幽闭恐惧症或存在磁共振扫描相关禁忌证者。
1.1.2 仪器:MR扫描仪为Magenetom Verio 3.0T大孔径(70cm)磁共振(Siemens,德国),T1扫描序列为T1_Vibe_fs,参数为:TR 3.92 ms,TE 1.43 ms,FA 9,层厚3.3 mm,FOV 380×280 mm。T2扫描序列为T2_haste_fs,参数为:TR 1 000 ms,TE 106 ms,FA 180,层厚4.5 mm,FOV 380×280 mm,两者采用屏气扫描,时间16 s。监护系统为美国Invivo MR兼容心电监护仪。微波发生器为EC0-100E磁共振兼容微波治疗仪(国械注标:20173251268,南京亿高微波系统工程有限公司),电压220 V,频率50 Hz,输出功率0~100 W可调节,微波刀规格1.8 mm×150 mm(型号ECO-100AI13),微波能量传输线长度为3.5 m。
1.2 方法
1.2.1 术前准备:所有患者术前3 d内完成血常规、电解质、肝肾功能、凝血功能、心肺功能检查和传染病4项,术前1周之内的增强CT或MR,完成临床/病理学诊断,签署知情同意书,若病灶直径≥3 cm,术前2~4周内行肝动脉化疗栓塞(TACE),以降低消融热沉效应,提高消融效率[5]。
1.2.2 消融过程:术前4~6 h禁食水,建静脉通路,常规心电监护。根据病灶所在肝叶和穿刺计划路径制定手术体位,体表放置定位鱼肝油矩阵定位。右美托咪定0.5μg/kg和地佐辛10 mg联合静脉麻醉,若患者(尤其是膈顶部小病灶)无法配合呼吸,可行插管全麻。先行T1WI和T2WI扫描定位肝内病灶,穿刺点消毒铺巾,2%利多卡因局麻,根据MR显示病灶位置,刺入16 GMWA针,采用分步进针法[6],并多次扫描确定针尖位置。刺中病灶后,根据病灶大小选择消融参数,术中水冷循系统降低针杆温度,若病灶≤2.5 cm,建议一次完成消融;若病灶>2.5 cm,建议采用重叠消融法,消融满意均为T1WI上高信号环覆盖中央低信号肿瘤至少5 mm以上(称之靶征),完成消融后5~8 min行T1WI扫描评价消融效果,满意后停止微波治疗,针道消融后拔针。停静脉麻醉,返回病房,并给予保肝、抑酸对症治疗。
1.2.3 疗效评价:对比术前及术后2个月生化指标(白细胞、红细胞、血小板、丙氨酸转氨酶、天冬氨酸转氨酶、胆红素、肌酐和尿素氮)和甲胎蛋白(AFP);术后2个月行3.0 T肝脏MR平扫+动态增强或64排肝脏平扫+增强CT,采用mRECIST评价肿瘤局部情况[7]。局部控制率(LCR)=完全缓解(CR)+部分缓解(PR)。
1.3 统计学分析
2 结果
2.1 治疗经过
15例患者中6例接受了消融前辅助性TACE治疗(阿霉素10 mg+碘化油10 mL),13例静脉麻醉完成,2例因拼气配合度差接受气管插管全麻。24个病灶均顺利完成穿刺和消融治疗,技术成功率100%。单病灶平均消融功率、平均消融时间见表1,平均消融次数为(1.7±0.7)次(范围1~3次)。术前及术后2月生化指标见表2。

表1 患者一般资料
表2 15例患者相关生化指标术前及术后比较 ±s

表2 15例患者相关生化指标术前及术后比较 ±s
?
2.2 MRI表现及病灶评价
微波刀在T1和T2上均表现为低信号,微波刀辐射头端(长度1.6 cm)显影较针杆纤细。消融后T1WI上病灶呈低信号,消融灶表现为明显高信号,两者对比鲜明呈同心圆状(称之“靶征”)。T2WI消融区呈低信号,周围见高信号水肿带。23个病灶一次性完成准确消融,2个月后增强CT或MR显示病灶完全去血管化,1处病灶(S7段,3.6 cm)靠近门脉区局部病变强化,评价PR,局控率100%。随访4.2个月(2.0~6.3个月),所有患者均存活。有2例患者出现肝外转移,图1、2。
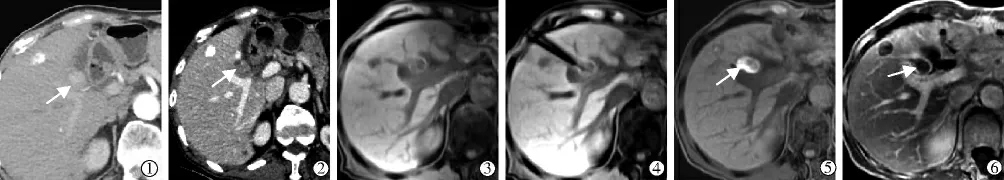
图1 患者男性,55岁,乙肝合并S4段原发性肝癌,AFP:1 009μg/mL
2.3 并发症
3例患者发生次要并发症。术后即刻1例出现包膜下出血(5~10 mL),嘱咐患者严格卧床休息,未予特殊处理;术后2例患者深吸气后肝区疼痛较重,彩超发现右侧反应性胸腔积液<100 mL,嘱患者深呼吸,3~5 d后症状明显缓解。未见大出血、肝脓肿、胆汁湖、膈肌穿孔、黄疸等主要并发症。
3 讨论
消融治疗的技术要求是精细定位、精准穿刺、精确评价[8]。目前最常用的导向设备是US和CT,US引导方便快捷、实时导航、无电离辐射、多层面成像,但易受气体、骨骼影响,且消融后局部气泡会干扰判断坏死范围;CT引导简单方便、适应证广、成像速度快、软组织分辨率高,但存在电离辐射、无法实时导航、消融范围判断欠佳。尽管术中增强CT或超声造影可以实现准确消融范围评估,但增加操作步骤和费用[9]。MR在肝脏肿瘤,尤其是小肝癌的定位、穿刺和消融评价中都可以发挥很大的技术优势:①对于小肝癌(≤2 cm)而言,仅有60.5%的病灶出现典型的“快进快出”[10],而MR有极高的软组织分辨率,有T1WI、T2WI、DWI等多个序列,还可以使用特异性肝癌对比剂普美显,提高诊断的灵敏度和特异度,进而准确定位肝癌;②MR无气体和骨胳伪影、电离辐射,可以实现任意角度成像,能够为非共面间接穿刺,尤其是膈下病灶穿刺提供更好的技术支持;③MR T1平扫上(无需增强)可精准判断坏死范围,这对消融的即刻评价拥有较高的临床 指 导 价 值[11]。
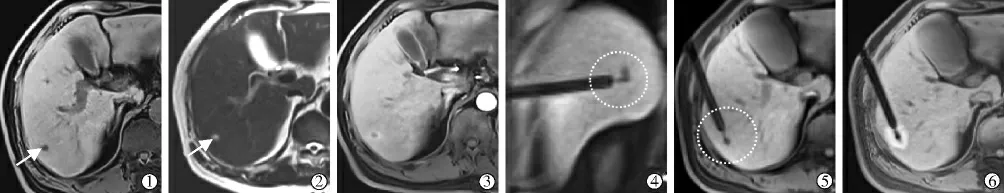
图2 患者男性,62岁,AFP:83.4μg/L临床诊断小肝癌
但由于高场强磁兼容相关设备和器械的发展滞后,加之国内医疗资源缺乏等现实问题,MR导向下介入发展相对缓慢。2002年,Morikawa等[12]首次报道30例患者采用0.5T开放式MR引导下肝转移瘤MWA,技术成功率100%,未见并发症,但当时微波发生仪磁兼容性研发不成熟,设备需要放置到MR手术间外,传输天线热损大,操作复杂,消融范围小且呈长椭球形不符合肿瘤生物学行为,成像质量差,之后多家研究中心报道0.5~1.0T开放式MR引导下消融,尽管操作稍繁,但MR在T1WI上明确的“靶征”对消融坏死范围的判断较常规US和CT具有明显的优势[13-17]。伴随磁兼容器械和MR大孔径设备发展,1.5T以上高场强闭合式MR引导下消融治疗成为可能。2010年,林征宇等[18]报道了1.5T闭合式(孔径65 cm)MR引导下肝肿瘤RFA治疗44个肝脏恶性肿瘤,局部完全消融率达100%,但射频发生器会对磁场信号造成干扰,且由于MR操作孔径65 cm,过度肥胖的患者操作受限。2016年,Hoffmann等[19]报道了1.5T高场强MR引导下18个肝恶性肿瘤的消融治疗,结果显示1.54 cm的肿瘤可以一次消融达到根治,进一步证实高场强MR下消融的可行性和安全性。理论上,3.0T MR拥有更快的成像速度,本研究的T1 Vibe快速序列扫描时间16 s,图像清晰,为手术提供更好更快的导向;其次,场强越高,软组织分辨率越高,磁敏感性更强,病灶和正常组织显示更清楚。本研究采用的MR为大孔径70 cm,为肥胖患者提供了更大的穿刺操作空间,当然高场强也为磁兼容微波刀提出更高的要求。
本研究显示,直径为2.6 cm的肝癌一次性MWA率达95.9%,无主要并发症,技术成功率100%,初步验证了该方案的安全性和可行性。MR导向消融的核心优势在于精确的消融范围评估,T1WI消融灶呈明显的高信号,与中央低信号肿瘤形成鲜明的靶征。靶征的本质是瘤周正常肝组织消融后肝窦扩张充血,红细胞因热损伤破裂,血红蛋白逸出,T1表现为高信号环,临床实践中发现,刚消融后即刻进行T1平扫,高信号环并不明显,5~8 min后会形成一个明确和稳定消融高信号环,并与中央的低信号肿瘤形成明显对比,可能与消融周围肝窦充血水肿带更加明显和稳定有关。动物实验和其他临床研究均证实依靠靶征判断消融范围安全可靠[20-22]。为进一步增大消融范围和缩短消融时间,对于≥3 cm肝癌仍然推荐术前进行辅助性TACE治疗,这样可以降低肿瘤内血流,提高消融效率[23],获得更大的消融范围。
尽管MR导向消融治疗仍面临很多困难,诸如扫描时间长,磁兼容器械稍贵,不适合闭气配合较差者,MR介入手术室建设周期长、要求高,对患者有较高要求,比如禁忌体内铁植入物和恐惧症者进入手术室等。对大部分三级医院而言,院内长期的影像医疗资源掌控和分配问题等具体困难仍需进一步克服。本研究证明3.0T闭合式大孔径MR引导下肝癌微波消融术安全可行有效。
