石墨烯量子点/PtAu复合电极应用于四环素的电化学检测
2021-11-15李爱莉朱建豪陈帅妤梅言玉
李爱莉, 朱建豪, 陈帅妤, 梅言玉, 许 贺
(东华大学环境科学与工程学院,上海 201620)
四环素(Tetracycline,TTC)抗生素具有广谱抗菌作用,被广泛应用于治疗和预防动物疾病。TTC在自然界中难以降解,多级富集后对生物体和环境产生极大的危害作用[1]。传统的检测技术,如高效液相色谱法(HPLC)[2]、质谱法(MS)、HPLC-MS、酶联免疫法[5]等方法,难以推广于TTC的现场快速检测。电化学法由于具有仪器设备相对简单,分析速度快,携带方便以及高灵敏的检测信号等优点,易推广到突发污染事件的现场、快速检测[6,7]。近年来电化学检测方面的研究取得一定的进展,主要采用适配体[8,9]和免疫传感器[10,11]检测。这些方法虽具有较高灵敏度,但操作繁琐和实验条件严苛,限制了它们的应用范围。因此,有必要发展简单、快速、灵敏、价廉的电化学分析方法。TTC在化学结构上均属于多环并四苯羧基酰胺母核的衍生物,催化电势较高,电化学反应较难进行。据报道,TTC的催化位点通常是10号位的羟基氧化,过高的氧化电位限制了直接电化学在TTC检测中的应用。因此,探索TTC的高灵敏、高准确性电极敏感材料,实现TTC定量检测具有重要的研究意义。
石墨烯量子点(GQDs)是近年来发展起来的一种新型零维石墨烯材料,具有比表面积大、导电性高、化学稳定性好等优势,在电化学方面具有良好的发展应用前景[16,17]。采用GQDs修饰电极作为基底材料,可以更好地提高电极的导电性和电活性面积。Au和Pt纳米粒子有独特的催化性能和导电特性,将其沉积在大比表面积的GQDs修饰电极界面,不仅进一步提高电极的催化性能,而且可很好地降低Au和Pt纳米粒子的用量。目前,采用电化学法直接检测TTC的研究较少,而以GQDs、Au和Pt复合电极应用于TTC的检测尚未见报道。
本文以石墨烯量子点修饰玻碳电极(GQDs/GCE)作为基底电极,采用电化学共聚方法制备Au和Pt复合材料,得到GQDs/PtAu/GCE复合电极,并将其应用于TTC的电化学检测,探讨GQDs/PtAu/GCE催化氧化TTC的电子转移途径和反应机理。结果表明,GQDs/PtAu/GCE复合电极对TTC表现出了良好的电催化性能,显著降低了TTC氧化电位。电氧化过程出现两个氧化峰,其中高电位氧化峰较稳定,用于TTC的氧化检测,具有良好的检测结果。该方法具有一定的稳定性和准确性,有望用于实际环境样品中四环素类抗生素的定量检测。
1 实验部分
1.1 仪器与试剂
所有电化学实验均在CHI760E电化学工作站上(上海辰华仪器有限公司)进行。采用三电极体系:工作电极为修饰的玻碳电极(GCE,直径3 mm),参比电极和辅助电极分别为饱和甘汞电极和铂丝。采用场发射扫描电子显微镜-能谱仪(S-4800型,日本)对复合电极的形貌和组成进行表征;通过场发射透射电镜(JEM-2100 F,日本)对GQDs的形貌和尺寸进行表征。
K3[Fe(CN)6]、K4[Fe(CN)6]、Na2HPO4、KH2PO4、H2PtCl4、HAuCl4、KCl、氯霉素、土霉素、无水乙醇均购于国药集团(上海)化学试剂有限公司;5%Nafion溶液(美国Sigma-Adlrich);盐酸四环素、氯四环素、硫酸卡那霉素、布洛芬和氟比洛芬均购于北京百灵威科技有限公司。所有的化学品均是优级纯,实验用水为去离子水。实验前溶液需通氮除氧。
1.2 GQDs/PtAu/GCE的制备
GQDs依据文献方法[18,19]制备。电化学实验前需对GCE进行预处理,在麂皮上将0.05 μm的Al2O3粉末与水混合形成糊状悬浊液,打磨抛光GCE成镜面。并将GCE依次在HNO3(1∶1)、乙醇和水中各超声5 min,晾干后待用。称取4 mg GQDs置于2 mL 0.5%Nafion乙醇溶液中,超声分散30 min,以形成均匀的黑色悬浊液。滴涂10 μL 2 mg/mL GQDs 的悬浊液于GCE表面,制得GQDs/GCE。
以GQDs/GCE为工作电极,在含1.8 mmol/L HAuCl4和2.0 mmol/L H2Pt2Cl4的0.5 mol/L H2SO4中,采用循环伏安法电沉积制备修饰电极。在电位区间-0.6~+1.05 V连续扫描40圈,扫速为100 mV/s,将Pt和Au粒子同时电镀至GQDs/GCE上,得到GQDs/PtAu/GCE复合电极。Pt/GQDs/GCE和Au/GQDs/GCE复合电极的制备方法与上述过程一致,只是电解质溶液中含2.0 mmol/L H2PtCl4或含1.8 mmol/L HAuCl4的0.5 mol/L H2SO4。Au和Pt粒子的电沉积均在室温条件下进行。
1.3 TTC的电化学检测方法
将TTC标准品溶于无水乙醇中配成2 g/L母液保存待用,使用前进行适量稀释。电化学检测TTC实验均采用0.1 mol/L KH2PO4-Na2HPO4缓冲溶液(PBS,pH=3.0)作为支持电解质。高浓度TTC采用循环伏安法进行检测,将0.1 mol/L PBS(pH=3.0)电解质置于电解池中,加入适量TTC标准溶液。循环伏安扫描电位范围为-0.2~+1.6 V,扫速为50 mV/s,吸附时间为10~20 s。每次检测结束后,采用线性伏安扫描,在+1.6~-0.2 V由正向负电位扫描数次,以减少氧化产物对电极表面的影响。低浓度TTC采用安培法(i-t)进行检测,施加电位为0.9 V,测定间隔20 s,检测溶液处于搅拌状态,搅拌速度保持恒定。电极每次安培检测TTC后,再利用i-t曲线,施加+1.0 V左右电位,在搅拌状态下清洗电极数秒,至电极表面反应完全,以处理吸附在复合电极上的TTC,实现电极的再生。
2 结果与讨论
2.1 GQDs的透射电镜(TEM)表征
图1是GQDs在不同放大倍数下的TEM表征图。从图中可以看出,GQDs尺寸微小,分散均匀,无团聚现象,粒径大约在10 nm以下。荧光实验已证明10 nm以下的GQDs呈现CQDs的性质[16,18]。

图1 GQDs的透射电镜(TEM)图Fig.1 TEM images of GQDs
2.2 复合电极的扫描电镜(SEM)表征
图2显示了不同复合电极的SEM和能谱(EDS)表征图。从图中可看出,GQDs在SEM图中并不明显,一方面由于SEM分辨率有限。另一方面,GQDs分散于Nafion溶液中得到GQDs/GCE。Nafion是网状聚合物,对GQDs有很好的分散作用,可以提高复合电极的稳定性。但由于Nafion本身导电性极差,对复合电极的形貌和性质有一定的影响[20]。考虑到Nafion的良好分散性和稳定性以及实验结果的可重复性,本实验仍采用Nafion作为GQDs的分散溶液。
图2A和2B是Pt/GQDs/GCE的SEM和EDX图,可以看出,Pt粒子成功电镀在GQDs/GCE表面,呈现球形且粒度较小,分布均匀性稍差。图2C和2D是Au/GQDs/GCE的SEM和EDX图,Au粒子亦成功沉积在GQDs/GCE表面,呈现不规则形状,部分区域有少量团簇现象。图2E和2F是GQDs/PtAu/GCE复合电极的SEM和EDX图,从图中可以看出,Pt和Au粒子同时电镀在GQDs/GCE表面,且Pt和Au粒子相互“包裹”形式沉积于电极表面,粒径适中且分布均匀。据EDS粗略统计分析(n=3),Pt/GQDs/GCE的Pt平均含量为15.24%,Au/GQDs/GCE的Au平均含量为42.42%,GQDs/PtAu/GCE的Pt平均含量为17.62%,Au平均含量为30.81%。再次证明Pt粒子和Au粒子同时成功沉积在GQDs/GCE表面,且与Pt/GQDs/GCE和Au/GQDs/GCE的含量与形貌不同。根据Au和Pt循环伏安制备方法和SEM、EDX表征可得知,Au和Pt是复合物而非合金材料。
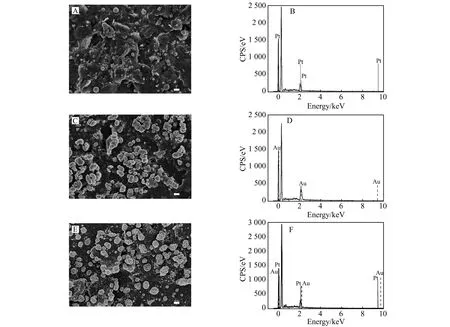
Fig.2 Pt/GQDs/GCE(A、B)、Au/GQDs/GCE(C、D)和GQDs/PtAu/GCE(E、F)复合电极的扫描电镜(SEM)和能谱(EDS)图Fig.2 SEM images and EDS of Pt/GQDs/GCE(A,B),Au/GQDs/GCE(C,D) and GQDs/PtAu/GCE(E,F)
2.3 GQDs/PtAu/GCE复合电极对TTC的电化学性能
图3为不同电极在0.1 mol/L PBS(pH=3.0)中对2.0×10-3mol/L TTC的循环伏安图。从图中可以看出,GQDs/GCE对TTC有较小的电流信号,氧化电位约为1.05 V,负电位扫描未出现还原峰,说明TTC在该电极上的电化学催化是不可逆反应。Pt/GQDs/GCE对TTC检测的性能比GQDs/GCE有一定程度提升,峰电流稍微提高,氧化电位负移至1.02 V,但峰形较宽,氧化峰位不明显。Au/GQDs/GCE复合电极对TTC的检测性能比GQDs/GCE和Pt/GQDs/GCE的信号稍强,出现明显的氧化峰。但起始氧化电位正移至1.1 V处,峰电位约为1.25 V。原因可能是单独Au粒子易于在电极表面团聚(SEM图也证实),不利于TTC的催化氧化。负电位扫描约0.7~0.8 V出现的峰是金属氧化物的还原峰[22],约0.1 V处出现的峰为H2析出峰[23]。然而,GQDs/PtAu/GCE复合电极对TTC的检测性能明显优于其他电极,起始氧化电位负移至0.8 V,峰电位约为0.9 V,并且峰电流显著提高,说明该复合电极具有更好的电化学性能,更有利于TTC的电催化氧化。此氧化峰电位(峰1,0.5 V和峰2,0.9 V)与文献方法相比,如Pt纳米粒子/碳电极(氧化电位:0.95 V和1.15 V vs.SCE)[14],石墨烯/L-半胱氨酸修饰电极(氧化电位:0.8 V和0.98 V vs.SCE)[15],碳纳米管修饰电极(氧化电位:+1.2 V vs.SCE)等,有很大程度的降低。TTC氧化电位降低,有利于采用电催化氧化对TTC进行准确检测。
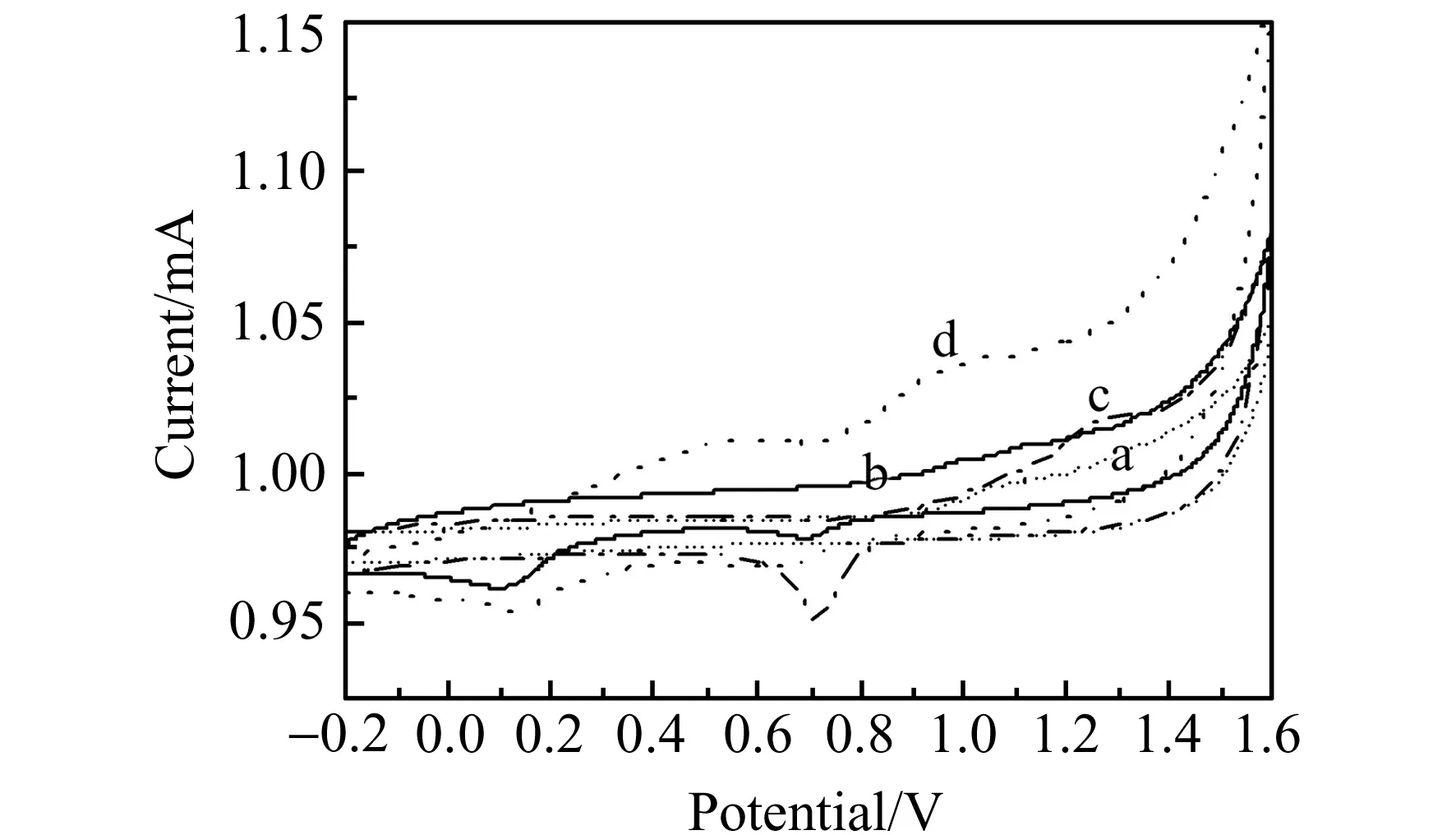
图3 GQDs/GCE(a)、Pt/GQDs/GCE(b)、Au/GQDs/GCE(c)和GQDs/PtAu/GQDs/GCE(d)对2.0×10-3 mol/L TTC检测的循环伏安图Fig.3 Cyclic voltammograms of GQDs/GCE(a),Pt/GQDs/GCE(b),Au/GQDs/GCE(c) and GQDs/PtAu/GCE(d) for the detection of 2.0×10-3 mol/L TTCThe electrolyte:0.1 mol/L PBS,pH=3.0.
2.4 GQDs/PtAu/GCE对TTC电化学特性


图4 (A) GQDs/PtAu/GCE对2.0×10-3 mol/L TTC在不同扫速下的循环伏安图(a→l:10,20,30,40,50,60,80,100,120,140,160,200 mV/s);(B)峰电位与logv的线性关系图(扫速范围10~100 mV/s)Fig.4 (A) Cyclic voltammograms for the detection of 2.0×10-3 mol/L TTC at the GQDs/PtAu/GCE in the different scan rates(a→l:10,20,30,40,50,60,80,100,120,140,160,200 mV/s;(B) Linear plot of peak potential vs.logv(Scan rate range:10 - 100 mV/s)
根据实验结果和前期研究,TTC的电氧化反应机理推测如下(图5):在相对较低的氧化电位下,TTC结构中10号位上的羟基会发生氧化,失去1个电子和1个质子,变成含氧自由基。但它在溶液中很不稳定,尤其在高氧化电位下,会迅速失去另一个电子,变成较稳定的双氧键结构。而7号位带有正电荷,有一部分TTC则直接失去个2电子和1个质子,生成带正电结构的物质(如虚线箭头所示)。接着,带正电结构的物质会结合电负性强的水分子中的氧,同时失去2个电子,这个过程在循环伏安曲线上以氧化峰2的形式表现出来。在循环伏安法的正向扫描中,这两步反应随电位的升高先后发生,产生相应的催化电流。通过实验也发现,低电位的氧化峰不稳定。根据氧化峰的稳定性和反应完全性,考虑约0.9 V作为检测的氧化电位。

图5 四环素的电化学氧化反应途径Fig.5 Reaction pathway of electrochemical oxidation of TTC
2.5 GQDs/PtAu/GQDs/GCE对四环素的电化学检测
2.5.1 循环伏安法图6为GQDs/PtAu/GQDs/GCE对高浓度TTC连续检测的循环伏安图。从图中可以看出,TTC的氧化峰电流随其浓度的增加而增大。以氧化电位0.9 V处峰电流与浓度之间的关系,得出TTC的氧化电流与其浓度在1.0×10-4~0.2 mol/L范围内呈现良好的线性关系,初步判断该复合电极可以对TTC进行连续检测,其氧化电流与TTC浓度具有良好的正相关性。

图6 GQDs/PtAu/GQDs/GCE对高浓度TTC连续检测的循环伏安图Fig.6 Cyclic voltammograms for the consecutive detection of high concentration of TTC at the GQDs/PtAu/GCE
2.5.2 安培法由于循环伏安法的灵敏度限制,低浓度的TTC采用安培法进行检测。图7为GQDs/PtAu/GCE对5.0×10-7~2.25×10-4mol/L TTC检测的i-t曲线。从图中可以看出,随着TTC浓度的增加,氧化电流逐渐增大,电流与TTC的浓度呈现两段线性范围,其中5.0×10-7~3.5×10-5mol/L的线性方程为:Ip(mA)=18.59cTTC+0.0364(R2=0.9922);4.5×10-5~2.25×10-4mol/L的线性方程为:Ip(mA)=3.368cTTC+0.5744(R2=0.9942)。通过两段线性关系的斜率(灵敏度)比较,该方法在TTC低浓度时灵敏度更高。TTC高浓度时,随着TTC浓度增加,电流信号增加缓慢,灵敏度降低,可能由于电极表面吸附造成饱和所致。本实验采用电位+1.0 V,在搅拌状态下氧化数秒,致使电极表面的产物彻底氧化以实现电极的再生。采用安培法更适用于低浓度TTC的定量检测。经过计算,该方法的检出限(S/N=3)为1.5×10-7mol/L,优于马铃薯淀粉/碳黑/GCE[6]、Au纳米粒子/分子印迹过氧化吡咯/碳电极[12]、Pt纳米粒子/碳电极[14]、石墨烯/L-半胱氨酸/GCE[15]、碳纳米管/GCE、氧化石墨烯修饰电极[25],可望用于实际样品中TTC的定量检测。
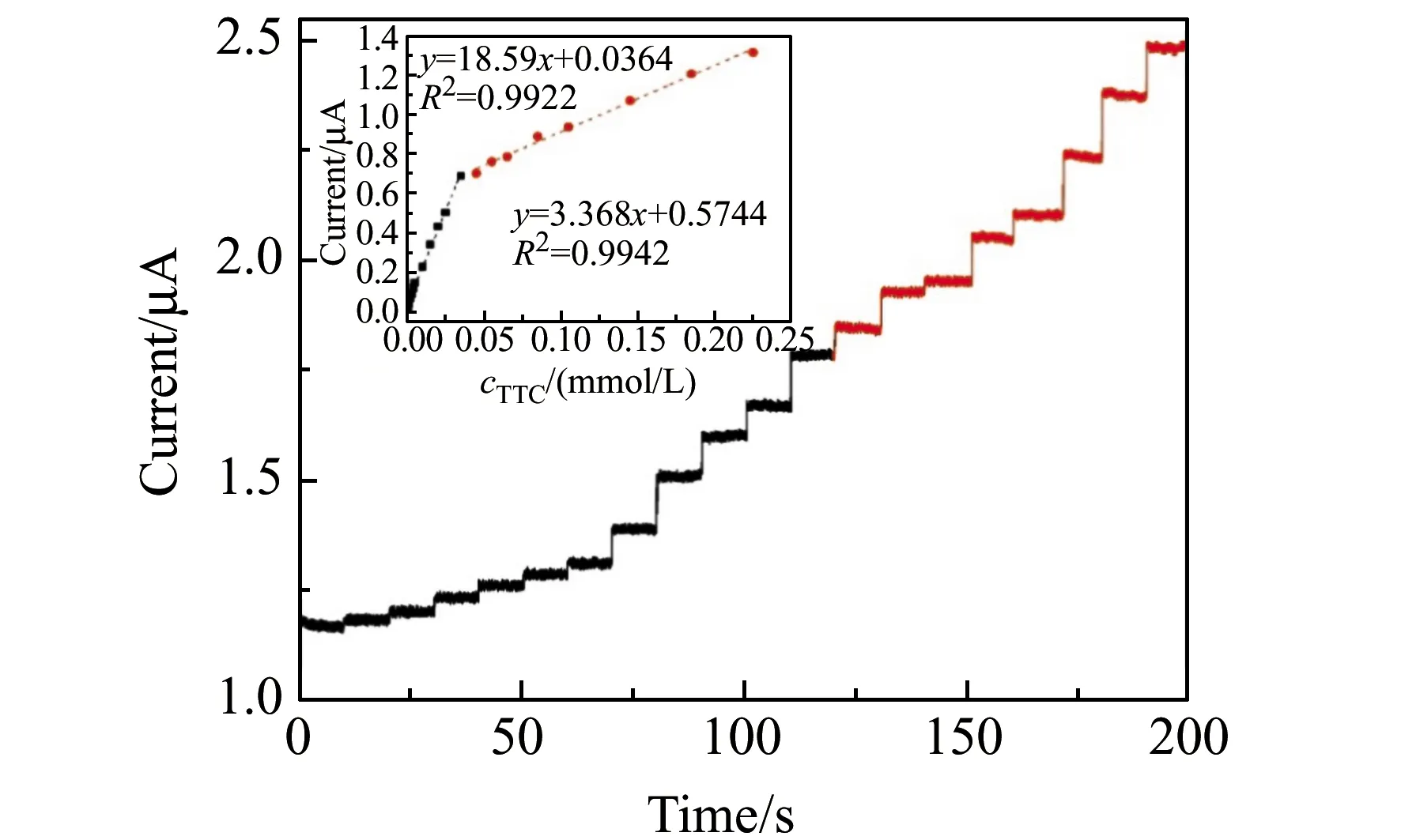
图7 GQDs/PtAu/GCE上不同浓度TTC在0.1 mol/L PBS(pH=3.0)中检测的安培曲线Fig.7 Amperometric curves for TTC detection at the GQDs/PtAu/GCE with different concentration in 0.1 mol/L PBS(pH=3.0)Inset:plot of peak current vs.TTC concentration.
2.6 GQDs/PtAu/GCE的性能评价
将同一支GQDs/PtAu/GCE在3.5×10-5mol/L TTC溶液中连续测定15次,其氧化峰电流的相对标准偏差(RSD)为4.72%。将6支不同GQDs/PtAu/GCE应用于3.5×10-5mol/L TTC溶液中检测,所得峰电流的RSD为4.95%,证明该电极具有良好的稳定性和重复性。
为了考察GQDs/PtAu/GCE对TTC检测的选择性,研究了不同干扰物如卡那霉素、氯霉素、氟比洛芬、布洛芬、盐酸四环素、氯四环素在3.5×10-5mol/L TTC溶液中的电流响应。研究表明,20倍浓度的卡那霉素、氯霉素、氟比洛芬、布洛芬在0.9 V氧化电位下对TTC检测无明显干扰。但同分异构体的盐酸四环素、氯四环素在该氧化电位下会增加TTC的催化电流,说明该方法对TTC的同分异构体无法区分,适用于检测TTC类抗生素的总含量。
2.7 实际样品的检测
取东华大学松江校区镜月湖水样,在最佳制备和测试条件下,考察GQDs/PtAu/GCE的实用性。水样经滤膜(直径0.45 μm)过滤后,取3 mL放入电化学检测池中,用0.1 mol/L PBS稀释至10 mL,调节pH为3.0,用标准加入法进行测定,加标回收率在95.6%~105.7%之间(表1)。

表1 样品分析结果及回收实验(n=3)Table 1 Analytical results of samples and recovery tests(n=3)
3 结论
本文基于GQDs/PtAu复合材料修饰电极,发展了一种简单、快速、直接检测TTC的电化学方法。研究了TTC在GQDs/PtAu/GCE上的电催化反应机理和氧化行为。GQDs/PtAu/GCE呈现出优良的电催化性能,显著降低了TTC的氧化电位,有利于TTC的催化氧化检测。GQDs/PtAu/GCE对于TTC的检测具有宽的线性范围和低的检出限,同时具有稳定性好、抗干扰能力强,对于环境样品中TTC类抗生素的总量测定具有潜在应用价值。
