合成锂皂土-海藻酸钠复合屏障膜的制备及研究
2021-11-09程东东邹多宏
程东东,周 璞,邢 新,邹多宏,2
目前临床上应用的可吸收引导骨再生 (guided bone regeneration,GBR) 膜通常受到机械强度弱、力学性能不足的限制,易发生穿孔和破裂。海藻酸钠 (sodium alginate,SA) 是组织工程支架的常用材料,能促进实验性骨缺损的骨再生,是GBR的合适材料。合成锂皂土 (Laponite®, LAP) 除了作为粘土材料应用于传统医药和化妆品,还可作为开发新的纳米医学功能材料,成为骨组织工程应用的理想选择。有序的“砖-泥”微观结构赋予了贝类优异的抗拉强度、刚度和韧性,受此启发,引入无机纳米填料制备类似特殊的层状微结构,成为近十年来提高“软基”聚合物力学性能的最常用方法。该研究采用喷涂组装方法构建仿贝壳结构的二元体系LAP -SA复合膜,通过测试该复合膜的抗拉强度及其对NIH/3T3增殖的影响,探讨其应用于组织工程屏障膜的可能性。
1 材料与方法
1.1 合成材料
SA[粘度(10 g/L,20 ℃)/(Pa·s)≥0.02,上海国药集团化学试剂有限公司];LAP(东莞市樟木头镇佳桐塑胶原料经营部);无水氯化钙(美国Sigma-Aldrich 公司)。1.2 主要试剂和仪器
DMEM、胰酶消化液(美国Hyclone公司);胎牛血清(美国Gbico 公司);CCK-8试剂盒(日本株式会社同仁化学研究所);力学万能实验机 (5565A,美国英斯特朗公司);CO孵箱 (美国Thermo 公司);扫描电镜 (Supra40,德国蔡司公司);透射电镜 (HT7700,日本日立公司);X 射线衍射仪 (X'Pert3 Powder,荷兰帕纳科公司);傅里叶变换红外光谱仪 (Nicolet 8700,美国热电尼高力仪器公司);酶标仪 (美国Bio-tek 公司);高温高压灭菌锅 (HVE-50,日本Hirayama 公司)。1.3 原料配制
分别配制质量浓度为 2% 的SA溶液及LAP溶液。分别称取 2 g 原料粉末溶于 98 ml 去离子水中,室温下搅拌直至完全溶解分散。1.4 复合薄膜的制备
首先制备LAP与SA的质量分数比为1 ∶10的复合膜(设为1组),取 1 ml LAP 溶液与 10 ml SA溶液混匀,磁子搅拌 0.5 h 直至完全分散,真空箱内除气泡后通过热喷涂组装方法,将混合液喷涂到热的基材上,待水蒸发后干燥成膜。同理分别制备 LAP 与SA的质量分数比为3 ∶10、5 ∶10、7 ∶10、9 ∶10 的复合膜和纯SA膜 (图1),分别命名为 3、5、7、9组和0组;随后取抗拉强度最大的复合膜用 Ca螯合后作为Ca组,共6组。同时为后面材料表征,将抗拉强度最大的复合膜组直接设为复合膜组,将制备的纯SA膜设为纯SA膜组。
图1 LAP-SA复合膜制备过程示意图与展示图
1.5 力学测试
在室温下将每组薄膜裁剪为长 50 mm、宽 4 mm的测试样品,并用螺旋测微仪测量每组样品厚度,通过力学万能实验机以 0.1 mm/s的拉伸速度直至样品断裂,记录其抗压强度,每组样品重复测试 6 次。取抗拉强度最大的复合膜组,重新制备测试样品后浸泡于 0.5 mol/L的氯化钙溶液中 5 s,室温下自然干燥后,以同样方法测试抗拉强度。最后绘制出相应的应力-应变曲线和断裂应力值表。1.6 样品表征
取抗拉强度最大的复合膜组和纯SA膜组,采用扫描电镜观察两组膜截面的微观结构。取 LAP 稀释溶液滴在透射铜网表面,待干燥后采用透射电镜观察 LAP 纳米片的形貌。取少量 LAP 纳米片、SA膜和复合膜分别平铺于观测台上,采用X射线衍射仪分析各组成分。研磨 LAP 纳米片、复合膜及SA膜,采用傅立叶变换红外光谱仪分析各成分。1.7 细胞相容性实验
取抗拉强度最大的复合膜组和纯SA膜组,用0.5 mol/L的CaCl溶液预处理 5 s 后 PBS 洗净。制备直径为 6 mm 的圆形复合膜和纯SA膜薄片,每组10个,高温高压灭菌。细胞系选用鼠胚胎成纤维细胞 (NIH/3T3细胞,由中国科学院细胞库提供),以8×10/孔接种,每组每个时间点5个复孔 (空白对照组仅接种NIH/3T3),37 ℃、5%CO培养。24、48 h后将CCK-8试剂与DMEM按1 ∶9 比例混合,每孔加100 μl,37 ℃、5%CO培养 2 h。用酶标仪在 450 nm 处读取吸光度值 (optical density, OD)。
2 结果
2.1 各组膜抗拉强度的比较
如图2所示各组膜样品的应力-应变曲线及断裂应力值。随着 LAP与SA质量分数比的增加,LAP-SA复合膜的抗拉强度也随之增加,当 LAP与SA的质量分数比为5 ∶10时,即5组复合膜的抗拉强度达最大,之后继续增加 LAP 含量,LAP-SA复合膜抗拉强度开始下降,各组总体差异有统计学意义 (F
=77.385,P
<0.001)。且5组膜样品用 Ca螯合后,即Ca组的抗拉强度相比螯合前有一定增加且差异无统计学意义。
图2 不同LAP-SA复合膜组和SA膜组样品的抗拉强度比较A:各组样品的应力-应变曲线;B:各组样品的断裂应力值;与0、1、3、7、9组比较: *P<0.05
2.2 样品表征
LAP与SA的质量分数比为 5 ∶10 时,扫描电镜下可见复合膜厚度约为 30 μm,截面呈明显的有序层状结构 (图3)。透射电镜示 LAP 纳米片呈薄片状,透光性和分散性良好(图4)。X 射线衍射仪、傅里叶变换红外光谱仪分析证实复合膜中存在LAP(图5)。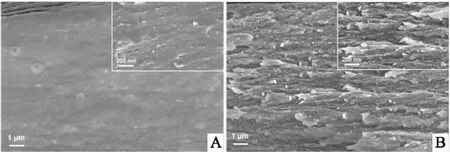
图3 扫描电镜下观察样品截面的微观结构×10 000A:纯SA膜组的截面;B:复合膜组的截面

图4 LAP纳米片不同倍数下的透射电镜观察A:×10 000; B:×20 000; C:×50 000; D:×100 000

图5 LAP-SA复合膜的组成成分分析A:复合膜的X射线衍射结果;B:复合膜的傅里叶变换红外光谱结果
2.3 细胞相容性实验结果
如图6所示,选取LAP与SA质量分数比为5 ∶10复合膜作为复合膜组进行细胞相容性实验,结果显示NIH/3T3与空白对照组、纯SA膜组和复合膜组共培养的24、48 h内,相同时间点各组OD值差异无统计学意义。
图6 各组膜材料与NIH/3T3共培养不同时间后细胞计数的比较
3 讨论
临床常用的GBR膜可分为不可吸收性膜和生物可吸收性膜。然而,不可吸收性膜在创口愈合过程中存在软组织开裂,导致屏障膜暴露的风险,可能造成创口感染甚至需要提前将其取出,从而影响GBR的再生效果;同时,在新骨形成之后必须实施第2次手术,将不可吸收性膜取出,从而不可避免地增加患者的痛苦和费用,并增加并发症发生的概率。生物可吸收性膜主要由可降解的合成或天然聚合物组成,无需二次手术,并且很少发生软组织开裂等并发症,但屏障膜的机械强度不足会导致成骨效果不确定,如临床上应用广泛的Bio-Gide及其他可吸收膜的抗拉强度均低于100 MPa。
因此,本研究拟制备一种新型可代谢高机械性能GBR膜。藻酸盐是一种天然存在的阴离子聚合物,其具有良好的生物相容性、低毒性,且成本相对低廉,以及通过添加二价阳离子(如Ca) 可发生凝胶化等特性,在生物医学领域中被大量研究。然而,由于该类聚合物在生理条件下的不稳定性和较差的机械性能限制了其临床应用。LAP是一种人工合成的可生物降解的层状硅酸盐,具有易于大量生产,廉价易得,纯度、组成和晶体尺寸均可控等优势,此外由于其纳米材料的层状结构,具有纳米晶体组成的附加优势,如较高的比表面积、吸附能力、表面反应性及阳离子的交换能力,因此能够作为具有流变特性的改性剂和成膜剂在技术层面广泛应用。其可通过带负电荷表面和带正电荷边缘与生物大分子发生多种物理结合,已有多个研究表明,向聚合物网络中引入LAP纳米颗粒可以大大提高复合物的机械性能。同时,近年来的研究表明,LAP可以释放Mg等离子,是一种极具潜力的骨修复材料,可以改善细胞黏附,诱导骨髓间充质干细胞成骨分化。Wang et al研究了LAP生物陶瓷在骨组织工程应用中潜在的适用性,其结论显示LAP生物陶瓷具有良好的生物安全性以及表面亲水性和蛋白质吸附活性,同时体内骨愈合效果良好,在骨组织工程中具有广阔的应用前景。
因此,本课题组拟向SA体系中加入LAP作为物理交联剂以及硅酸盐填料来提高复合膜的机械性能和成骨诱导功能。为使纳米晶体在体系中分散均匀,本课题组将混有LAP的SA悬浮溶液喷涂到热的基材上,待水蒸发后便可形成有序的层状微结构。完成复合膜制备后便进行力学抗拉强度测试,当LAP与SA的质量分数比为5 ∶10时,复合膜的抗拉强度达到最大 (166.9±11.5) MPa。为了进一步提高复合膜的机械性能,本课题组采用氯化钙浸泡的方法,使Ca与 SA 产生螯合作用从而稳固复合膜,并测试其抗拉强度。结果显示 Ca螯合后的抗拉强度可增加至 (178.0±14.8) MPa,相比螯合前有一定增加,但差异无统计学意义。
