UPLC-Q-TOF-MS/MS快速分析六味地黄苷糖片化学成分
2021-11-08樊晓荃胡军华王振中1
樊晓荃,付 娟,胡军华,肖 伟,王振中1, *
UPLC-Q-TOF-MS/MS快速分析六味地黄苷糖片化学成分
樊晓荃1, 3,付 娟2, 3,胡军华2, 3,肖 伟2, 3,王振中1, 2, 3*
1. 南京中医药大学,江苏 南京 210000 2. 江苏康缘药业股份有限公司,江苏 连云港 222001 3. 中药制药过程新技术国家重点实验室,江苏 连云港 222001
采用UPLC-Q-TOF-MS/MS技术对六味地黄苷糖片中的化学成分进行分析和鉴定。色谱柱为Phenomenex Luna C18(250 mm×4.6 mm,5 μm),以乙腈-0.3%甲酸水溶液作为流动相,梯度洗脱,体积流量1 mL/min,柱温35 ℃,进样量10 μL;采用电喷雾离子源,负离子模式下采集数据,根据精确质荷比、二级碎片离子信息,结合对照品和文献数据鉴定六味地黄苷糖片中的化学成分。共鉴定和推测出71个化合物,其中25个来自酒萸肉、19个来自熟地黄、31个来自牡丹皮、2个来自泽泻、3个来自茯苓、2个来自山药。其中22个化合物经对照品验证。基本明确了六味地黄苷糖片的化学物质基础,为六味地黄苷糖片的质量控制及药效物质基础研究提供了参考。
六味地黄苷糖片;质谱分析;质量控制;化学成分谱;酒萸肉;熟地黄;牡丹皮;泽泻;茯苓;山药
六味地黄汤是中医滋补肾阴的经典名方,由熟地黄、酒萸肉、牡丹皮、山药、茯苓、泽泻组成[1],由宋朝名医钱乙首创,主要用于腰膝酸软、头晕目眩、耳聋耳鸣、盗汗自汗等肾阴不足之症[2]。近代实践证明,六味地黄方广泛应用于治疗肾脏疾病、更年期综合症、高血压、肝脏疾病等数10种疾病[3-5]。
六味地黄苷糖片是基于对六味地黄汤的大量基础研究开发而成,用于治疗伴有肾阴虚的更年期综合症。该药从汤剂出发,经过2步醇沉、2步色谱分离得到了苷类、多糖以及寡糖3个有效部位,在此基础上得到了六味地黄苷糖片。
研究表明六味地黄苷糖片具有改善慢性多重不可预期应激所致焦虑抑郁样行为及阿尔茨海默病动物模型转基因小鼠认知缺陷的作用[5],其中苷类成分对免疫及内分泌调节起重要作用[6]。为阐明六味地黄苷糖片的药效物质基础,本实验对六味地黄苷糖片中的化学成分(主要为苷类成分)进行了研究,运用UPLC-Q-TOF-MS/MS技术对六味地黄苷糖片中的成分进行定性分析,为六味地黄苷糖片的质量控制及药效物质基础研究提供依据。
1 材料
Agilent 1290超高效液相色谱仪(DAD检测器,美国安捷伦公司);Agilent 6538 Q-TOF质谱仪(美国安捷伦公司);Mettler Toledo XP6型电子分析天平(百万分之一,瑞士梅特勒公司);Mettler Toledo AL204电子分析天平(十万分之一,瑞士梅特勒公司);KQ-500DB型超声波清洗器(昆山超声仪器有限公司);Milli-Q Academic纯水仪(美国密理博公司)。色谱乙腈(德国默克公司);色谱甲酸(美国天地公司)。
莫诺苷(批号111998-201703,质量分数97.4%)、马钱苷(批号111640-201808,质量分数99%)、芍药苷(批号110736-201943,质量分数95.1%)、毛蕊花糖苷(批号111530-201914,质量分数95.2%)、马钱苷酸(批号111865-201704,质量分数97.4%)、獐芽菜苦苷(批号110785-201404,质量分数98.3%)、没食子酸(批号110831-201605,质量分数90.8%)、中国食品药品检定研究院;牡丹酚原苷(批号200302,质量分数98%)、腺苷(批号201901,质量分数98%)、松果菊苷(批号201904,质量分数98%)、没食子酰芍药苷(批号201901,质量分数98%),南京森贝伽生物科技有限公司;獐芽菜苷(批号7001,质量分数98%)、异毛蕊花糖苷(批号7283,质量分数98%)、地黄苷D(批号7433,质量分数98%)、焦地黄苯乙醇苷B(批号LOT8184,质量分数98%),上海施丹德生物技术有限公司;氧化芍药苷(批号19120604,质量分数99.67%)、山茱萸新苷(批号19080905,质量分数98%)、连翘酯苷E(批号DSTDL008301,质量分数98%)、丹皮酚新苷(批号DST200910-076,质量分数98%)、8-表番木鳌酸(批号DST200422-157,质量分数98%),成都德思特生物技术有限公司。六味地黄苷糖片(批号20181001),江苏康缘药业股份有限公司。
2 方法
2.1 检测条件
2.1.1 色谱条件 色谱柱为Phenomenex Luna C18(250 mm×4.6 mm,5 μm),流动相为乙腈(A)-0.3%甲酸水溶液(B),梯度洗脱(0~22 min,4%~8% A;31~60 min,8%~14% A;65~80 min,18%~25% A;85 min,90% A),柱温35 ℃,体积流量1 mL/min,检测波长250 nm,进样量10 μL。
2.1.2 质谱条件 电喷雾离子源(ESI),负离子模式,毛细管电压4000 V,质量扫描范围100~2000;干燥气温度350 ℃;干燥气体积流量10 L/min;雾化气压力275.75 kPa;裂解电压100 V;锥孔电压65 V;碰撞能量根据不同化合物的需要选取15~40 eV。
2.2 溶液的配制
2.2.1 对照品溶液的配制 分别取莫诺苷、马钱苷、芍药苷、牡丹酚原苷、丹皮酚新苷、山茱萸新苷、腺苷、獐芽菜苷、毛蕊花糖苷、异毛蕊花糖苷、松果菊苷、氧化芍药苷、地黄苷D、没食子酰芍药苷、8-表番木鳌酸、焦地黄苯乙醇苷B、獐牙菜苦苷、连翘酯苷E、马钱苷酸、没食子酸适量置于量瓶中,用水溶解稀释至刻度,制备成含各成分50~100 μg/mL混合对照品溶液,经0.22 μm微孔滤膜滤过备用。
2.2.2 供试品溶液的配制 取六味地黄苷糖片10片,研细,取约0.2 g,精密称定,置10 mL量瓶中,加纯水适量,超声处理(功率250 W,频率40 kHz)5 min,放冷,用水稀释至刻度,摇匀,滤过,取续滤液,经0.22 μm微孔滤膜滤过,即得。
3 结果与分析
按“2.1”项下条件检测六味地黄苷糖片供试品溶液,得到对照品及六味地黄苷糖片负离子模式下总离子色谱图,见图1、2。根据精确质荷比,二级碎片离子信息,结合对照品和文献数据共鉴定和推测出71个化合物,其中25个来自酒萸肉,19个来自熟地黄,31个来自牡丹皮,2个来自泽泻,3个来自茯苓,2个来自山药。所测得成分中有20个化合物经与对照品比对得到鉴定,结果见表1。
3.1 苯乙醇苷类化合物
此类化合物均来自熟地黄药材。该类化合物通常是由咖啡酰基、苯乙醇苷元和糖连接而成,通常在质谱中均可检测出[M-H-162]−,是由准分子离子脱去1个葡萄糖基[M-H-C6H10O5]−或1个咖啡酰基[M-H-C9H6O3]−得到的,因此可以根据化合物的结构来判断脱掉的基团。以峰58为例,在负离子模式下有准分子离子峰/799.266 0,二级质谱得到了/623.220 5、477.162 7、297.133 5297.133 5等碎片,推测为峰58化合物母离子先后丢失了1个CH2、1个咖啡酰基(C9H6O3)、1个鼠李糖基(C6H10O4)以及1分子葡萄糖(C6H12O6),结合文献报道[14]碎片推测峰58为焦地黄苯乙醇苷A,见图3、4。
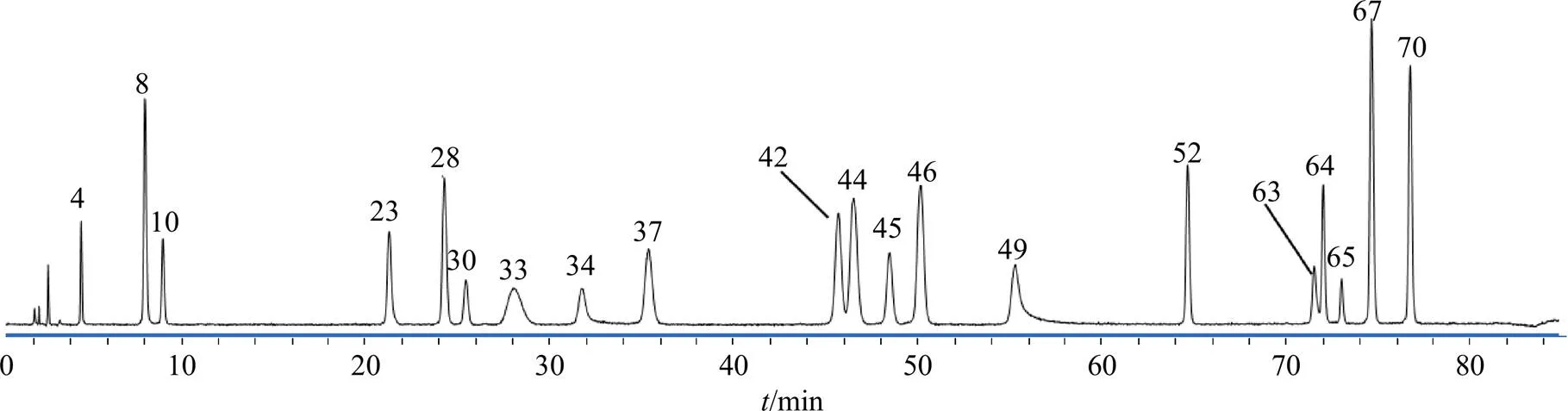
图1 负离子模式下对照品总离子流图

图2 负离子模式下六味地黄苷糖片总离子流图

表1 六味地黄苷糖片化学成分的UPLC-Q-TOF-MS/MS分析
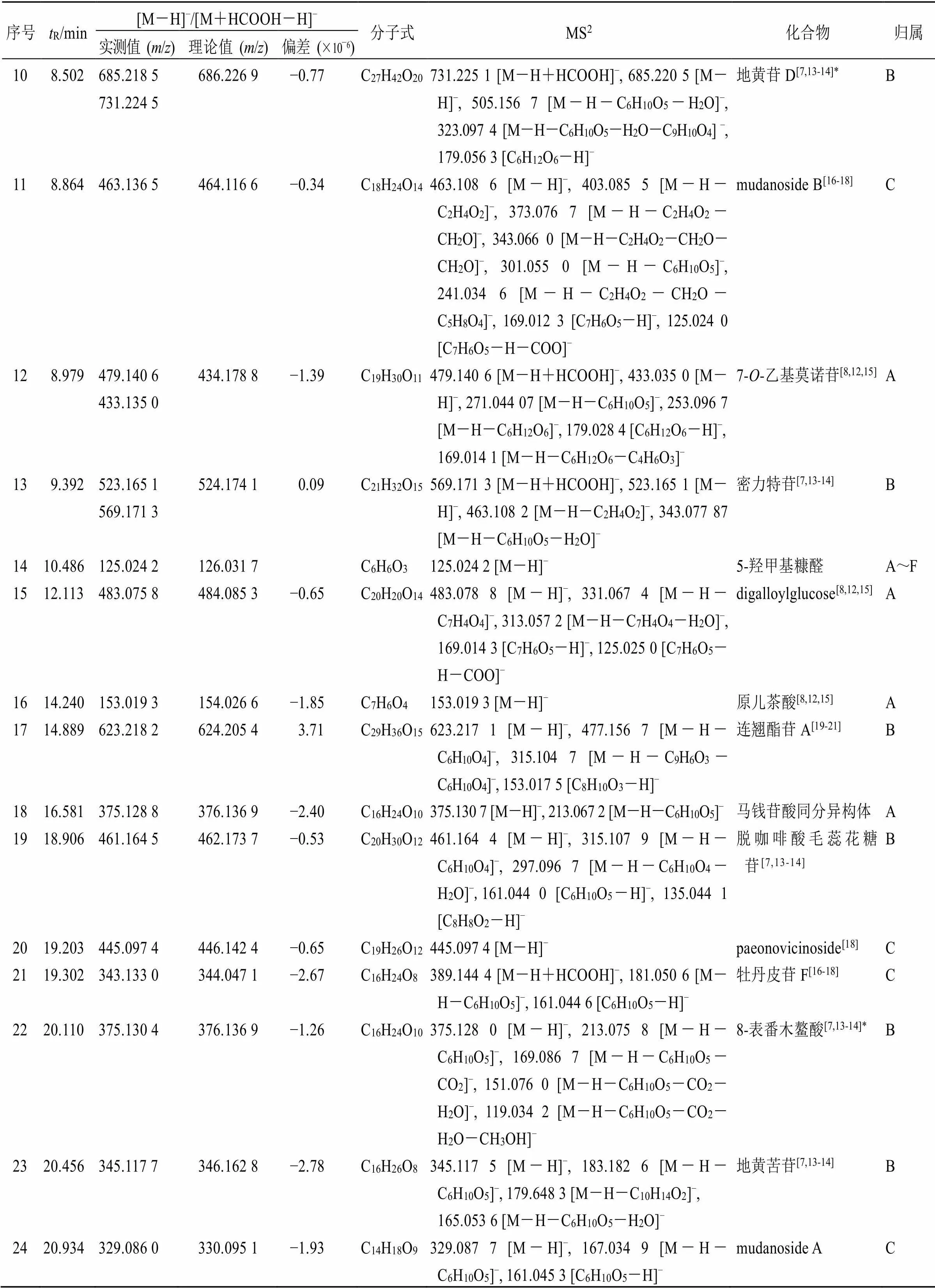
续表1

续表1

续表1

续表1

续表1
*通过对照品比对确认的成分 A-酒萸肉 B-熟地黄 C-牡丹皮 D-泽泻 E-茯苓 F-山药
*-comfirmed by reference materials A-B-C-D-E-F-

图3 焦地黄苯乙醇苷A的MS/MS图

图4 焦地黄苯乙醇苷A可能的裂解途径
结合碎片离子及文献报道[7,14],峰52、53、64、65、67、71分别为脱咖啡酸毛蕊花糖苷、洋地黄叶苷C、松果菊苷、毛蕊花糖苷、焦地黄苯乙醇苷B、异毛蕊花糖苷、焦地黄苯乙醇苷D。
3.2 单萜苷类
单萜苷类化合物主要来自于牡丹皮,这类成分通常由单萜部分(蒎烷骨架C9H9O3)与葡萄糖脱水缩合同时进行与芳香酸类化合物的酯化得到。在流动相中有甲酸的情况下,单萜苷类化合物通常会得到[M-H+HCOOH]−的离子峰,以峰49为例(图5),经对照品比对后确认为芍药苷,负离子模式下,一级质谱中有准分子离子峰/479.151 0同时出现了[M-H+HCOOH]−峰/525.157 7,二级质谱中可以观察到丢失了HCHO后的碎片离子/449.130 0 [M-H-HCHO]−、丢失了HCHO和苯甲酸的碎片离子/327.095 7 [M-H-HCHO-C7H6O2]−以及丢失了糖基和苯甲酸的碎片离子[M-H-C6H10O5-C7H6O2]−/195.065 0,此外还发现了蒎烷骨架的碎片离子/165.055 5 [M-H-HCHO-C7H6O2-C6H10O5]−,可能的裂解途径见图6。峰11,负离子模式下,一级质谱中有准分子离子峰/463.136 5,二级质谱中可以观察到蒎烷骨架离子/165.062 0,结合碎片及文献报道[16-18]推断峰11为mudanpioside B。峰34经对照品指认为氧化芍药苷,有准分子离子峰/495.150 3,二级质谱下可见/465.132 5 [M-H-HCHO]−及蒎烷骨架离子/165.053 6。峰38、39、50、63有相同规律,分别推测为mudanpioside I、mudanpioside E、galloyloxypaeoniflorin、没食子酰芍药苷。

图5 芍药苷的MS/MS图

图6 芍药苷可能的裂解途径
3.3 糖苷类
糖苷类化合物主要来自酒萸肉、牡丹皮、熟地黄,多具有没食子酸或葡萄糖结构。以峰57为例(图7),准分子离子峰为/787.096 3,二级质谱中可见碎片/635.194 8、617.075 6、465.068 5、447.059 5、313.059 3、295.044 5,结合文献,推测为1,2,3,6-四没食子酰葡萄糖,可能的裂解途径见图8。结合碎片离子及文献报道[16-18],推测峰9、15为digalloylglucose,峰40、48、51为三没食子酰葡萄糖,峰66为五没食子酰葡萄糖。结合对照品及推测峰42、46分别为牡丹酚原苷、丹皮酚新苷。结合文献报道[16-18]推测峰55、56为suffruticoside A/C,峰61、62为suffruticoside B/D。
峰33经对照品指认为莫诺苷,准分子离子峰为/405.139 0,一级质谱下可以观察到/451.130 0 [M-H+HCOOH]−,二级质谱中观察到/243.077 2 [M-H-C6H10O5]−、225.066 4 [M-H-C6H10O5-H2O]−、141.048 7 [M-H-C6H10O5-C4H6O3]−,质谱信息及可能的裂解途径见图9、10。结合碎片离子及文献报道[12,22-27]推测峰10、12、13、30、32、37、43~45、70分别为地黄苷D、7--乙基莫诺苷、密力特苷、金吉苷、二氢山茱萸苷、獐芽菜苦苷、马鞭草苷、獐芽菜苷、马钱苷、山茱萸新苷。

图7 1,2,3,6-四没食子酰葡萄糖的MS/MS图

图8 1,2,3,6-四没食子酰葡萄糖可能的裂解途径

图9 莫诺苷的MS/MS图

图10 莫诺苷可能的裂解途径
4 讨论
近年来,随着社会经济的发展,生活节奏逐渐变快,更年期综合征的发病率呈上升趋势,给患者带来很大困扰,并影响其生活质量和身心健康。针对这一问题,在中医药理论指导下,按照由“中药饮片组方(饮片配伍)向中药复方活性成分群组方(组分配伍)发展”的中药经典方剂“二次开发”思路,对六味地黄方活性物质组方进行了探讨,从汤剂出发,经过两步醇沉、两步色谱分离得到了苷类、多糖以及寡糖3个有效部位,在此基础上得到了六味地黄苷糖片。六味地黄苷糖片现有的质量标准缺乏完善的质量控制方法,为阐明药效物质基础,后续会对六味地黄苷糖片中的化学成分进行定量、入血实验研究。
本实验采用UPLC-Q-TOF-MS/MS技术对六味地黄苷糖片中的化学成分进行了快速分析,结合单味药材对质谱峰进行了归属,并通过一级质谱获得的准分子离子峰推测鉴定出了71个六味地黄苷糖片中可能含有的化合物。其中莫诺苷、马钱苷、芍药苷、牡丹酚原苷等20个化合物经由对照品指认,其余成分通过二级质谱提供的碎片离子结合相关文献推测指认,因六味地黄苷糖片中含有较多环烯醚萜苷类成分,结合文献报道[20-21]及实际情况选择了在负离子模式下检测,指认结果显示来自泽泻、茯苓、山药中的成分较少,推测3味药材在六味地黄苷糖片中主要提供糖类成分,因此未能检出,后续需进一步完善。本实验运用UPLC-Q-TOF-MS/MS技术对六味地黄苷糖片进行了全面系统地解析,为六味地黄苷糖片后续的入血实验研究和关键成分定量控制提供了理论基础。
利益冲突 所有作者均声明不存在利益冲突
[1] 邱伊星. 六味地黄丸及其相关制剂的指纹图谱质量控制方法研究 [D]. 长沙: 湖南中医药大学, 2016.
[2] 王泷. 易水学派医家运用六味地黄丸经验[J]. 长春中医药大学学报, 2018, 34(1): 70-72.
[3] 虞学军, 林齐鸣, 曹小玉. 近年研究六味地黄丸的文献分析 [J]. 中国中医药信息杂志, 2002, 9(3): 87-88.
[4] 耿丽, 蔡云芳. 六味地黄丸HPLC指纹图谱建立及主要成分分析[J]. 世界中医药, 2019, 14(11): 2875-2878.
[5] 王晓燕. 六味地黄苷糖中糖苷部位的化学成分研究 [D]. 北京: 中国人民解放军军事医学科学院, 2009.
[6] 周青儒, 程肖蕊, 周文霞, 等. 六味地黄苷糖对脂多糖所致神经炎症模型小鼠学习记忆损伤的作用 [J]. 国际药学研究杂志, 2019, 46(5): 363-370.
[7] 张波泳, 江振作, 王跃飞, 等. UPLC/ESI-Q-TOF MS法分析鲜地黄、生地黄、熟地黄的化学成分 [J]. 中成药, 2016, 38(5): 1104-1108.
[8] 杜伟锋, 张云, 丛晓东, 等. HPLC-ESI- MS法分析山茱萸炮制前后的化学成分 [J]. 中华中医药学刊, 2012, 30(1): 62-65.
[9] 林鹏, 李银保. 山药的化学成分及其生物活性研究进展 [J]. 广东化工, 2015, 42(23): 118-119.
[10] 袁书林. 山药的化学成分和生物活性作用研究进展 [J]. 食品研究与开发, 2008, 29(3): 176-179.
[11] 龚凌霄, 池静雯, 王静, 等. 山药中主要功能性成分及其作用机制研究进展 [J]. 食品工业科技, 2019, 40(16): 312-319.
[12] 赵婷秀, 曹迪, 茆文莉, 等. HPLC-QTOF-MS分析六味地黄丸不同部位的化学成分 [J]. 中药新药与临床药理, 2018, 29(4): 489-496.
[13] 张振凌, 吴若男, 于文娜, 等. 生地黄产地加工炮制一体化工艺研究 [J]. 中草药, 2018, 49(20): 4767-4772.
[14] Wang X, Wu C, Xu M,. Optimisation for simultaneous determination of iridoid glycosides and oligosaccharides inby microwave assisted extraction and HILIC-UHPLC-TQ-MS/MS [J]., 2020, 31(3): 340-348.
[15] Deng S X, West B J, Jensen C J. UPLC-TOF-MS characterization and identification of bioactive iridoids infruit [J]., 2013, 2013: 1-7.
[16] 夏成凯, 詹云武, 胡云飞, 等. HPLC法同时测定不同产地牡丹皮中13种化学成分的含量 [J]. 中草药, 2019, 50(4): 970-974.
[17] 赵文军, 林阳, 李鹏飞, 等. 牡丹皮化学成分的HPLC-QTOFMS分析 [J]. 药学实践杂志, 2014, 32(4): 261-265.
[18] 胡云飞, 裴月梅, 吴虹, 等. 基于UPLC-Q-TOF-MS技术研究不同产地牡丹皮药材化学成分的差异 [J]. 中草药, 2016, 47(17): 2984-2992.
[19] 白雪, 黄惠锋, 吴修红, 等. HPLC-DAD-MS/MS法分析金银花中化学成分 [J]. 食品与药品, 2015, 17(1): 5-8.
[20] 霍金海, 孙国东, 魏文峰, 等. UPLC-Q-TOF/MS法分析牛黄清感胶囊成分 [J]. 中成药, 2018, 40(10): 2340-2348.
[21] 李泮霖, 李楚源, 刘孟华, 等. 基于UFLC-Triple-Q- TOF-MS/MS技术的金银花、山银花化学成分比较 [J]. 中南药学, 2016, 14(4): 363-369.
[22] 李存满, 梁鑫淼, 薛兴亚. 电喷雾离子源正离子模式下环烯醚萜苷的质谱裂解行为 [J]. 高等学校化学学报, 2013, 34(3): 567-572.
[23] 牟德华, 胡高爽, 李存满. UPLC/Q-TOF MS/MS负离子模式下环氧烷型环烯醚萜苷的结构表征 [J]. 质谱学报, 2019, 40(2): 197-207.
[24] 周丹丹, 邹秦文, 林瑞超. 基于超高效液相色谱-四级杆-静电场轨道阱质谱的胃复春片化学成分研究[J]. 世界中医药, 2020, 15(13): 1841-1848.
[25] 吴昕怡, 刘小莉. 环烯醚萜类成分生物合成途径及关键酶基因研究进展 [J]. 中国民族民间医药, 2017, 26(8): 44-48.
[26] Wu Q, Yuan Q, Liu E H,. Fragmentation study of iridoid glycosides and phenylpropanoid glycosides inby rapid resolution liquid chromatography with diode-array detection and electrospray ionization time-of-flight mass spectrometry [J]., 2010, 24(8): 808-819.
[27] 刘桦, 周婷婷, 范国荣. 液质联用技术在环烯醚萜苷类化合物研究中的应用 [J]. 药学服务与研究, 2011, 11(1): 45-49.
Rapid identification of chemical components in Liuwei dihuang gantang Tablets by UPLC-Q-TOF-MS/MS
FAN Xiao-quan1, 3, FU Juan2, 3, HU Jun-hua2, 3, XIAO Wei2, 3, WANG Zhen-zhong1, 2, 3
1. Nanjing University of Chinese Medicine, Nanjing 210000, China 2. Jangsu Kanion Pharmaceutical Co., Ltd., Lianyungang 222001, China 3. State Key Laboratory of New-tech for Chinese Medicine Pharmaceutical Process, Lianyungang 222001, China
To study the chemical constituents in Liuwei Dihuang gantang tablets (六味地黄糖苷片) by using UPLC-Q-TOF-MS/MS.The chromatographic conditions were as follows: Phenomenex Luna C18(250 mm × 4.6 mm, 5 μm) column with acetonitrile and 0.3% formic acid as mobile phase, gradient elution, flow rate of 1 mL/min, The column temperature was 35 degrees, the injection volume was 10 L; mass spectrometry conditions: The data were collected by electrospray ion source (ESI) under negative ion mode. These components were further analyzed based on the accurate mass ratio, the two level fragment ion information, the reference materials and literature data.A total of 71 compounds were identified and speculated, 25 of which came from liquor cornus, 19 from, 31 from, 2 from, 3 fromand 2 from. Among them, 22 compounds were verified by reference substance.The results basically clarified the chemical basis of Liuwei Dihuang gantang tablets, and provided a reference for the quality control and pharmacodynamic material basis of Liuwei Dihuang gantang tablets.
Liuwei Dihuang gantang tablets;mass spectrometry;quality control;chemical composition spectrum;liquor cornus;;;;;
R284.1
A
0253 - 2670(2021)21 - 6473 - 12
10.7501/j.issn.0253-2670.2021.21.004
2021-03-18
重大新药创制科技重大专项(2013ZX09402203)
樊晓荃,男,硕士研究生,研究方向为药物分析。Tel: 15720600226 E-mail: 815405571@qq.com
王振中,男,高级工程师,博士,主要从事中药新剂型研发。Tel: (0518)81522367 E-mail: wzhzh-nj@163.com
[责任编辑 王文倩]
