MoS2纳米材料高效析氢研究进展*
2021-11-05温丽珍龙洁清杨显德
温丽珍,龙洁清,杨 晶,韦 良,杨显德
(南宁师范大学 广西天然高分子化学与物理重点实验室,广西 南宁 530001)
0 引言
氢能储量丰富、可再生,有效避免能源的枯竭,同时氢能燃烧的产物不会造成污染,具有巨大的发展潜能[1,2]。光催化制氢具有高效、廉价以及环境友好等优点,在高效析氢领域中具有较大的发展前景[3-5]。常见的半导体光催化剂(如TiO2、CdS等)存在对太阳光利用率低等缺点,光催化析氢效率不够理想[6,7]。过渡金属硫化物的二硫化钼(MoS2)纳米材料具有类石墨烯结构,可调的带隙宽度,复杂的边缘结构提供大量活性位点,成为近年来光催化析氢领域的研究热点[8,9]。本文首先介绍MoS2的性质和应用,重点分析了通过贵金属沉积、离子掺杂、缺陷调控以及复合改性的方法改善MoS2的光催化析氢性能。最后,对MoS2纳米材料在光催化析氢领域的应用前景做了概述。
1 MoS2的性质
MoS2具有类石墨烯结构,通常以辉钼矿形式存在于自然界中,不溶于水、酸、碱以及有机溶剂,但可以溶于煮沸后的浓硫酸和王水。如图1(a)所示,层状的MoS2由提供2个空轨道的S原子和提供4个电子的Mo原子通过较强的共价键相互连接形成与“三明治”相似的S-Mo-S结构;块状MoS2一层一层堆叠形成块状MoS2,层与层由比较弱的范德华力连接[10]。如图1(b)所示,不同的堆叠方式使MoS2形成了三种不同的晶体结构,1T-MoS2和3R-MoS2

图1 (a)MoS2层状结构[10] (b)MoS2的2H、3R、1T晶体结构[10]
都属于亚稳态,而2H-MoS2常态下是稳定的[11]。MoS2纳米材料带隙具有可调性,当多层块状结构的层数减少时,导带会升高,价带则会降低,因此禁带宽度也会随之变化,最大可调至1.9 eV。此外,外界应力以及高压等多种情况也能够对能带结构产生影响,当块状MoS2纳米材料转变为单层MoS2纳米材料时,间接带隙半导体变为了直接带隙半导体[12-14]。单层MoS2纳米材料能够提供更高的能量使其具有分解水的能力,同时较宽的带隙对可见光的吸收效果更好,特征吸收峰为620~720 nm[15]。
2 MoS2的应用
2.1 润滑领域
MoS2纳米材料层与层之间的S原子以较弱的范德华力相连接,层间距大约为0.349 nm,而S-Mo之间是以较强的共价键相互连接,厚度大约是0.315 nm,与层平行的平面方向存在较低的剪切强度,而垂直方向则表现出非常高的硬度和强度,摩擦系数较低。产生的静电力作用时,容易产生滑离,表现出良好的摩擦性能,因此被广泛用于润滑领域。以MoS2纳米材料作为原料的润滑油不仅有良好的润滑效果,在使用过后还可将其部分回收用于其他领域,如催化领域[16,17]。
2.2 电化学领域
MoS2具有高达670 mAh/g的比容量,层与层之间弱范德华力容易让锂离子插入,有效改善充放电时体积膨胀的问题,因此MoS2在电化学领域最常用作锂离子电池电极材料。MoS2纳米材料也可以用于比锂电池具有更高比功率的超级电容器[18,19],但是MoS2纳米片的电容性比较差,一般需要与碳纳米管和石墨烯等材料来提高性能。MoS2纳米材料还可以和贵金属、聚合物、碳材料等耦合,用于研发电化学传感器,这些传感器可应用于食品安全、药物和环境污染物等领域[20]。
2.3 催化领域
近年来,MoS2纳米材料在催化领域中也得到了广泛的应用:(1)加氢脱硫(DHS),层状MoS2纳米材料边缘存在很多不饱和的带负二价的硫离子,使其具有更好的加氢活性[21];(2)降解有机废水,MoS2因其独特的能带结构、大比表面积和高反应活性,对可见光利用率较高,使其降解有机污染物的能力比较强[22];(3)催化水分解析氢,具有半导体性质的2H-MoS2,带隙可调,同时具有良好的光、电性能,自由能接近于0,有望代替Rh、Pt等贵金属进行析氢,在光、电以及光电催化析氢领域都有很大的应用前景[23-25]。
3 MoS2光催化析氢
MoS2纳米材料具有良好的带隙宽度,与太阳光谱的匹配性高;层状结构的边缘复杂,富含不饱和键,具有高的活性位点,能很好的抑制光生载流子复合,提高电子、空穴的分离效果。因此,近年来MoS2纳米材料用于光催化分解水析氢的研究越来越多。但是,目前报道的大多都是将MoS2纳米材料作为助催剂改性其他半导体(如TiO2、ZnS等)的光催化性能。
3.1 MoS2作为助催化剂析氢
MoS2纳米材料可改善氧化物光催化剂的活性,如MoS2与ZnO、TiO2等复合。He H Y等人[26]制备了MoS2沿基面和边缘与TiO2相连的复合物TiO2/MoS2(E),结果显示负载MoS2含量为3 wt%的TiO2/MoS2(E)的光催化活性最高(析氢效率为4.300 mmol/(g·h),比纯TiO2高36倍。MoS2纳米材料同样能够提高硫化物半导体光催化剂的催化析氢活性,如CdS、ZnIn2S4等。邓洪课题组[27]制备MoS2负载量为0.75 wt%的ZnIn2S4/MoS2光催化剂,其光催化析氢活性比纯ZnIn2S4和ZnIn2S4/Pt高,析氢效率为4.974 mmol/(g·h)。MoS2还可以作为其他一些光催化剂的助催剂,如唐华课题组[28]制备了零维MoS2与二维g-C3N4的复合材料MoS2QD/g-C3N4,当MoS2的负载量为7%时,析氢速率比纯的g-C3N4高8.8倍。MoS2还可以与其他的助催剂制备双助催剂催化剂,如LiY J等人[29]利用MoS2和Ti3C2制备含Mo空位的双助催剂MoS2@TiO2@Ti3C2复合材料,Mo空位增加了活性位点,MoS2和Ti3C作为双助催剂提高了光催化剂的电子转移效率,使得该复合材料光催化剂具有更高的催化活性,析氢效率为2.128 mmol/(g·h)。
3.2 MoS2作为主催化剂析氢
纯MoS2纳米材料容易发生团聚,且反应部位比较少,限制了其在光催化析氢领域的应用。为了提高光催化析氢活性,可以通过贵金属沉积、缺陷调控、离子掺杂和复合改性等多种手段对其进行改性。
3.2.1 贵金属沉积
贵金属(Ag、Au)等沉积在MoS2纳米材料半导体表面的时,MoS2纳米材料半导体的功函数小于贵金属,MoS2纳米材料半导体的费米能级会低于贵金属,MoS2纳米材料的导带上光生电子会不断地向贵金属表面迁移,而空穴仍然留在MoS2纳米材料的价带上,这个过程会一直持续到两者之间的费米能级相等。因此在MoS2纳米材料半导体与贵金属之间的界面会形成肖特基势垒,形成的势垒在一定程度上阻碍了光生电子与空穴的复合,促进了两者的分离和转移,因而改善了MoS2纳米材料半导体的光催化性能。
纳米金性质稳定并且极易制备,被广泛应用于纳米材料领域,拥有很强的表面等离子共振效应(SPR),因此可用于光催化领域。李炫华等人[30]将3~6个金纳米颗粒(AuNPs)按5~10 nm的粒子间距离进行合理的结构调控制备多聚体Au@MoS2。由于AuNPs之间有很强的同相耦合,太阳光能量能够储存在AuNPs的间隙中。将AuNPs作为核引入MoS2纳米材料后,改善了MoS2纳米材料的光吸收能力,吸收峰扩展至560~670 nm,如图2(a)所示,并且有利于产生电子。因此多聚体Au@MoS2核壳结构4小时内催化析氢量高达2.997 mmol/g,大概是纯MoS2纳米材料(881.6 μmol/g)和单体Au@MoS2核壳结构(2.112 mmol/g)的3.4倍和1.4倍,如图2(b)所示。负载AuNPs不仅增强了析氢的量,在实验中还发现了AuNPs与MoS2之间的电荷转移能够抑制部分的光腐蚀,表现出良好的光催化稳定性。
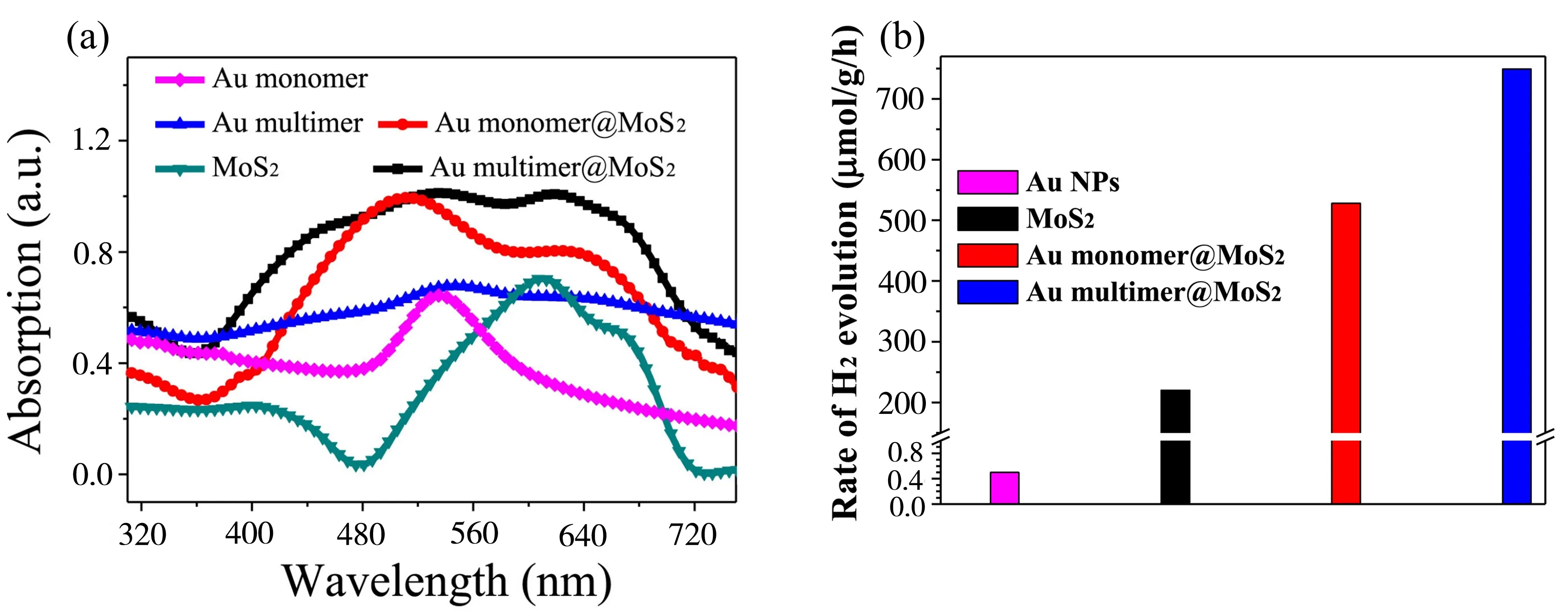
图2 (a)纳米Au单体、纳米Au多聚体、MoS2、单体Au@MoS2和多聚体Au@MoS2紫外-可见吸收光谱[30] (b)纳米金Au、MoS2、单体Au@MoS2和多聚体Au@MoS2光催化析氢效率[30]
除了纳米金,纳米银也常用于纳米材料领域,也可作为光催化半导体的助催剂。Yang L等人[31]利用0.008 mmol的AgNO3和2 mg的MoS2纳米片制备了Ag-MoS2杂化纳米片。Ag纳米粒子沉积在MoS2纳米片表面后,界面存在明确的金属-半导体结构,能够消除光催化剂的光吸收,表面的Ag纳米粒子能够作为抑制MoS2纳米片的光生电子与空穴复合的俘获位点。因为捕集效应,Ag-MoS2杂化纳米片的光致发光强度被广泛地猝灭。用Ag-MoS2杂化纳米片和CdS光催化剂进行光催化析氢实验,析氢效率达10.7 mmol/(g·h),较MoS2纳米片(1.8 mmol/(g·h))有明显的提高。此外,Ag-MoS2杂化纳米片也表现出了较高的抗光腐蚀性。
3.2.2 离子掺杂
通过掺杂将杂质原子或者离子掺入MoS2纳米材料中,所掺入的杂质取代S原子或者Mo原子,进而对MoS2纳米材料进行改性。主要是因为所掺入的杂质原子半径、离子半径和电荷与原来的S、Mo原子的不一样,会导致新的晶格畸变或是晶格缺陷,从而引起MoS2纳米材料的能带结构发生改变。
掺杂物替代MoS2纳米材料中的Mo原子是离子掺杂改性MoS2纳米材料最见的方法。李美琴[32]用AgNO3作为掺杂物,制备了Ag替代Mo原子掺杂MoS2纳米材料。在光催化性能研究中,掺杂浓度为7.37%的Ag掺杂MoS2纳米片显示出比较优异的光催化析氢性能,析氢效率高达2.695 mmol/(g·h),明显高于未掺杂的MoS2纳米片(1.708 mmol/(g·h)),如图3(a)所示。同时,该催化剂具有更优异的稳定性,如图3(b)所示。随后,基于第一性原理分析掺杂后体系的禁带宽度由原体系的1.68 eV减小至0.76 eV,对紫外光和可见光的吸收较强,对光的利用率明显增强,其价带向上移动,导带出现下移,改善了光催化析氢的反应,从而MoS2半导体的光催化活性得到了提高,这与之前所得出的实验结果基本上一致。

图3 (a)MoS2和Ag掺杂MoS2光催化析氢效率[32](b)MoS2和Ag掺杂MoS2光催化析氢稳定性[32]
相对于替代Mo原子的掺杂,关于S原子替代的报道相对偏少。在最新的替代S原子的掺杂研究中,李炫华课题组[33]采用一步水热法将非金属P掺杂入MoS2纳米薄片并分析了材料的光催化活性。首先,掺杂的P取代了S原子,与纯的MoS2相比,P掺杂的MoS2光催化剂的电阻比较低,有利于电子的转移,能够有效阻碍光生电子和空穴的重新组合。其次,具有丰富皱边的P掺杂的MoS2比纯的MoS2的活性位点更多,还可以加入牺牲剂来消耗孔洞。最后,P掺杂后的光催化材料的带隙宽度由1.84 eV减小为1.77 eV,扩大了对光的吸收范围,提高了可见光利用率。在相同的实验条件下,P掺杂的MoS2纳米材料在第一个循环中析氢效率为278.8 μmol/(g·h),是纯MoS2(99.4 μmol/(g·h))的2.8倍,如图4所示。
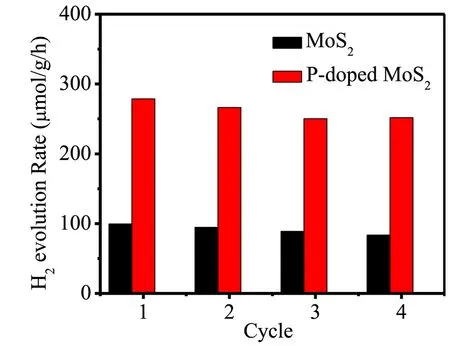
图4 P掺杂MoS2和MoS2进行4次循环光催化析氢效率[33]
3.2.3 缺陷调控
离子掺杂能够影响MoS2半导体的能带结构,通过缺陷调控同样能够影响MoS2纳米材料半导体的光学性能,但是关于缺陷调控的研究报道偏少。对于单层MoS2纳米材料来说,点缺陷可以分为空位、反位缺陷和间歇原子这三种。空位缺陷又可以分为少一个S原子的S空位缺陷和少一个Mo原子的Mo空位缺陷;反位缺陷分为S原子代替Mo原子的缺陷以及Mo原子代替S原子的缺陷;间歇原子则是位于原子间歇之间加入一个S原子或是Mo原子。
对于S原子空位缺陷的理论研究,李玥等人[34]进行了S空位缺陷对MoS2纳米材料性能的影响实验,在球磨和超声的结合下,不使用任何化学或活性剂,就能够将块状MoS2剥落成单层MoS2,并成功将S空位和原子大小的空隙引入基面,最终形成了S空位的MoS2纳米网。富含缺陷的MoS2纳米网还原层、空穴和缺陷的相互作用,提供更多的活性位点和充分利用基面,其电催化活性和光催化活性都得到了进一步的增强。结果显示,S空位MoS2纳米网的析氢效率为4.84 mmol/(g·h),大约是MoS2纳米片(0.81 mmol/(g·h))的5.97倍,以及S空位MoS2纳米片(1.86 mmol/(g·h))的2.41倍,如图5(a)所示。此外,S空位MoS2纳米网还表现出良好的光催化稳定性,如图5(b)所示。
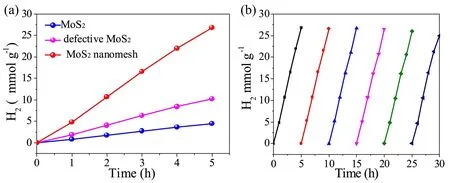
图5 (a)MoS2、缺陷MoS2和MoS2纳米网光催化析氢情况[34](b)光催化析氢稳定性测试[34]
相对于S原子空位缺陷的研究,Mo空位缺陷的报道相对偏少。最新的研究报道中,张峰君课题组[35]通过控制NaBH4的浓度对MoS2进行处理,制备了具有不同数量Mo空位的MoS2纳米薄片。一定数量的Mo空位与邻近的Mo空位会在MoS2表面形成悬空键,在Mo空位的表面或者边缘就会产生大量的不饱和S原子。更多的H+可以被未饱和的S原子吸附,增加了MoS2纳米薄片的反应位点。在进行光催化时,Mo空位可以产生局域的电荷富集,从而提高光催化效率。随着Mo空位的增加,析氢效率随之升高,用0.09 mol/L NaBH4处理的MoS2-0.09/TiO2光催化剂析氢效率最高(5.424 mmol/(g·h))。
3.2.4 复合改性
将MoS2纳米材料与其他材料进行复合制备光催化半导体能够实现有效的太阳光催化析氢,提高催化剂的光催化性能。主要是因为他们之间发生了相互作用而形成的异质结,MoS2与具有不同能带结构的半导体材料复合时,异质结之间界面使能带发生弯曲,空间位置会出现内部电场,从而有利于光生电子和空穴之间的转移和分离。
MoS2纳米材料与金属化合物材料进行复合,可形成异质结。Khalid等[36]利用水热合成法制备了Bi2O3/MoS2异质结复合材料。Bi2O3含量为11 wt%的Bi2O3/MoS2光催化剂表现出最优异的光催化析氢性能,析氢效率高达10 mmol/(g·h),明显比Bi2O3(1.1 mmol/(g·h))和MoS2(1.2 mmol/(g·h))光催化剂高,如图6(a)所示。较高的光催化活性可能归因于较大的表面积、对太阳光利用率较高、Bi2O3的加入能够提高光生电子-空穴的转移、分离效率,并且Bi2O3和MoS2之间形成的p-n异质结能够有效阻碍载流子的复合。另外,Bi2O3/MoS2异质结复合材料光催化剂以经过四个循环,稳定性保持在86%,如图6(b)所示。此外,Khalid等人[37]还在不添加任何表面活性剂的情况下,成功制备了用Ag2O纳米棒修饰3D MoS2的Ag2O/MoS2复合材料光催化剂。在进行光催化性能的实验中,随着Ag2O含量增加至5%,可以提高Ag2O/MoS2复合材料光催化剂的光催化效率,析氢效率达95 μmol/(g·h),是纯MoS2(9.7μmol/h)的9.8倍。但是,当Ag2O含量增加至7%时,其光催化性能会降低。主要原因可能是掺入Ag2O的量过多会造成遮光效应,减少表面活性,同时减少MoS2的吸光范围。
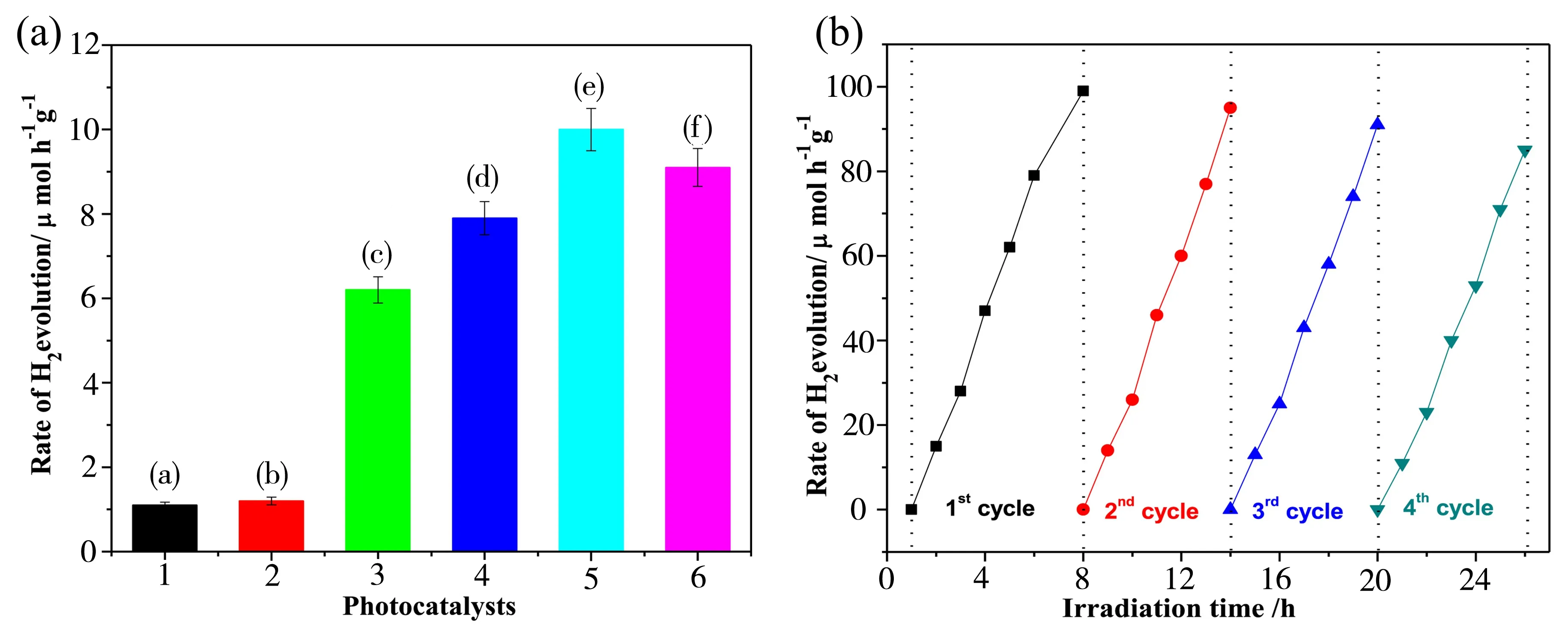
图6 (a)不同样品光催化析氢率[36](b)11%BiO3/MoS2光催化剂稳定性实验[36]
MoS2纳米材料不仅可以和金属化合物材料形成异质结,也可以与非金属材料进行复合。Nagaraja等人[38]采用一锅溶剂热合成法制备了MoS2微流体(S1)和MoS2与g-C3N4比例分别为1∶1(S2)、1∶2(S3)、1∶3(S4)的MoS2/g-C3N4异质结。在光催化分解水析氢研究中,显示出S1、S2、S3、S4和纯g-C3N4的光催化析氢速率分别为291.23 μmol/(g·h)、1787.1 μmol/(g·h)、1112.7 μmol/(g·h)、471.1 μmol/(g·h)和43.46 μmol/(g·h)。当MoS2与g-C3N4的比例为1∶1时,析氢的效率会比较高,主要是因为MoS2与g-C3N4(1∶1)的协同作用,对可见光吸收最佳以及MoS2的边缘反应位点能够提高质子还原能力。当g-C3N4浓度增加时,MoS2的边缘反应位点会被覆盖,从而降低了催化剂的活性。在光致发光研究中,S2的猝灭强度最高,也可以说明S2的析氢活性高于其他样品。此外,比例为1∶1的MoS2/g-C3N4光催化剂经过几次循环也没有显著的催化活性损失,表现出良好的光稳定性和回收性。
4 结 语
MoS2纳米材料具有独特的晶体结构、电子结构以及光学性质,使其在润滑领域、电化学领域和催化领域等都有广泛的应用。在光催化析氢领域中,MoS2纳米材料不仅可以作为助催剂提高氧化物、硫化物及其他半导体光催化剂的催化活性,还可以通过对MoS2进行改性来提高析氢效率。通过贵金属沉积、离子掺杂、缺陷调控和复合改性的方法提高MoS2纳米材料的光催化析氢性能。
总的来说,将MoS2纳米材料作为光催化剂,最主要的挑战包括抑制光生电子和空穴的复合和丰富催化反应活性位点。通过缺陷调控和离子掺杂的方式,改变MoS2半导体的能带结构,增加反应活性位点,可以有效地激发MoS2纳米材料作为光催化剂的潜力。MoS2纳米材料无论是作为助催剂还是主催化剂都会得到飞跃式的发展。
