两种检测策略在细胞库病原体污染的检出分析
2021-11-03曾劲峰梅秋红张耿邬林枫李然许晓绚赵钰熊文刘沐芸王立林
曾劲峰 梅秋红 张耿 邬林枫 李然 许晓绚 赵钰 熊文 刘沐芸★ 王立林★
在细胞库供者样本病原体检测方面,我国还未制定专门的标准。可参照的标准为《脐带血造血干细胞库技术规范(试行)》[1],其对于病原体检测指定参照《血站管理办法》[2]。而在国际方面,全球先进输血和细胞治疗联盟(Advancing Transfusion and Cellular Therapies Worldwide,AABB)与细胞治疗认证机构(Foundation for the Accreditation of Cellular Therapy,FACT)均列出要检测乙型肝炎病毒(Hepatitis B virus,HBV)、丙型肝炎病毒(Hepatitis C virus,HCV)、人类免疫缺陷病毒(HIV1/2)等病毒,并且指明必须采取病毒核酸检测(Nucleic Acid Testing)方法。因此,依据目前国际行业规范,结合我国政策法规,有两种检测策略可供选择:一种为参照《血站技术操作规程(2015 版)》[3]规定采用1~2 种血清学酶联免疫吸附分析(Enzyme Linked Immune Sorbent Assay,ELISA)法检测病原体抗原抗体,同时采用1 种核酸检测试剂检测病毒核酸,简称血筛检测策略(Blood screen strategy,BSS);另一种为参照卫健委发布的病毒临床诊断检测标准[4-8],采用1种临床诊断血清学试剂检测病原体抗原或抗体,简称临床检测策略(Clinical detection strategy,CDS)。本研究采用BSS 与CDS 检测病原体,病原体类型包括HBV、HCV、HIV 与梅毒螺旋体(Treponema pallidum,TP),并对检测结果的差异进行综合分析,判断两种策略在检测细胞库病原体污染效果的差异,同时分析血筛检测策略中血清学检测方法与核酸检测方法之间的差异性,以确定核酸检测在细胞库病原体污染风险防控中的作用及效果。
1 材料与方法
1.1 标本来源
选取深圳综合细胞库2016年2月至2017年7月7 981 例细胞供体的外周血标本,其中来源于孕产妇的标本7 571 例,均为孕产妇生产前或生产后7 天内进行采样,来源于非孕产妇的成人标本410例,为细胞样本采集前或细胞样本采集后7 天内采集供者外周血标本。
1.2 检测设备及试剂
设备:FAME24/30 酶免疫检测仪器(瑞士HAMILTON),TECAN RSP/200 酶免疫加样器(瑞士TECAN),美国Grifols 公司全自动核酸检测平台Procleix Tigris 核酸检测系统;试剂:进口检测试剂有意大利Diasorin HBsAg ELISA 检测试剂、美国强生ORTHO 抗-HCV ELISA 检测试剂、美国伯乐Genscreen ULTRA 抗-HIV/Ag ELISA 检测试剂、意大利Diasorin 梅毒螺旋体特异性抗体检测试剂,美国Grifols Procleix Ultrio Assay 试剂,国产试剂有北京万泰HBsAg ELISA 检测试剂、珠海丽珠抗-HCV ELISA 检测试剂、北京万泰抗-HIV ELISA 检测试剂、珠海丽珠梅毒螺旋体特异性抗体检测试剂、北京万泰HTLV ELISA 检测试剂。
1.3 临床检测策略
由细胞标本采集医院按照术前或产前传染病检测要求及标准对供者在细胞采集前抽血进行HBV、HCV、HIV1/2 及TP 的抗原/抗体检测,深圳综合细胞库收集汇总检测报告结果。
1.4 血筛检测策略
由深圳市血液中心参照血筛检测标准,采用上述进口及国产试剂对深圳市综合细胞库细胞供者抗凝血样本进行HBsAg、抗HCV、抗HIV、梅毒螺旋体抗体及HBV/HCV/HIV 病毒核酸定性检测,所有检测结果均为非反应性则报为非反应性结果,否则计为反应性结果。
1.5 确诊实验
抗-HIV 阳性样本送深圳市疾病预防控制中心做HIV 蛋白印迹法确证试验检测,梅毒螺旋体特异性抗体阳性样本送深圳市慢性病防治中心采用日本富士(FUJIREBIO)TPPA 法进行检测。
1.6 统计方法
采用IBM SPSS Statistics 21.0 软件进行统计学分析;采用Kappa 检验上述两种检测策略及方法的一致性;两种检测策略及方法比较采用配对卡方检验;P<0.05 为差异有统计学意义。
2 结果
2.1 CDS 与BSS 检测结果对比
两者检测结果比较,差异有统计学意义(P<0.05)。见表1。
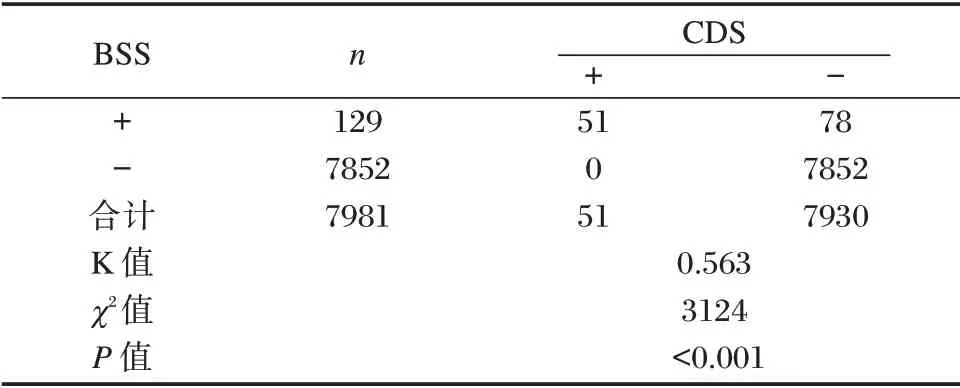
表1 CDS 与BSS 检测结果对比Table 1 Comparison of detection results between CDS and BSS
2.2 各检测项目两种检测策略结果对比
两种检测策略在HBV、TP、HCV 检测结果比较,差异有统计学意义(P<0.005)。见表2。
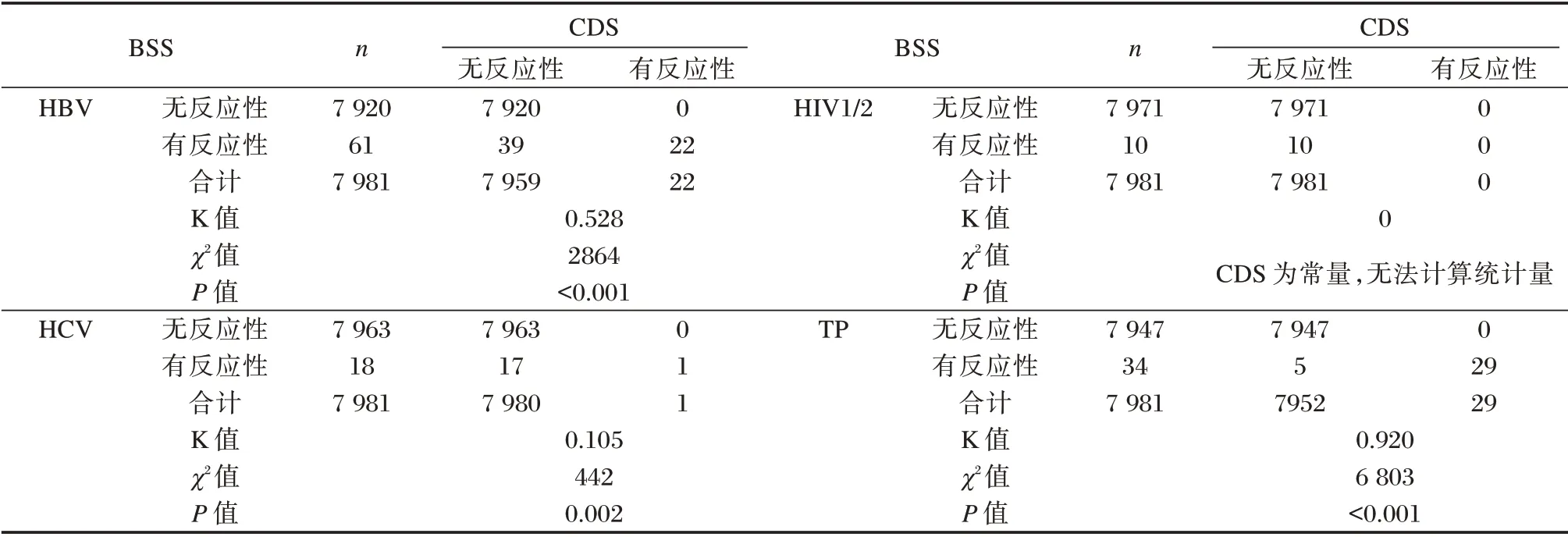
表2 各检测项目两种检测策略结果对比Table 2 Comparison of results of two test strategies for each test item
2.3 血筛策略中血清学ELISA 检测与NAT 检测结果分析比较
血筛检测策略中HBV、HCV、HIV 血清学ELISA 检测与病原体核酸检测(nucleic acid detection,NAT)两种方法检测结果一致性一般(K=0.651);两种检测方法检测结果比较,差异有统计学意义(P<0.001)。见表3。两种检测方法对HBV 检测结果一致性非常好(K=0.833);两种检测方法检测结果比较,差异有统计学意义(P<0.001);两种方法对HCV 与HIV 检测结果一致性较差(K=0)。见表4。
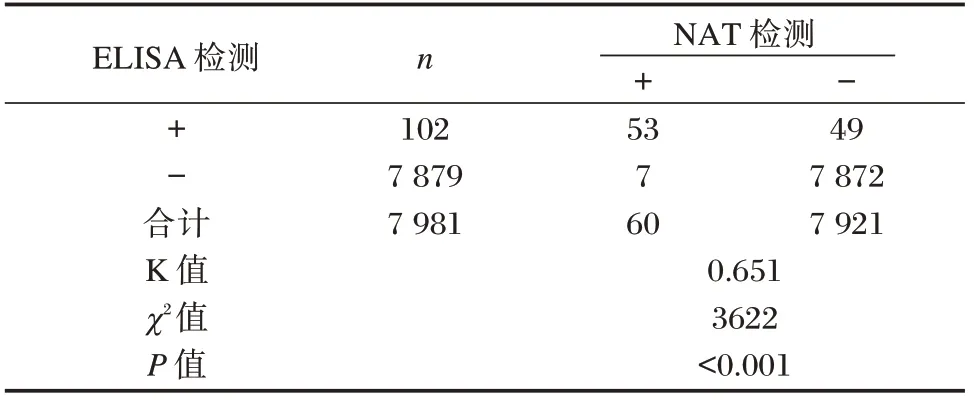
表3 BSS 中ELISA 检测与NAT 检测结果总体分析Table 3 Overall analysis of ELISA and NAT detection results in DSS
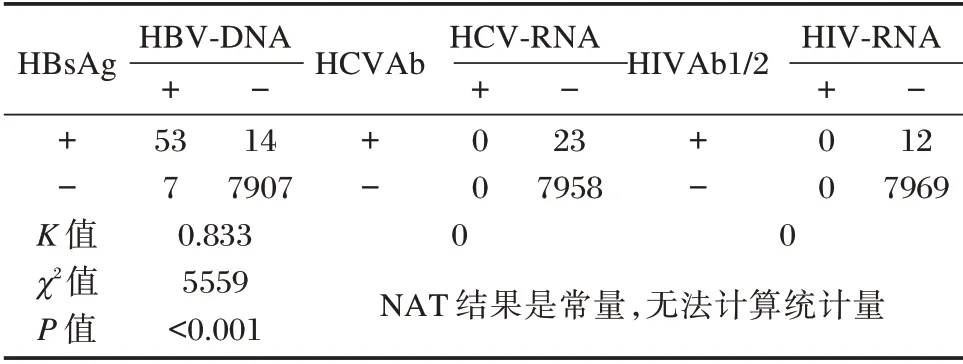
表4 BSS 中ELISA 检测与NAT 检测对HBV、HCV、HIV结果分析Table 4 ANALYSIS of HBV,HCV and HIV results by ELISA and NAT in BSS
2.4 血筛检测阳性样本中各项目占比分析
各项目阳性检出率及占比为:HBsAg 与HBVDNA 是占比最高的项目,分别为30.45%与27.27%。见表5。
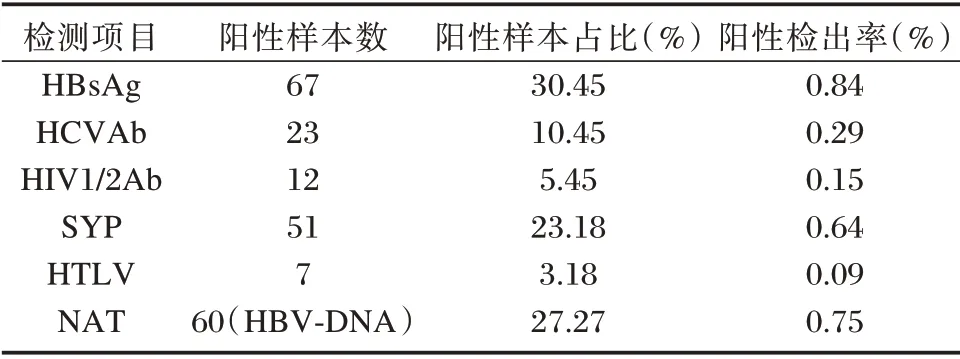
表5 血筛检测各项目阳性占比分析统计Table 5 Analysis and statistics of the positive proportion of each item in BSS
2.5 确证试验
对23例抗-HCV阳性样本进行RIBA确证实验发现样本均为阴性和不确定,无一例阳性;对51 例SYP阳性样本进行TPPA 检测,结果显示20 例阳性,31 例阴性,真阳性率为39.22%;对12例抗HIV阳性样本进行蛋白印迹法确证实验,证实其样本均为阴性。
3 讨论
CDS 与BSS 两种检测策略在细胞库样本供体血液标本检测结果上存在差异,其产生的原因可能是因为BSS 采用ELISA 和NAT 两种方法,共同来确定结果,从而导致与CDS 结果出现显著差异。采用BSS 对细胞供者进行筛查检验,ELISA 双试剂较单试剂检测具有更高的检测灵敏度,同时采用NAT方法对HBV、HCV 和HIV 进行筛查,能提高病原体感染窗口期的检出率,尤其是在HBV 方面显示出较好效果(提高HBV 窗口感染期检出率11.67%),能更好的防范病原携带样本混入正常的细胞库。
从血清学检测的确认结果(HBV 除外)可以发现,本研究中样本的假阳性率高于普通献血人群,分析原因可能为研究样本多来源为孕产妇血清样本,其孕产期受激素和孕期的影响,较一般人群更易产生非特异性抗体,易产生假阳性结果。根据Wesolowski 等的研究报道孕妇初筛试验的假阳性率约为0.14%[9]。国内研究者也分析了孕妇的传染病检测项目的假阳性情况,蒋春云等研究者对7例ELISA HIV 反应性孕妇追踪确认检测中发现,有3 例孕妇在追踪后抗体阳转,而其余4 名孕妇HIV 抗体和核酸检测持续阴性[10]。目前血筛HIV检测主要采用第四代检测试剂[11],另有研究者分析了孕妇HIV 电化学发光的假阳性情况,16 例筛查反应性样本中,HIV 确认检测1 例阳性,其余15例为阴性[12]。对孕妇的梅毒ELISA 研究也发现,ELISA 检测的假阳性较高,可达8.49%[13]。
由此可见,采用DSS 对细胞库供体血液检测,灵敏度较高,可以有效防止细胞库的病原体污染。但针对孕妇这一特殊群体,在初筛之外,应结合确认实验或NAT 结果,可减低假阳性率。
虽然BSS 中应用的双试剂检测可提高检测灵敏度,但ELISA 存在因“窗口期”、病毒变异、免疫沉默等造成的漏检,在目前使用的ELISA 检测试剂的条件下,HBsAg、抗-HCV 及抗-HIV 的平均“窗口期”分别约为59 d、72 d 及22 d[14]。而采用NAT,可将HBV、HCV 及HIV 的平均“窗口期”分别缩短至20 d、10 d 及7 d[15-16],专家甚至建议有必要采用高灵敏度的核酸检测技术应用于术前筛查[17],可见应用NAT 可提高整体检测系统的灵敏度,降低检测后感染的残余风险。
由此可见,BSS 检测灵敏度更高,在细胞库病原体污染风险防控中应采用此策略,整体上降低任何单一检测方法不准确导致的病原体漏检风险,避免病原体交叉污染,保证细胞库储存样本安全。
