宫颈癌患者根治性手术辅助放化疗后复发的早期死亡影响因素分析
2021-10-29颜文娟朱慧婷
颜文娟,朱慧婷
0 引 言
宫颈癌是最常见的女性生殖道恶性肿瘤,根据2018年癌症数据报告,全球新增约57万宫颈癌病例和31.1万死亡病例[1]。中国每年新发宫颈癌病例约13.15万例,死亡病例达5.3万例[2]。宫颈癌在女性人口中的发病率和死亡率分别为6.6%和7.5%,在女性易发癌症中居第四位,且发病率呈现逐年上升趋势[3]。宫颈癌已有相对完善的筛查和预防手段,但在某些地区筛查技术不够普及完备,宫颈癌仍严重威胁女性生命安全。
根据国际妇产科联合会分期系统术前诊断为IB-IIA期的宫颈癌患者采用根治性子宫切除术加盆腔淋巴结清扫术治疗,根据术后病理组织学检查中存在的危险因素再决定是否行术后辅助放疗或同步放化疗[4]。但仍有10% ~ 20%的患者在宫颈癌根治术及放化疗后出现复发,复发患者治疗困难疗效差,5年生存率仅为3.2%~13%[5]。宫颈癌患者根治性手术后复发死亡的影响因素有待进一步研究。本研究通过对接受根治性手术辅助放化疗的宫颈癌复发患者的临床资料进行回顾性分析,探讨宫颈癌复发患者的临床病理特征以及影响患者早期死亡的相关因素,以期为改善宫颈癌复发患者预后提供科学依据。
1 资料与方法
1.1 研究对象回顾性分析2012年1月至2018年5月在辽宁省肿瘤医院妇产科接受根治性手术辅助放化疗后出现复发的153例宫颈癌患者临床病理资料。纳入标准:①组织学确诊为宫颈癌;②治疗方式为手术治疗(接受广泛性子宫切除加双附件切除加盆腔淋巴结清扫术,包括经腹和腔镜)并辅助40Gy或以上的盆腔放疗,有(或无)同步化疗;③经两位及以上副主任医师根据相关检查确诊宫颈癌术前分期为IB1-IIA2,术后分期为IB-IIA,IIIC1-2期;④所有患者病历资料、病理资料和随访情况完整。排除标准:①有新辅助化疗史;②治疗前有远处转移迹象;③伴有心、肝、肾等重大并发症的患者;④合并其他肿瘤患者;⑤未能按要求规律随访者。
1.2研究方法
1.2.1 治疗方法所有患者手术方式均为根治性子宫切除联合盆腔淋巴结清扫术,术后均行辅助放疗/同步放化疗治疗。术后4~6周内开始施行放疗或调强放疗,依据《2020 NCCN子宫颈癌临床实践指南(第1版)》,临床靶体积包括宫旁区域、阴道上部和盆腔淋巴引流区(髂总血管区、髂内外血管区、闭孔淋巴区和骶前淋巴结区),腹主动脉旁淋巴结阳性患者的CTV另外包括腹主动脉旁淋巴结区域。剂量范围为44.0~50.4 Gy(22~28次),每日照射剂量为1.8~2.0 Gy,每周接受5次放疗,时长共4.5~6周。腔内近距离放疗用于阴道病灶与切缘接近(≤5 mm)或切缘阳性的患者,总剂量为10~18 Gy,分2~6次完成。危及器官的剂量限制如下:脊髓D0.1cc≤45 Gy,小肠D2cc≤54 Gy,膀胱D50%≤45 Gy,直肠D50%≤45 Gy。对于同步化疗,以顺铂为基础的同步化疗方案包括顺铂单药周疗(30~40 mg/m2),或每3周共3~4个疗程的紫杉醇+顺铂/卡铂联合用药治疗。
1.2.2分组方法患者在治疗结束后1个月接受第一次随访评估。随后时间2012年5月至2020年4月,在治疗结束后的前2年内每3个月复查一次,3~5年内每6个月复查一次,5年后每年复查一次。常规随访检查包括妇科检查、SccAg、胸腹CT、盆腔MRI。怀疑患者病情复发时完善PET-CT检查。根据患者术后1年的生存情况,将生存时间≤1年的患者纳入死亡组,其余纳入存活组。相关因素包括患者年龄、手术方式、复发部位、术后FIGO分期、组织学亚型、病灶大小、病理类型、分化程度、间质浸润程度、淋巴导管浸润、宫旁浸润、手术标本切缘阳性、淋巴结阳性、复发后治疗方式等。
1.2.3判定标准复发定义为出现临床、影像或组织学疾病证据。局部复发被定义为盆腔复发,包括阴道残端和主动脉分叉以下的盆腔淋巴结区域。远处转移定义为局部复发区域以外的疾病复发。疾病复发后死亡定义为宫颈癌特异性死亡,即因肿瘤在相关器官过度生长而导致器官衰竭的死亡,排除因其他原因导致的死亡。
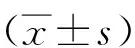
2 结 果
2.1 患者一般情况153例患者年龄29~67岁,平均年龄(47.67±8.99)岁。随访1年,死亡44例,病死率28.76%;存活109例,存活率71.24%。基础资料见表1。
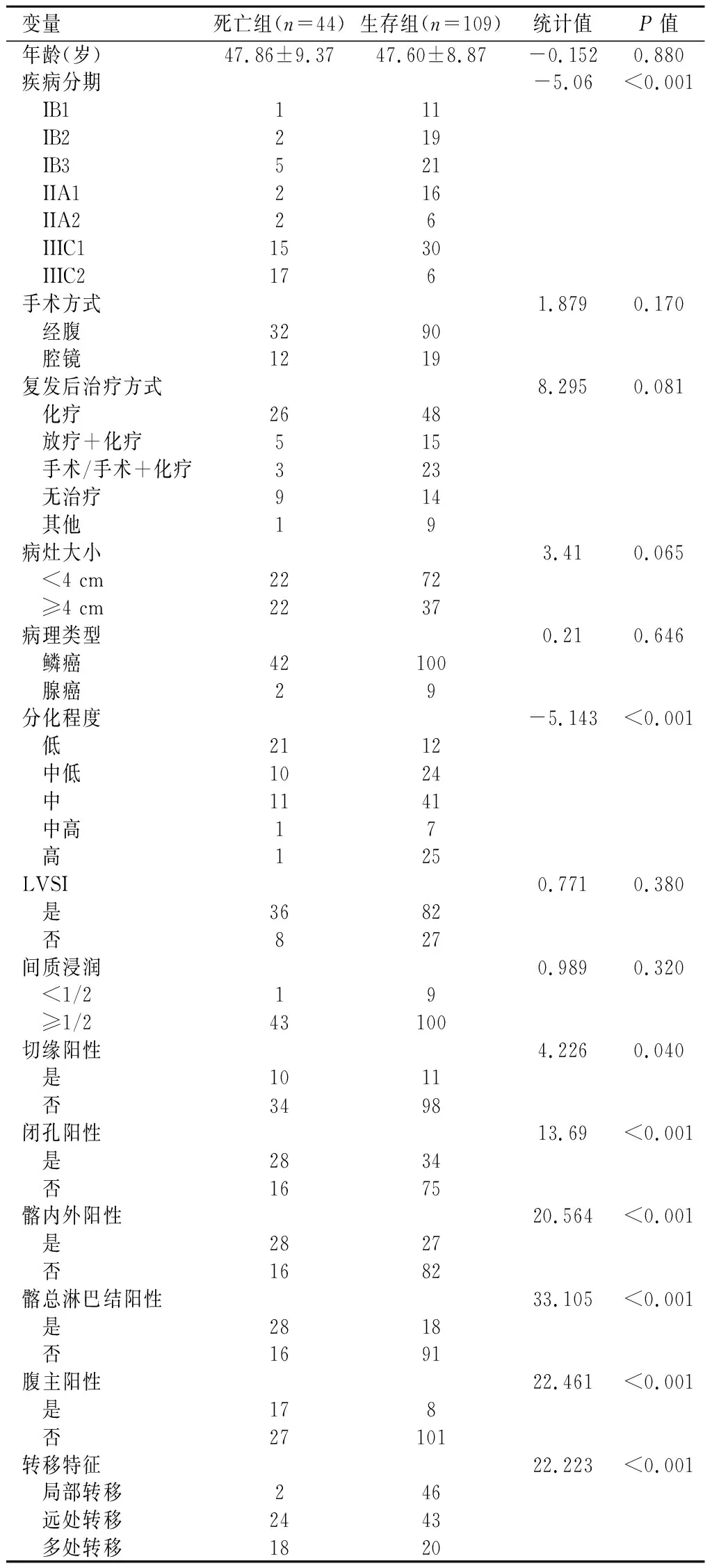
表1 宫颈癌复发患者1年内死亡单因素分析
2.2影响宫颈癌复发患者早期死亡的单因素分析将可能的变量纳入单因素分析,结果显示疾病分期、分化程度、切缘阳性、闭孔阳性、髂内外阳性、髂总阳性、腹主阳性和转移部位与患者1年内死亡相关(P<0.05)。见表1。
2.3多因素分析将单因素分析中差异有统计学意义的因素纳入Logistic回归分析,结果显示分化程度、切缘是否阳性、髂总淋巴结是否阳性及转移部位是宫颈癌复发患者早期死亡的影响因素(P<0.05)。见表2。
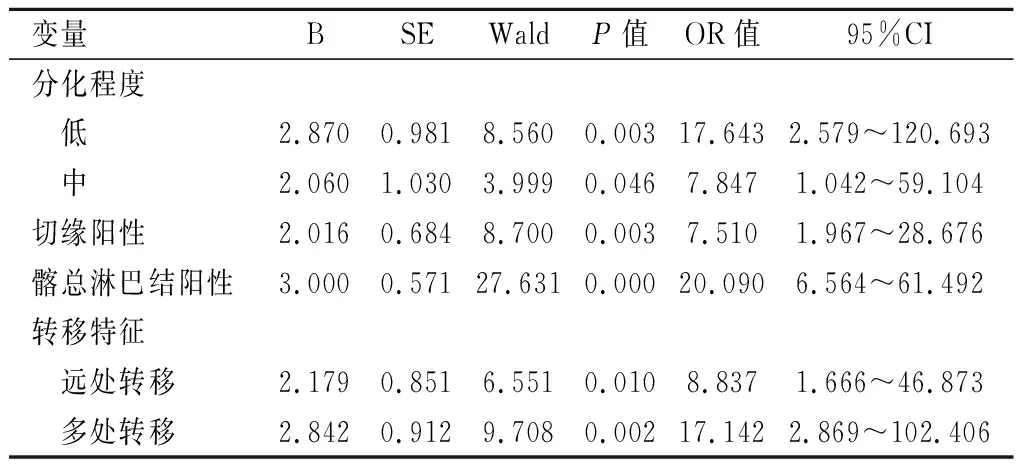
表2 宫颈癌复发患者1年内死亡Logistic回归分析
3 讨 论
2018年7月宫颈癌国际妇产科联盟(FIGO)发布了2018版的FIGO宫颈癌分期,相较于2009版做了一些调整[6]。如在肿瘤局限于子宫颈,镜下最大浸润深度≥5.0 mm情况下,根据肿瘤最大径大小分为IB1-IB3 3个等级,III期根据是否累及盆腔和/或主动脉胖淋巴结增加IIIC1及IIIC2级,可见临床病理高危因素对宫颈癌患者肿瘤分期及预后判断的重要性。
本研究宫颈癌复发患者1年内生存率为71.24%,患者预后受多种临床病理因素影响,其中,肿瘤中低分化、手术切缘阳性、髂总淋巴结阳性和远处及多处部位转移是患者不良预后的危险因素。在影响宫颈癌根治术后的预后影响因素中,大多研究均提示淋巴转移是高危因素[7-8],淋巴转移是宫颈癌转移的重要途经,肿瘤病灶侵入淋巴管,随淋巴液引流进入局部淋巴结,本研究将淋巴结位置具体细分,单因素分析发现闭孔、髂内外、髂总和腹主淋巴结阳性均有统计学意义,经多因素调整发现髂总淋巴结阳性是独立影响因素,提示髂总淋巴结阳性可能相较于其他位置淋巴结对宫颈癌复发患者具有更重要的预后意义。
切缘阳性也是宫颈癌不良预后的高危因素之一,由于肿瘤细胞切除不完全,残留组织可能导致术后复发及不良预后风险,McCann等[9]通过分析119例IA2-IIA期宫颈癌根治术患者的临床资料,切缘阳性患者复发率为24%高于阴性患者的9%。本研究中,44例早期死亡病例切缘阳性患者占22.7%,生存患者切缘阳性率10.1%,通过多因素分析,切缘阳性为复发患者不良预后的独立影响因素。肿瘤细胞低组织学分化通常提示肿瘤生物学行为差,往往预示患者不良预后,但对于分化程度是否为宫颈癌患者不良预后的影响因素尚存有争议。谢绍菊等[10]通过分析120例中晚期同步放化疗宫颈癌患者资料,发现临床分期、肿瘤分化程度、术前SCC-Ag水平、淋巴结转移及肌层浸润为影响生存率的风险因子。Wang等[11]研究发现,不同分化程度的早期宫颈癌患者术后复发率无统计学差异,提示肿瘤分化程度与早期宫颈癌患者预后无显著关系。本研究结果显示中低分化患者预后显著低于高分化患者,提示中低分化为复发患者不良预后的独立影响因素。复发转移部位也是影响宫颈癌预后的重要影响因素,田校源[12]研究发现复发转移部位是影响宫颈癌复发转移的重要预后因素之一。有研究通过分析205例放疗后复发转移宫颈癌患者的生存情况,远处淋巴转移和肺转移患者5年生存率为44.8%高于其他部位转移患者的生存期,盆腔复发、其他远处转移患者、多处转移患者5年生存率分别为15.3%、8.5%和10.3%[13]。本研究结果显示,转移部位是宫颈癌复发患者早期死亡的影响因素,远处转移及多处转移患者早期死亡风险高于局部复发患者。
宫颈癌不良病理类型包括腺癌、腺鳞癌和小细胞癌等,有研究认为宫颈腺癌患者由于诊断率相对较低,淋巴结转移较早,相对于鳞癌患者的生存期短,预后差,肿瘤病理类型为腺癌是影响术后预后不良的独立因素之一[14-15]。本研究结果与上述结论不一致,单因素和多因素分析均显示,患者肿瘤病理类型与肿瘤预后无关,并非影响预后的独立因素,可能由于本研纳入病例数量较少,早期死亡组腺癌病例仅为2例,需要后期纳入多中心更多病例进行研究探讨。根据NCCN指南,LVSI是影响宫颈癌预后的中危因素,但是否为宫颈癌预后的独立影响因素目前尚不明确。Gülseren等[16]通过分析194例IA2-IIA期宫颈癌患者资料,Cox回归分析结果显示FIGO分期、肿瘤大小、宫旁浸润、阴道切缘阳性、宫颈间质浸润和LVSI是影响预后的独立因素。本研究结果显示,LVSI非宫颈癌复发患者预后影响因素。
综上,本研究通过对153例宫颈癌复发患者临床病理资料进行回顾性分析,对该类患者的早期死亡影响因素进行初步探索,研究发现肿瘤分化程度、切缘阳性、髂总淋巴结阳性和肿瘤复发转移部位是影响患者早期死亡的因素。但本研究由于病例来自单中心,并且样本量较小,存在一定局限性,以期日后能联合多中心收集更大样本量进行更深入的探讨。
