元素形态分析仪测定水体中汞形态的研究
2021-10-15李艳苹王翠翠刘小骐赵剑超
李艳苹,王翠翠,刘小骐,赵剑超
(自然资源部天津海水淡化与综合利用研究所,天津 300192)
1 前言
随着水环境污染的日趋严重,环境的监测力度也逐渐增强。汞及其化合物是毒性极强的元素之一,对人类健康和生态环境的危害性很大[1-2],是水环境监测的重要对象。汞及其化合物的存在形式主要有单质汞、无机汞和有机汞,其中有机汞主要有甲基汞、乙基汞和苯基汞。不同形态的汞的毒性相差较大,其中有机汞(甲基汞、乙基汞)毒性远大于无机汞,元素汞基本无毒,苯基汞分解较快,毒性不大[3]。目前,人们已经达成共识,元素的生物有效性或毒性不仅与其总量有关,还与其存在形态有关。因此如何准确快速测定水环境中的汞形态,并进行安全性风险评估有着重要的意义。
目前元素形态分析仪具有全自动进样、仪器简单便于操作、价格较低、元素形态测定的专用性等特点,在环境中砷、汞、硒等元素的形态测试方面有不少应用。为了合理使用元素形态分析仪,提高测试水中汞形态的工作效率和质量,健全相应的测试方法,实验采用元素形态分析仪主要进行了水中汞形态的系列测试研究。
2 仪器及试剂
元素形态分析仪(北京海光仪器公司),海光HG C18柱:规格5 μm,100 Å,4.6 mm×150 mm;其它实验室常用设备。
除另有说明,所用试剂均为优级纯。
所用试剂:盐酸、氢氧化钾、硼氢化钾、过硫酸钾、溴化钾、吡咯烷二硫代氨基甲酸铵(APDC);甲醇、乙腈(色谱纯,天津康科德科技有限公司);乙酸铵(国药集团分析纯)、L-半胱氨酸(国药集团生化试剂,国药集团化学试剂有限公司)。
所用标准物质,有中国计量科学研究院研制的无机汞(MC) GBW(E)080124、甲醇中甲基汞(MMC)GBW08675、甲醇中乙基汞(EMC)GBW(E)081524;德国进口的标准品氯化苯汞(PMC,货号:C16065000,规格0.25 g,93.8%)。
3 仪器工作参数及实验方法
3.1 元素形态分析仪的工作参数(表1)

表1 仪器工作参数Tab.1 Working parameters of the instrument
3.2 实验方法
(1)标准溶液配制。分别取一定量无机汞、甲基汞、乙基汞、苯基汞的标准使用液,用去离子水定容,配成100 ng/mL的汞形态混合标准溶液,配好后并及时冷藏储存(4 ℃)。然后分别移取一定量的汞混合标准溶液,并用相应的流动相定容,配制成0 μg/L、0.5 μg/L、1 μg/L、2 μg/L、4 μg/L、8 μg/L、10 μg/L的标准系列溶液,需要现用现配。
(2)载流的配制。量取70 mL盐酸,倒入预先加入去离子水的1 000 mL烧杯中,再用去离子水稀释至刻度,摇匀备用。
(3)还原剂的配制。称取5 g氢氧化钾溶于约200 mL去离子水中,加入5 g硼氢化钾并使之溶解,用去离子水稀释至1 000 mL,摇匀备用。
(4)氧化剂的配制。称取5 g氢氧化钾溶于约200 mL去离子水中,加入10 g过硫酸钾并使之溶解,用去离子水稀释至1 000 mL,摇匀备用。
(5)流动相的配制。流动相Ⅰ。配制流动相Ⅰ 500 mL,先取0.123 g APDC和5.90 g KBr,溶于125 mL去离子水中,再加入150 mL甲醇和225 mL乙腈,摇匀备用,然后用0.45 μm微孔滤膜(有机膜)过滤,再经超声脱气后方可使用;流动相Ⅱ。配制流动相Ⅱ 500 mL,先称取1.8 g L-半胱胺酸和2.31 g乙酸铵,再加入25mL 甲醇,最后用去离子水稀释至500 mL,摇匀备用,然后用0.45 μm微孔滤膜过滤,再经超声脱气后方可使用。
3.3 不同流动相下的分离试验
在汞形态分析中,流动相中常加入一定量的甲醇、乙腈等有机改性剂,吡咯烷二硫代氨基甲酸铵(APDC)、L-半胱胺酸、双硫腙、2-巯基乙醇等络合剂[4]。一般改性试剂影响着流动相的极性,会影响组分的保留时间以及峰与峰之间的分离效果。络合剂一般含有络合功能团,能够和汞离子络合,加速汞组分的洗脱[5],常用的有吡咯烷二硫代氨基甲酸铵和L-半胱胺酸。实验基于HG C18柱反相分离,研究了两种流动相下汞形态的分离效果。分别以吡咯烷二硫代氨基甲酸铵(APDC)和L-半胱胺酸为络合剂的两种流动相,分别称作流动相Ⅰ和流动相Ⅱ。按3.1工作参数设定好仪器,按照(1)~(5)的实验条件,考察了3种~4种汞形态的分离情况。分离图谱如图1,具体分离实验数据分别见表2和表3。实验表明,在使用流动相Ⅰ的情况下,能分离出MMC、EMC、PMC及MC四种汞形态,保留时间约在5 min~11 min范围内,但是约在21 min出现鼓包,可能是PMC不稳定易分解导致;而在流动相Ⅱ的情况下,对MC、MMC、EMC三种汞形态进行测定,结果表明有着很好的分离效果,保留时间分别为1.861 min、3.228 min、7.038 min,与流动相Ⅰ相比,分离时间大大缩短,约在7 min内即可完成以上三种汞形态的分离,与文献[4]相比,基本一致。另外,由于流动相Ⅰ中需使用大量的甲醇和乙腈试剂,苯基汞也不太稳定,综合考虑选用L-半胱胺酸为络合剂的流动相。
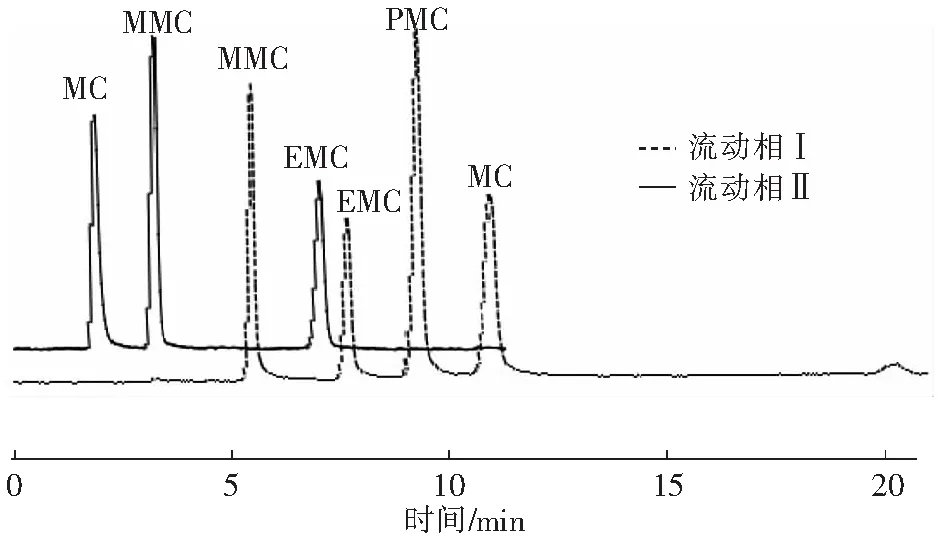
图1 不同流动相下汞形态的分离谱图Fig.1 Separation spectra of mercury species in different mobile phases
3.4 检出限与精密度
在优化的实验条件下,设定进样量100 μL,在采用流动相Ⅰ的情况下,MMC、EMC、PMC及MC四种汞形态的检出限分别为0.042 μg/L、0.079 μg/L、0.036 μg/L、0.070 μg/L;在采用流动相Ⅱ的情况下,MC、MMC、EMC三种汞形态的的检出限分别为0.026 μg/L、0.023 μg/L、0.039 μg/L。另外,连续测定6次浓度为10 μg/L的汞形态混合标准溶液,分别对不同汞形态的峰面积进行积分计算,相对标准偏差在2.15%~4.18%范围内(见表2和表3),精密度良好。相比之下,在采用流动相Ⅱ的情况下,三种汞形态的信号更强、检出限更低、精密度更好。
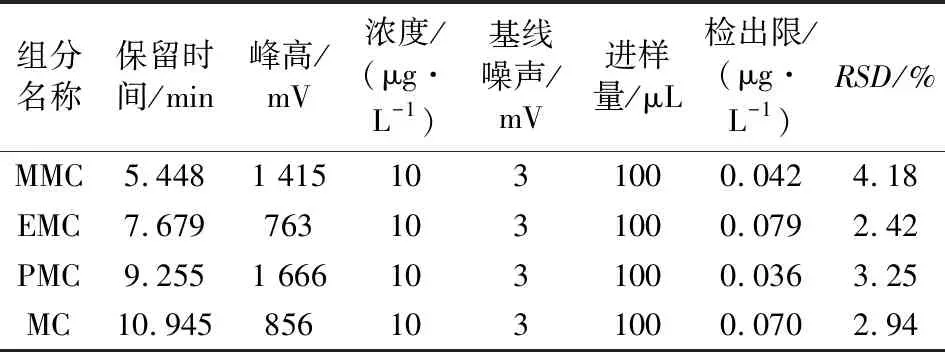
表2 流动相Ⅰ条件下汞形态的分离实验数据Tab.2 Experimental data of mercury speciation separation in mobile phaseⅠ

表3 流动相Ⅱ条件下汞形态的分离实验数据Tab.3 Experimental data of mercury speciation separation in mobile phase Ⅱ
3.5 线性方程
考虑到流动相Ⅰ的情况下,汞形态分离的保留时间相对较长,检出限不够低,而且分离图谱上出现小鼓包的情况,因此在优化的实验条件下,采用流动相Ⅱ,又进一步测定了MC、MMC、EMC三种汞形态的标准系列溶液,以浓度点为横坐标,相应的峰面积为纵坐标,绘制工作曲线,获得线性方程,数据具体见表4。从表4可看出,在0 μg/L~10 μg/L范围内,三种汞形态的相关系数R均大于0.999,具有很好的线性关系。

表4 3种汞形态的标准曲线Tab.4 Standard curves of three mercury forms
4 结论
基于C18柱反相分离,分别采用流动相Ⅰ(以APDC为络合剂)和流动相Ⅱ(以L-半胱胺酸为络合剂)进行汞形态的分离实验。结果表明,与流动相Ⅰ先比,采用L-半胱胺酸为络合剂的流动相,可在更短时间内(7 min)完成MC、MMC、EMC三种汞形态的分离,分离效果好、检出限低、精密度高、实用性强,而且耗费有机试剂少,采用L-半胱胺酸为流动相的方法更适用于水环境中汞形态的分析和监测。
